



Preview text:
Machine Translated by Google BÀI BÁO DOI: 10.1038/s42004-018-0046-7 MỞ
Phân tích điện hóa pha khí của các axit amin và các mảnh của chúng Maria Calleja1 ,
Atif Elahi1 & Daren J. Caruana1 1234567890():,;
Tất cả các phản ứng hóa học đều liên quan đến sự sắp xếp lại electron bên trong hoặc giữa các phân
tử. Những thay đổi này được nghiên cứu tốt nhất bằng các phương pháp như điện hóa học, nhưng các
phương pháp này chủ yếu được phát triển cho chất lỏng và chất rắn chứ không phải chất khí. Sự loại
trừ này hạn chế sự hiểu biết của chúng ta về các quá trình chuyển electron, vốn là trung tâm trong
các hệ thống plasma, có tầm quan trọng cao về khoa học, công nghiệp và môi trường. Ở đây, chúng tôi
mô tả các phép đo điện hóa trong pha khí của các phân tử hữu cơ nhỏ có trong plasma ngọn lửa, bằng
cách thăm dò hoạt tính oxy hóa khử của các mảnh hóa học tạo thành bằng phương pháp đo điện thế tuần hoàn.
Chúng tôi ghi nhận được phổ điện áp-dòng điện độc đáo cho tám axit amin và các mảnh của chúng, thông
qua các phản ứng truyền electron đặc hiệu tại giao diện rắn/khí. Chúng tôi xác định và gán các đỉnh
Faradaic trong phổ điện áp-dòng điện cho các mảnh bằng cách sử dụng các chất tương tự ổn định của các
mảnh và phương pháp đo phổ khối lượng tại chỗ. Chúng tôi chứng minh rằng phương pháp này cung cấp khả
năng nhận dạng rõ ràng các phân tử hữu cơ, với độ nhạy và khả năng phân loại sánh ngang với phương
pháp đo phổ khối lượng.
1 Phòng thí nghiệm Christopher Ingold, Khoa Hóa học, Đại học College London, 20 Gordon Street, London WC1H 0AJ, Vương quốc Anh. Mọi thư từ và yêu cầu tài liệu xin vui lòng gửi đến DJC (email: DJCaruana@ucl.ac.uk)
HÓA HỌC TRUYỀN THÔNG | (2018) 1:48 | DOI: 10.1038/s42004-018-0046-7 | www.nature.com/commschem 1 Machine Translated by Google BÀI BÁO
HÓA HỌC TRUYỀN THÔNG | DOI: 10.1038/s42004-018-0046-7
Sự khử điện hóa của mảnh cacboxylat COOH (hoặc HCOO) được chỉ ra
sự phong phú đáng kinh ngạc của kiến thức hóa học làm nền tảng cho tất cả mọi thứ.
bởi mảnh trong phổ khối lượng (MS) đối với axit formic và axit
Sự chuyển electron giữa các nguyên tử hoặc phân tử dẫn đến...
Các quá trình cơ bản, từ hình thành sao đến duy trì sự
ethanoic ở 45 m/z, Hình 2b14–16. Để hỗ trợ cho cách giải thích này,
sống1,2. Trao đổi electron cũng rất cần thiết trong công nghiệp.
axit amin alanin có cùng đỉnh. Mảnh COOH (hoặc HCOO) trái ngược với
và nghiên cứu để đạt được các chuyển đổi hóa học mong muốn. Tiếp tục-
CO2 là hợp lý khi xét đến plasma khử nhẹ với tỷ lệ hydro cao trong
Do đó, các kỹ thuật giúp hiểu rõ hơn về các phản ứng oxy hóa khử là ngọn lửa trộn sẵn. Thật vậy, việc thêm CO2 vào ngọn lửa đến nồng độ
vô cùng quan trọng. Phân tích điện hóa thường được thực hiện tại
10%/thể tích không tạo ra tín hiệu khử có thể đo được, rất có thể
giao diện rắn/lỏng để nghiên cứu các phản ứng gắn electron tại bề
là do năng lượng gắn kết electron dương lớn tương ứng17.
mặt điện cực dưới các mức năng lượng tương ứng với nhau3. Tuy nhiên,
giao diện rắn/lỏng đặt ra hai hạn chế: các chất phân tích nằm ngoài
phạm vi hoạt động điện hóa nội sinh của dung môi bị loại trừ khỏi
Phân tích sâu hơn cho thấy axit ethanoic nhưng không phải axit methanoic có thêm một đỉnh ở 9,0 ± 0,2
quá trình phát hiện và chất lỏng tạo ra một rào cản khuếch tán đáng V (Hình 2a). Tín hiệu + rất có thể là do mảnh CH2 có nguồn gốc từ nhóm methyl, được thấy trong phổ MS hỗ
kể. Cách triệt để nhất để khắc phục những hạn chế này là loại bỏ
trợ của axit ethanoic dưới dạng đỉnh ở 14 m/z nhưng không thấy đối với axit methanoic (Hình 2b). Việc lấy
hoàn toàn dung môi4–8. Tuy nhiên, một yêu cầu quan trọng vẫn là đạt mẫu MS được thực hiện tại cùng một điểm mà điện cực sẽ được đặt để đo điện hóa. Để hỗ trợ, alanin cũng cho
được độ dẫn điện để duy trì sự truyền tải điện tích6,9–11.
thấy các đỉnh trong cả hai phương pháp phân tích. Điện thế cao 9,0 ± 0,2 V nhấn mạnh ưu điểm của phương
pháp đo điện thế pha khí mới vì phương pháp điện hóa dựa trên chất lỏng cổ điển với phạm vi giới hạn từ 2
đến +3 V so với NHE do sự phân hủy của dung môi, điện cực hoặc chất điện giải sẽ không cho phép phát hiện.
Ở đây, chúng tôi trình bày một phương pháp khác biệt so với
điện hóa học thông thường và đo – trong pha khí – sự khử điện hóa
trực tiếp các hợp chất hữu cơ thông qua phép đo điện thế. Nguyên lý
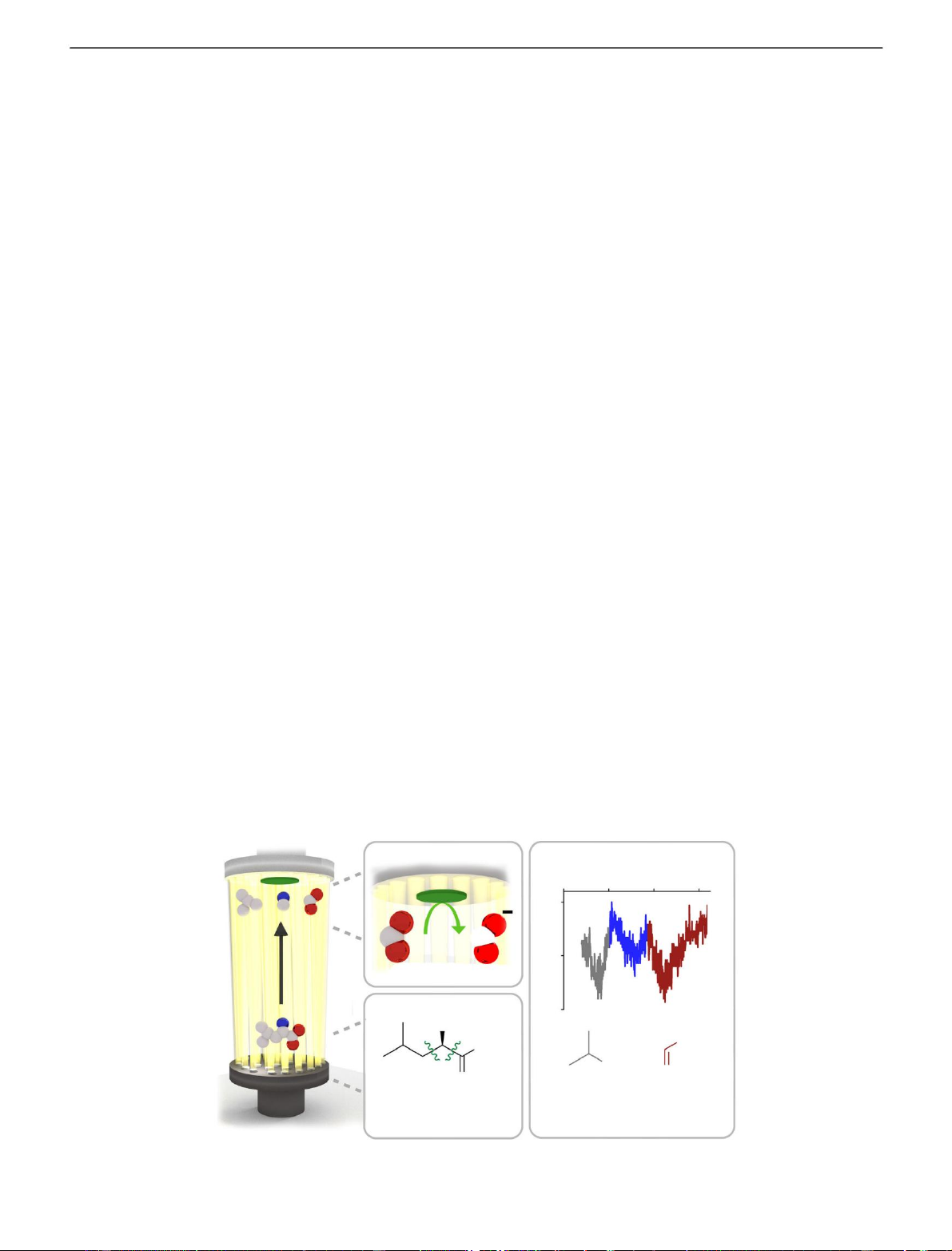
của phương pháp được tóm tắt sơ lược trong Hình 1. Một phân tử mục
tiêu được thêm vào ngọn lửa hydro/oxy đóng vai trò là chất điện
phân trong pha khí. Ngọn lửa cũng phân mảnh phân tử thành các đơn
vị ổn định cũng như một số loài gốc tự do tạm thời12.
Sau khi xác định rằng các nhóm axit cacboxylic tạo ra các dấu hiệu điện hóa
Các loài gốc tự do này tương tác với bề mặt điện cực làm việc bằng
đặc trưng, các nhóm hydroxyl đã được thử nghiệm. Các đường cong điện thế-dòng
cách nhận một electron, tạo ra một loạt các đỉnh khử tương ứng
điện của metanol và etanol tạo ra một đỉnh rộng ở 4,1 ± 0,4 V (Hình 2a), do
trong biểu đồ điện thế. Sự nhiễu từ các ion của ngọn lửa hydro/oxy
đó xác nhận rằng sự phân mảnh do ngọn lửa gây ra cũng tạo ra một dấu hiệu đặc
là tối thiểu vì phân tử mục tiêu được đưa vào ở mật độ xấp xỉ 1,2
trưng cho C–OH. Tuy nhiên, các tín hiệu điện hóa này có thể bắt nguồn từ nhóm
± 0,2 × 1018 hạt m-3, cao hơn khoảng một
CHO bị oxy hóa, nhóm này cũng được phát hiện trong MS dưới dạng đỉnh 29 m/z
nghìn lần so với sự ion hóa nền. Điện thế khử được ghi lại được xác (Hình 2b). Sự phân mảnh oxy hóa của rượu trong quá trình đốt cháy đã được biết
định so với một điện cực tham chiếu nhiệt độ cao được phát triển
đến rộng rãi18,19 (xem Chú thích bổ sung 1) và chiếm ưu thế trong môi trường
đặc biệt dựa trên oxit zirconi dẫn oxy (YSZR)13. Tất cả
khử nhẹ của plasma. Tín hiệu điện hóa khác ở 8,0 ± 0,3 V chỉ có ở etanol có
các điện thế được trích dẫn ở đây đều so với điện cực tham chiếu
thể phản ánh một mảnh dicarbon không được quan sát thấy trong MS. này. Kết quả
Phân tích điện hóa pha khí của các axit và rượu đơn giản. Để kiểm
chứng phương pháp mới, trước tiên chúng tôi đã thêm vào plasma hai
Phân tích axit amin. Tiếp theo, serine được kiểm tra để xem liệu
loại hợp chất hữu cơ đơn giản mang nhóm axit cacboxylic và ghi lại
nhóm hydroxyl và nhóm carboxyl, vốn được phát hiện riêng biệt trước
các tín hiệu khử. Giả thuyết làm việc của chúng tôi là nhóm chức sẽ đó, có thể được xác định trong cùng một phân tử hay không.
tạo ra một gốc tự do, được đo lường như một dấu hiệu đặc trưng
Thật vậy, biểu đồ điện thế của serine cho thấy một tín hiệu chung
trong các đường cong điện thế-dòng điện.
ở mức 4,1 ± 0,4 V tương tự như hai loại rượu tham chiếu đơn giản
Thực tế, cả axit metanoic và axit etanoic đều tạo ra một đỉnh nổi
(Hình 2a). Đồng thời, alanine đối chứng âm tính thiếu nhóm hydroxyl
bật ở 5,80 ± 0,3 V (Hình 2a), rất có thể đại diện cho
không có tín hiệu này. Để củng cố thêm điều này, serine b c E (V) -10 –8 –6 -4 0 Trong trường hợp) -5 Sự giảm bớt Một -10 NH2 HCNH2 Ồ Ồ CH2 CÁI CÁI Sự phân mảnh do Điện thế kế ngọn lửa gây ra
Hình 1. Sơ đồ phân tích điện hóa các chất hữu cơ trong plasma ngọn lửa. Thể hiện quá trình đưa các chất hữu cơ vào ngọn lửa, tiếp theo là a) sự phân mảnh và
b) phân tích điện hóa. Các đỉnh trong biểu đồ điện thế kế ở hình c được gán cho các mảnh vỡ từ quá trình đốt cháy không hoàn toàn. 2
HÓA HỌC TRUYỀN THÔNG | (2018) 1:48 | DOI: 10.1038/s42004-018-0046-7 | www.nature.com/commschem Machine Translated by Google
HÓA HỌC TRUYỀN THÔNG | DOI: 10.1038/s42004-018-0046-7 BÀI BÁO Một b 105 H Ồ Methyl Axit Rượu bia H Ồ H3C Ồ 104 CÁI CÁI 103 Ồ H3C Ồ H3C 102 CÁI CH3 Ồ 105 Ồ H3C Ồ Ồ H2N H2N 104 CÁI CÁI CÁI 103 10 nA 102 Amin Thơm Cường độ (cps) 105 H3C Ồ Ồ 104 H3C 103 NH2 Ồ 102 Ồ Ồ H2N H2N 105 HOH 3C CÁI CÁI 104 Ồ H2N 103 CÁI 102 –8 –6 –4 -2 0 2 –8 –6 –4 –2 0 2 0 10 20 30 40 50 60 E so với YSZR (V) E so với YSZR (V) m/z (au)
Hình 2. Điện thế kế và phổ khối lượng tại chỗ trong plasma ngọn lửa chứa các hợp chất hữu cơ đơn giản. a. Điện thế kế của ngọn lửa chứa axit metanoic, axit etanoic
và alanin, metanol, etanol và serine, metylamin và glycin, phenol, tyrosin và phenylalanin, được đưa vào ngọn lửa bằng dung dịch nước được phun sương với nồng độ
5 mM, ngoại trừ tyrosin là 1 mM. b. Phổ khối lượng của ngọn lửa chứa axit metanoic, axit etanoic, metanol và etanol, tất cả đều được hiệu chỉnh cho ngọn lửa nền chứa
nước khử ion. Các mũi tên màu chỉ ra các khối lượng cần quan tâm.
Đỉnh axit xuất hiện ở 5,9 ± 0,15 V, gần như giống hệt với giá Một b
trị của axit metanoic và ethanoic ở 5,80 ± 0,3 V. Đáng chú ý, cả
serine và alanine đều hiển thị một đỉnh ở 7,9 ± 0,2 V, có thể
phản ánh nhóm amin. Sự giải thích này được hỗ trợ bởi tín hiệu Ồ H2N
7,9 ± 0,2 V với cùng độ bất đối xứng đối với metylamin có cấu CH3 CÁI Ồ
trúc hóa học đơn giản hơn, cũng như glycine (Hình 2a). Metylamin H2N
cho thấy các đỉnh khác như dự kiến từ quá trình đốt cháy phức tạp Ồ CÁI
hơn đã biết của nó20,21. Ồ CH3
Các nhóm thơm như phenol và các axit amin tyrosine và H2N
phenylalanine cũng tạo ra các đỉnh voltammogram đặc trưng. CÁI CH3
Ví dụ, phenol thể hiện rõ hai đỉnh tại 3,9 ± 0,3 V và 2,5 ± Ồ CH3 H2N
0,3 V ở cùng mức điện thế như đối với phenylalanine và tyrosine CH3 CÁI
(Hình 2a). Các tín hiệu này có thể liên quan đến sự mở vòng của Dòng điện (A)
các nhóm thơm và sự phân hủy tiếp theo. Khoảng cách giữa hai đỉnh, Ồ H2N
ΔE đối với phenol và phenylalanine lần lượt là 1,05 ± 0,10 V và CÁI
1,10 ± 0,08 V, nhưng đối với tyrosine là 0,93 ± 0,08 V, gần như Ồ giống hệt nhau. Ồ H2N
Bất kỳ sự khác biệt nhỏ nào giữa chúng có thể là do sự thay thế CÁI khác nhau trên vòng benzen.
Để khẳng định rằng điện hóa pha khí có thể phân biệt giữa một Ồ H3C CH3 H2N
loạt các phân tử chất phân tích có liên quan chặt chẽ với các nhóm CÁI Ồ
chức khác nhau, một tập hợp rộng gồm tám axit amin đã được kiểm H2N 10 nA
tra. Các đặc điểm trong biểu đồ điện thế-dòng điện cho mỗi axit CÁI
amin, Hình 3, phản ánh dấu hiệu của các nhóm chức chính của axit –8 –6 –4 –2
amin, như đã được xác định từ các phân tử đơn giản đã được phân E so với YSZR (V)
tích trước đó (Hình 2a). Ví dụ, biểu đồ điện thế-dòng điện của
glycine, alanine và serine với các đỉnh ở khoảng -4,1, -5,8, -7,7
Hình 3. Điện thế kế của tám axit amin được thêm vào plasma ngọn lửa.
và -9,0 V được gán cho các nhóm hóa học đã được xác định trước đó
Hình a thể hiện cấu trúc hóa học được mã hóa màu và hình b thể hiện đồ thị
là nhóm rượu, axit, amin và metyl, tương ứng. Sự giải thích này
điện thế tương ứng trong ngọn lửa chứa glycine, alanine, serine, leucine,
được hỗ trợ bởi MS vì mô hình phân mảnh phản ánh các tín hiệu điện isoleucine, phenylalanine, tyrosine, được đưa vào ngọn lửa bằng dung dịch nước
hóa của ba axit amin (Hình 3). Tương tự, các axit amin thơm cho
dạng phun sương có nồng độ 5 mM, ngoại trừ tyrosine có nồng độ 1 mM.
các đỉnh dự kiến cho sự mất nhóm axit ở -5,8 V ± 0,3 V, và các đặc
điểm khác có thể là do sự phân hủy của phần thơm. Đúng như dự
(Hình 3b) với -5,8, -7,5 và -9,0 V tương ứng do quá trình khử
đoán, các axit amin đồng phân leucine và isoleucine có cùng cấu
cacbon, amin và các mảnh aliphatic. Đồ thị điện thế của valine, trúc.
leucine và isoleucine chỉ khác nhau về số lượng hoặc cấu trúc của
các nguyên tử cacbon, do đó có các đặc tính điện hóa liên quan. 3
HÓA HỌC TRUYỀN THÔNG | (2018) 1:48 | DOI: 10.1038/s42004-018-0046-7 | www.nature.com/commschem Machine Translated by Google BÀI BÁO
HÓA HỌC TRUYỀN THÔNG | DOI: 10.1038/s42004-018-0046-7
các tín hiệu cũng như các kiểu phân mảnh được thể hiện bằng MS trong Hình
Lời giải thích này rõ ràng khác với điện hóa pha lỏng truyền thống, trong bổ sung 1.
đó quá trình chuyển electron diễn ra khi mức Fermi cao hơn ER (Hình 5), như
được chứng minh bằng các mức dòng điện theo từng bước trong các biểu đồ
Nghiên cứu cơ chế. Dữ liệu điện thế kế cho thấy quá trình khử điện hóa diễn
điện thế-dòng điện truyền thống25.
ra trên bề mặt điện cực. Để cung cấp bằng chứng trực tiếp cho phản ứng xảy
Tính độc đáo của điện hóa pha khí được nhấn mạnh bằng cách chứng minh
ra trên bề mặt này, phương pháp quang phổ Raman tại chỗ đã được áp dụng
rằng các đỉnh trong đồ thị điện thế chỉ thể hiện sự khử chứ không phải sự
(Hình 4). Theo đó, một điện cực graphit được tiếp xúc với ngọn lửa pha thêm
oxy hóa của các mảnh phân tử.
nước chứa 5 mM leucine, và phổ Raman được ghi lại ở các bước 1 V từ 0 V đến
Về mặt trực quan, có thể suy ra sự vắng mặt của quá trình oxy hóa từ việc
-10 V và ngược lại. Phân tích tập trung vào dải Raman carbon G ở 1560 cm⁻¹
không có các đỉnh ở chiều dương trên đồ thị điện thế-dòng điện.
Đối với một hệ thống như thế này với sự vận chuyển khối lượng thủy động hiệu
vì nó tương ứng với chế độ quang học E2g , trong đó sự kéo giãn của tất cả
quả của các chất bị oxy hóa đến bề mặt điện cực, dự kiến sẽ xuất hiện trong
các liên kết với các nguyên tử sp2 nhạy cảm với các quá trình oxy hóa
biểu đồ điện thế dưới dạng một vùng ổn định, được biểu diễn bằng đường liền
khử²²,²³. Như thể hiện trong Hình 4b, cường độ của dải thay đổi theo điện
màu xanh lam trong Hình 5. Tính chất độc đáo này cũng có thể được chính thức
thế tĩnh được áp dụng và tương quan mạnh mẽ với các đỉnh điện hóa về sự phụ
hóa bằng phương trình (1), dự đoán dòng điện được hiển thị bằng đường liền
thuộc vào điện áp và cường độ tín hiệu. Điều này có nghĩa là ở các điện thế
màu đỏ trong Hình 5, tương tự như những gì chúng ta quan sát được trong thực
có sự khử điện hóa mạnh, dải G có cường độ thấp. Mối tương quan này là như
nghiệm, thông qua các tích phân cho quá trình khử và quá trình oxy hóa
nhau khi điện thế được quét theo cả hai hướng; nó không xảy ra khi không có
lysine (Hình 4a). Do đó, dữ liệu Raman cung cấp bằng chứng thuyết phục về 1 1
phản ứng oxy hóa khử tại bề mặt điện cực tiếp xúc với plasma khí. I ¼ nFA mOCOνR Z PRð TH E DOWN TH E dE 1
POÔ Þ E ÝÔ Þ E dE mRCRνO Z1 ð1Þ
trong đó n, F và A lần lượt là số electron tham gia vào quá trình khử, hằng
số Faraday và diện tích điện cực. Hệ số vận chuyển khối lượng đến điện cực
Khung lý thuyết. Sau khi chứng minh tính hợp lệ thực nghiệm của phương pháp
và nồng độ của các chất bị oxy hóa (chỉ số phụ O) và bị khử (chỉ số phụ R)
điện hóa, tiếp theo chúng tôi tìm cách đặt nó trong một khung lý thuyết. Những
được biểu thị bằng m và C tương ứng, và v là tần số chuyển tiếp cho phản ứng
xem xét đầu tiên của chúng tôi tập trung vào thực tế là các đường cong điện
chuyển electron. Tích phân định lượng sự chồng chéo của các trạng thái
thế pha khí có các đỉnh thay vì các mức dòng điện bậc thang điển hình cho điện
electron trong điện cực N(E) và sự phân bố các trạng thái trong khí, P(E)
hóa pha lỏng (Hình 5). Để giải thích các đỉnh này, chúng tôi sử dụng năng lượng như một hàm của điện thế đặt vào (xem Chú thích bổ sung 2). Sử dụng phương
Fermi của điện cực cho quá trình chuyển electron, EF, và thế khử đặc trưng,
trình (1), các đường cong I/V được tính toán cho quá trình oxy hóa và khử
ER, cho các mảnh hữu cơ bị oxy hóa trong pha khí24. Quá trình chuyển electron
trong pha khí được thể hiện bằng đường chấm đỏ trong Hình 5. Sự vắng mặt của
giữa điện cực và các mảnh được giả định chỉ diễn ra khi EF và ER trùng nhau
quá trình oxy hóa có thể được giải thích ở cấp độ phân tử bằng cách xem xét
về mặt năng lượng (Hình 5, EF-2 = ER). Điều này có thể đạt được bằng cách thay
độ lớn tương đối của mO và mR. Vì cả hai đều tính đến sự vận chuyển phân tử
đổi EF theo thế. Ngược lại, các mức năng lượng không khớp EF-1 < ER hoặc EF-3
qua lớp khuếch tán trên bề mặt điện cực, thuật ngữ mO—đồng nghĩa với việc
> ER không dẫn đến quá trình chuyển electron (Hình 5). Điều này
cung cấp chất bị oxy hóa Một 0 b –10V -10 60 -9V –8V -20 -7V Dòng điện (nA) 40 -6V -30
D (Cường độ tương đối) (au) -5V –4V –3V -40 20 –2V –1V -50 25 đến 0 -10 –8 -6 -4 -2 0 1520 1600 E so với YSZR (V)
Độ dịch chuyển Raman (cm–1)
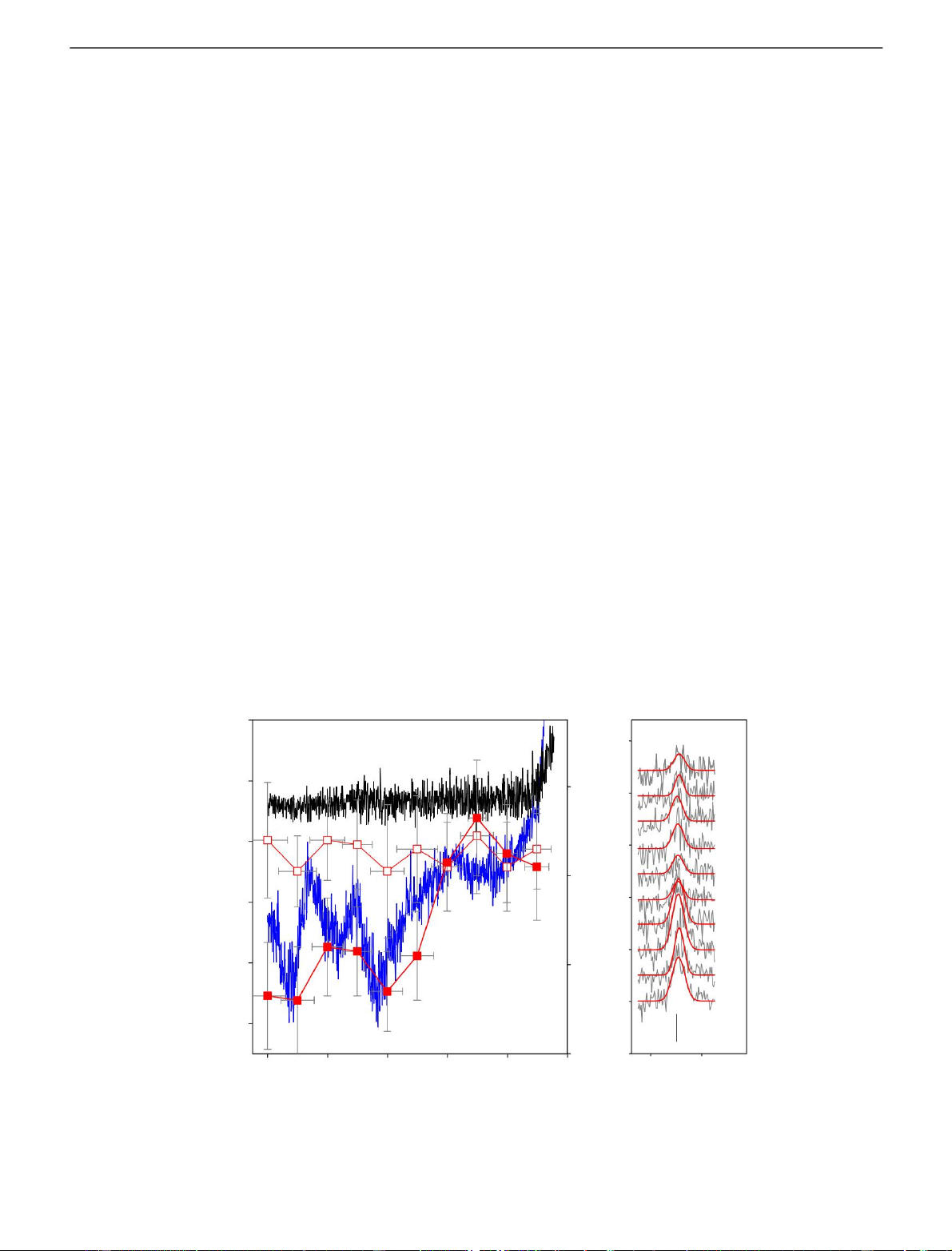
Hình 4. Phổ Raman tại chỗ của bề mặt điện cực dưới sự kiểm soát điện hóa. a. Điện thế kế và chiều cao đỉnh Raman động học ở 1560 cm 1 của điện cực làm việc bằng than chì được giữ
, ở điện thế không đổi trong 1 phút, trong plasma ngọn lửa được pha thêm nước tinh khiết (điện thế kế, đường màu xanh nhạt; động học, hình vuông rỗng) và
leucine 5 mM (điện thế kế, đường màu xanh đậm; động học, hình vuông đặc). Vạch lỗi biểu thị sai số chuẩn của ba phép đo. b. Phổ Raman giữa 1500 và 1630 cm 1 (đường
màu xám) được khớp với hàm Gaussian (đường màu đỏ), được giữ ở điện thế từ -1 đến -10 V so với YSZR. 4
HÓA HỌC TRUYỀN THÔNG | (2018) 1:48 | DOI: 10.1038/s42004-018-0046-7 | www.nature.com/commschem Machine Translated by Google
HÓA HỌC TRUYỀN THÔNG | DOI: 10.1038/s42004-018-0046-7 BÀI BÁO EF-3
các phản ứng tại giao diện rắn/khí. Mặc dù ở đây chúng tôi chỉ hiển
thị các phép đo trong khoảng từ 0 đến -10 V, nhưng chúng tôi kỳ vọng MỘT- Và- LÀ EF-2
sẽ có nhiều thông tin điện hóa phong phú hơn có thể được khai thác LÀ LÀ MỘT ngoài phạm vi này.
+ Năng lượng electron (eV) –
Thiết kế tiết kiệm của cụm điện cực vừa chắc chắn vừa đơn giản, tạo ĐÂY ĐÂY ĐÂY EF-1
nên một công cụ rất mạnh mẽ cho phân tích hóa học26. Chúng tôi dự đoán
rằng phương pháp này sẽ mở rộng tiện ích của các đầu dò Langmuir bằng Plasma rắn
cách cung cấp thông tin hóa học thay vì chỉ đo độ dẫn điện đơn giản
để phát triển các công cụ chẩn đoán plasma mới27,28, kích thích các
máy phân tích mới cho plasma hấp thụ nguyên tử và plasma ghép nối cảm ứng. Huyết tương Phương pháp
Thiết kế đầu đốt. Một đầu đốt kiểu Méker được thiết kế đặc biệt (dựa trên
thiết kế được mô tả bởi Goodings và Hayhurst29) được sử dụng cho nghiên cứu này
được mô tả trong Ghi chú bổ sung 3 và Hình bổ sung 2, cung cấp ngọn lửa dòng
chảy tầng hai ngăn bao gồm hỗn hợp hydro, oxy và nitơ được trộn sẵn. Các dung dịch – Dòng điện (A) +
nước được chuẩn bị bằng nước khử ion (Millipore Milli- Q® gradient, <0,05 S
cm 2). Dung dịch được đưa vào dòng khí dưới dạng sol khí được tạo ra từ một máy Chất lỏng
phun siêu âm cải tiến (Index Ltd. UK).
Tấm đồng thau phía trên của đầu đốt được làm sạch bằng cách cạo lớp cặn trên bề
mặt, và các lỗ được làm sạch cẩn thận bằng mũi khoan đường kính 0,5 mm trước EF-3 EF-2 EF-1
mỗi lần thí nghiệm. Đầu đốt được lắp đặt thẳng đứng trên một bàn nhôm nối đất.
Hai ngọn lửa được cung cấp bởi hai luồng khí độc lập với tốc độ dòng chảy lần lượt
– Điện thế đặt vào (V) +
là 1,6, 0,4 và 1,0 L min 1 đối với nitơ (99,99%), oxy (99,9+%) và hydro
(99,995%) (khí do BOC cung cấp); với tổng tốc độ dòng chảy cho toàn bộ ngọn lửa
Hình 5. Sơ đồ liên hệ giữa điện thế điện hóa được áp dụng với mức năng lượng
là 6,0 L min 1, được thể hiện trong Phụ lục 3. Bộ điều khiển lưu lượng khối kỹ
electron và các đường cong I/V dự kiến. Sơ đồ mức năng lượng thể hiện mối quan
thuật số được điều khiển riêng lẻ (5850 S, Brooks, Hoa Kỳ, với giao diện điều
hệ giữa các mức năng lượng electron được biểu thị dưới dạng trạng thái khả
khiển IGI, Anh) được sử dụng để điều chỉnh tốc độ dòng chảy của hydro, oxy và
nitơ. Trước khi đến đầu đốt, mỗi trong hai luồng khí được trộn kỹ trong một
dụng ở ba điện thế điện hóa, EF-1, EF-2 và EF-3 và các trạng thái pha khí đối
buồng, bao gồm một tấm chắn để bảo vệ chống lại hiện tượng bắt lửa ngược; NB. Hỗn
với các loài bị khử, ER và bị oxy hóa, EO . Các đường màu đỏ là các đường cong
hợp khí hydro và oxy dễ cháy nổ và các biện pháp an toàn thích hợp đã được thực
I/V được tính toán bằng cách sử dụng phương trình (1), đường nét đứt là khi mR
hiện. Đường dẫn khí cho cả hai luồng đều giống hệt nhau ngoại trừ buồng tạo
= mO và CR = CO và đường liền nét khi mR = 0 và CR = 0. Đường cong I/V màu xanh
sol khí được sử dụng để đưa các chất hữu cơ vào ngọn lửa, trong đường dẫn khí
nitơ, trước buồng trộn cung cấp cho phần bên phải của ngọn lửa. Trong tất cả các
lam là quá trình tương đương trong chất điện phân lỏng.
thí nghiệm, dung dịch được thêm vào ngọn lửa bên phải, ngọn lửa bên trái được giữ
nguyên là ngọn lửa sạch và được sử dụng làm ngăn điện cực tham chiếu. Quy
trình hiệu chuẩn để cung cấp chất pha tạp cho ngọn lửa bên phải được trình bày
chi tiết trong Phụ lục 4.
mR—tương đương với quá trình khử—sẽ cao vì các mảnh gốc tự do không
mang điện tích có thể khuếch tán đến bề mặt điện cực mang điện tích
âm. Ngược lại, mR—tương đương với quá trình oxy hóa—sẽ cực kỳ nhỏ vì
Thiết bị đo. Nhiệt độ bề mặt điện cực, khi được nhúng trong ngọn lửa, được đo
mảnh bị khử và do đó mang điện tích âm sẽ bị đẩy tĩnh điện bởi bề mặt
bằng nhiệt kế hồng ngoại (800–3000 K) model M9100 do công ty Mikron
điện cực phân cực âm. Mức độ đẩy có thể được tính toán. Một chất mang
instrument Company Inc. (Mỹ) cung cấp, được hiệu chuẩn theo tiêu chuẩn có thể
điện tích đơn sẽ chịu một điện trường khoảng 50.000 V m 1 khi hiệu
truy vết. Điện thế kế tuần hoàn được ghi lại bằng máy đo điện thế (Autolab
PGSTAT 100, Eco Chemie BV do Windsor Scientific Ltd., Anh cung cấp) với điện áp
điện thế 5 V được đặt vào lớp vỏ plasma. Điều này sẽ dẫn đến gia tốc
giới hạn 100 V; chỉ có lần quét đầu tiên của điện thế kế tuần hoàn được trình
2 × 1011 m s 2 ra xa bề mặt điện cực.
bày và được gọi là 'điện thế kế'.
Các phép đo phổ khối lượng được thực hiện bằng máy HPR-60 MBMS (Hiden, Anh),
một thiết bị chuyên dụng để phân tích plasma khí quyển. Các phép đo Raman
được thực hiện bằng kính hiển vi Raman inVia (Renishaw, Anh) với đầu dò
sợi quang, được tập trung vào bề mặt điện cực làm việc (xem Hình bổ sung 3). Thảo luận
Chúng tôi trình bày một phương pháp có khả năng phân biệt nhiều loại hợp chất
hữu cơ khác nhau, đạt được bằng cách sử dụng môi trường plasma khí được khảo
Lắp ráp và quy trình điện cực. Điện cực tham chiếu được chế tạo bằng cách nghiền
sát bằng điện hóa. Bằng cách kết hợp phép đo phổ khối lượng và pha tạp với
kỹ zirconia ổn định bằng yttria với một lượng nhỏ ethanol để tạo thành hỗn hợp
đồng nhất, sau đó được nhồi vào đầu ống alumina tái kết tinh (đường kính ngoài
một số ít các chất được lựa chọn cẩn thận, chúng tôi đã thành công trong việc
2,75 mm, đường kính trong 1,6 mm, Dynamic Ceramic, Anh) với độ sâu 3,0 mm, tiếp
gán các tín hiệu điện hóa cho các sản phẩm phân mảnh của tám axit amin khác
xúc với dây vonfram (đường kính 1 mm, Goodfellow, Anh) để kết nối điện. Cụm điện
nhau. Chúng tôi suy luận rằng một số nhóm hữu cơ tạo ra các gốc tự do trong
cực đối và điện cực làm việc được đặt cách đỉnh đầu đốt 10,0 mm. Vỏ hình trụ bằng
ngọn lửa, có thể được khử bằng điện hóa và phân giải theo điện thế áp dụng.
thép không gỉ có một đĩa bạch kim đường kính 25,0 mm, dày 2,0 mm được giữ
Chúng tôi trình bày những hiểu biết mới về sự gắn kết electron điện hóa trong
cố định ở đáy vỏ. Đĩa bạch kim có một lỗ đường kính 3,0 mm ở tâm để chứa điện cực
làm việc (xem Chú thích bổ sung 3).
plasma và trình bày điện hóa pha khí thực sự của các hợp chất hữu cơ.
Toàn bộ cụm thiết bị được đặt phía trên ngọn lửa, với lỗ chứa điện cực làm việc
nằm chính xác trên đường đi của phần bên phải ngọn lửa. Một thanh vàng hoặc than
Sự khác biệt căn bản này so với điện hóa học pha lỏng thông thường
chì nhiệt phân (Goodfellow Ltd., Anh) đường kính 2,4 mm được sử dụng làm điện cực
làm việc, được kẹp trong một giá đỡ bằng gốm (Macor®) và được đặt chính xác trong
cho phép đo các sự kiện gắn electron trong pha khí, vốn thường bị hạn
một lỗ 3,0 mm trên điện cực đối bằng lá bạch kim. Khi ở trong ngọn lửa, nhiệt độ
chế ở các kỹ thuật như quang phổ chùm electron hoặc quang phổ quang
bề mặt điện cực làm việc là 1236 ± 15 K. Các đường cong điện thế-dòng điện được
điện tử17. Có lẽ không có gì đáng ngạc nhiên khi có những khác biệt
ghi lại sau khi các điện cực được đặt trong ngọn lửa trong 30 giây, quét từ 0
đáng kể so với các quá trình chuyển electron tương tự trong các pha
đến -10 V với tốc độ 1 V s 1, đây là tốc độ quét tối ưu cho môi trường này như đã
báo cáo trong Tài liệu tham khảo 11. Ba lần quét liên tiếp đã được ghi lại; lần
ngưng tụ. Những khác biệt này mở ra những hướng nghiên cứu lý thuyết
quét thứ hai được trình bày. Một điện cực tham chiếu mới được sử dụng cho mỗi
đầy hứa hẹn để phát triển sự hiểu biết ở cấp độ cơ học lượng tử về sự
loạt đường cong điện thế-dòng điện. Sai số trên các điện thế được trích dẫn được chuyển electron.
tính toán dựa trên sự thay đổi độ ổn định của đỉnh khi lặp lại chu kỳ, số chu kỳ tối thiểu là 6. 5
HÓA HỌC TRUYỀN THÔNG | (2018) 1:48 | DOI: 10.1038/s42004-018-0046-7 | www.nature.com/commschem Machine Translated by Google BÀI BÁO
HÓA HỌC TRUYỀN THÔNG | DOI: 10.1038/s42004-018-0046-7
Tính sẵn có của dữ liệu. Tất cả dữ liệu được tạo ra trong nghiên cứu hiện tại đều có sẵn từ
23. Gao, YX và cộng sự. Nghiên cứu cơ chế về sự biến đổi giao diện của carbon
tác giả liên hệ khi có yêu cầu hợp lý.
điện cực dưới quá trình oxy hóa điện hóa. J. Electroanal. Chem. 783, 90–99 (2016).
24. Gerischer, H. Những tiến bộ trong điện hóa học và điện hóa học
Ngày nhận bài: 19 tháng 4 năm 2018 Ngày chấp nhận đăng bài: 17 tháng 7 năm 2018
Kỹ thuật. Tập 1 (do Delahay, D. biên tập) 139–232 (Interscience, New York, 1961).
25. Girault, HH, Điện hóa học phân tích và vật lý, ấn bản thứ nhất, trang 375 (EPFL) (Nhà xuất bản, 2004).
26. Richmonds, C. và cộng sự. Phản ứng chuyển electron tại giao diện plasma-chất lỏng.
J. Am. Chem. Soc. 133, 17582–17585 (2011).
27. King, IR & Calcote, HF Ảnh hưởng của kích thước đầu dò đến phép đo nồng độ ion Tài liệu tham
trong ngọn lửa. J. Chem. Phys. 23, 2203–2204 (1955).
khảo 1. Rumbach, P., Bartels, DM, Sankaran, RM & Go, DB Sự hòa tan của
28. Maclatchy, CS & Smith, HCL Dòng điện electron đến đầu dò Langmuir trong plasma áp suất
electron bởi plasma áp suất khí quyển. Nat. Commun. 6, 7248 (2015).
cao đang chảy. IEEE Trans. Plasma Sci. 19, 1254–1258 (1991).
2. Caruana, DJ & Holt, KB Điện hóa học thiên văn: vai trò của các phản ứng oxy hóa khử trong
hóa học bụi vũ trụ. Phys. Chem. Chem. Phys. 12, 3072–3079 (2010).
29. Axford, SDT, Goodings, JM & Hayhurst, AN Phổ khối lượng
3. Bard, AJ & Faulkner, LR Phương pháp điện hóa: Nguyên lý cơ bản và
Lấy mẫu ion từ ngọn lửa ở áp suất khí quyển: tác động của điện trường đặt vào và sự
Ứng dụng, ấn bản thứ 2, trang 123 (Wiley, 2000).
thay đổi điện thế trong ngọn lửa. Combust. Flame 114, 294–302 (1998).
4. Ghoroghchian, J. và cộng sự. Điện hóa học trong pha khí—sử dụng
Điện cực siêu nhỏ dùng để phân tích các chất có hoạt tính điện hóa trong hỗn hợp khí.
Anal. Chem. 58, 2278–2282 (1986).
5. Vijh, AK Điện thế điện cực và plasmon giao diện trong vùng giao pha giữa kim loại và
Lời cảm ơn Các tác giả xin chân
chất điện phân khí (tức là plasma). Mater. Chem. Phys. 14, 47–56 (1986).
thành cảm ơn EPSRC (EP/H049398/1) đã hỗ trợ tài chính. AE và MC xin cảm ơn EPSRC đã cấp học bổng. Chúng tôi
xin cảm ơn Giáo sư Stefan Howorka (UCL) đã hỗ trợ chuẩn bị bản thảo và Tiến sĩ Jonathan Burns đã giúp đỡ
6. Vennekamp, M. & Janek, J. Điện hóa plasma trong tần số vô tuyến
trong việc chuẩn bị Hình 1. Nguồn tài trợ từ chương trình năng lực cốt lõi của EPSRC dành cho nghiên cứu
phóng điện - quá trình oxy hóa bạc trong plasma clo. Tạp chí Điện hóa học. 150, C723–
Hóa học (EP/K03930X/1) đã được sử dụng để mua máy quang phổ khối Hiden HPR-60 MBMS. C729 (2003).
7. Ogumi, Z., Uchimoto, Y. & Takehara, Z. Điện hóa sử dụng plasma. Khuyến cáo.
Tôi xin cảm ơn J. Stevenson vì chuyên môn kỹ thuật của ông trong việc chế tạo cụm điện cực và cụm Mater. 7, 323–325 (1995). thiết bị lấy mẫu MS.
8. Hickling, A. & Ingram, MD Điện phân phóng điện tiếp xúc.
Giao dịch của Hội Faraday 60, 783–793 (1964).
Đóng góp của các tác giả:
9. Caruana, DJ & McCormack, SP Điện hóa học trong ngọn lửa: một thông báo sơ bộ. Electrochem. Ý tưởng cho thí nghiệm này do DJC đề xuất. Việc phát triển phương pháp do Commun. 2, 816–821 (2000).
DJC, AE và MC thực hiện, và dữ liệu điện hóa được thu thập bởi AE.
10. Elahi, A., Fowowe, T. & Caruana, DJ. Điện hóa động trong chất điện phân plasma ngọn
MC đã thu thập dữ liệu Raman và MS. DJC đã viết bài báo, còn MC và AE đóng góp vào bản thảo.
lửa. Angew. Chem. Int Ed. Engl. 51, 6350–6355 (2012).
11. Elahi, A. & Caruana, DJ Điện hóa plasma: phép đo điện thế trong chất điện phân plasma
ngọn lửa. Phys. Chem. Chem. Phys. 15, 1108–1114 (2013).
12. Frenklach, M., Wang, H. & Rabinowitz, MJ Tối ưu hóa và phân tích các cơ chế động học
Thông tin bổ sung Thông tin bổ sung kèm theo
hóa học lớn bằng phương pháp lập bản đồ giải pháp - Đốt cháy Methane. Tiến bộ.
bài báo này tại https://doi.org/10.1038/s42004-018-0046-7 .
Khoa học năng lượng và đốt cháy. 18, 47–73 (1992).
13. Fowowe, T., Hadzifejzovic, E., Hu, J., Foord, JS & Caruana, DJ Điện hóa plasma: phát
triển vật liệu điện cực tham chiếu cho plasma nhiệt độ cao. Adv. Mater. 24, 6305–
Xung đột lợi ích: Các tác giả tuyên bố không có xung đột lợi ích. 6309 (2012).
14. Christensen, M. & Konnov, AA Tốc độ cháy tầng của ngọn lửa axit axetic cộng với không
Thông tin về bản in lại và quyền sử dụng có sẵn trực tuyến tại http://npg.nature.com/
khí. Combust. Flame 170, 12–29 (2016). reprintsandpermissions/
15. Gallois, N., Templier, J. & Derenne, S. Phân tích nhiệt phân-sắc ký khí-khối phổ của
20 axit amin protein khi có mặt TMAH. J. Anal.
Ghi chú của nhà xuất bản: Springer Nature giữ lập trường trung lập đối với các tuyên bố về thẩm quyền pháp
Ứng dụng Nhiệt phân 80, 216–230 (2007).
lý trong các bản đồ đã xuất bản và các liên kết tổ chức.
16. Chiavari, G. & Galletti, GC Pyrolysis-gas chromatography/mass
Quang phổ của axit amin. J. Anal. Appl. Pyrolysis 24, 123–137 (1992).
17. Rienstra-Kiracofe, JC, Tschumper, GS, Schaefer, HF, Nandi, S. & Ellison, GB
Ái lực electron nguyên tử và phân tử: thí nghiệm quang điện tử và tính toán lý thuyết.
Bài viết này được cấp phép theo Giấy phép Quốc tế Creative Commons Ghi công 4.0, cho
Chem. Rev. 102, 231–282 (2002).
phép sử dụng, chia sẻ, điều chỉnh, phân phối và sao chép trên mọi phương tiện hoặc định
18. Sarathy, SM, Osswald, P., Hansen, N. & Kohse-Hoinghaus, K. Hóa học đốt cháy rượu.
dạng, miễn là bạn ghi rõ nguồn gốc tác giả và nguồn, cung cấp liên kết đến giấy phép Creative Commons và
Tiến bộ. Khoa học đốt cháy năng lượng. 44, 40–102 (2014).
cho biết nếu có bất kỳ thay đổi nào được thực hiện. Hình ảnh hoặc các tài liệu của bên thứ ba khác trong
19. Aranda, V. và cộng sự. Nghiên cứu thực nghiệm và mô hình động học về sự bắt lửa
bài viết này được bao gồm trong giấy phép Creative Commons của bài viết, trừ khi có ghi chú khác trong dòng
và oxy hóa metanol ở áp suất cao. Tạp chí quốc tế về Hóa học và Động học 45, 283–
ghi công cho tài liệu đó. Nếu tài liệu không được bao gồm trong giấy phép Creative Commons của bài viết và 294 (2013).
mục đích sử dụng của bạn không được phép theo quy định pháp luật hoặc vượt quá phạm vi sử dụng cho phép,
20. Skreiberg, O., Kilpinen, P. & Glarborg, P. Hóa học amoniac dưới 1400 K trong điều kiện
bạn cần phải xin phép trực tiếp từ chủ sở hữu bản quyền. Để xem bản sao của giấy phép này, hãy truy cập
giàu nhiên liệu trong lò phản ứng dòng chảy. Combust. Flame 136, 501–518 (2004).
http://creativecommons.org/licenses/by/4.0/ .
21. Mendiara, T. & Glarborg, P. Hóa học amoniac trong quá trình đốt nhiên liệu oxy của
metan. Đốt cháy. Ngọn lửa 156, 1937–1949 (2009).
22. Ferrari, Quang phổ Raman AC của graphene và graphite: rối loạn, ghép nối electron-
phonon, pha tạp và hiệu ứng không thuận nghịch. Solid State Commun. 143, 47–57
© Bản quyền thuộc về tác giả(các tác giả) năm 2018 (2007). 6
HÓA HỌC TRUYỀN THÔNG | (2018) 1:48 | DOI: 10.1038/s42004-018-0046-7 | www.nature.com/commschem




