












Preview text:
lOMoAR cPSD| 45148588 THỰC HÀNH HÓA SINH
BÀI 1: HÓA HỌC GLUCID VÀ LIPID
1. Phản ứng Fehling -> để xác định tính khử của phản ứng Fehling 1.1. Cơ chế phản ứng
Trong môi trường kiềm và nhiệt độ sôi, các monosaccarid khử hydroxyd đồng II thành hydroxyd đồng I.
Hydroxyd đồng I bị mất nước tạo thành oxyd đồng I kết tủa đỏ gạch. Kiềm
R-CHO + 2 Cu(OH)2 R-COOH + 2 CuOH + 2 H2O o T sôi 2 CuOH Cu2O (đỏ gạch) H2O
1.2. Thuốc thử trong phản ứng này là gì? Thuốc thử Fehling1.3. Cách tiến hành phản ứng Ống nghiệm 1 2 3 Thuốc thử Fehling (A+B) 1 1 1
Dung dịch glucose 1% (giọt) 10
Dung dịch fructose 1% (giọt) 10 Nước cất (giọt) 10
1.4. Kết quả và kết luận của phản ứng -
Kết quả: Cả 2 ống nghiệm đều có kết tủa đỏ gạch -
Giải thích: MS có 2 loại là aldose (glucose) có nhóm chức khử -CHO và cetose (fructose) có nhóm chức khử
-CO nên tất cả chúng đều có tính khử. -
Kết luận: Tất cả các MS đều có tính khử 1.5. Ứng dụng của phản ứng này
Định lượng sơ bộ đường trong nước tiểu
2. Tác dụng của iot với tinh bột và glycogen -> để xác định tính bắt màu của tinh bột và glycogen 2.1. Cơ chế phản ứng
Dựa vào tính chất của iot tác dụng với tinh bột cho màu xanh tím, với glycogen cho màu đỏ nâu để phát
hiện tinh bột và glycogen
2.2. Tại sao có sự khác biệt màu khi tinh bột và glycogen phản ứng với iot? -
Glycogen có nhiều nhánh hơn, nhưng mỗi nhánh ngắn hơn (8-12 nhánh) còn tinh bột có ít nhánh hơn nhưng
mỗi nhánh lại dài hơn (24-30 nhánh)
2.3. Sự giống và khác nhau giữa tinh bột và glycogen? Tinh bột Glycogen Giống nhau
- Đều là polysaccarid thuần - Đơn phân: -D-glucose
- Đều có liên kết: 1,4-osid; 1,6-osid Khác nhau
Số lượng nhánh ít hơn, chiều dài nhánh dài Số lượng nhánh nhiều hơn, chiều dài hơn (24-30 gốc)
nhánh ngắn hơn (8-12 gốc)
2.4. Cách tiến hành thí nghiệm Lỗ 1 Lỗ 2 Lỗ 3 Hồ tinh bột 1% (giọt) 1 lOMoAR cPSD| 45148588 Glycogen 1 Nước cất 1 Iot 1 1 1
2.5. Kết quả, kết luận của thí nghiệm này là gì? -
Kết quả: lỗ 1 chuyển sang màu xanh tím, lỗ 2 chuyển sang màu đỏ nâu -
Giải thích: do tb và glycogen có sự khác biệt về số lượng nhánh (glycogen có nhiều nhánh hơn) và chiều dài
nhánh (tb có mỗi nhánh dài hơn) nên có sự khác biệt về màu sắc - Kết luận:
+ Tinh bột + iot ra màu xanh tím, glycogen + iot ra màu đỏ nâu
+ Đây là tính chất vật lí, không phải tính chất hóa học (TB và glycogen chỉ hấp phụ iot trên bề mặt của chúng)
+ Sự khác biệt là do số lượng nhánh và chiều dài nhánh quy định: Glycogen có nhiều nhánh hơn, nhưng
mỗi nhánh ngắn hơn (8-12 nhánh) còn tinh bột có ít nhánh hơn nhưng mỗi nhánh lại dài hơn (24- 30 nhánh)
2.6. Ứng dụng của phản ứng này -
Dùng để phát hiện sản phẩm thủy phân tinh bột -
Xác định tinh bột còn sót lại trong VSATTP
3. Nhũ tương hóa lipid -> minh họa tính tan và sự tạo nhũ tương lipid (dung môi không phân cực) 3.1. Cơ chế phản ứng
Lipid không tan trong nước, khi lắc mạnh với nước sẽ tạo thành nhũ tương không bền. Nếu thêm các chất
nhũ hóa như Na2CO3, protein, xà phòng, muối mật thì lipid sẽ tạo thành nhũ tương bền. Lipid tan trong dung
môi hữu cơ như ete, cloroform
3.2. Nhũ tương là gì? Khi cho 2 dung dịch không tan vào nhau, tạo thành những giọt mắt thường có thể nhìnthấy 3.3. Cách tiến hành Ống nghiệm 1 2 3 Thuốc thử Nước cất (ml) 1 Na2CO3 1% (ml) 1 Ete (ml) 1 Dầu lạc (giọt) 2 2 2 Quan sát: -
Trước khi lắc -> tan hay không tan -
Trong khi lắc -> nhũ tương hóa -
Sau khi lắc 1p -> xem NT bền hay không
3.4. Kết quả, kết luận và giải thích của hiện tượng nhũ tương bền, nhũ tương không bền và tan hoàn toàn- Kết quả:
+ Ống 1: Nhũ tương không bền + Ống 2: Nhũ tương bền + Ống 3: Tan hoàn toàn - Giải thích
+ Ống 1: Nước là dung môi phân cực, lipid là dung môi không phân cực => chúng không tan vào nhau + Ống 2: Có Na+ và CO -
3 của Na2CO3 là ion ưa nước, xung quanh giọt lipid của ion ưa nước nên giọt
lipid không thể đẩy nước ra xa, nên giọt lipid không thể trở lại trạng thái ban đầu
+ Ống 3: Ete là dung môi hữu cơ, lipid tan trong dung môi hữu cơ, nên lipid tan trong ete hoàn toàn
3.5. Ứng dụng của hiện tượng nhũ tương -
Dùng xà phòng rửa trôi lipid lOMoAR cPSD| 45148588 -
Tiêu hóa lipid trong ruột non: muối mật nhũ tương hóa hạt lipid (tách hạt lớn thành nhiều hạt nhỏ) để enzym lipase thoái hóa lipid -
Tách chiết lipid ra khỏi nhiều chất
BÀI 2: HÓA HỌC ACID AMIN VÀ PROTEIN
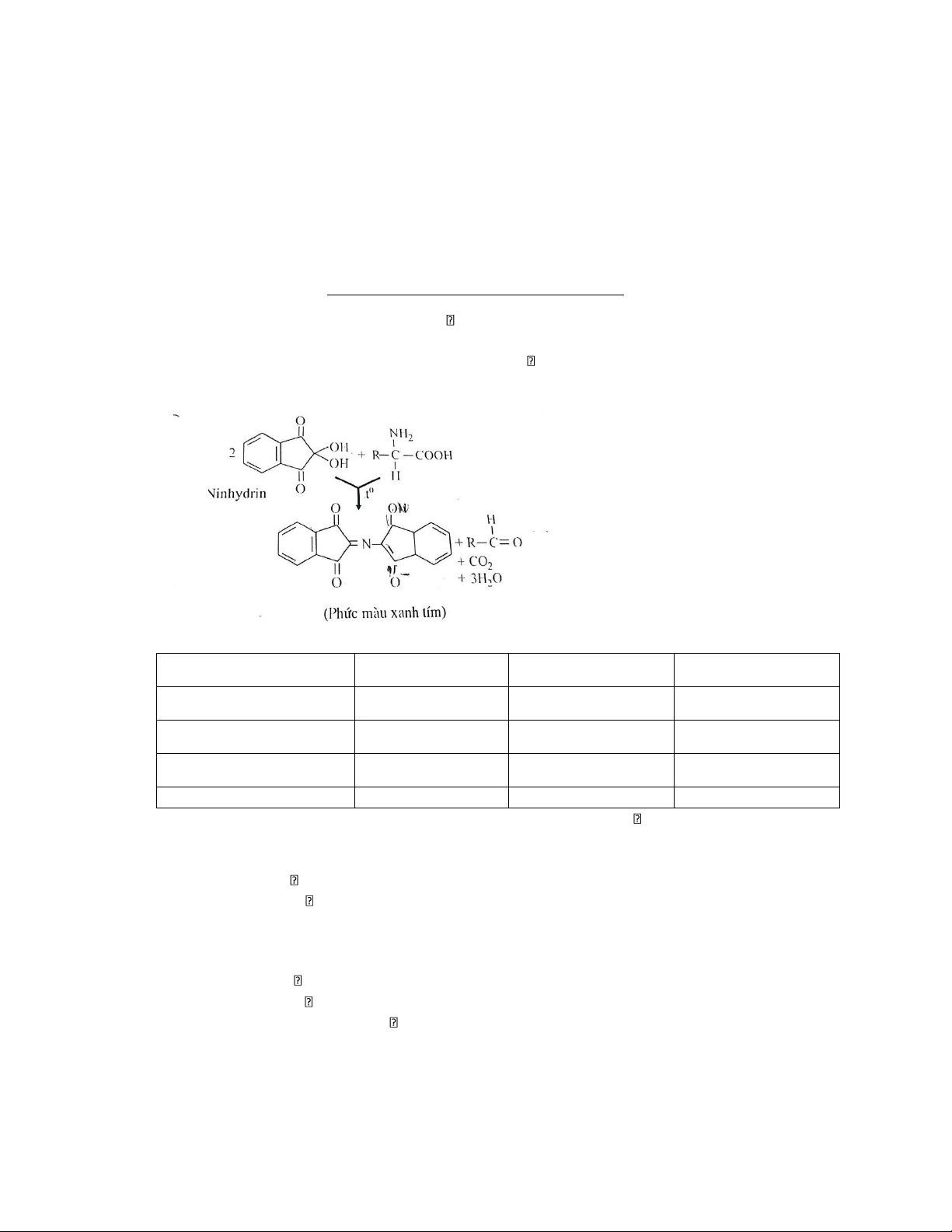
1. Phản ứng Ninhydrin -> xác định các axid amin 1.1. Cơ chế phản ứng
Dưới tác dụng của nhiệt độ và ninhydrin, các acid amin sẽ khử amin oxy hóa và khử carboxyl tạo thành
NH3, CO2 và aldehyd kém 1 carbon so với acid amin ban đầu. Còn ninhydrin sẽ bị khử thành hydrindantin.
Sau đó có sự ngưng tụ giữa hydrindantin với NH3 và ninhydrin tạo thành phức hợp có màu xanh tím
1.2. Cách tiến hành thí nghiệm 1 2 3 Glycin 1% 1 Cystein 1% 1
Protein lòng trắng trứng (ml) 1 Ninhydrin 0,1% (giọt) 5 5 5
1.3. Trong dung dịch pr lòng trắng trứng có gì? Albumin, Globulin, axid amin tự do, chất vô cơ
1.4. Kết quả, kết luận, giải thích -
Kết quả: cả 3 ống đều cho màu xanh tím -
Kết luận: axit amin tham gia phản ứng với ninhydrin cho màu xanh tím -
Giải thích: axid amin sẽ khử amin oxy hóa và khử carbon tạo thành NH3, CO2 và aldehyd, ninhydrin bị
khử thành hydrindantin, sự ngưng tụ giữa hydrindantin với NH3 và ninhydrin tạo thành phức có màu xanh tím
1.5. Ứng dụng của phản ứng ninhydrin là gì? - Nhận biết axit amin -
Định lượng axit amin trong 1 mẫu nhất định trong nghiên cứu -
Trong sắc kí để phân tích axit amin và nhận biết prolin trong hỗn hợp axit amin
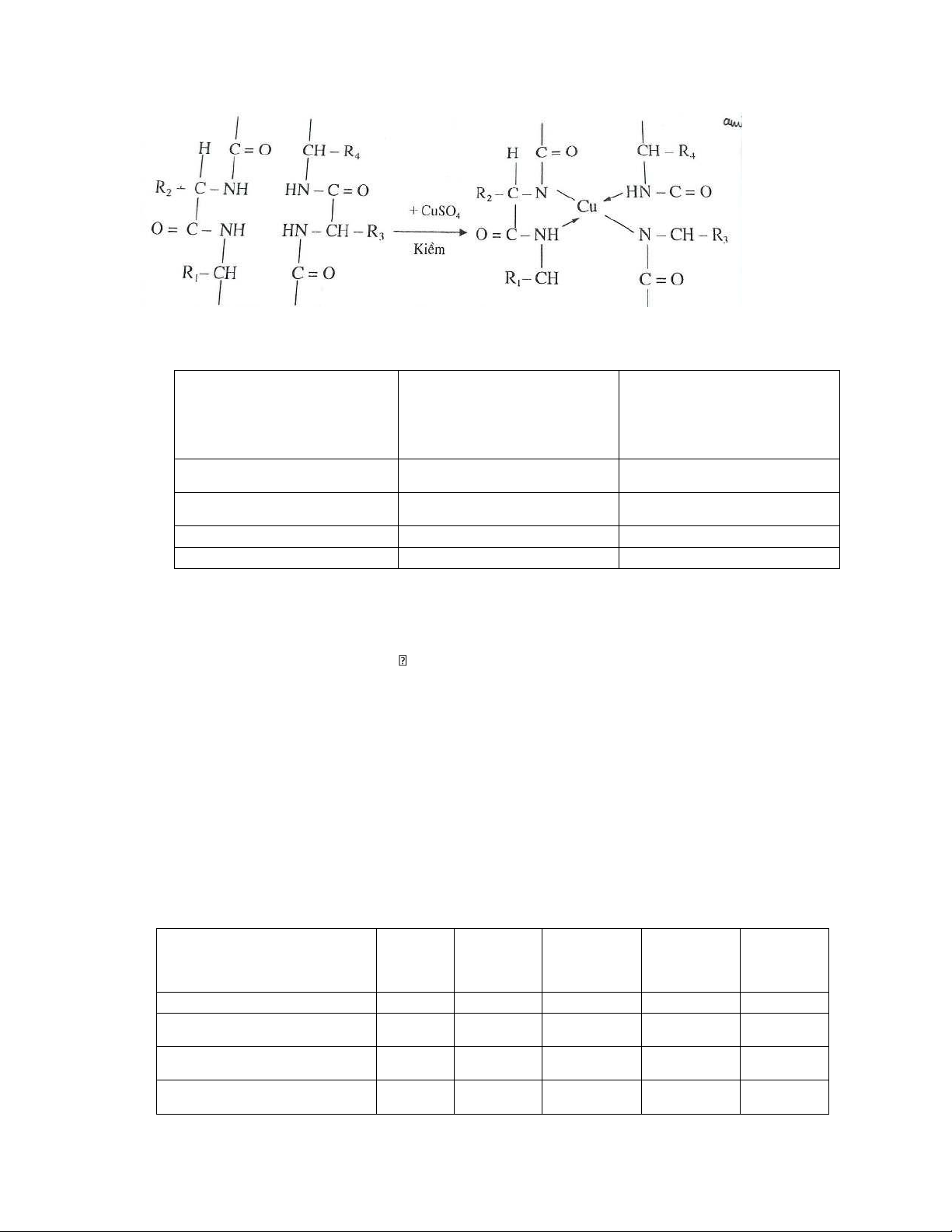
2. Phản ứng Biure -> xác định có liên kết peptid hay không 2.1. Cơ chế phản ứng
Trong môi trường kiềm, các liên kết peptit trong phân tử protein sẽ kết hợp với ion Cu2+ tạo phức hợp màu tím.
Đậm độ của màu tỉ lệ thuận với nồng độ protein lOMoAR cPSD| 45148588
Thường cứ 4 liên kết peptid và 1 ion Cu2+ cho 1 phức hợp biure. Phản ứng này tạo phức màu bền, ổn định, được
dùng để định lượng protein 2.2. Cách tiến hành Ống nghiệm 1 2 Thuốc thử
Protein lòng trắng trứng (ml) 0,5 Glycin 1% 0,5 NaOH 10% (giọt) 5 5 CuSO4 1% (giọt) 2 2
2.3. Kết quả, kết luận và giải thích -
Kết quả: ống 1 có màu tím hồng, ống 2 không xuất hiện màu tím hồng - Giải thích:
+ Ống 1 có pr lòng trắng trứng có albumin có liên kết peptid nên cho phản ứng biure tạo thành phức màu tím hồng
+ Ống 2 có glycin là axid amin không chứa liên kết peptid nên không cho phản ứng màu biure nên
không tạo phức có màu tím hồng -
Kết luận: các liên kết peptid sẽ kết hợp với Cu2+ tạo thành phức màu tím hồng 2.4. Ứng dụng của phản ứng Biure -
Định tính, định lượng pr trong huyết thanh, dịch sinh học,... (đậm độ pr tỉ lệ thuận với nồng độ pr trong huyết thanh...)
3. Tủa pr bởi nhiệt độ 3.1. Cơ chế phản ứng
Khi đun sôi, các tiểu phân pr bị mất lớp áo nước, nếu các tiểu phân này bị trung hòa điện tích bằng NaCl
hoặc đưa pH của dung dịch về gần pH của pr, thì pr sẽ bị tủa
3.2. Pr đã thẩm tích là gì? Tại sao phải dùng pr đã thẩm tích? -
Pr đã thẩm tích là pr đã được lọc qua màng thẩm tích, giữ lại những phân tử có trọng lượng lớn -
Nếu dùng pr chưa thẩm tích, muối vẫn còn trong dung dịch pr (muối có tác dụng như NaCl bão hòa), nên
nếu dùng pr chưa thẩm tích để dùng làm TN thì đun sôi đã kết tủa 3.3. Cách tiến hành của thí nghiệm Ống nghiệm 1 2 3 4 5 Thuốc thử Pr đã thẩm tích (ml) 1 1 1 1 1 Acid axetic 1% (ml) 2 5 5
Dung dịch NaCl bão hòa (giọt) 2 Dung dịch NaOH 10% (giọt) 5 lOMoAR cPSD| 45148588
3.4. Kết quả, kết luận, giải thích của thí nghiệm -
Kết quả, giải thích: pr chỉ kết tủa khi đồng thời mất 2 yếu tố: lớp áo nước và khả năng tích điện của tiểu phân pr ON 1 2 3 4 5 Yếu tố Lớp áo nước Mất Mất Mất Mất Mất
Tích điện cùng dấu pHmt>pHi pHmt pHi => pHmt pr pHmt pHi => pHmt>pHi (khi pH=4,66)
=> pr tích điện (-) cùng dấu, tích điện cùng dấu, => pr tích điện (-)
nên pr không mất mất tích điện (+) nên pr mất tích điện nên pr không mất điện không mất điện điện Kết quả
Mất 1 yếu tố -> Mất 2 yếu tố -> Mất 1 yếu tố -> Mất 2 yếu tố -> Mất 1 yếu tố -> không kết tủa kết tủa không kết tủa kết tủa không kết tủa - Kết luận: 3.5. Ứng dụng -
Bảo quản những chất có bản chất là pr -
Khử trùng pr bằng cách hấp, sấy -
Tìm pr trong những chế phẩm sinh học BÀI 3: HÓA SINH ENZYME
1. Thủy phân tinh bột bằng amylaze 1.1. Cơ chế phản ứng
Amylaze là enzyme thủy phân tham gia thủy phân liên kết glucosid
Amylaze xúc tác phản ứng thủy phân tinh bột thành maltose qua sản phẩm trung gian là dextrin. Dextrin có
nhiều loại, các loại này có màu sắc khác nhau khi tác dụng với iot
Trong cơ thể người, amylaze được sản xuất từ tuyến nước bọt và tuyến tụy. Những tuyến này cũng đồng
thời sản xuất enzym maltase có tác dụng thủy phân maltose thành glucose
2. Tính đặc hiệu của enzyme 2.1. Cơ chế phản ứng
Enzyme có tính đặc hiệu với cơ chất và kiểu phản ứng
Theo dõi tác dụng của enzyme amylaze với 2 cơ chất là tinh bột và saccarose. Trên cơ sở đó xác định tính đặc hiệu của enzyme
2.2. Cách tiến hành của thí nghiệm lOMoAR cPSD| 45148588
Thủy phân 2 cơ chất bởi enzyme amylaze ON 1 2 Thuốc thử Nước bọt 1/20 (ml) 0,5 0,5 Hồ tinh bột 1% (ml) 1 Saccarose 1% (ml) 1
Lắc đều, để ở nhiệt độ phòng trong 10p. Lấy dịch thủy phân làm phản ứng 2 Làm phản ứng Fehling ON 1 2 Thuốc thử Dịch thủy phân HTB (ml) 0,5 Dịch thủy phân saccarose 0,5 Fehling A+B (ml) 1 1
2.3. Kết quả, giải thích và kết luận -
Kết quả: dịch thủy phân HTB có kết tủa đỏ gạch, dịch thủy phân saccarose không có kết tủa đỏ gạch - Giải thích:
+ ON1: có kết tủa đỏ gạch là do tb bị thủy phân thành maltose có tính khử phản ứng với Fehling tạo kết
tủa đỏ gạch, HTB không tạo được kết tủa đỏ gạch với Fehling => amylase thủy phân được HTB thành maltose
+ ON2: không có kết tủa đỏ gạch chứng tỏ saccarose không bị thủy phân thành glucose và fructose có
tính khử tạo kết tủa đỏ gạch với Fehling => amylase không thủy phân được saccarose thành glu và fruc -
Kết luận: amylase đặc hiệu với hồ TB mà không đặc hiệu với saccarose
Làm ống trắng, ống mẫu, ống thử để làm gì? -
Làm ống trắng để đo mật độ quang của thuốc thử lên màu -
Làm ống mẫu để tìm hệ số tỷ lệ -
Làm ống thử để lên màu đặc trưng chất cần ĐL trong huyết tương tác dụng với thuốc thử
Huyết thanh khác gì với huyết tương? lOMoAR cPSD| 45148588
Khi máu không có TB máu trở thành huyết tương, khi huyết tương không có yếu tố đông máu trở thành huyết thanh
Định lượng glucose, cho, tri, pr, al, acid uric huyết thanh bằng phương pháp nào? -
Phương pháp đo quang phổ hấp thụ (pp lên màu) -
Cách bước tiến hành chung (bonus để nhớ cách tiến hành)
B1: lên màu: làm 3 ống: ống thử, ống mẫu, ống trắng -> lên màu đặc trưng. Đậm độ màu tỷ lệ thuận với
nồng độ ... trong huyết thanh
B2: Dựa vào mật độ quang đo được ở bước sóng ở bước sóng 540nm hoặc 600nm để xác định nồng
độ ... trong huyết thanh
BÀI 4: ĐỊNH LƯỢNG GLUCOSE, CHOLESTEROL, TRIGLYCERID HUYẾT THANH
1. Định lượng glucose huyết thanh 1.1. Cơ chế phản ứng
Glucose trong mẫu thử được xác định theo các phản ứng sau
Phản ứng tạo phức màu hồng cánh sen. Đậm độ màu tỷ lệ thuận với nồng độ glucose trong huyết thanh. Dựa
vào mật độ quang (MĐQ) đo được ở bước sóng 540nm để xác định nồng độ glucose 1.2. Cách tiến hành Trắng Mẫu Thử Dd thuốc thử lên màu 1 1 1 (ml) Nước cất (µl) 20 Dd glucose mẫu 5,56 20 mmol/l (µl)
Huyết tương hoặc huyết 20 thanh bênh nhân (µl)
1.3. Cách tính kết quả, Kết quả, kết luận, giải thích -
Nồng độ glucose máu được tính theo công thức: Glucose (mmol/l) = Ethử/ Emẫu * 5,56
1.4. Cho 1 giá trị. Biện luận: Giá trị bình thường hay bất thường? Bình thường thì duy trì bằng cách nào? Bất
thường trong bệnh lí nào, có ý nghĩa gì? -
Giá trị glucose máu bình thường 3,9-6,68 mmol/l -
Glucose được duy trì bình thường do
+ Thận THT 100% với đk <10 mmol/l
+ HM: insulin làm giảm đường máu trong khi glucagon, T3, T4 (tuyến giáp), cortisol (VTT), adrenalin
(TTT), ACTH, TSH (tuyến yên)
+ TK: khi căng thẳng, stress thì tăng tiết cortisol, adrenalin
+ Gan: xa bữa ăn gan tăng phân giải glycogen thành glucose trong khi sau ăn gan, lượng đường trong
máu thường tăng -> tăng chuyển glucose thành glycogen
Giá trị glucose bất thường - Tăng (>6,68 mmol/l):
+ Do tụy: ĐTĐ tụy (do đề kháng insulin hoặc giảm tiết insulin của tụy)
+ Do cường tuyến giáp, tuyến yên, VTT, TTT, u tuyến yên - Giảm: lOMoAR cPSD| 45148588
+ Do thận: ĐTĐ thận (ngưỡng THT của thận giảm)
+ Do gan: chức năng gan giảm (xơ gan, viêm gan,…) -> giảm chuyển glucose thành glycogen -> G máu tăng - Ý nghĩa:
+ Chuẩn đoán ĐTĐ tụy khi G máu >= 7mmol/l
+ Khi bệnh nhân có biểu hiện của ĐTĐ: ăn nhiều, uống nhiều, đái nhiều, gầy,… kết hợp XN G máu để xác định
2. Định lượng cholesterol huyết thanh 2.1. Cơ chế phản ứng
Cholesterol tác dụng với thuốc thử tạo phức hợp có màu hồng.
Đậm độ màu hồng tỷ lệ thuận với nồng độ cholesterol. Đo mày trên máy quang kế, từ đó tính được nồng độ cholesterol
2.2. Định lượng cholesterol huyết thanh là cholesterol nào? Cholesterol trong huyết thanh là những cholesterol
nào? Bản chất của các cholesterol trong huyết thanh. Cholesterol este do cơ quan nào sản xuất? - Định lượng
cholesterol huyết thanh là cholesterol toàn phần. -
Cholesterol toàn phần = Cholesterol tự do + Cholesterol este -
Bản chất của cholesterol tự do là ancol vòng, của cholesterol este là lipid -
Cholesterol este do gan sản xuất 2.3. Cách tiến hành Trắng Mẫu Thử Dd thuốc thử lên màu 1 1 1 (ml) Nước cất (µl) 20 Dd cholesterol mẫu 5,2 20 mmol/l (µl) Huyết tương hoặc 20 huyết thanh bênh nhân (µl)
Lắc đều, để ở nhiệt độ phòng 10p
2.4. Cách tính kết quả, Kết quả, kết luận, giải thíchCholesterol (mmol/l) = Ethử/ Emẫu * 5,2
2.5. Cho 1 giá trị của cholesterol. Biện luận: Giá trị bình thường hay bất thường? Bình
thường thì duy trì bằng cách nào? Bất thường trong bệnh lí nào, có ý nghĩa gì? -
Cholesterol huyết thanh bình thường khi < 5,2 mmol/l -
3. Định lượng triglycerid huyết thanh 3.1. Cơ chế phản ứng
Triglycerid tác dụng với thuốc thử tạo phức hợp có màu hồng. lOMoAR cPSD| 45148588
Đậm độ màu hồng tỷ lệ thuận với nồng độ triglycerid. Dựa vào mật độ quang (MĐQ) đo được ở bước sóng
540nm để xác định nồng độ triglycerid 3.2. Cách tiến hành Trắng Mẫu Thử Dd thuốc thử lên màu 1 1 1 (ml) Nước cất (µl) 20 Dd triglycerid mẫu 5,2 20 mmol/l (µl) Huyết tương hoặc 20 huyết thanh bênh nhân (µl)
Lắc đều, để ở nhiệt độ phòng 10p 3.3. Cách tính kết quả
Triglycerid (mmol/l) = Ethử/ Emẫu * 2,3 -
3.4. Cho 1 giá trị. Biện luận: Giá trị bình thường hay bất thường? Bình thường thì duy trì bằng cách nào? Bất
thường trong bệnh lí nào, có ý nghĩa gì?
Tổng hợp: ý nghĩa của ĐL cholesterol và triglycerid trong huyết thanh
- Cholesterol và triglycerid là yếu tố nguy cơ của xơ vữa động mạch, dẫn đến tai biến, vỡ mạch, mắc mạch có thể
dẫn đến nhồi máu cơ tim, nhồi máu não, nhồi máu DDM chi, xuất huyết não => ĐL cholesterol và triglycerid để tiên lượng bệnh
BÀI 5: ĐỊNH LƯỢNG PROTEIN, ALBUMIN, ACID URIC HUYẾT THANH
1. Định lượng protein toàn phần huyết thanh 1.1. Cơ chế phản ứng
Protein tác dụng với Cu2+ trong môi trường kiềm tạo thành phức hợp màu tím hồng. Đậm độ màu tím hồng
tỷ lệ với nồng độ protein. Đo màu trên máy quang kế, từ đó tính được nồng độ protein. 1.2. Cách tiến hành Thử Mẫu
Dd thuốc thử lên màu (ml) 1 1 Dd protein mẫu 80 g/l (µl) 20
Huyết tương hoặc huyết thanh (µl) 20 1.3. Cách tính kết quả - Cách tính kết quả lOMoAR cPSD| 45148588
Protein (g/l) = Ethử/ Emẫu * 80
1.4. Giá trị này có bình thường hay không? Bình thường thì duy trì bằng cách nào? Bất thường trong bệnh lí nào?
ĐL protein toàn phần có ý nghĩa không? -
Pr huyết thanh: albumin 65% (được TH 100% ở gan và không qua được màng lọc cầu thận vì nó tích điện
(-)), globulin 38% (qtr globulin đóng vai trò qtr trong miễn dịch, là kháng thể chống KN gây viêm, được
TH ở gan và hệ thống võng nội mô (lách, tủy xương)), fibrinogen 7% -
Protein giảm khi albumin giảm, globulin giảm hoặc cả 2 cùng giảm: - Albumin giảm: Giảm tổng hợp
+ Thiếu nguyên liệu đầu vào: suy dinh dưỡng (suy kiệt), chế độ ăn thiếu protid, rối loạn hấp thu protid,
tăng nhu cầu sử dụng (phụ nữ có thai,…)
+ Giảm khả năng tổng hợp (giảm cn gan): xơ gan, suy gan, … Tăng đào thải:
+ Thận: hội chứng thận hư, viêm cầu thận mạn + Bỏng nặng - Globlulin giảm:
Giảm tổng hợp: xơ gan, suy gan,…
Suy giảm miễn dịch: thiếu hụt miễn dịch nguyên phát, thiếu hụt miễn dịch thứ phát (HIV/AIDS,…) Thận: hội chứng thận hư, … Bỏng nặng -
Cả albumin và globulin cùng giảm:
+ Giảm tổng hợp: bệnh gan (xơ gan, suy gan), suy dinh dưỡng hoặc kém hấp thu, sử dụng thuốc ức chế
miễn dịch hoặc corticoid
+ Tăng đào thải: hội chứng thận hư (mất protein qua thận), mất máu cấp hoặc mạn tính
2. Định lượng albumin huyết thanh
2.1. Vai trò của albumin trong huyết thanh? Albumin do cơ quan nào sản xuất? -
Vai trò quan trọng của pr trong huyết thanh
+ Tạo áp suất keo nhằm tham gia vào quá trình trao đổi nước
+ Albumin có khả năng gắn và vận chuyển một số chất chuyển hóa, ion kim loại, bilirubin, acid béo tự do, hormon,…
+ Cung cấp acid amin cho tổng hợp protein ở mô ngoại vi 2.2. Cơ chế phản ứng
Albumin kết hợp với bromocresol green đệm ở pH=4,2 hình thành 1 phức hợp màu xanh lá cây. Đậm độ
màu tỷ lệ thuận với nồng đọ albumin. Đo màu bằng quang kế ở bước sóng 540nm từ đó suy ra nồng độ của albumin 2.3. Cách tiến hành Trắng Mẫu Thử Dd thuốc thử lên màu 1 1 1 (ml) Nước cất (µl) 20 Dd albumin mẫu 40 g/l 20 (µl) Huyết tương hoặc 20 huyết thanh (µl) 2.4. Cách tính kết quả
Albumin (g/l)= Ethử/ Emẫu * 40
2.5. Bất thường trong bệnh lí nào? ĐL albumin có ý nghĩa không?
Albumin trong huyết thanh giảm: lOMoAR cPSD| 45148588 - Giảm tổng hợp
+ Thiếu nguyên liệu đầu vào: suy dinh dưỡng (suy kiệt), chế độ ăn thiếu protid, rối loạn hấp thu protid,
tăng nhu cầu sử dụng (phụ nữ có thai,…)
+ Giảm khả năng tổng hợp (giảm cn gan): xơ gan, suy gan, … - Tăng đào thải:
+ Thận: hội chứng thận hư, viêm cầu thận mạn + Bỏng nặng
Albumin trong huyết thanh tăng: mất nước, mất máu,… -> cô đặc máu -
ĐL albumin huyết thanh có ý nghĩa:
+ Để đánh giá chức năng gan
+ Chuẩn đoán xác định hội chứng thận hư khi nồng độ albumin <30g/l
3. Định lượng acid uric huyết thanh 3.1. Cơ chế phản ứng
Acid uric tác dụng với thuốc thử tạo phức hợp màu hồng. Các phản ứng ra như sau: 3.2. Cách tiến hành Trắng Mẫu Thử Dd thuốc thử lên màu 1 1 1 (ml) Nước cất (µl) 20 Dd axid uric mẫu 357 20 (µl) Huyết tương hoặc 20 huyết thanh (µl)
3.3. Cách tính kết quả, Kết quả, kết luận, giải thích Uric
(µmol/L) = Ethử/ Emẫu * 357
3.4. Nguồn gốc của acid uric
Acid uric là sản phẩm thoái hóa của các base purin, một thành phần của acid nucleic
3.5. Giá trị này có bình thường hay không? Bình thường thì duy trì bằng cách nào? Bất thường trong bệnh lí nào?
ĐL axit uric có ý nghĩa không? -
Bình thường Bình thường, duy trì bằng cách thải trừ qua nước tiểu (95% lương axit uric đi qua cầu thận được
tái hấp thu ở ống lượng gần và bài xuất tích cực ở ống lượn xa), qua đường tiêu hóa (con đường bài xuất chủ yếu) -
Tăng axit uric trong những trường hợp: + Bệnh gout
+ Ăn nhiều thức ăn chứa nhiều base nito nhân purin + Suy thận -
Ý nghĩa của ĐL axit uric trong huyết thanh:
+ Phân biệt bệnh gout do axit uric tăng với nguyên nhân gây viêm khớp khác
+ Trong suy thận để tiên lượng bệnh
BÀI 7: XÁC ĐỊNH CÁC CHẤT BẤT THƯỜNG TRONG NƯỚC TIỂU
Các chất bất thường trong nước tiểu là những chất nào?
Glucose, protein, hemoglobin, cetonic, muối mật, sắc tố mật, hồng cầu
Vì sao bước sóng khi đo các chất bất thường trong nước tiểu khác với các chất glucose, cholesterol, triglycerid,
protein, albumin, acid uric huyết thanh?
Vì phương pháp khác nhau nên đo bước sóng cũng khác nhau
1. Định lượng pr niệu 1.1. Cơ chế phản ứng lOMoAR cPSD| 45148588
Dùng acid tricloacetic kết tủa protein trong nước tiểu, đo độ đục trên máy quang kế. Đối chiếu mật độ quang
trên biểu đồ mẫu để tính ra lượng protein trong nước tiểu 1.2. Cách tiến hành Thử Trắng Nước tiểu (ml) 0,5 0,5 Acid tricloacetic 5% (ml) 1,5 NaCl 0,9% (ml) 1,5
1.3. Cách tính kết quả, kết quả
Protein (g/l) = E thử/ E mẫu * 80
1.4. Khi đo nồng được nồng độ > 4g/l thì làm thế nào? Lấy
nước tiểu chưa làm thí nghiệm và pha loãng
1.5. Bình thường trong nước tiểu có pr không? Vì sao không có? Nếu có thì bệnh lí nào, tại sao bị bệnh đó pr lại có trong nước tiểu? -
Bình thường pr không có trong nước tiểu vì pr tích điện âm và kích thước lớn không qua được màng lọc cầu
thận, trong một số trường hợp sinh lí pr có trong nước tiểu đầu thì cũng sẽ bị tái hấp thu hoàn toàn ở thận. - Pr có trong nước tiểu
+ Nguồn gốc cầu thận: độ lọc tăng (khi xuất hiện pr bất thường kích thước nhỏ hơn albumin hoặc tổn
thương cầu thận trong viêm cầu thận, viêm thận nhiễm mỡ), độ khuếch tán tăng khi nồng độ pr máu
ở cầu thận tăng hoặc khi có sự ứ đọng lưu lượng cầu thận tiếp giáp ở màng lọc cầu thận (suy tim,
tắc tĩnh mạch thận,...)
+ Nguồn gốc ống thận: do rối loạn tái hấp thu pr sau khi đã lọc bth bởi cầu thận (tổn thương bẩm sinh
ống thận, ngộ độc kim loại nặng,...)
2. Định lượng sơ bộ glucose nước tiểu 2.1. Cơ chế phản ứng
Trong môi trường kiềm và nhiệt độ sôi, glucose khử Cu2+ tạo Cu2O. Căn cứ vào màu của tủa (Cu2O) tạo
thành có thể sơ bộ đánh giá được lượng glucose trong nước tiểu 2.2. Cách tiến hành
Cho vào 1 ống nghiệm 1ml thuốc thử Bennedic, đun sôi, rồi thêm vào 4 giọt nước tiểu Lắc
đều, đun sôi lại, quan sát kết quả
2.3. Cách nhận định kết quả -
Phản ứng (-): nước tiểu không có glucose khi dung dịch trong ống nghiệm vẫn giữ màu xanh (màu của thuốc
thử Bennedic), không có tủa -
Phản ứng (+): nước tiểu có glucose, tủy theo lượng Cu2O mà có các kết quả:
+ Lượng glucose niệu <5 g/l => màu xanh lá cây, đáy ống có ít kết tủa
+ Lượng glucose niệu 5 10 g/l => tủa vàng
+ Lượng glucose niệu 10 20 g/l => tủa đỏ gạch
+ Lượng glucose niệu > 20 g/l => tủa đỏ gạch sẫm 2.4. Kết quả
2.5. Bình thường trong nước tiểu có glucose không? Vì sao không có? Nếu có thì bệnh lí nào, tại sao bị bệnhđó
glucose lại có trong nước tiểu? Xét nghiệm này có ý nghĩa không? -
Bình thường trong nước tiểu không có glucose, vì glucose sẽ bị tái hấp thu hoàn hoàn ở ống thận khi lượng
đường trong máu dưới 10 mmol/L vì ngưỡng tái hấp thu của ống thận là dưới 10 mmol/L -
Glucose xuất hiện trong nước tiểu khi
+ Trước thận: Đái tháo đường tụy do tụy giảm tiết insulin hoặc do đề kháng insulin làm cho đường trong
máu tăng quá 10 mmol/L nên thận không thể THT hoàn toàn glucose nên glucose sẽ xuất hiện trong nước tiểu lOMoAR cPSD| 45148588
+ Tại thận: do ngưỡng tái hấp thu của thận giảm khiến glucose không được hấp thu hoàn toàn ở thận (VCT mạn, )
3. Tìm cetonic trong nước tiểu 3.1. Cơ chế phản ứng
Trong môi trường amoniac, các chất cetonic sẽ tác dụng với natrinitroprusiat tạo màu tím hồng 3.2. Cách tiến hành
Cho vào lỗ của khay sứ bột Lestrande
Nhỏ vào bột Lestrande 2 giọt nước tiểu
3.3. Cách nhận định kết quả -
Pư (+): trong nước tiểu có cetonic, khi hỗn hợp trong lỗ khay sứ xuất hiện màu tím đỏ -
Pư (-): trong nước tiểu không có cetonic, khi hỗn hợp trong lỗ khay sứ không chuyển màu 3.4. Kết quả
3.5. Bình thường trong nước tiểu có cetonic không? Vì sao không có? Nếu có thì bệnh lí nào, tại sao bị bệnh
đóglucose lại có trong nước tiểu? -
Bình thường không có cetonic trong nước tiểu vì cetonic là dạng vận chuyển của acetyl-CoA, các cơ quan
(nhất là não và tim) tiêu thụ lượng lớn acetyl CoA để duy trì hoạt động bình thường nên lượng cetonic trong
máu rất ít, sẽ không xuất hiện trong nước tiểu -
Cetonic xuất hiện trong nước tiểu khi
+ Đái tháo đường tụy giai đoạn không kiểm soát được đường máu
Vì ĐTĐ tụy do thiếu insulin hoặc đề kháng insulin của receptor khiến hexokinase không thể hoạt
hóa được -> k t.h được G6P nên G6P không thể tg con đường đường phân tạo oxaloaxetat là chất
mồi để acetyl CoA tg vào ctri Creps sinh NL và G6P không thể tg con đường pentose tạo NADPH2
để tổng hợp các chất, nên lượng acetyl CoA tạo ra được bao nhiêu đều biến thành cetonic => làm
nồng độ cetonic tăng trong máu, và khi thiếu hụt NL thì cơ thể thoái hóa L,Pr, G để tạo thành acetyl
CoA nhưng k đi vào ctr Creps được, khiến lượng cetonic tăng cao trong máu.
+ Nhịn đói kéo dài (glycogen dự trữ trong gan chuyển thành glucose hết), nhiễm độc thai nghén -> nôn
nhiều, nôn kéo dài (k hấp thu được glucose) khiến nồng độ glucose trong máu giảm -> nồng độ
glucose máu giảm, cơ thể sử dụng chất béo làm nguồn năng lượng thay thế, qtr này tạo ra ceton làm
ceton máu tăng -> trong nước tiểu xuất hiện ceton
4. Tìm máu và hemoglobin trong nước tiểu 4.1. Cơ chế phản ứng
Hb tác dụng như 1 peroxydase, phân hủy H2O2 thành oxy hoạt động. Oxy hoạt động sẽ oxy hóa bột benzidin tạo màu xanh 4.2. Cách tiến hành Cho vào ống nghiệm: + Nước tiểu: 1ml + H2O2 10 thể tích: 1ml
+ Acid acetic đặc: 2 giọt + Bột Benzidin
4.3. Cách nhận định kết quả -
Pư (-): trong nước tiểu k có máu hoặc Hb, khi hỗn hợp trong ống nghiệm không chuyển màu -
Pư (+): trong nước tiểu k có máu hoặc Hb, khi hỗn hợp trong ống nghiệm chuyển sang màu xanh
Trường hợp pư (+) cần xác định rõ trong nước tiểu có máu, có Hb bằng cách: lấy nước tiểu quay li tâm và
đem soi cặn trên kính hiển vi. Nếu:
+ Soi có nhiều hồng cầu thì kết luận trong nước tiểu có máu
+ Soi không có hồng cầu thì kết luận trong nước tiểu có Hb
4.4. Tại sao cho axid acetic đặc vào?
Phá vỡ hồng cầu để giải phóng Hb hoạt động như 1 peroxydase, phân hủy H2O2 thành oxy hoạt động, oxy
hoạt động sẽ oxy hóa bột benzidin tạo màu xanh 4.5. Kết quả lOMoAR cPSD| 45148588
Xuất hiện màu xanh chứng tỏ có máu hoặc Hb trong nước tiểu
4.6. Bình thường trong nước tiểu có máu hoặc Hb không? Vì sao không có? Nếu có thì bệnh lí nào, tại sao
bịbệnh đó máu hoặc hemoglobin lại có trong nước tiểu? -
Bình thường trong nước tiểu không có máu vì các tế bào máu không qua được màng lọc cầu thận (cụ thể là
lớp nội mạc), không có Hb vì - Máu có trong nước tiểu khi:
+ Tại thận: viêm cầu thận cấp tổn thương đến lớp nội mạc khiến các tế bào máu có trong nước tiểu,
HCTH tổn thương sâu khiến lượng máu thoát ra nhiều hơn VCTC
+ Tổn thương niệu đạo, ung thư tuyến tiền liệt, ung thư thận, lao thận, sỏi thận, sỏi bàng quang -
Hb có trong nước tiểu khi:
+ Trước gan: do tan huyết, trong sốt rét, bỏng nặng,… khiến số lượng lớn hồng cầu bị vỡ khi chưa bị
lách tiêu hủy nên lượng Hb trong máu tăng khiến Hb niệu (+)
5. Tìm sắc tố mật trong nước tiểu 5.1. Cơ chế phản ứng
Bilirubin liên hợp có trong nước tiểu kết hợp với bariclorua tạo muối baribilirubinat không tan. Dưới tác
dụng của hỗn hợp FeCl3 và acid tricloacetic sẽ làm tan tủa và oxy hóa bilirubin tạo thành biliverdin có màu xanh ve 5.2. Cách tiến hành Cho vào ống nghiệm: + Nước tiểu: 1ml
+ Dung dịch BaCl2 10ml: 0,5ml
Lắc đều, lọc lấy tủa (cho chảy kiệt nước)-> nhỏ vào tủa 3 giọt thuốc thử Fuxe
5.3. Cách nhận định kết quả -
Pư (+): trong nước tiểu có bilirubin khi xuất hiện vòng xanh ve -
Pư (-): trong nước tiểu không có bilirubin khi không xuất hiện vòng xanh ve 5.4. Kết quả
5.5. Bình thường trong nước tiểu có sắc tố mật không? Vì sao không có? Nếu có thì bệnh lí nào, tại sao bị bệnhđó
sắc tố mật lại có trong nước tiểu? -
Bình thường trong nước tiểu không có sắc tố mật (hay bili LH) vì bili LH 20% sẽ được THT tạo thành bili
tự do, 80% qua ruột trở thành urobilin (màu vàng) và stercobilin (màu nâu), stercobilin được thải ra qua phân,
trong khi một phần urobilin có thể được tái hấp thu vào máu và thải qua nước tiểu - Sắc tố mật có trong nước tiểu khi:
+ Tại gan: viêm gan do rượu/virus khiến TB gan phù nề, chèn ép vi quản mật, gây tắc vi quản mật khiến
mật ứ lại tại gan -> mật vào máu khiến bili LH trong máu tăng nên có sắc tố mật trong nước tiểu
+ Sau gan: tắc mật do ống mật chủ bị tắc, sỏi mật, giun chui lên OMC, u chèn ép vào OMC (u đầu
tụy,…) khiến mật ứ lại tại gan -> mật vào máu khiến bili LH trong máu tăng nên có sắc tố mật trong nước tiểu
6. Tìm muối mật trong nước tiểu 6.1. Cơ chế phản ứng
Sự có mặt của muối mật sẽ làm giảm sức căng bề mặt của nước tiểu. Dùng bột lưu huỳnh thăng hoa để phát
hiện sự giảm sức căng bề mặt đó 6.2. Cách tiến hành
Cho vào 1 cốc có chân 50ml nước tiểu, cho nhẹ nhàng lên bề mặt của nước tiểu 1 ít bột lưu huỳnh thăng hoa và quan sát
6.3. Cách nhận định kết quả -
Pư (-): không có sắc tố mật trong nước tiểu, khi bột lưu huỳnh k rơi xuống đáy cốc -
Pư (+) nhẹ: nước tiểu có ít muối mật, khi bột lưu huỳnh dàn mỏng ra từ từ và gõ nhẹ vào thành cốc thì chúng
mới rơi xuống đáy cốc -
Pư (+) mạnh: nước tiểu có nhiều muối mật, khi bột lưu huỳnh dàn mỏng ra một cách nhanh chóng rồi rơi xuống đáy cốc lOMoAR cPSD| 45148588 6.4. Kết quả
6.5. Bình thường trong nước tiểu có muối mật không? Vì sao không có? Nếu có thì bệnh lí nào, tại sao bị bệnh
đó muối mật lại có trong nước tiểu? -
Bình thường trong nước tiểu không có muối mật vì phần lớn được đào thải qua phân và 1 phần nhỏ được
THT nên có trong máu nhưng không đủ để xuất hiện trong nước tiểu - Muối mật có trong nước tiểu khi:
+ Tại gan: viêm gan (do VK, rượu, tự miễn), xơ gan (chức năng gan suy giảm), ung thư gan (ảnh hưởng
con đường bài tiết mật)
+ Sau gan: tắc mật (sỏi mật, khối u,… gây tắc đường mật)



