





Preview text:
Họ tên: Trần Thị Quỳnh Thương
Mã sinh viên: 21012612 Lớp: K15-CNSH
Ngày thực hành: 15/03/2023 Nhóm: 1 BÁO CÁO THỰC HÀNH Học phần: Hóa sinh
Bài thực hành số 2
Tên bài thực hành: Protein và Axit amin I. Lý thuyết II. Nội dung thực hành 1. Chuẩn bị chung
Dung dịch mẫu lòng trắng trứng a. Hóa chất:
Trứng gà và vịt (2 quả) Nước cất Dung dịch NaOH b. Dụng cụ: Cân Bình định mức 100ml Ống nghiệm Pipet Ống đong
c. Các bước tiến hành
Bước 1: Tách riêng lòng trắng trứng gà và vịt vào 2 ống đong khác nhau
Bước 2: Cân lần lượt các mẫu lòng trắng trứng và vịt
Lấy 0,5076g lòng trắng trứng vịt vào bình tam giác
Lấy 0,5206g lòng trắng trứng gà vào bình tam giác
Bước 3: Cho từ từ nước cất vào 2 bình định mức đến bình thì
dừng lại, sau đó lắc đều. Quan sát thấy, lòng trắng trứng không
tan vẫn xuất hiện mảng trắng phía dưới.
- Vì albumin lòng trắng trứng không tan, ta nhỏ thêm vài giọt NaOH vào
2 bình định mức để hòa tan mẫu.
- Tiếp tục, cho thêm nước cất sao cho tổng dung dịch bằng 100ml không tính bọt khí.
Giải thích: Bản chất của albumin là không tan trong nước cất nên phải
cho thêm dung dịch NaOH để hòa tan.
2. Thí nghiệm 1: Phản ứng màu Biure
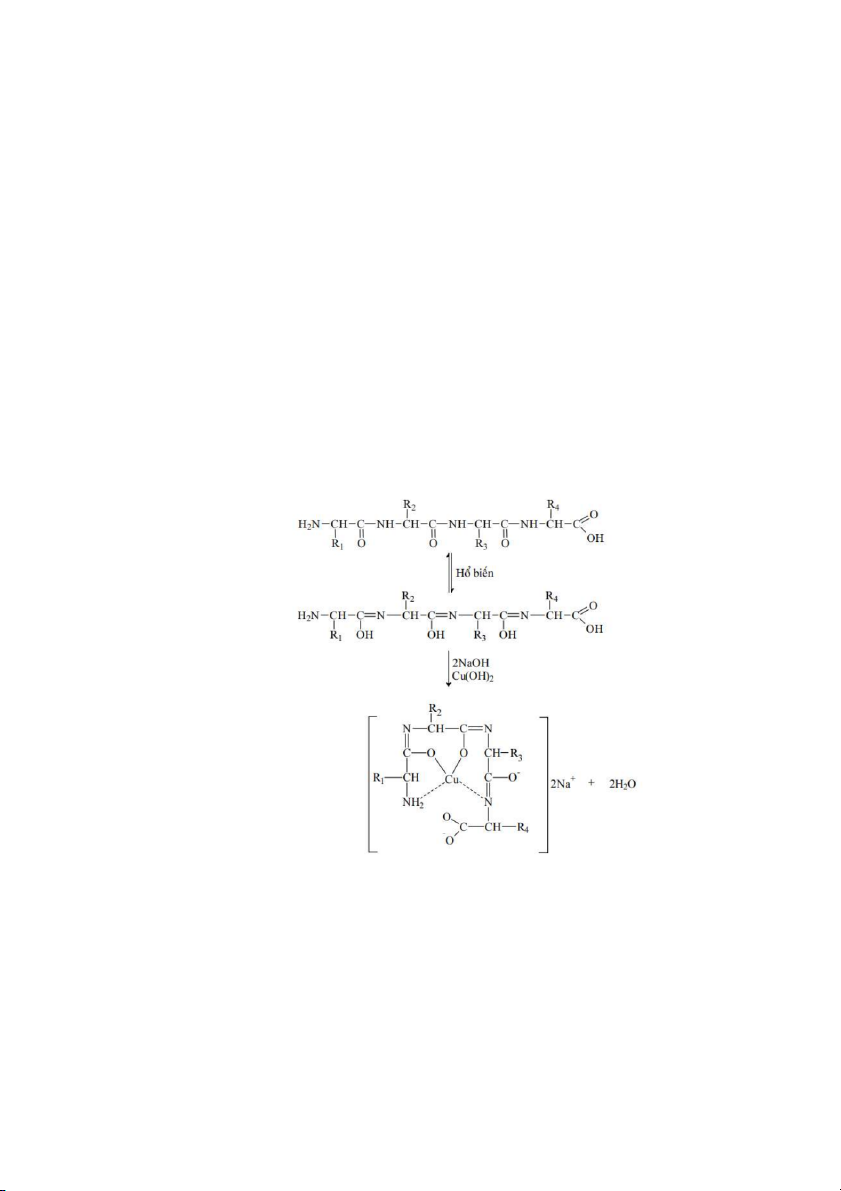
a. Nguyên tắc: Trong phân tử protein có mặt nhóm - CO - NH - nên có thể
tạo phức biure với Cu2+ trong môi trường kiềm. Cơ chế phản ứng có thể trình bày như sau:
Trong môi trường kiềm, các hợp chất có chứa từ 2 liên
kết peptit trở lên có thể phản ứng với tạo thành phức
chất màu xanh tím, tím đỏ hoặc đỏ. b. Chuẩn bị Hóa chất: - Dung dịch protein - Dung dịch 2% - Dung dịch NaOH 30% Dụng cụ - Ống nghiệm - Pipet
c. Các bước tiến hành
Chọn dung dịch mẫu lòng trắng trứng vịt
Bước 1: Cho 1ml dung dịch protein (lòng trắng trứng vịt) vào ống nghiệm
Bước 2: Thêm dung dịch NaOH 30% (1ml) => Tạo môi trường
Bước 3: Thêm 5 giọt 2% có màu xanh lam vào, dung dịch màu
xanh lam sẽ chuyển sang màu tím (xanh tím) d. Xử lý kết quả
Trong môi trường kiềm, các hợp chất có 2 liên kết peptit trở lên có
thể phản ứng với tạo thành phức chất có màu xanh tím, tím.
Màu sắc c]ng như đô ^ đâ ^m nhạt của phức hợp tùy thuộc vào số
lượng liên kết peptit nhiều hay ít, số lượng nguyên tử Nitơ tham gia
tạo liên kết phối trí với Cu2+.
Các polypeptit trong dung dịch lòng trắng trứng thường tạo 2 hay 3
liên kết phối trí với Cu2+ nên cho sản phẩm màu xanh tím. Đô ^ đâ ^m
nhạt tùy thuô ^c ncng đô ^ của protein có trong mẫu.
Hiện tượng xảy ra ở phản ứng trên:
Ở bước 3, sau khi thêm NaOH vào gây phân tầng. còn ở bước 4,
sau khi thêm dung dịch vào thì có hiện tượng dung dịch chuyển từ
màu xanh lam sang màu xanh tím.
3. Thí nghiệm 2: Phản ứng kết tủa
a. Nguyên tắc: Dung dịch keo protein bền vững do các tiểu phần protein
mang lớp áo nước bị ngăn cách nhau và do sự tích điện cùng dấu nên
chúng đẩy nhau. Nếu làm mất một trong hai yếu tố trên thì sẽ dẫn tới sự
kết tủa các tiểu phần protein đó.
Làm mất lớp áo nước bằng cách: thêm các chất điện giải hoặc khử
nước như NaCl, (NH4)2SO4, alcol, aceton...
Trung hòa điện tích của protein bằng cách:
Thêm chất điện giải như NaCl, (NH4)2SO4...
Hoặc đưa pH của môi trường chứa protein về gần điểm đẳng điện pI của protein.
Ngoài ra khi làm biến tính protein bằng nhiệt độ cao hay dưới tác
dụng của các chất như acid, kiềm mạnh hoặc muối của kim loại
nặng... c]ng dẫn tới kết tủa protein. b. Chuẩn bị Hóa chất: - Dung dịch protein
- Dung dịch Ethanol tuyệt đối
- Dung dịch NaCl bão hòa 5ml-25֯C Dụng cụ - Ống nghiệm - Pipet
c. Các bước tiến hành
Chọn dung dịch mẫu lòng trắng trứng vịt
Bước 1: Cho 1ml dung dịch protein (lòng trắng trứng vịt) vào ống nghiệm
Bước 2: Nhỏ từ từ 20 giọt Ethanol tuyệt đối vào ống nghiệm
Thấy dung dịch bên trong ống nghiệm, bắt đầu chuyển sang màu đục.
Bước 3: Cho thêm từ từ 5 giọt NaCl bão hòa vào ống nghiệm
Tủa protein bắt đầu xuất hiện rõ rệt. d. Xử lý kết quả
Protein là chất keo ưa nước, độ bền của dung dịch keo protein tùy
thuộc vào nhiều yếu tố như: sự tích điện của phân tử protein, mức
độ hidrat hóa, nhiệt độ,…
Với các phản ứng kết tủa thuận nghịch của protein: dưới tác dụng
của các chất như: muối trung tính kim loại kiềm, kiềm thổ (NaCl,
…), các dung môi hữu cơ. Trong điều kiện nhiệt độ thấp có tác
dụng gây kết tủa protein.
4. Thí nghiệm 3: Định lượng protein theo phương pháp Lowry
a. Nguyên tắc: Cơ sở của việc định lượng protein theo phương pháp Lowry
là dựa vào phản ứng màu của protein với thuốc thử Folin tạo thành phức
chất có màu xanh hấp thu cực đại ở bước sóng 750nm. Cường độ màu của
dung dịch tỉ lệ thuận với ncng độ protein.
Phương pháp này có độ nhạy cao, cho phép xác định
dung dịch mẫu chứa vài chục microgam protein. b. Chuẩn bị Hóa chất:
- Dung dịch BSA chuẩn 200 g/mL pha trong dung dịch NaCl 0,9%.
- Dung dịch A: 2% trong NaOH 0,1N
- Dung dịch B: 0,5% trong kali natri tartrat 1%
- Dung dịch C: Pha dung dịch A và B theo tỉ lệ thể tích 49:1 trước khi dùng. - Thuốc thử Folin 1N Dụng cụ: - Ống nghiệm - Pipet - Bình định mức - Máy Elisa
c. Các bước tiến hành
Chuẩn bị dung dịch A: pha 150ml
Bước 1: Chia 2 bình định mức 100ml 50 ml
Bước 2: Cân lần lượt các chất cần để pha dung dịch và cho lần lượt vào các bình định mức Bình 100ml - Cân 0,4g NaOH - Cân 2,0408g Bình 50 ml - Cân 0,2g NaOH - Cân 1,0204g
Bước 3: Cho nước cất từ từ vào các bình định mức để đạt được
tổng số dung dịch cần thiết.
Chuẩn bị dãy dung dịch protein chuẩn Trắng Trắng 50x Đỏ 50x 10x Đỏ 50x 1 2 3 4 5 6 7 8 9 BSA 0 50 100 150 200 - - - - NaCl 0,9% - - - - - - - - - Dung dịch C 2,5 2,5 2,5 2,5 2,5 2,5 2,5 2,5 2,5 Dung dịch mẫu 0,5 0,5 0,5 0,5 Folin 0,5 0,5 0,5 0,5 0,5 0,5 0,5 0,5 0,5 d. Xử lý kết quả
Kết quả đo máy Elisa Độ pha Mẫu Trắng Đỏ Trắng Đỏ loãng trắng 200 150 100 50 10x 10x 50x 50x Ống 1 2 3 4 5 6 7 8 9 0,09 0,12 0,12 0,14 0,07 0,07 Kết quả 0,089 5 3 9 5 0,211 1 0,278 7
Xây dựng đường chuẩn
Bước 1: Tính toán số liệu Ống 1 2 3 4 5 6 7 8 9 Ncng độ 0 1 1.33 2 4 BSA () 0,12 Kết quả 0,089 0,095 0,123 9 0,145 0,211 0,071 0,278 0,077 Bước 2: Đc thị:
Nhập vào Excel bảng số liệu như sau:
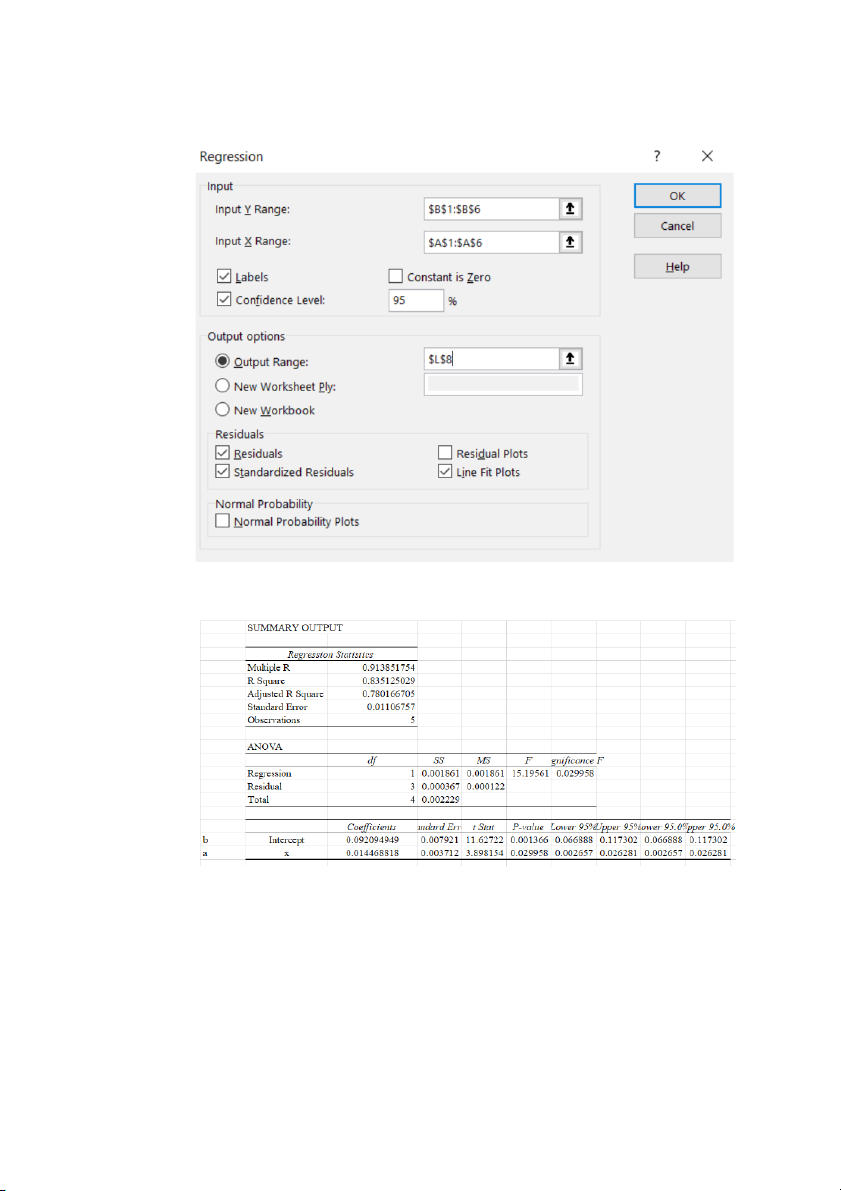
Vào Data, chọn Data Analyze => Regression
Thu được bảng số liệu và đc thị
Hình 1: Bảng tương quan hồi quy tuyến tính
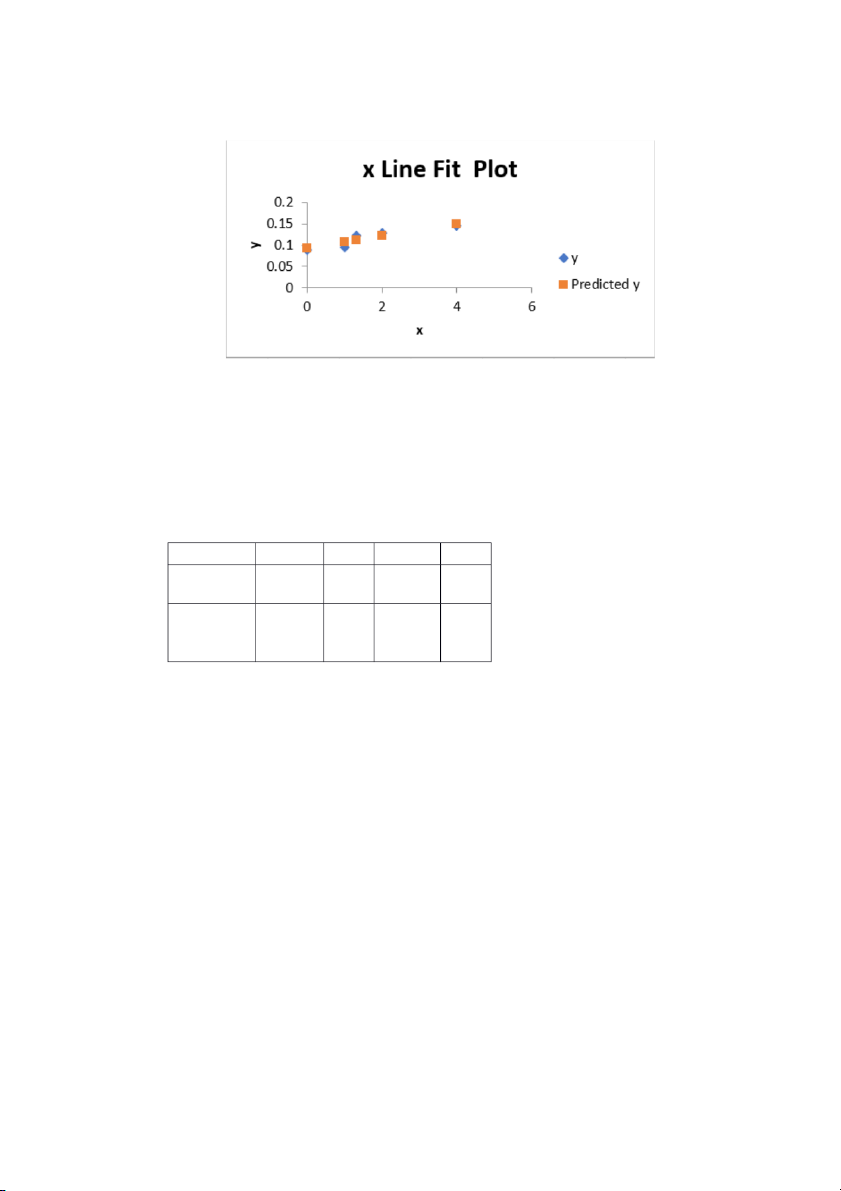
Hình 2: Đồ thị tương quan giữa nồng độ và mật độ quang
Từ hình 1, ta có phương trình hci quy tuyến tính: D = 0,014.C + 0,092
Tính ncng độ protein trong trứng: C = Ống 6 7 8 9 Mật độ quang D 0,211 0,071 0,278 0,077 Ncng độ BSA ()




