

Preview text:
3 AMINO ACID
Có 2 cách để mô tả cách các phân tử sinh học sẽ được sử dụng.
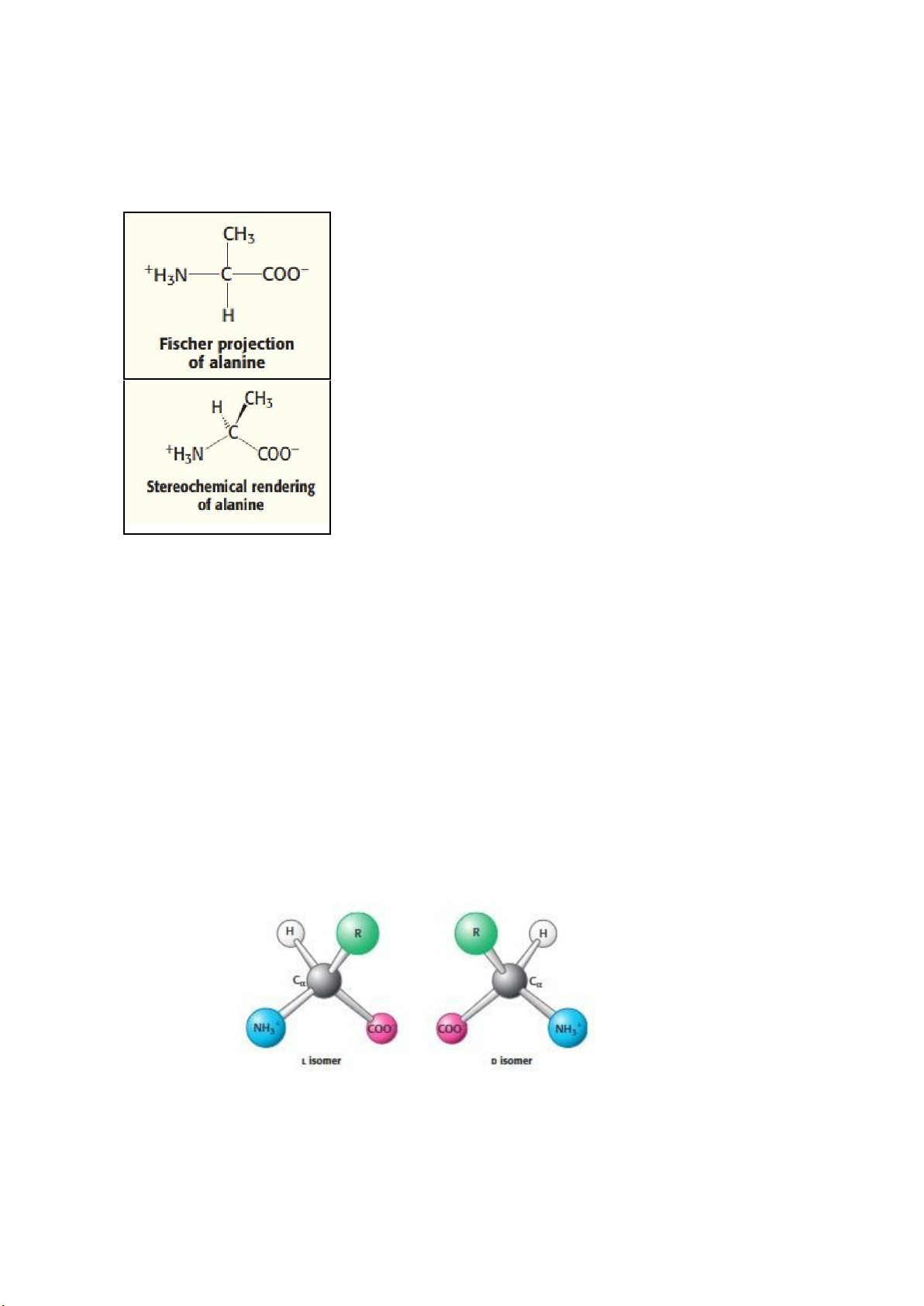
Phép chiếu Fischer: Mỗi nguyên tử được xác định và các
liên kết với nguyên tử trung tâm được mô tả là các đường
thẳng đứng và nằm ngang. Các liên kết ngang được đưa ra
khỏi mặt phẳng hướng về phía người xem, trong khi các liên
kết dọc được đưa ra sau mặt phẳng hướng ra xa người xem. ì
H nh ảnh lập thể: Các nêm (Wedges) mô tả hướng chiếu của liên kết. Một nêm rắn cho
thấy liên kết chiếu về phía người xem ra khỏi mặt phẳng,
nêm đứt nét cho thấy liên kết ra xa người xem. Các liên kết
còn lại được mô tả dưới dạng đường thẳng.
3.1 Khái niệm amino acid:
- Là đơn vị cơ bản cấu tạo nên protein (xây dựng bởi 20 amino acid).
- Cấu tạo từ một nguyên tử cacbon trung tâm gọi là cacbon α liên kết với nhóm amino
(-NH₂), nhóm carboxyl (-COOH), nguyên tử hydro, và một nhóm R (nhóm chức năng
quyết định tính chất của amino acid). ● L và D Isomer
- Hầu hết các loại amino acid đều tồn tại ở dạng hai ảnh phản chiếu.
- Khi bốn nhóm khác nhau liên kết với cacbon alpha, các amino acid sẽ không đối
xứng (Một phân tử không đối xứng là một phân tử không thể chồng lên ảnh phản
chiếu của nó), nghĩa là chúng tồn tại dưới dạng ảnh phản chiếu hay còn gọi là đồng
phân L và D (trừ Glycine).
- Chỉ có đồng phân L được tìm thấy trong protein.
● Tất cả amino acid đều có ít nhất 2 nhóm tích điện
- Các amino acid tự do trong dung dịch ở độ pH trung tính (pH sinh lí ~ 7.4) tồn tại
dưới dạng ion lưỡng cực.
- NH3+ và COO- mang điện tích.
- Một amino acid lưỡng cực: Ở pH sinh lí, nhóm animo được proton hóa và nhóm
carboxyl không được proton hóa.
pH<2 (+), pH 2-9 (lưỡng cực), pH>9 (-)
pH=pKa: tồn tại 2 trạng thái icon bằng nhau pH
pH>pKa: nhóm mất giữ proton
● Điểm đẳng điện (pI): giá trị pH mà tại đó phân tử không mang điện tích.
Amino acid có mạch bên trung tính: pI=1/2x(pK1+pK2)
Amino acid có chuỗi bên acid (-): pI=1/2x(pK1+pKR)
Amino acid có chuỗi bên cơ bản (+): pI=1/2x(pK2+pKR)
● Tại điểm đẳng điện:
- Amino acid kém tan nhất.
- Amino acid không di chuyển được trong điện trường.
- Amino acid không liên kết tốt với các hợp chất khác.
+ pH+ pH>pI: aa (-), di chuyển về cực (+).
3.2 Amino acid chứa nhiều nhóm chức năng
- 20 loại amino acid trong protein chứa các chuỗi bên khác nhau về kích thước, hình
dạng, điện tích, khả năng liên kết hidro, tính kỵ nước và khả năng phản ứng hóa học.
- Có 4 nhóm amino acid dựa trên đặc điểm chung của nhóm R:
+ Kỵ nước (9): Alanine, Valine
+ Mạch nhánh phân cực (6): Serine, Threonine
+ Mạch nhánh tích điện (+)(base) (3): Lysine
+ Mạch nhánh tích điện (-)(acid) (2): Aspatic
- Các amino acid trong chuỗi mang điện tích (+) rất ưa nước.
- Các amino acid trong chuỗi chỉ có C và H thì kỵ nước.
- Các amino acid kỵ nước, đặc biệt là các amino acid mạch thẳng và mạch thơm lớn
hơn có xu hướng tập trung lại với nhau bên trong protein, tránh xa môi trường nước của tế bào.
- Các nhóm kỵ nước có xu hướng kết hợp với nhau gọi là hiệu ứng kỵ nước và là
động lực thúc đẩy sự hình thành cấu trúc 3 chiều độc đáo của protein tan trong nước.
- Phân cực trong nhóm chức có O,S,N.
3.3. Các amino acid thiết yếu phải lấy từ chế độ ăn uống
- Hầu hết các vsv có thể tổng hợp toàn bộ 20 loại amino acid cơ bản, trong khi con
người chỉ tạo ra 11 loại.
- Các amino acid không thể được tạo ra trong cơ thể, phải được cung cấp thông qua
chế độ ăn uống và được gọi là các amino acid thiết yếu. Các loại khác gọi là không thiết yếu.
● Vai trò Amino acid trong cơ thể
- Quan trọng cho sự phát triển, sửa chữa và duy trì cơ bắp.
- Hệ thần kinh: amino acid rất cần thiết cho việc sản xuất chất dẫn truyền thần kinh,
truyền tín hiệu giữa các tb thần kinh. Chúng đóng vai trò trong chức năng nhận thức,
điều chỉnh tâm trạng và chất lượng giấc ngủ.
- Hệ tiêu hóa: các amino acid tham gia vào quá trình sản xuất các enyme tiêu hóa,
giúp phân hủy thức ăn thành các phân tử nhỏ dễ hấp thụ.
- Hệ miễn dịch: amino acid cần thiết cho việc sản xuất kháng thể bảo vệ cơ thể chống
lại mầm bệnh và các chất lạ.



