












Preview text:
Bài 2: CƠ SỞ CỦA QUÁ TRÌNH CHUYỂN
KHỐI (TRUYỀN CHẤT, KHUẾCH TÁN) Do Xuan Truong truong.doxuan@hust.edu.vn I. KHÁI NIỆM CHUNG 1. Phân loại
Chemical Engineering: Bao gồm nhiều lĩnh vực: Hóa học, dầu khí, thực phẩm, dược phẩm, vật liệu…
Chưng luyện (distillation): Là quá trình tách các hỗn hợp lỏng thành các cấu tử riêng
biệt, trong đó vật chất di chuyển từ pha lỏng vào pha hơi và ngược lại
Hấp thụ (absorption): Là quá trình hút khí hoặc hơi bằng chất lỏng, trong đó vật chất di
chuyển từ pha khí và pha lỏng.
Hấp phụ (adsorption): Là quá trình hút khí hoặc hơi bằng chất rắn xốp, trong đó vật
chất di chuyển từ pha khí và pha rắn.
Trích ly (extraction): Là quá trình tách chất hòa tan trong chất lỏng hay rắn, bằng một chất lỏng khác
Sấy (drying): Là quá trình tách nước ra khỏi vật liệu ẩm trong đó vật chất (hơi nước) đi
từ pha rắn hay pha lỏng và pha khí
Kết tinh (crystallization): Là quá trình tách chất rắn trong dung dịch, trong đó vật chất
di chuyển từ pha lỏng và pha khí
Trao đổi ion (ion exchange): Là quá trình tách dựa trên khả năng của một số chất trao
đổi ion có thể trao đổi các nhóm ion linh động của mình với các ion trong dung dịch
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer) I. KHÁI NIỆM CHUNG
2. Phương pháp biểu diễn thành phần pha
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer) I. KHÁI NIỆM CHUNG
2. Phương pháp biểu diễn thành phần pha
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer) II. CÂN BẰNG PHA
1. Khái niệm cân bằng pha 2. Quy tắc pha của Gibbs
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer) II. CÂN BẰNG PHA 2. Quy tắc pha của Gibbs Ví dụ:
- Hệ 1 cấu tử nguyên chất tồn tại 3 pha: C = 1-3+2 = 0
- Hệ 1 cấu tử 2 pha (hơi nước bão hòa): C = 1-2+2 = 1
- Hệ chưng luyện 2 cấu tử, áp suất không đổi
C= 2-2+1 = 1. Nồng độ và Nhiệt độ Sôi có quan hệ với nhau
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer) II. CÂN BẰNG PHA
2. Các định luật cân bằng pha 2.1 Định luật Henry
Áp suất riêng phần p của khí trên chất lỏng tỷ lệ với nồng độ mol x của nó trong dung dịch
Ψ là hệ số Henry, thứ nguyên áp suất, phụ thuộc vào tính chất của khí, lỏng và nhiệt độ.
m là hằng số cân bằng không có thứ nguyên Tổng quát:
Định luật Henry chỉ đúng với chất khí, thường áp dụng trong quá trình tính toán hấp thụ
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer) II. CÂN BẰNG PHA
2. Các định luật cân bằng pha 2.1 Định luật Henry 2.2. Định luật Raoult
Áp suất riêng phần của cấu tử i pi trên dung dịch bằng áp suất hơi bão hòa của
cấu tử đó (ở cùng nhiệt độ) nhân với nồng độ mol x của nó trong dung dịch Hệ 2 cấu tử:
Định luật Raoult thường được ứng dụng để tính toán quá trình chưng luyện
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
III. CÁC ĐỊNH LUẬT KHUẾCH TÁN
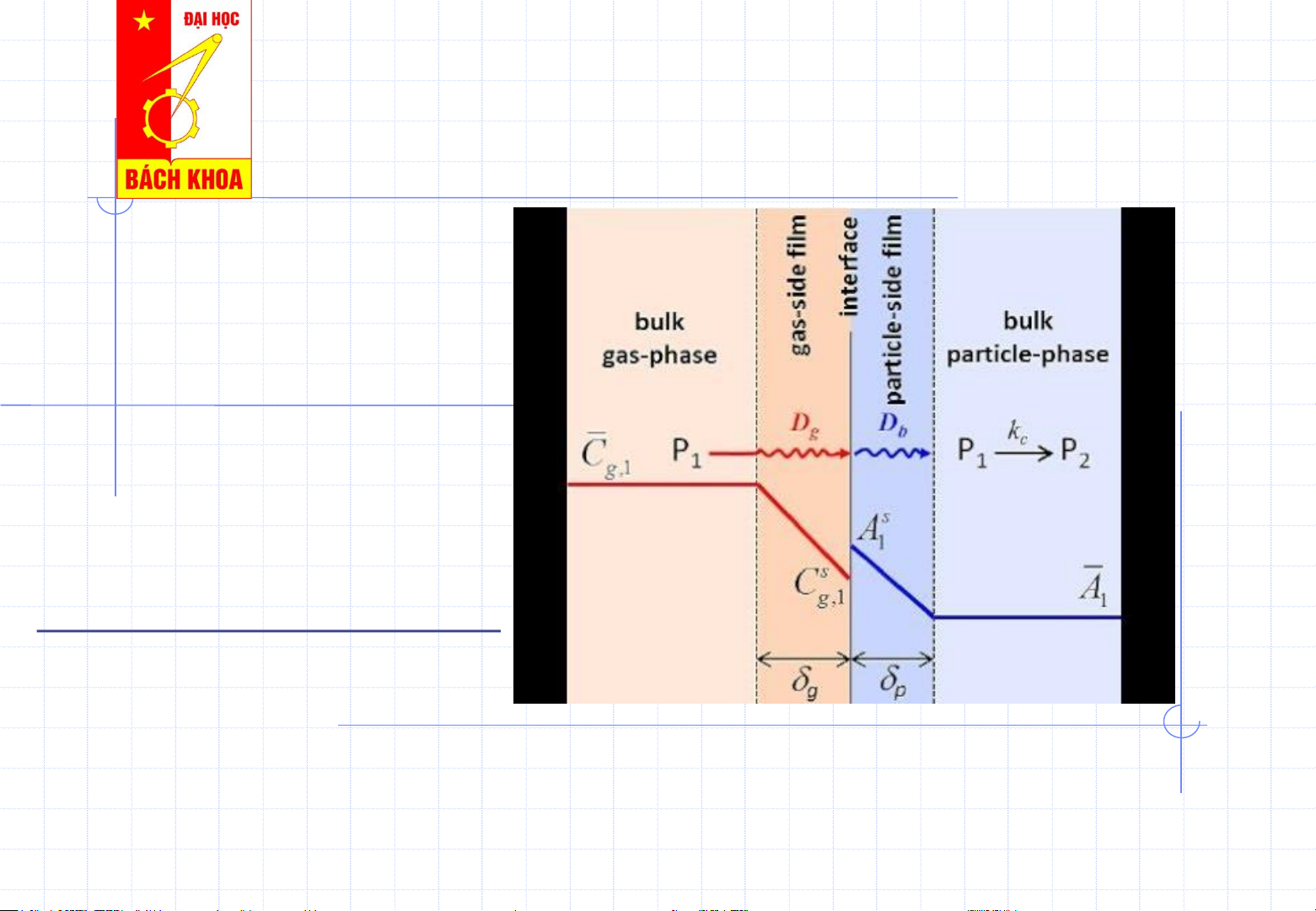
Chế độ chuyển động ở trong màng và trong nhân
pha có đặc trưng khác nhau:
- Trong màng luôn chuyển động dòng, còn nhân có thể chuyển động xoáy.
- Quá trình di chuyển vật chất trong màng cơ bản
là nhờ tiếp xúc giữa các phân tử - Khuếch Tán phân tử.
- Ở nhân của dòng, sự di chuyển vật chất nhờ sự
xáo trộn của các phần tử trong dòng – Khuếch tán đối lưu
- Vận tốc KT trong màng (KT phân tử) rất
chậm so với KT trong nhân (KT đối lưu) do vậy sẽ
có vai trò quyết định
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
III. CÁC ĐỊNH LUẬT KHUẾCH TÁN
1. Khuếch tán phân tử - Định luật Fick
- Tương tự KT nhiệt – định luật dẫn nhiệt Fourier
- Xảy ra trong lớp màng, hay môi trường đứng yên
- Động lực: gradient nồng độ
Phát biểu: Vận tốc KT là lượng vật chất đi qua một đơn vị bề mặt trong một đơn vị
thời gian (dG/Fd↊). Theo định luật Fick thì vận tốc KT tỷ lệ với gradient nồng độ
Hệ số KT là lương vật chất đi qua một đơn vị bề mặt trong
một đơn vị thời gian khi nồng độ vật chất giamrmootj đơn vị
trên một đơn vị chiều dài hướng KT.
D đặc trưng tính chất lý học, khả năng di chuyển của chất đó
trong môi trường nào đó.
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
III. CÁC ĐỊNH LUẬT KHUẾCH TÁN Tính hệ số KT D
Hệ số KT của khí trong khí
MA, MB: khối lượng phân tử của khí A và B, kg/kmol T: oK P: at
VA, VB: thể tích mol của khí A và B, cm3/mol
a,b: hệ số hiệu chỉnh của khí và dung môi
µ: độ nhớt của dung môi, cP
Hệ số KT của khí trong lỏng
Ở nhiệt độ khác hệ số KT được xác định:
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
III. CÁC ĐỊNH LUẬT KHUẾCH TÁN 2. KT đối lưu
- Tương tự đối lưu nhiệt
- Đinh luật cấp nhiệt Newton KT đối lưu Giả thiết:
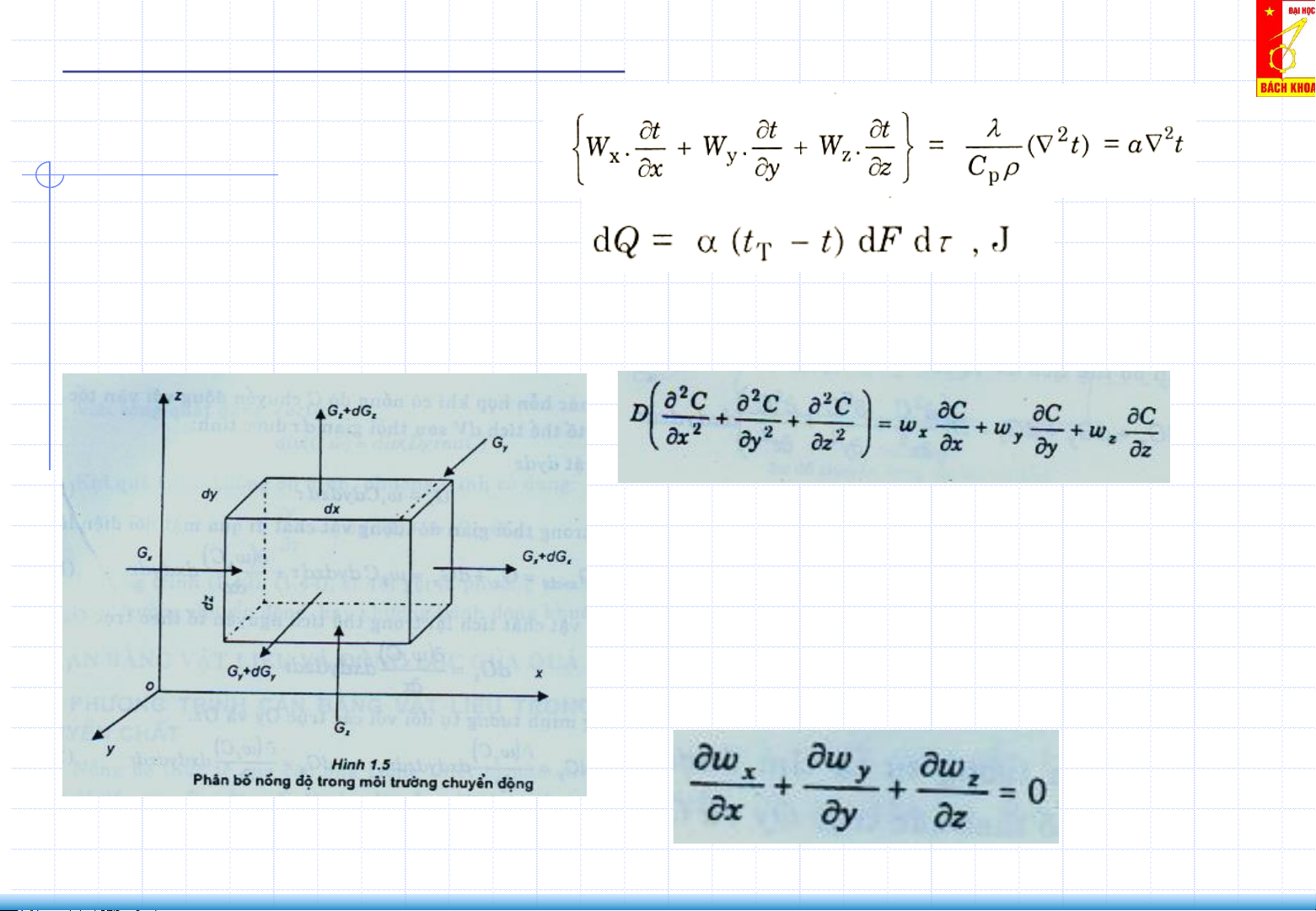
- Dòng chảy ổn định w = f(x,y,z) - Nồng độ C= f(x,y,z) - D = constant - Dòng chảy liên tục
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
III. CÁC ĐỊNH LUẬT KHUẾCH TÁN Chứng minh
Tương tự theo trục Oy, Oz: Toàn bộ thể tích dV:
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
III. CÁC ĐỊNH LUẬT KHUẾCH TÁN Chứng minh
Mặt khác hỗn hợp khí có nồng độ C chuyển động với vận
tốc w đi vào nguyên tố thể tích dV sau thời gian d↊: Qua mặt dydz:
Tương tự theo trục Oy, Oz: Toàn bộ thể tích dV:
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
III. CÁC ĐỊNH LUẬT KHUẾCH TÁN Chứng minh PT dòng liên tục:
Lượng vật chất do kt phân tử và đối lưu phải bằng nhau:
Khi quá trình không ổn định:
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)




