

Preview text:
Bài 4: CHƯƠNG 2 – CHƯNG - Distillation Do Xuan Truong truong.doxuan@hust.edu.vn
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
NHÀ MÁY LỌC DẦU DUNG QUẤT
https://www.youtube.com/watch?v=798d5LL1aq4
https://www.youtube.com/results?search_query=nh%C3%A0+m
%C3%A1y+l%E1%BB%8Dc+d%E1%BA%A7u+dung+qu%E1% BA%A5t
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer) I. KHÁI NIỆM
Chưng – distillation: là phương pháp tách hỗn hợp chất lỏng thành những cấu tử riêng biệt
dựa trên nhiệt độ bay hơi khác nhau của các cấu tử trong hỗn hợp.
Chưng: các cấu tử đều bay hơi
Cô đặc: Chỉ dung môi bay hơi, chất tan không bay hơi. Ứng dụng
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer) I. KHÁI NIỆM
- Hỗn hợp nhiều cấu tử: thu được nhiều sản phẩm theo chiều cao của tháp hoặc hệ nhiều tháp.
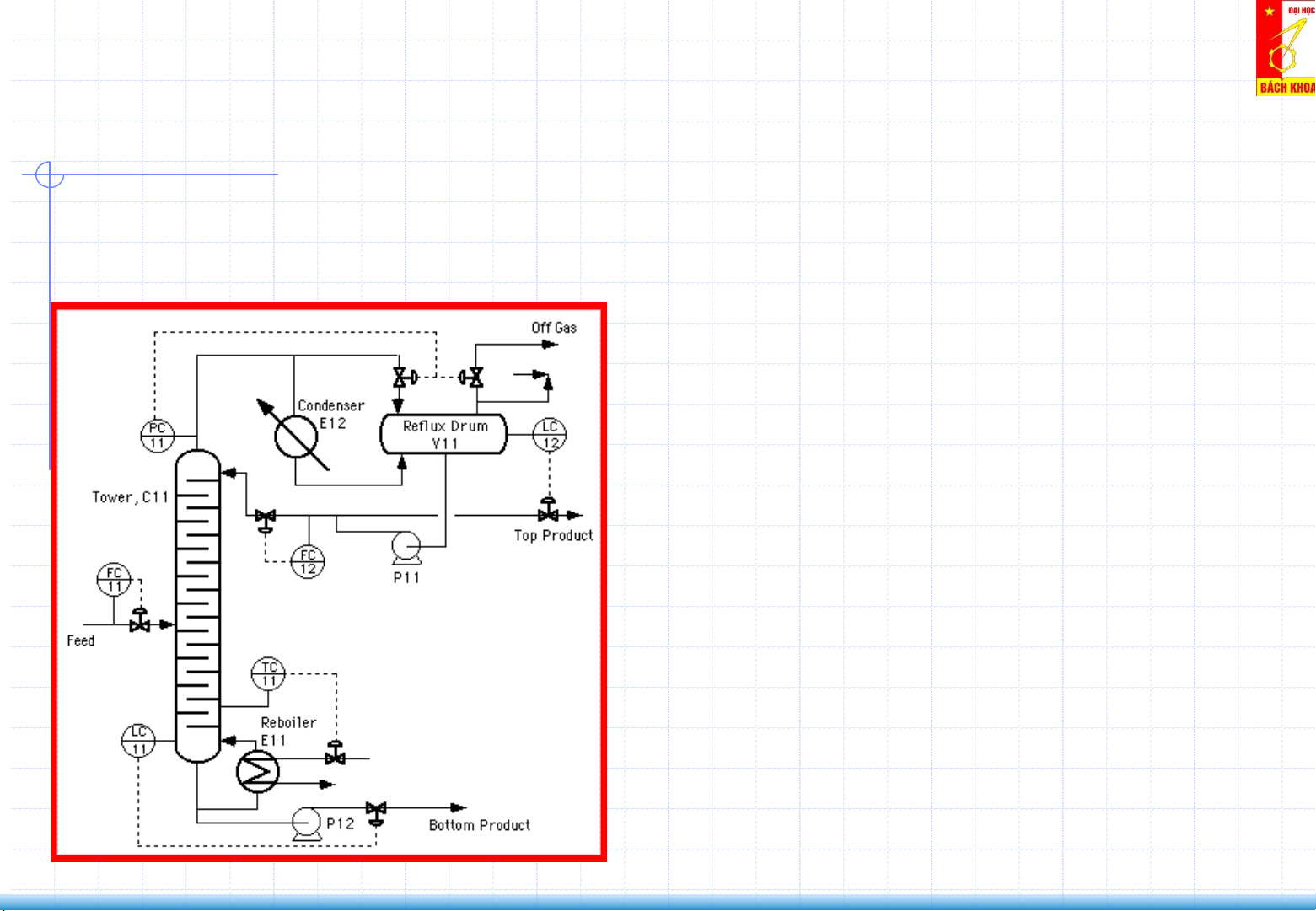
- Hỗn hợp 2 cấu tử: thu được sản phẩm đỉnh (Distillate – top product) giầu cấu
tử dễ bay hơi và một phần cấu tử khó bay hơi; sản phẩm đáy (bottom product)
giầu cấu tử khó bay hơi và một phần cấu tử dễ bay hơi Phân loại:
- Áp suất làm việc: chân không, áp suất thường, áp suất dư.
- Số cấu tử: 2 cấu tử, 3 cấu tử hoặc hệ
nhiều cấu tử (lọc dầu – hàng nghìn cấu tử)
- Phương thức làm việc: liên tục (chưng đơn
giản liên tục và chưng luyện liên tục), gián
đoạn (Chưng đơn giản gián đoạn và chưng luyện gián đoạn)
- Các phương thức chưng đặc biệt: chưng
bằng hơi nước trực tiếp (sx tinh dầu),
chưng trích ly – chưng đẳng phí, chưng phân tử...
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ 1. Khái niệm
Hỗn hợp 2 cấu tử: A và B
Ký hiệu: m – khối lượng (kg) hoặc lưu lượng khối lượng (kg/h)
V: thể tích (m3) hoặc lưu lượng thể tích (m3/h)
n: số mol (kmol) hoặc lưu lượng mol (kmol/h)
Các công thức về khí (hơi): Khí lý tưởng ĐK tiêu chuẩn Áp suất bất kỳ
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ 1. Khái niệm
Hỗn hợp 2 cấu tử: A và B
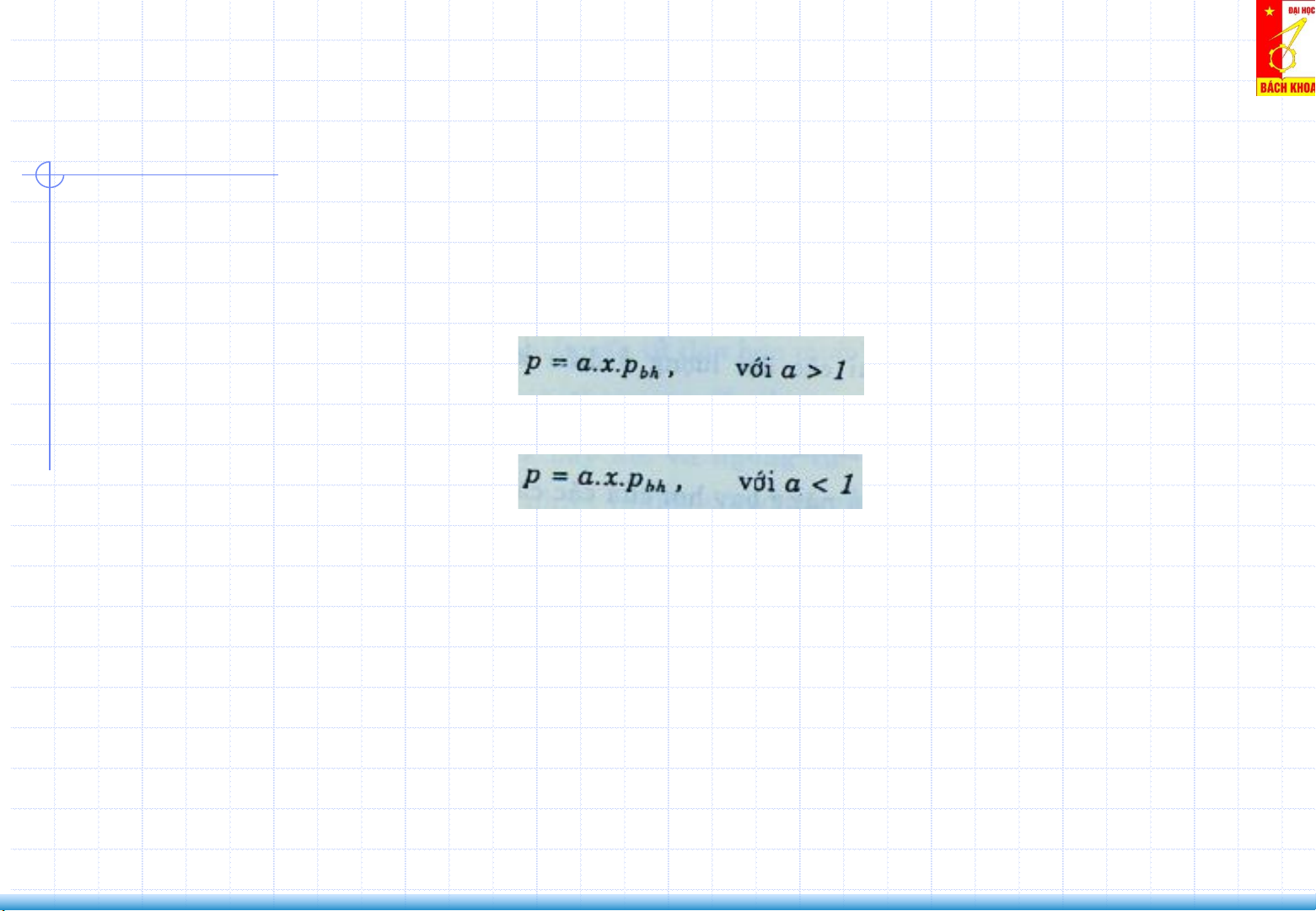
Hỗn hợp lỏng có sai lệch với định luật Raoult, aA, aB hệ số hiệu chỉnh:
Định luật Raoult: 𝑝𝐴 = 𝑝𝑏ℎ𝐴. 𝑥𝐴
𝑝𝐴 = 𝑎𝐴. 𝑝𝑏ℎ𝐴. 𝑥𝐴
𝑝𝐵 = 𝑎𝐵. 𝑝𝑏ℎ𝐵. 𝑥𝐵
𝛼 𝑐à𝑛𝑔 𝑙ớ𝑛, 𝐴 𝑐à𝑛𝑔 𝑑ễ 𝑡á𝑐ℎ 𝑟𝑎 𝑘ℎỏ𝑖 𝐵, 𝛼=1 đẳng phí, không thể tách
𝛼: độ 𝑏𝑎𝑦 ℎơ𝑖 𝑡ươ𝑛𝑔 đố𝑖
Quy ước: A là cấu tử dễ bay hơi hơn
x – nồng độ pha lỏng của cấu tử dễ bay hơi hơn (A), nồng độ B = 1-x
y – nồng độ pha hơi của cấu tử dễ bay hơi hơn (A), nồng độ B = 1-y
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium) C=1-2+2=1 C=2-2+2=2
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium)
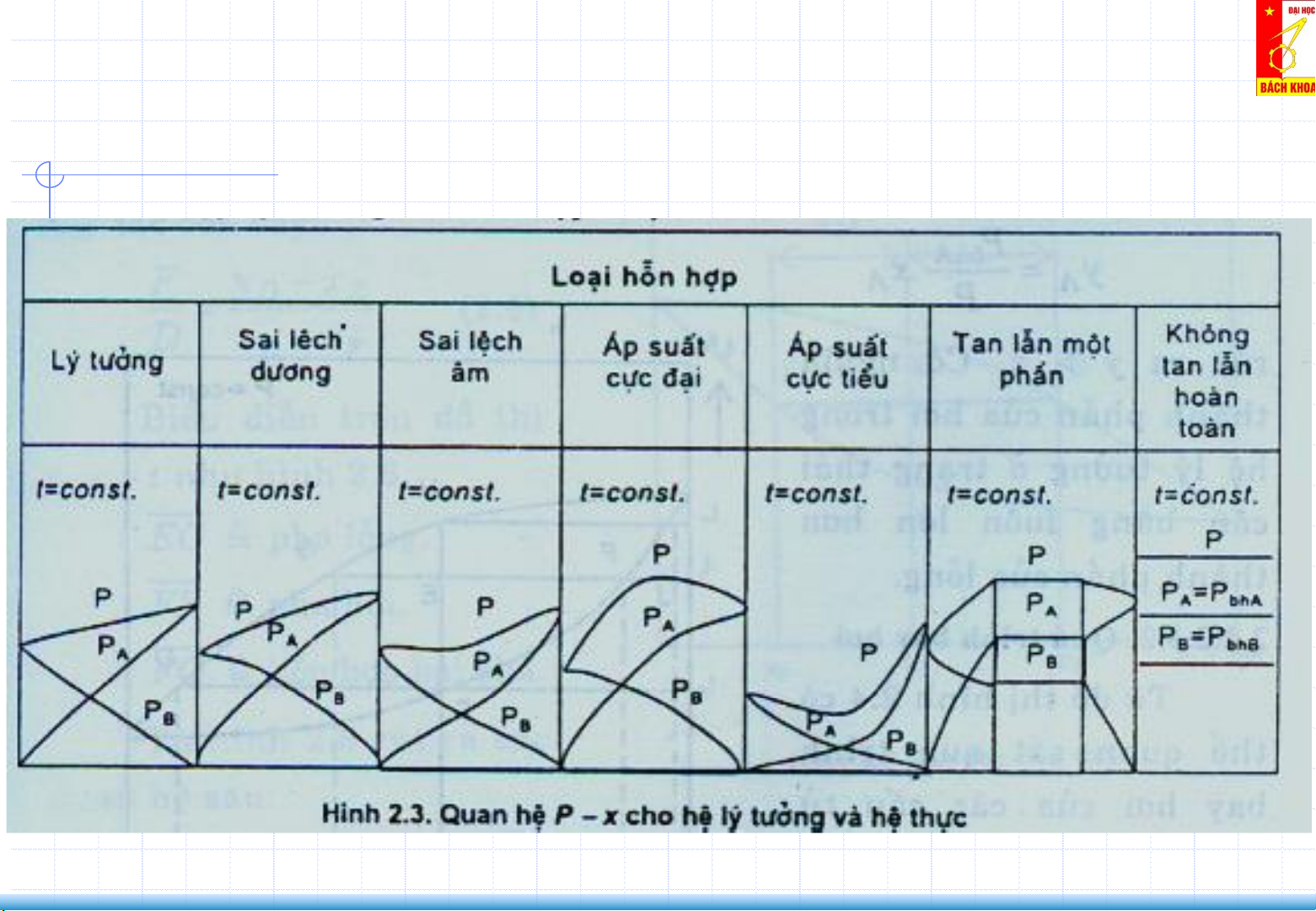
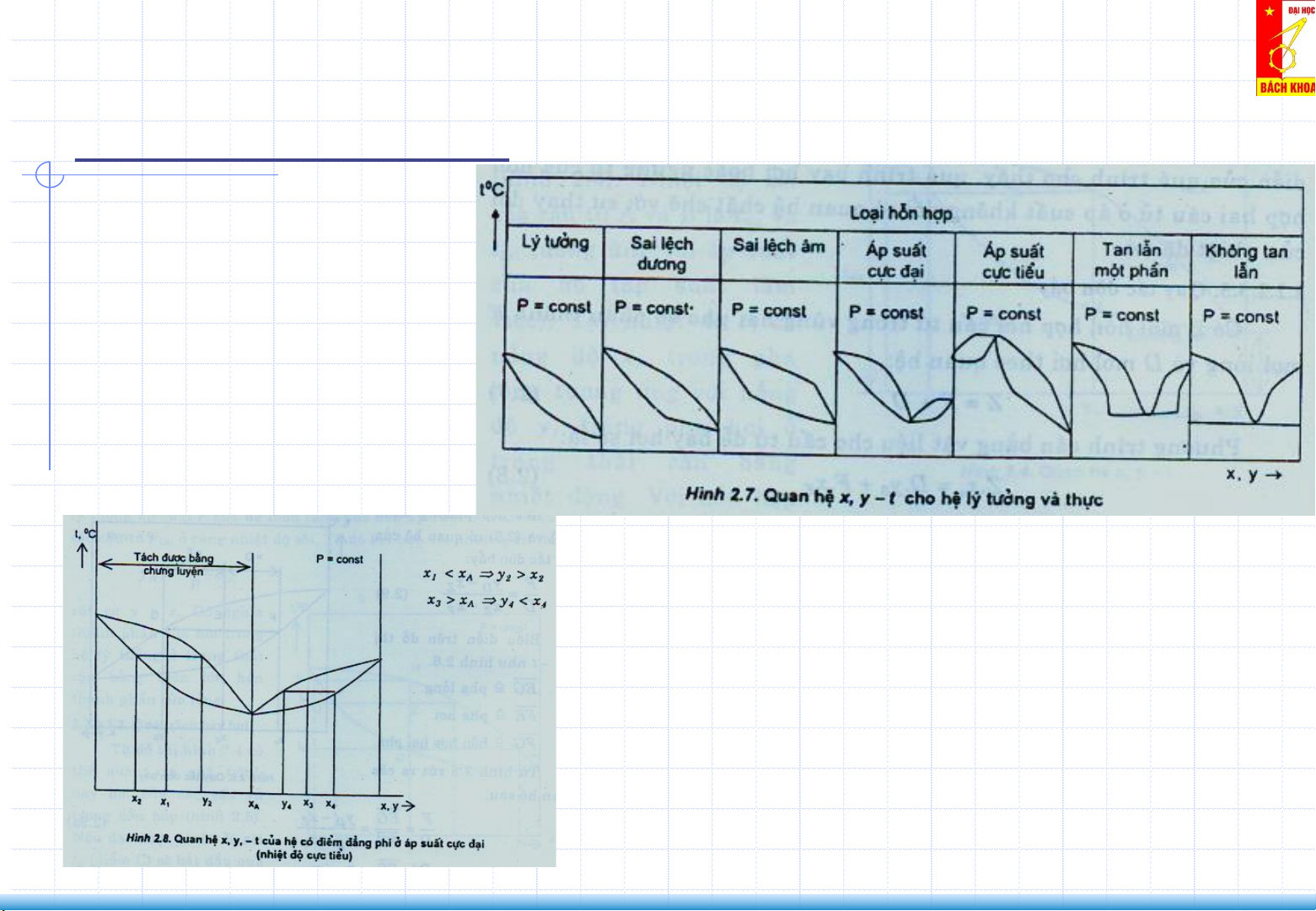
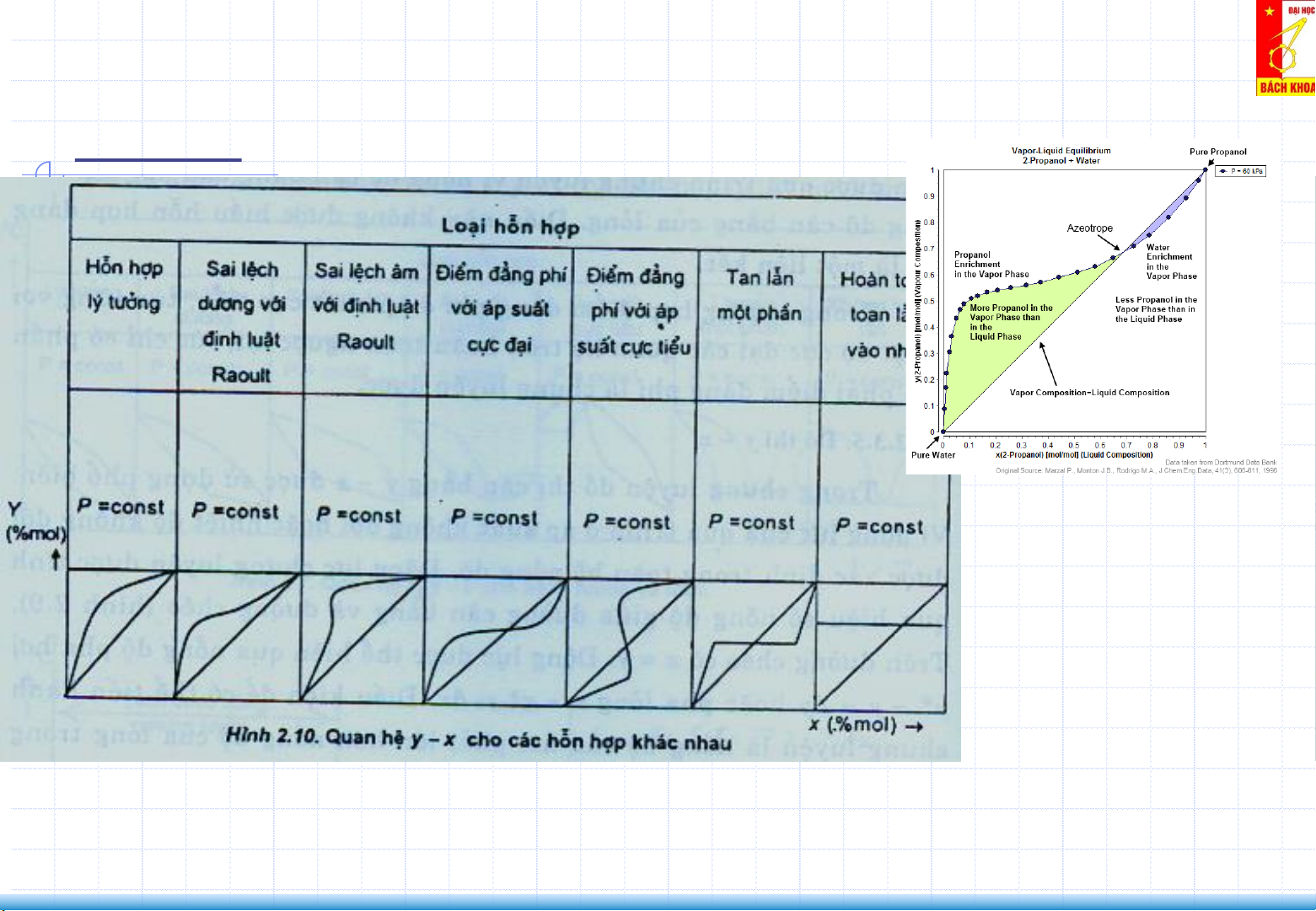
Hỗn hợp lý tưởng: Hoàn toàn ta lẫn vào nhau theo bất kỳ tỷ lệ nào Hỗn hợp thực:
- Hoàn toàn tan lẫn vào nhau, nhưng có sai lệch dương với ĐL Raoult
- Hoàn toàn tan lẫn vào nhau, nhưng có sai lệch âm với ĐL Raoult
- Hoàn toàn tan lẫn vào nhau, nhưng có tồn tại điểm đẳng phí. Tại đó áp suất
hơi đạt giá trị cực đại
- Hoàn toàn tan lẫn vào nhau, nhưng có tồn tại điểm đẳng phí. Tại đó áp suất
hơi đạt giá trị cực tiểu
- Tan lẫn một phần vào nhau
- Hoàn toàn không tan lẫn vào nhau
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
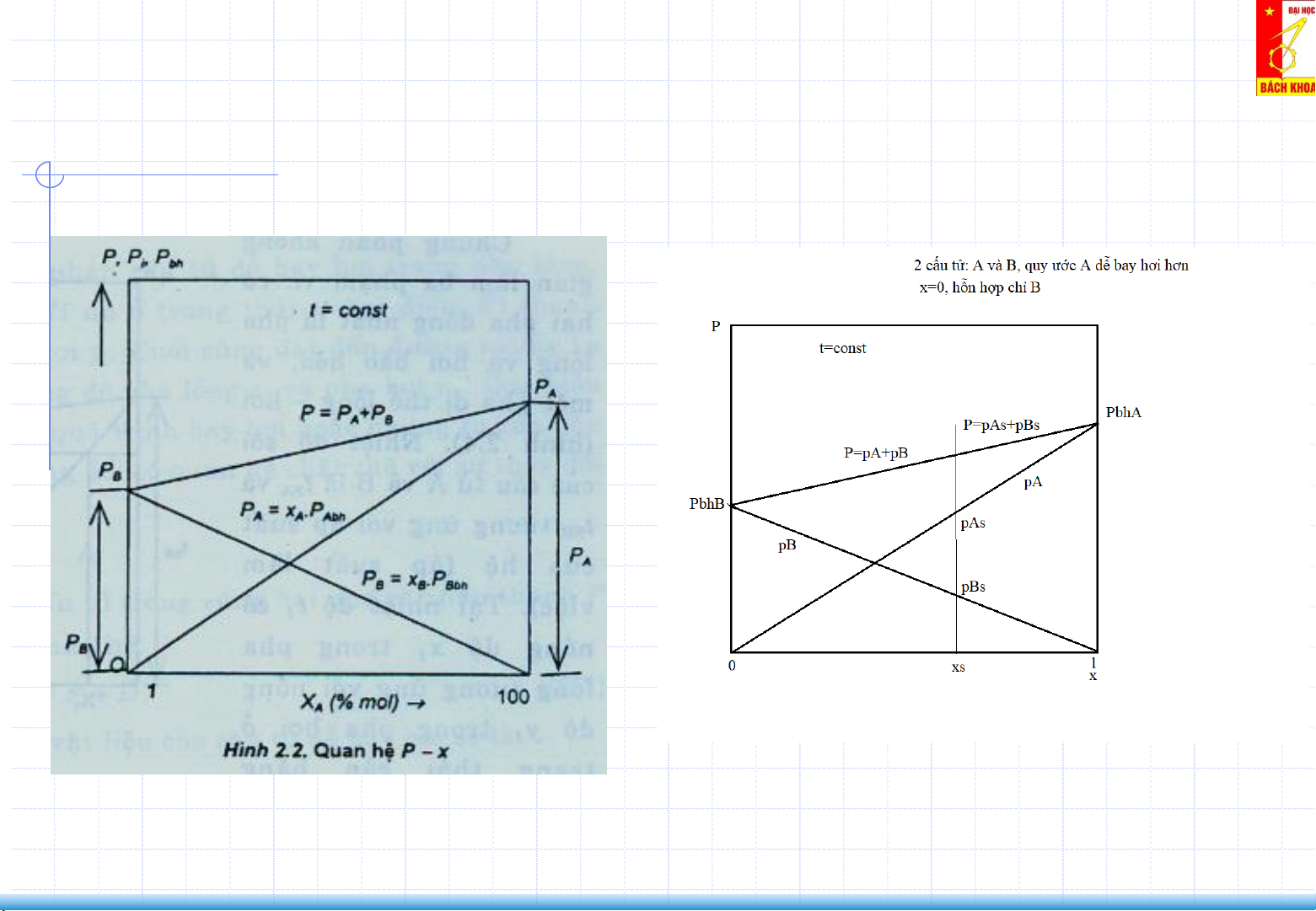
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium) Đồ thị x-p
Hỗn hợp lý tưởng: Hoàn toàn ta lẫn vào nhau theo bất kỳ tỷ lệ nào
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium) Hỗn hợp thực
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
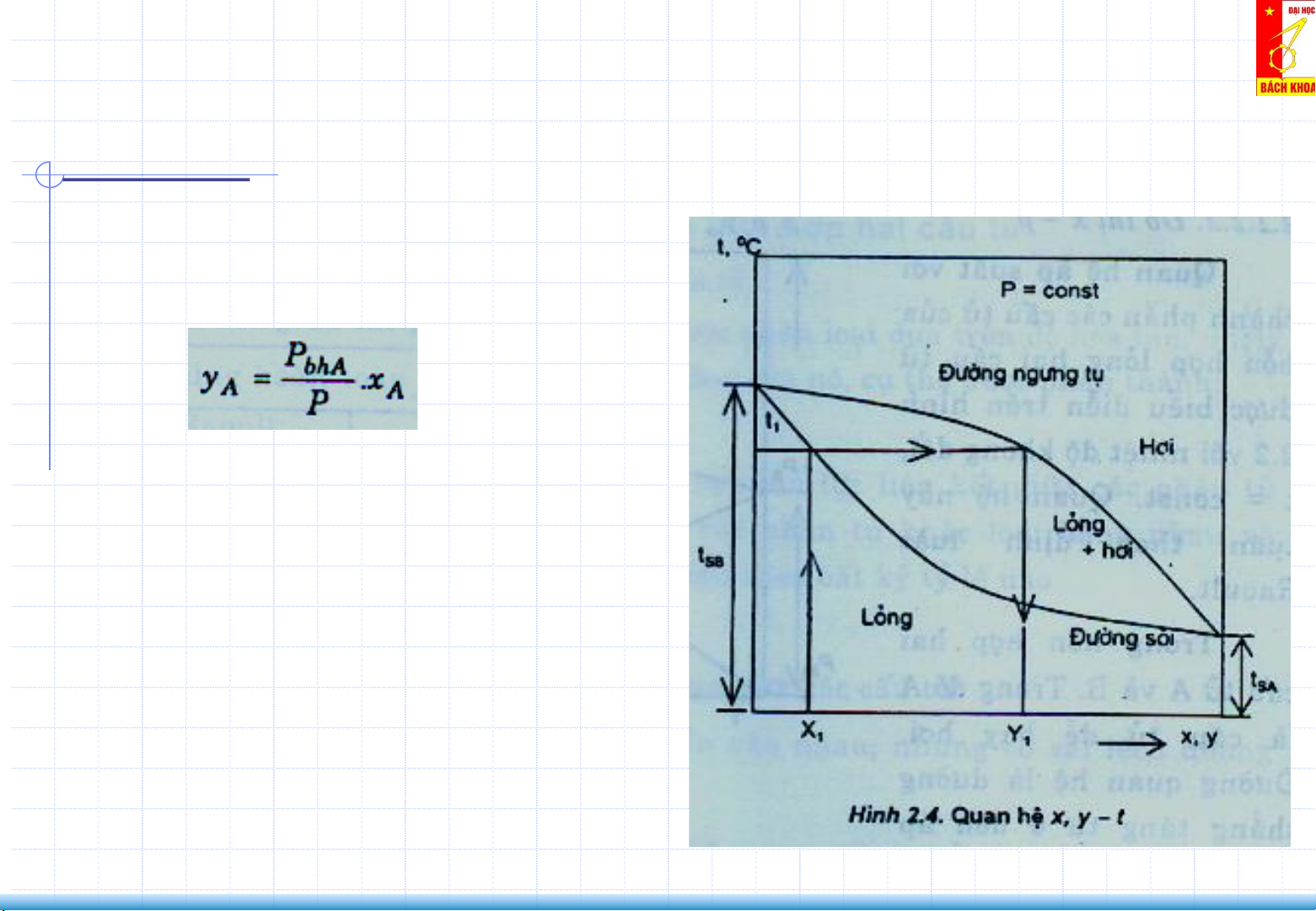
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium) Đồ thị x,y,t
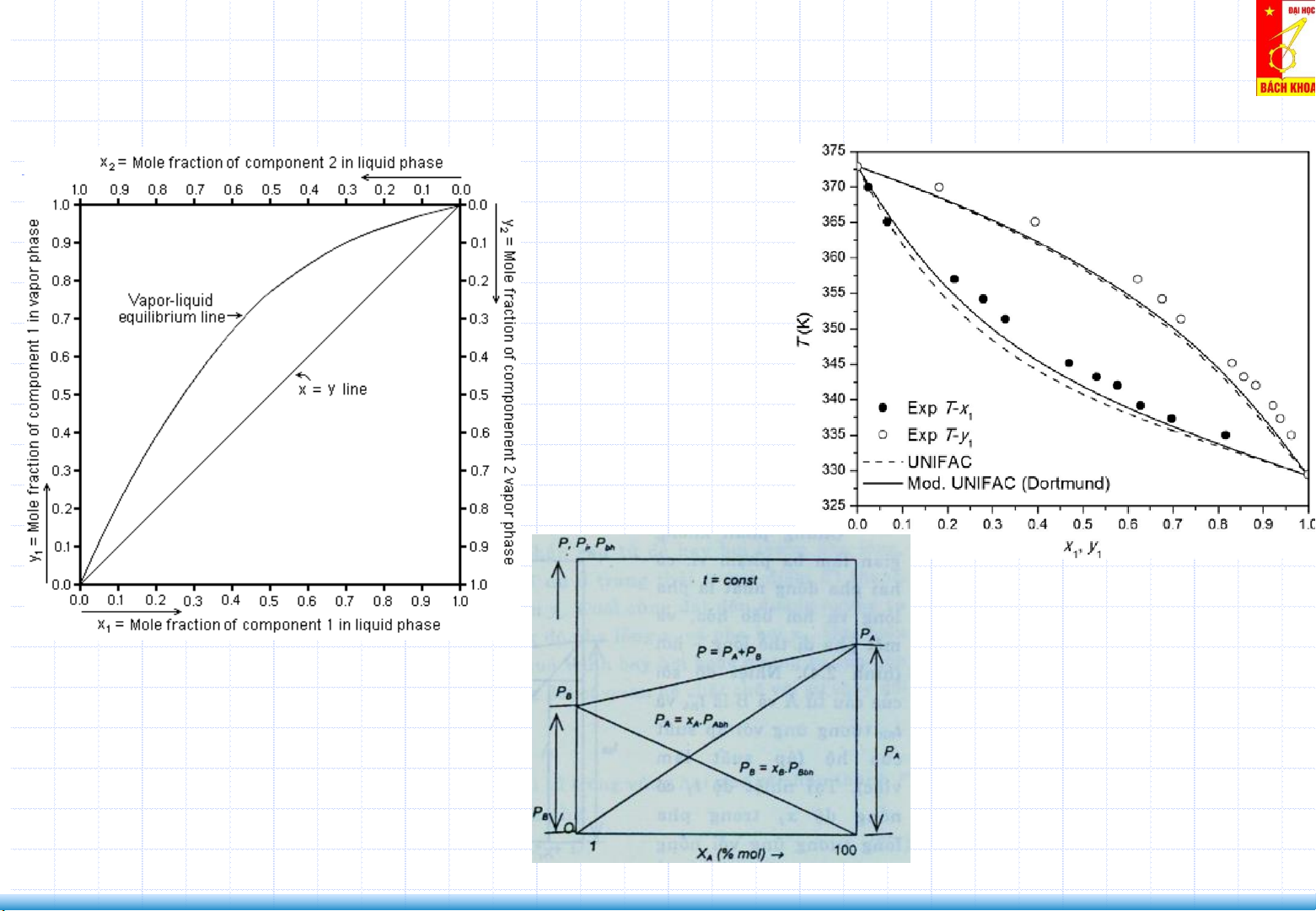
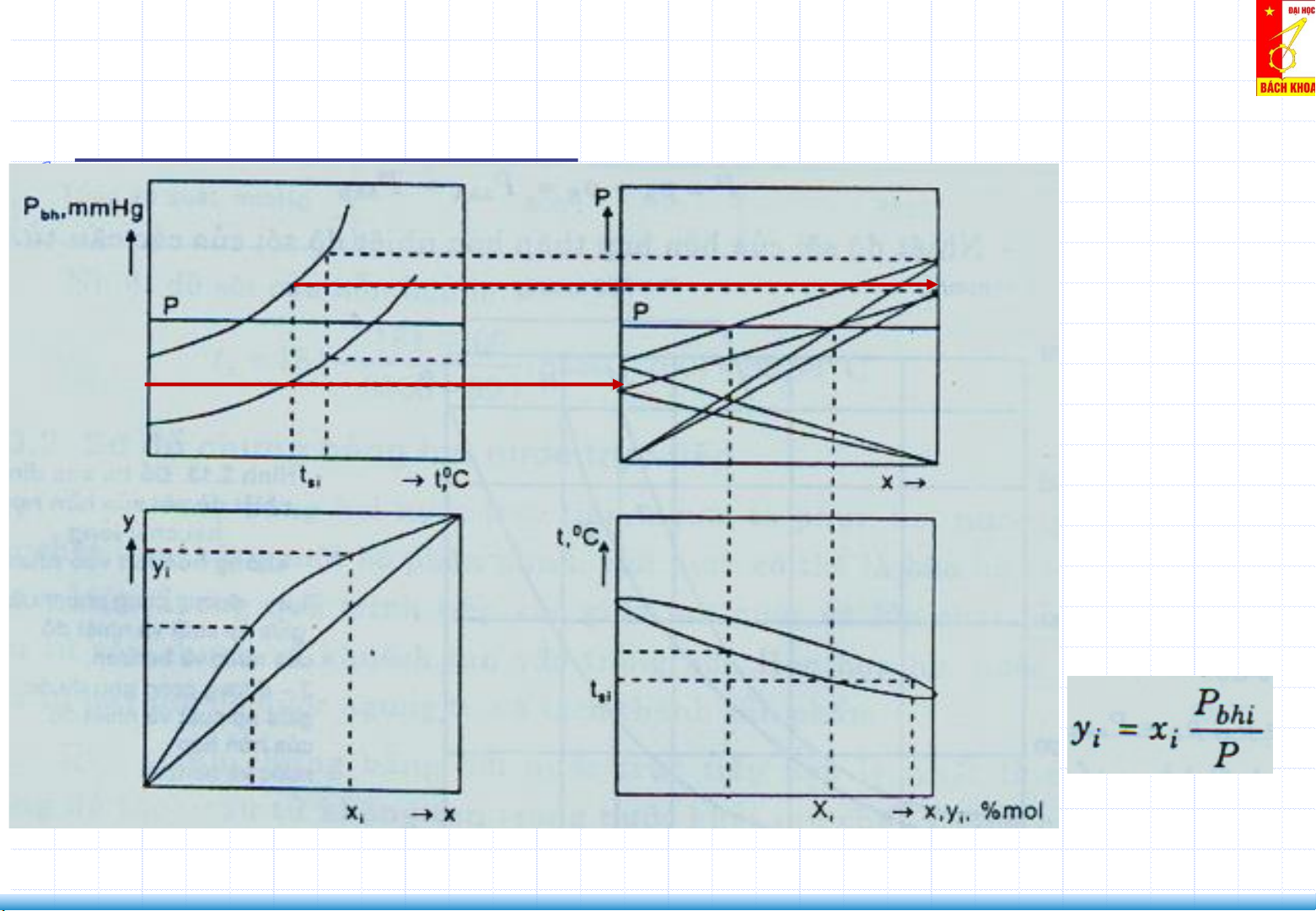
Hỗn hợp lý tưởng: Áp suất P của hệ luôn
nhỏ hơn áp suất hơi bão hòa của cấu tử
Pbhi ở cùng nhiệt độ sôi. y>x
𝑝𝐴 = 𝑃𝑏ℎ𝐴. 𝑥𝐴
𝑝𝐵 = 𝑃𝑏ℎ𝐵. 𝑥𝐵 𝑃 = 𝑝 + 𝐴 𝑝𝐵
𝑝𝐴 = 𝐴 = 𝑦𝐴. 𝑃
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium) Đồ thị x,y,t
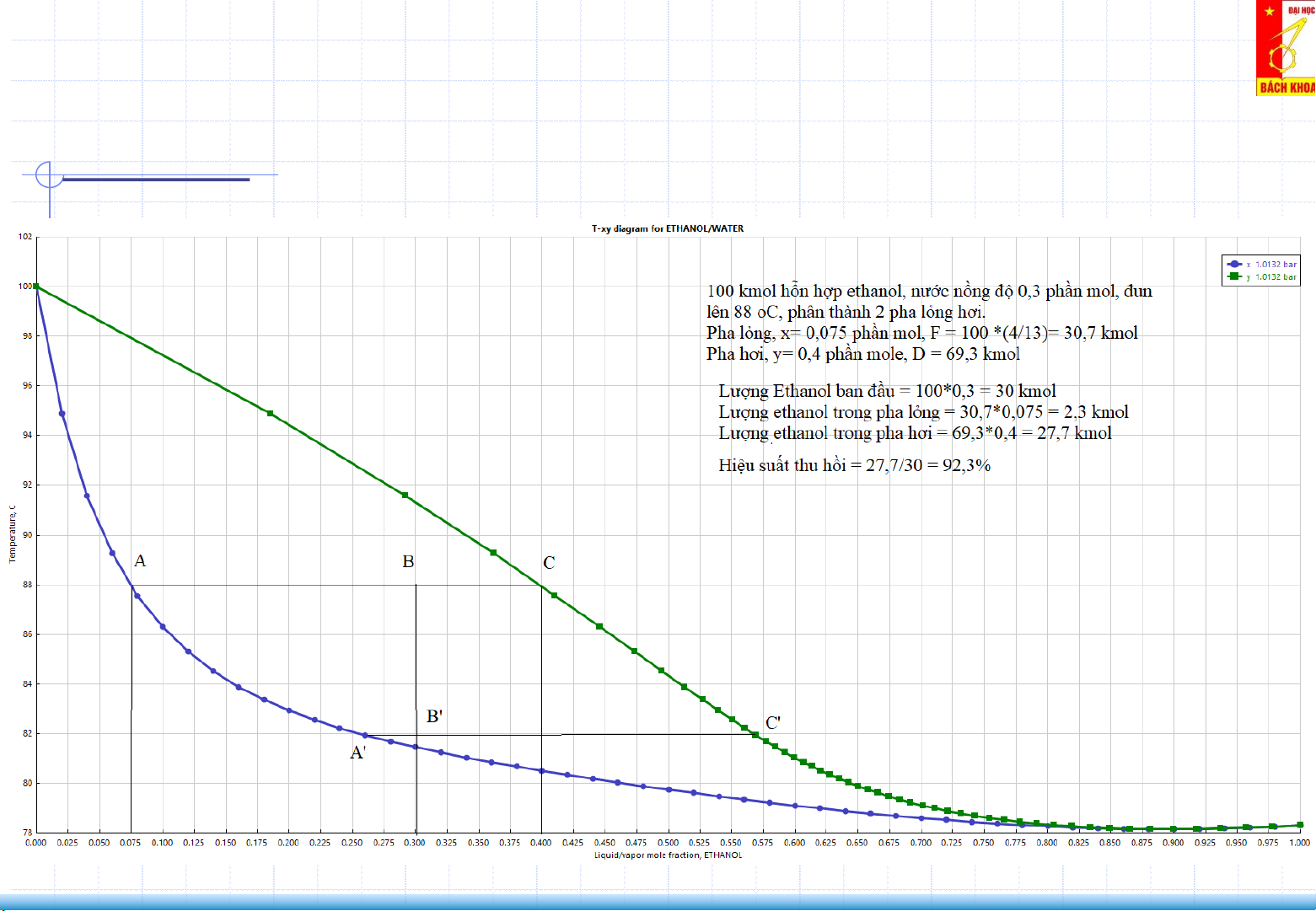
Nhiệt độ điểm sôi ts (điểm C) sẽ bắt đầu
Hỗn hợp lý tưởng: Quá trình bay hơi
quá trình bay hơi, có thành phần hơi là ys.
Thành phần cấu tử dễ bay hơi trong pha
lỏng giảm, ts tăng. Tại điểm E thành pha
lỏng xi, pha hơi yi. Cuối cùng đạt trạng thái
ngưng tụ (điểm H), nồng độ pha lỏng xt,
pha hơi là yt. Ví dụ hệ ethanol – nước
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
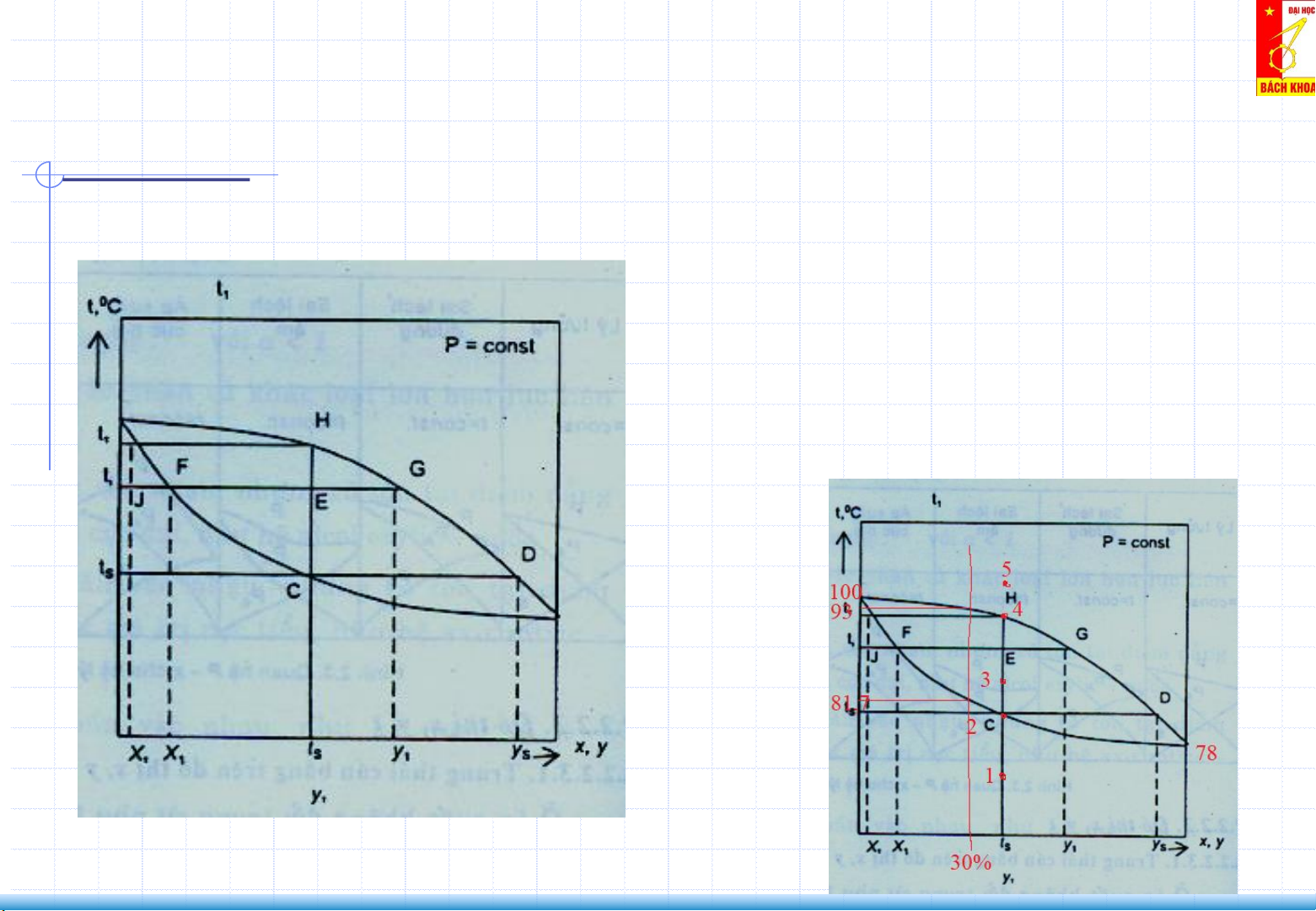
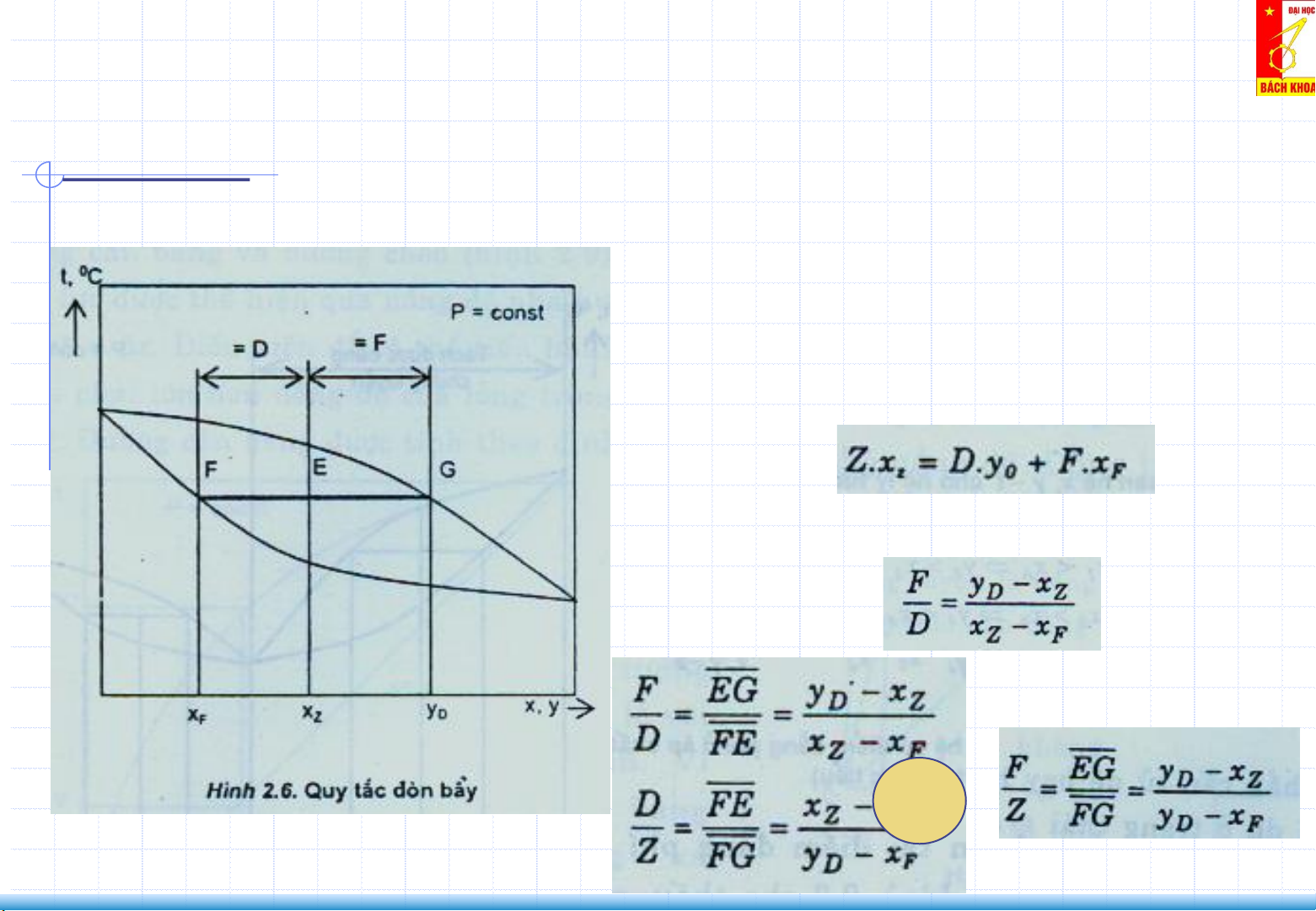
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium) Đồ thị x,y,t Quy tắc đòn bẩy
Z: mol hỗn hợp 2 cấu tử trong vùng 2 pha. F: mol lỏng D: mol hơi Z= F+D
PTCBVL cho cấu tử dễ bay hơi: Rút ra quy tắc đòn bẩy: EG: pha lỏng FE: Pha hơi FG: cả 2 pha xF
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium) Đồ thị x,y,t
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium)
Đồ thị x,y,t: hỗn hợp thực
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
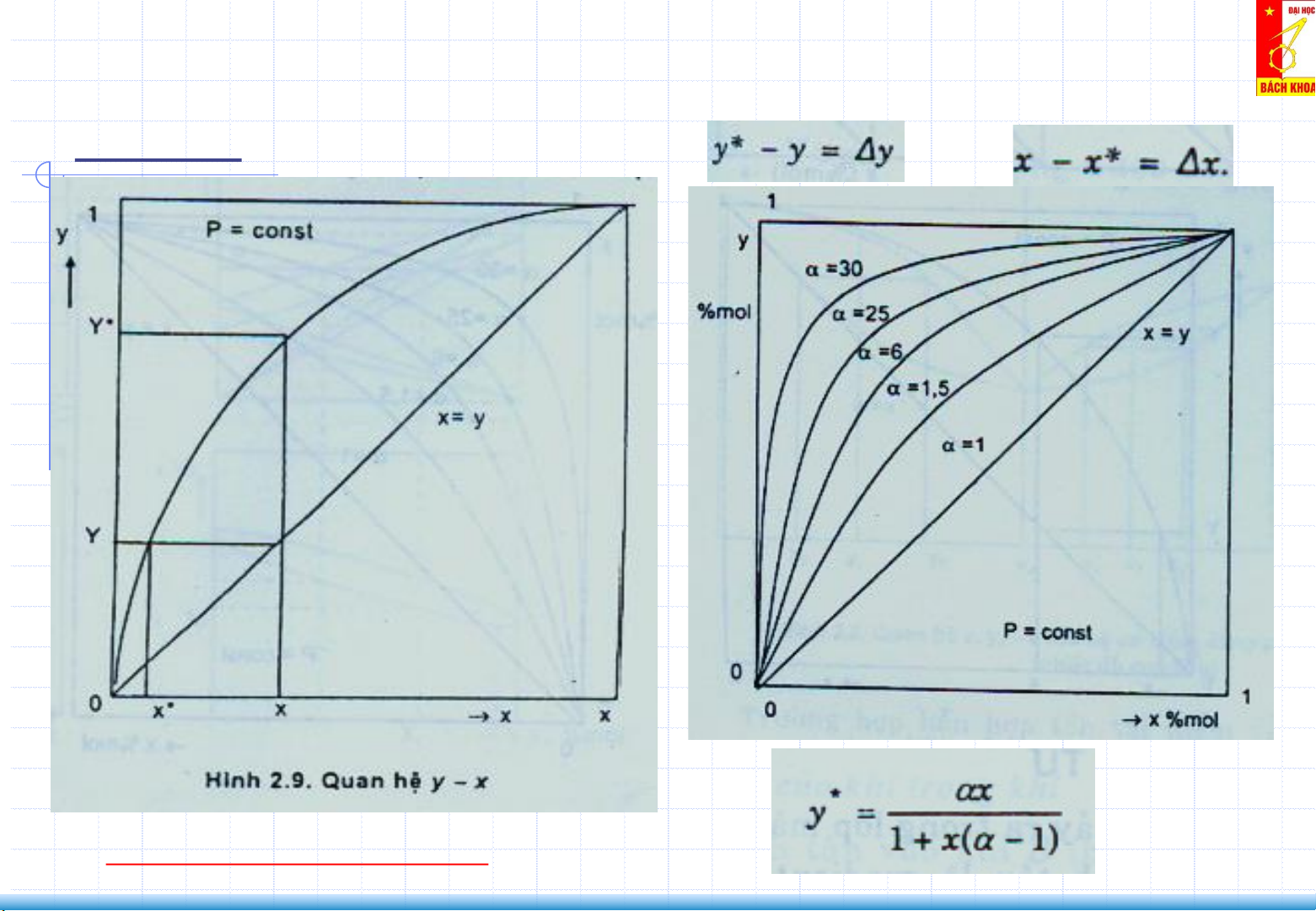
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium) Đồ thị x-y
𝜶 𝒄à𝒏𝒈 𝒍ớ𝒏, 𝒄à𝒏𝒈 𝒅ễ 𝒕á𝒄𝒉
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium) Đồ thị x-y
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
II. HỖN HỢP LỎNG 2 CẤU TỬ
2. Cân bằng lỏng – hơi của hỗn hợp 2 cấu tử (Liquid–Vapor Equilibrium)
Cách biểu thị đường cân bằng Pbhi t-x,y: cần I thành phần xi ở i nhiệt độ sôi Đường ngưng tụ:
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
III. CHƯNG BẰNG HƠI NƯỚC TRỰC TIẾP
1. Nguyên lý chưng hệ chất lỏng không hòa tan vào nhau
Hỗn hợp cấu tử không tan nhẫn vào nhau: Benzene – nước, tinh dầu – nước…
có thể tách bằng pp lắng gạn.
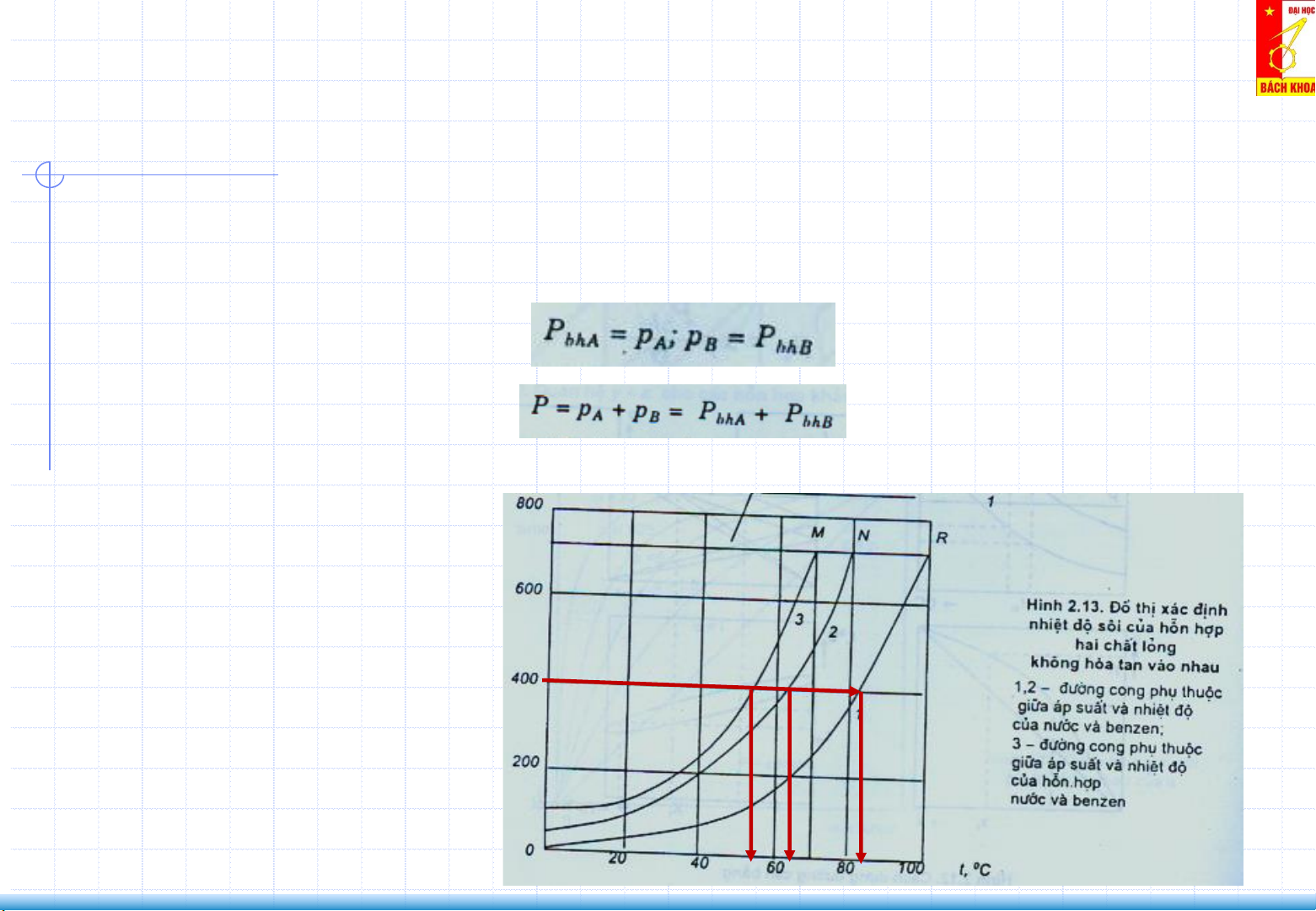
- Áp suất riêng phần của cấu tử này không phụ thuộc vào sự có mặt của cấu tử
kia trong hỗn hợp và bằng áp suất hơi bão hòa của các cấu tử nguyên chất ở cùng nhiệt độ:
- Áp suất chung của hỗn hợp:
- Nhiệt độ sôi của hỗn hợp thấp hơn nhiệt độ sôi của các cấu tử:
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)
III. CHƯNG BẰNG HƠI NƯỚC TRỰC TIẾP
1. Nguyên lý chưng hệ chất lỏng không hòa tan vào nhau
- Nhiệt độ sôi của hỗn hợp thấp
hơn nhiệt độ sôi của các cấu tử:
Ứng dụng chưng hỗn hợp có nhiệt
độ sôi cao, gồm cả cấu tử không hòa tan vào nước
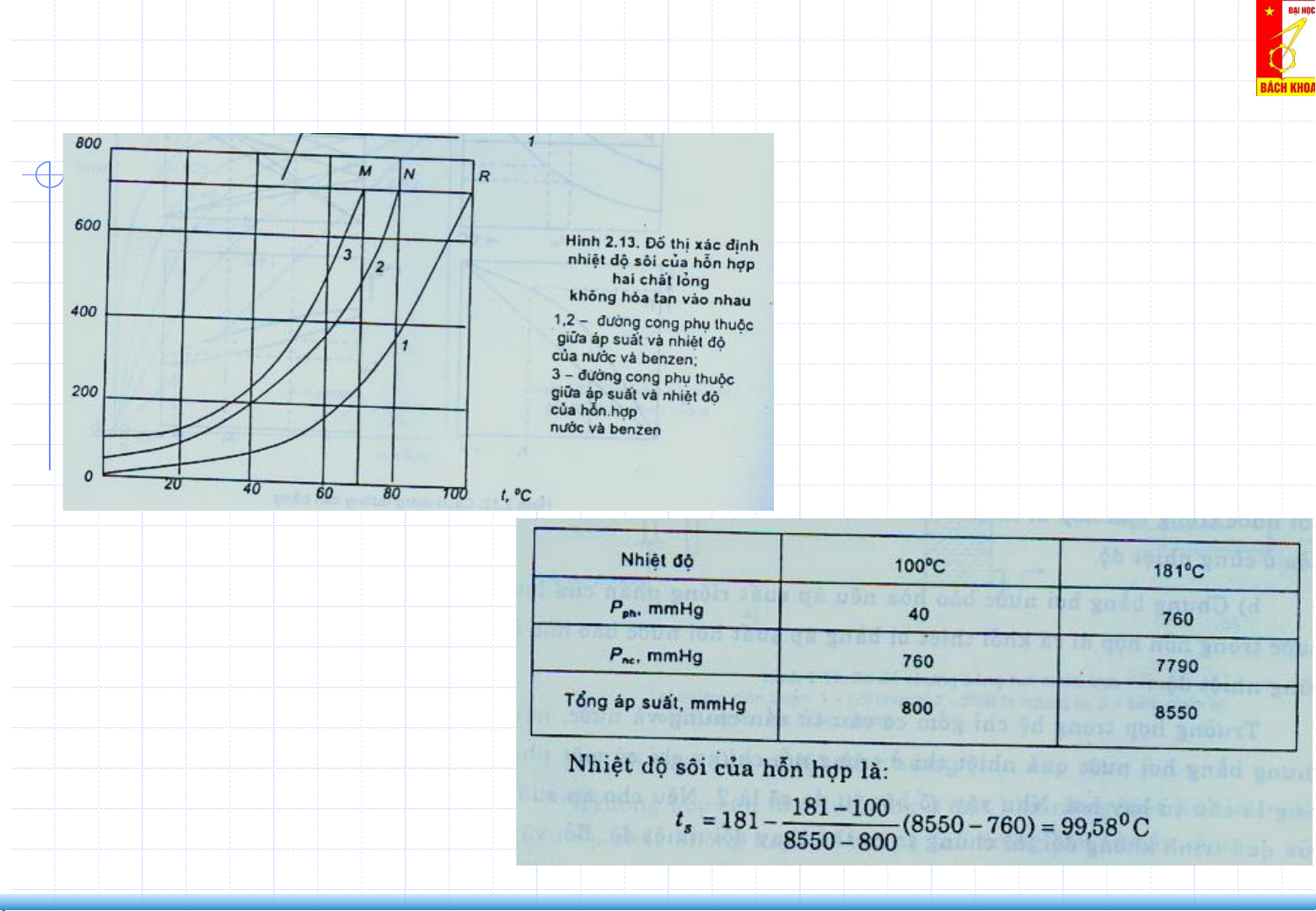
Tính nhiệt độ sôi của Hỗn hợp phenol-nước ở 760 mmHg:
- Tại 760 mmHg: nước sôi 100 oC, Phenol 181 oC.
- Tại 100 oC, PbhPhenol = 40 mmHg. - Tạo 181 oC, PbhH2O = 7790 mmHg
Quá Trình thiết bị III – Phân riêng dưới tác dụng của nhiệt (Mass transfer)