







Preview text:
lOMoAR cPSD| 58794847
TRƯỜNG ĐH SƯ PHẠM KỸ THUẬT TPHCM THÍ NGHIỆM
KHOA CÔNG NGHỆ HOÁ HỌC & THỰC PHẨM PHÂN TÍCH CÔNG CỤ
BỘ MÔN CÔNG NGHỆ HOÁ HỌC
BÁO CÁO THÍ NGHIỆM BÀI 5
XÁC ĐỊNH HỖN HỢP CAFFEIN VÀ PARACETAMOL TRONG
MẪU DƯỢC PHẨM BẰNG HPLC-UV
Ngày thí nghiệm: 06/05/2025 ĐIỂM Lớp: 23128CL2A Nhóm: 02 Tên: Lê Tấn Tài MSSV: 23128055 CHỮ KÝ GVHD
I. NGUYÊN TẮC 1. Giới thiệu về Paracetamol, Caffein và lý do phải xác định
Paracetamol và Caffein trong viên thuốc Panadol
Paracetamol: Paracetamol (còn gọi là acetaminophen) là một hoạt chất giảm đau và hạ sốt
phổ biến, được sử dụng rộng rãi trong điều trị các triệu chứng như đau đầu, đau răng, đau cơ,
sốt do cảm cúm hay nhiễm khuẩn. Nó thuộc nhóm thuốc không steroid nhưng không có tác
dụng chống viêm rõ rệt như các NSAIDs (ví dụ: ibuprofen).
Tác dụng của Paracetamol:
• Giảm đau: Paracetamol làm giảm cảm giác đau bằng cách ức chế enzym cyclooxygenase
(COX), ảnh hưởng đến quá trình tạo ra prostaglandin – chất trung gian gây đau.
• Hạ sốt: Hoạt chất này tác động lên trung tâm điều nhiệt ở vùng dưới đồi của não, giúp hạ
thân nhiệt khi cơ thể sốt.
Paracetamol thường dùng cho cả người lớn và trẻ em (với liều lượng điều chỉnh phù hợp).
Phù hợp cho những người không dung nạp NSAIDs hoặc có vấn đề dạ dày, tim mạch (do ít gây
kích ứng niêm mạc dạ dày hơn các thuốc khác).
Khi sử dụng Paracetamol quá liều có thể gây tổn thương gan nghiêm trọng, thậm chí suy gan
cấp, đặc biệt ở liều trên 4 gram/ngày ở người lớn. Ngoài ra, người bị bệnh về gan không nên lOMoAR cPSD| 58794847
dùng paracetamol vì có nguy cơ cao hơn với tổn thương gan dù dùng liều bình thường. Hơn
nữa, paracetamol có thể tương tác với rượu, thuốc chống co giật, thuốc chống lao... làm tăng độc tính trên gan.
Caffein: Caffein là một chất kích thích thần kinh trung ương thuộc nhóm xanthine, thường
có trong cà phê, trà, nước tăng lực và chocolate. Trong y học, Caffein còn được kết hợp trong
một số thuốc để tăng hiệu quả giảm đau. Caffein có tác dụng:
• Kích thích hệ thần kinh: Giúp tỉnh táo, giảm buồn ngủ, tăng tập trung.
• Tăng hiệu quả thuốc giảm đau: Khi kết hợp với Paracetamol hoặc Aspirin, Caffein có thể
tăng cường tác dụng giảm đau.
• Tăng tuần hoàn máu não: Hữu ích trong điều trị đau đầu, đặc biệt là đau đầu do co mạch.
Một số sản phẩm chứa Caffein: Cà phê, trà, nước ngọt có ga (cola), nước tăng lực. Một số
thuốc trị đau đầu, cảm cúm, thuốc giảm đau kết hợp.
Tuy nhiên, khi sử dụng Caffein quá mức có thể gây ra một số triệu chứng như mất ngủ, lo
âu, hồi hộp, đánh trống ngực. Tăng huyết áp, rối loạn tiêu hóa. Dùng lâu dài có thể dẫn đến lệ
thuộc hoặc hội chứng cai Caffein khi ngừng sử dụng.
Lý do xác định: Việc xác định chính xác hàm lượng hai hoạt chất này là cần thiết để:
• Đảm bảo an toàn cho người sử dụng: Cả Paracetamol và Caffein đều có giới hạn liều dùng
an toàn. Việc xác định rõ hàm lượng giúp tránh quá liều, đặc biệt khi người bệnh dùng nhiều
sản phẩm chứa các hoạt chất này cùng lúc.
• Tối ưu hóa hiệu quả điều trị: Lượng Caffein cần được xác định chính xác để tăng cường hiệu
quả giảm đau mà không gây tác dụng phụ không mong muốn.
• Đáp ứng yêu cầu quản lý dược: Đây là yêu cầu bắt buộc của cơ quan quản lý thuốc nhằm
đảm bảo chất lượng và sự nhất quán trong sản phẩm dược phẩm.
• Hỗ trợ bác sĩ và dược sĩ trong kê đơn, tư vấn sử dụng thuốc hợp lý, tránh tương tác và hạn
chế tác dụng không mong muốn. 2.
3. Xác định Paracetamol và Caffein bằng HPLC
• Mẫu (viên thuốc Panadol) được hòa tan và lọc sạch để loại tạp chất không tan.
• Mẫu dung dịch được đưa vào hệ thống HPLC. lOMoAR cPSD| 58794847
• Trong cột HPLC, các thành phần trong mẫu sẽ di chuyển với tốc độ khác nhau do có
tính phân cực và ái lực khác nhau với pha tĩnh, nên được tách ra tại các thời điểm khác
nhau (thời gian lưu khác nhau).
• Detector UV sẽ ghi nhận tín hiệu tại bước sóng phù hợp.
• So sánh diện tích peak (diện tích dưới đường cong) của mẫu với chuẩn để tính ra hàm lượng. II.NỘI DUNG
1. Chuẩn bị dung môi pha động
Nước cất HPLC
- Lọc nước cất 2 lần với màng lọc 0.45 μm, sau đó, chiết ra bình chứa rồi cho vào bể
siêu âm để đuổi khí trong 35 phút. MeOH HPLC
- Chiết MeOH ra bình chứa, sau đó, cho vào bể siêu âm để đuổi khí tầm 15 phút 2. Chuẩn bị mẫu
Dung dịch chuẩn gốc
-Chuẩn gốc 500mL Caffein 100ppm lOMoAR cPSD| 58794847 Cân 0.05g Hòa tan chất rắn Cho vào fiol mL mL Lắc đều Dung dịch caffeine 100 ppm
- Chuẩn gốc 500ml paracetamol 100ppm lOMoAR cPSD| 58794847 Cân 0.05g Hòa tan chất rắn Cho vào fiol mL mL Lắc đều Dung dịch paracetamol 100ppm
• Dung dịch làm việc
+ Chuẩn hỗn hợp (A): 100ml hỗn hợp 10ppm CAF & 2.5ppm PAR
𝐻ú𝑡 10 𝑚𝑙 𝑝𝑎𝑟 và 2 mL 𝑐𝑎𝑓 𝑡ừ 𝑐ℎ𝑢ẩ𝑛 𝑔ố𝑐 Cho vào bình fiol 100ml Đong lên 100ml bằng nước cất 2 lần. lOMoAR cPSD| 58794847
+ Chuẩn hỗn hợp (B): 100ml CAF 10ppm
Hút 10ml CAF từ chuẩn gốc Cho vào bình fiol 100ml Định mức lên 100ml bằng nước cất 2 lần.
+ Chuẩn hỗn hợp (C): 100ml PAR 2.5ppm
Hút 2.5ml PAR từ chuẩn gốc Cho vào fiol 100ml Định mức lên 100ml bằng nước cất 2 lần.
• Dung dịch dãy chuẩn Viết nhãn Blank STD1 STD2 STD3 STD4 STD5 Nồng độ CAF: 0 CAF: 1 CAF: 2 CAF: 5 CAF: 10 CAF: 20 dãy chuẩn PAR: 0 PAR: 1 PAR: 2 PAR: 5 PAR: 10 PAR: 20 Định mức
Định mức với vạch 100 mL bằng nước cất 2 lần
3. Khảo sát hệ dung môi
- Dùng chuẩn hỗn hợp A để khảo sát pha động tại 𝜆 = 263𝑛m MeOH H2O 50 50 60 40 70 30 lOMoAR cPSD| 58794847 Lưu ý:
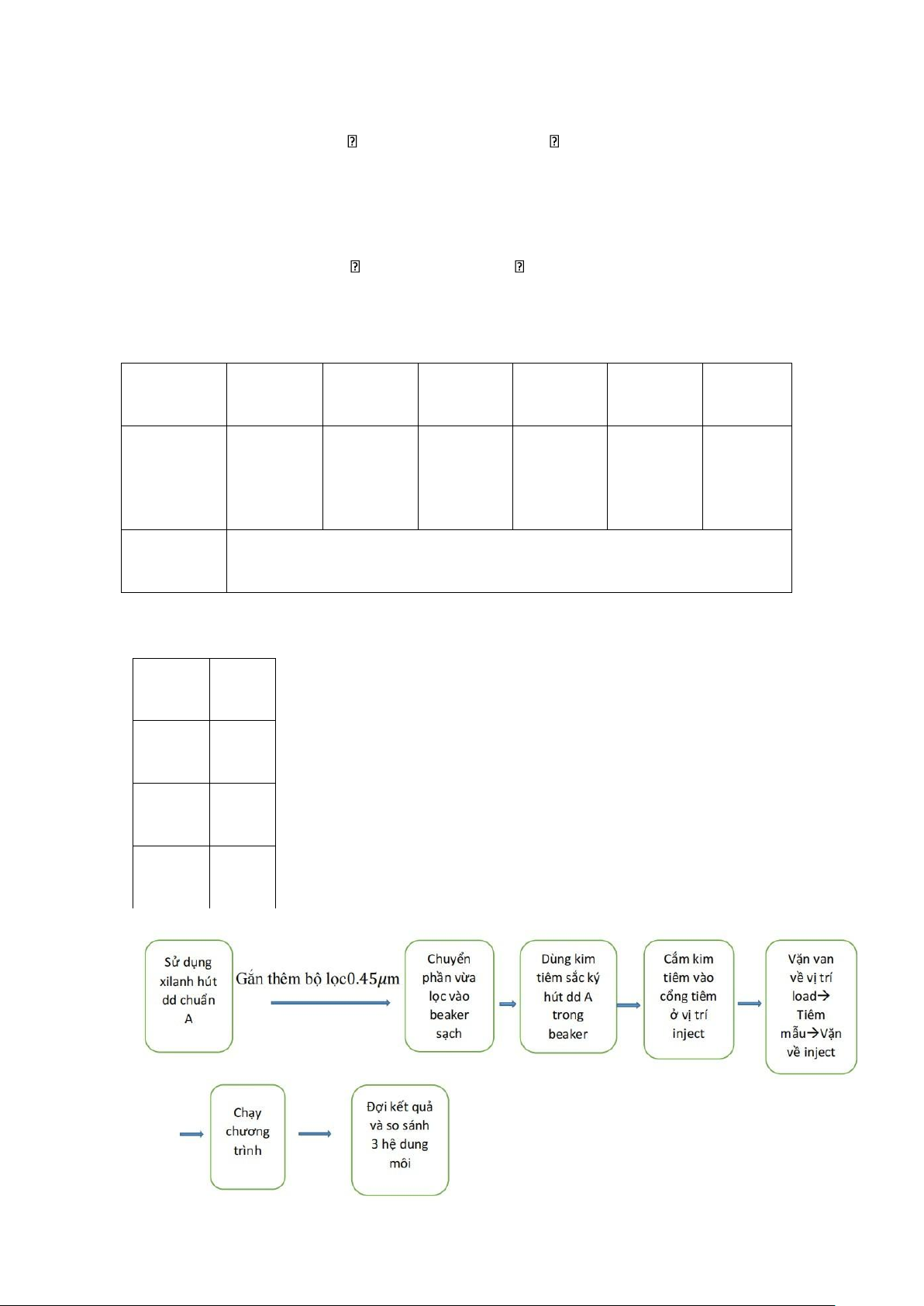
- Phải tráng rửa thật kỹ becher và xlanh bằng hệ dung dịch chuẩn A.
- Không sử dụng những kim tiêm có đầu nhọn( vì có thể đâm thủng màng seal)
- Trước khi tiêm phải kiểm tra xem trong kim tiêm có bọt khí hay không.
- Không nên hút quá nhiều lượng mẫu vì có thể kim tiêm bị cong.
4. Định danh Peak và khảo sát bước sóng -
Tiến hành chuẩn đơn B (Caffein): 272 nm.
- Tiến hành chuẩn đơn C (Paracetamol): 207 nm.
- So sánh thời gian lưu của chuẩn hỗn hợp A và chuẩn đơn B, C.
5. Xây dựng phương trình hồi quy tuyến tính.
Chạy dãy chuẩn với hệ dung môi đã khảo sát được Xác định 𝑡, 𝑅 𝑣à 𝑆 Sử dụng Excel để sử
vẽ đường chuẩn bằng đường hồi quy.
6. Phân tích mẫu chưa biết tỉ lệ
Nhận hỗn hợp Caffein và Paracetamol từ nhóm 02, tiến hành chạy mẫu với hệ dung môi đã
chọn. Ghi nhận kết quả rồi dùng kỹ thuật đường chuẩn và một chuẩn để xác định nồng độ có
trong mẫu cần phân tích. So sánh kết quả của hai phương pháp và nhận xét III. THỰC HÀNH 1. 2. Dụng cụ: Dụng cụ Số lượng Fiol 25mL 5 Fiol 100mL 2 Becher 2 Pipette 5 Ống tiêm mẫu 1 lOMoAR cPSD| 58794847 Máy HPLC 1 Máy siêu âm 1 3.
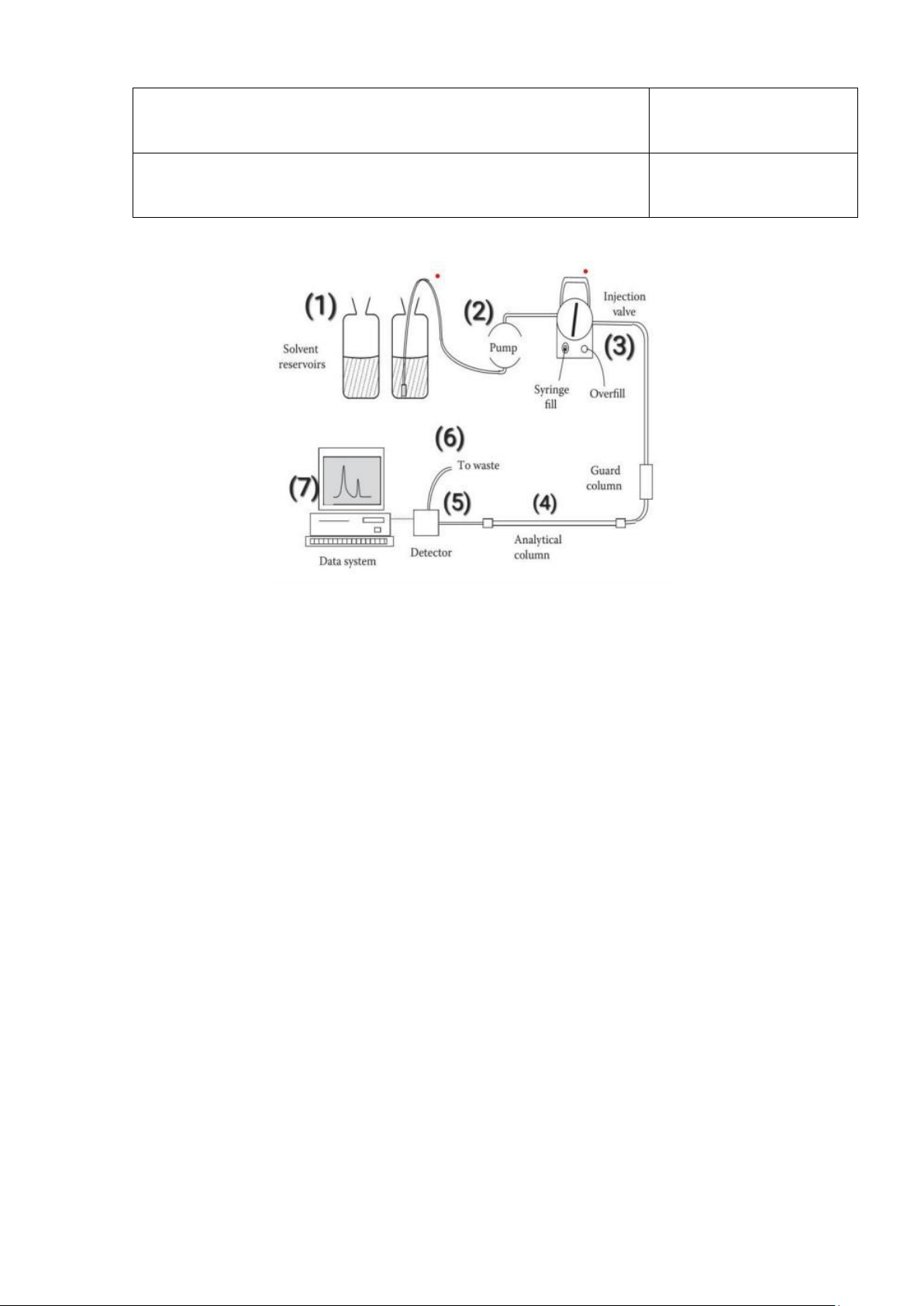
Cấu tạo máy HPLC và cột sắc kýCấu tạo máy:
Hình 1. Cáu tạo chung của máy HPLC (1) Bình dung môi
(2) Bơm – bộ phận phân phối dung môi (3) Bộ tiêm mẫu (4) Cột sắc ký (5) Đầu dò-Detector (6) Bình thải
(7) Thiết bị ghi nhận dữ liệu lOMoAR cPSD| 58794847
Hình 2.Hình ảnh máy HPLC thực tế
Thông tin cột sắc ký
Tên sản phẩm: CỘT SẮC KÝ COSMOSIL 5C18-AR-II Model: 5C18-AR-II
Hãng sản xuất: Nacalai Tesque Inc. (Nhật Bản) Kích thước cột: Đường kính trong: 4.6mm Chiều dài cột: 250mm
Hình 3. Thông tin cột sắc ký lOMoAR cPSD| 58794847 4. Hoá chất
ST Tên Hóa chất Nồng độ T 1 Mẫu thuốc 2 Paracetamol 1171 ppm 3 Caffein 1040 ppm 4 Nước cắt 5 Methanol 5. Thực nghiệm
Chuẩn bị dung dịch chuẩn gốc
- Điều chế dung dịch caffein 100ppm( nồng độ thực tế là 104ppm) từ dung dịch caffein
1000ppm ( nồng độ thực tế là 1040ppm) bằng cách hút ra 10ml dung dịch caffein 1000ppm (
nồng độ thực tế là 1040ppm) vào bình định mức 100ml rồi định mức lên 100ml.
- Điều chế dung dịch paracetamol 100ppm( nồng độ thực tế là 117ppm) từ dung dịch caffein
1000ppm ( nồng độ thực tế là 1171ppm) bằng cách hút ra 10ml dung dịch caffein 1000ppm (
nồng độ thực tế là 1171ppm) vào bình định mức 100ml rồi định mức lên 100ml. Chuẩn bị mẫu
- Điều chế mẫu thuốc: sử dụng 1 viên thuốc sau đó nghiền mịn. Cân lấy 0,5g ( khối lượng
thực tế lấy được là 0.5034g) sau đó hòa tan trong 20ml Methanol và lọc lại để tránh bị thất
thoát. Sau khi lọc xong tiến hành đánh siêu âm. Hút lấy 2ml dung dịch định mức lên 100ml.
Tiếp tục từ dung dịch vừa định mức hút 1ml định mức lên 25ml. Tổng cộng chúng ta sẽ pha loãng 1250 lần. IV.
KẾT QUẢ THỰC NHIỆM 1. Khảo sát hệ dung môi Hệ khảo sát Hình ảnh Nhận xét (MeOH:H2O) lOMoAR cPSD| 58794847 80:20 Ta có thể thấy 2 peak trong hệ dung môi này không tách với nhau => Loại 70:30 Ta thấy 2 peak tách hoàn toàn khỏi nhau và thời gian lưu tr quá dài => Chọn 50:50 Với hệ dung môi này, 2 peak tách hoàn toàn khỏi nhau nhưng thời gian lưu dài => Loại
2. Định danh peak và khảo sát bước sóng Kết quả đo Nhận xét lOMoAR cPSD| 58794847 Định danh Ta thấy thời gian Caffein lưu tR của Caffein (tR1) và Paracetamol (tR2) lần lượt là: tR1=3.442 phút tR2=3.15 phút Định danh Trong hỗn hợp ta có Paracetamol thời gian lưu của peak 1 và peak 2 là: tR1= 3.017 phút tR2= 3.483 phút Vậy thứ tự rửa giải Định danh là paracetamol đến hỗn hợp Caffein
3. Xây dựng đường hồi quy tuyến tính a. Kết quả khảo sát Caffein STT Mẫu
Nồng độ (ppm) Diện tích peak 1 STĐ 1 1.171 1958 2 STĐ 2 2.342 4131 3 STĐ 3 5.855 8572 4 STĐ 4 11.71 18857 lOMoAR cPSD| 58794847 5 STĐ 5 23.42 41753
Xây dựng đường chuẩn
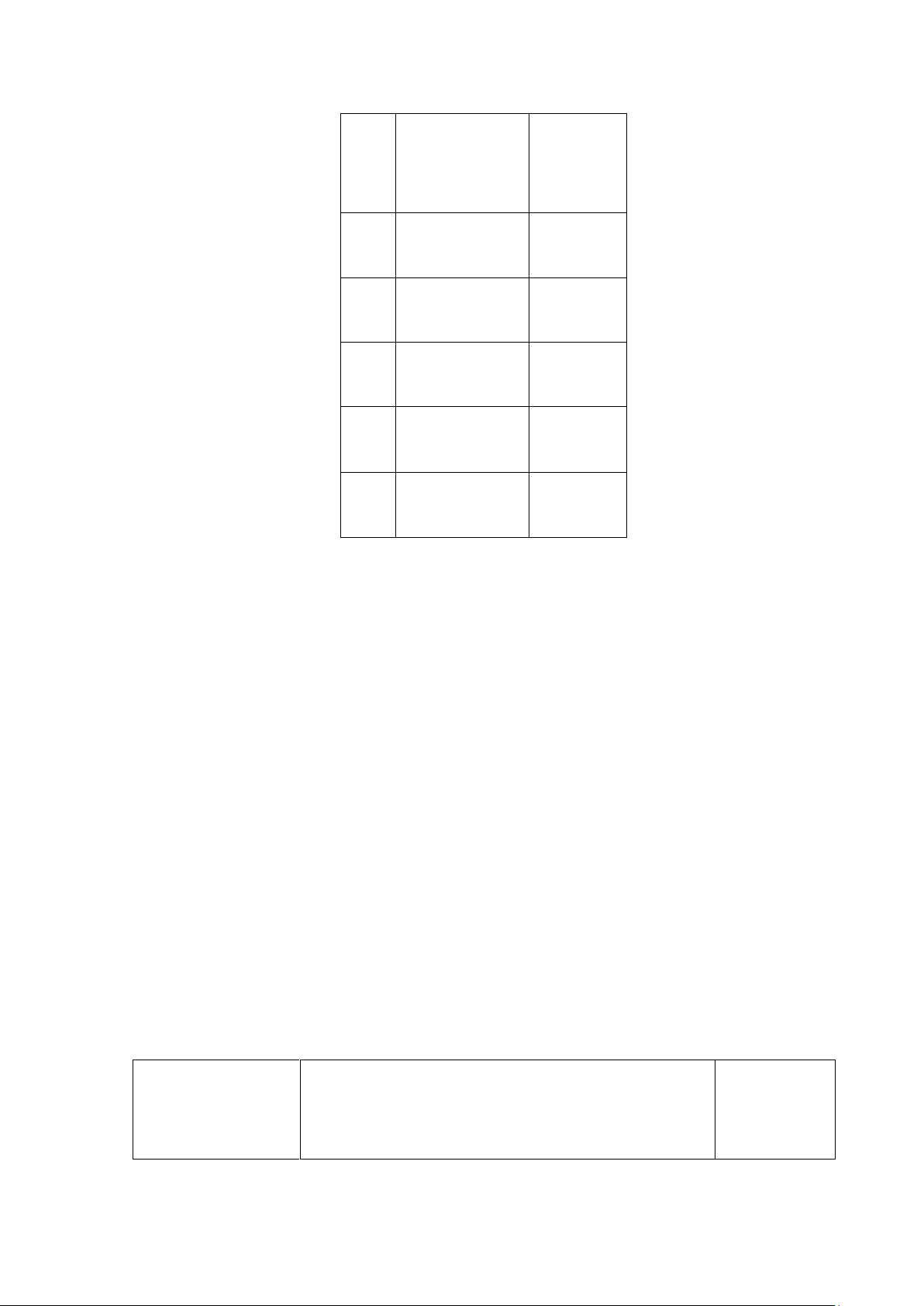
Hình 4. Đồ thị đường chuẩn S=f(C) của Caffein
b. Kết quả khảo sát Paracetamol STT Mẫu
Nồng độ (ppm) Diện tích peak 1 STĐ 1 1.04 2929 2 STĐ 2 2.08 6353 3 STĐ 3 5.2 14218 4 STĐ 4 10.4 31025 5 STĐ 5 20.8 66486 lOMoAR cPSD| 58794847
Xây dựng đường chuẩn
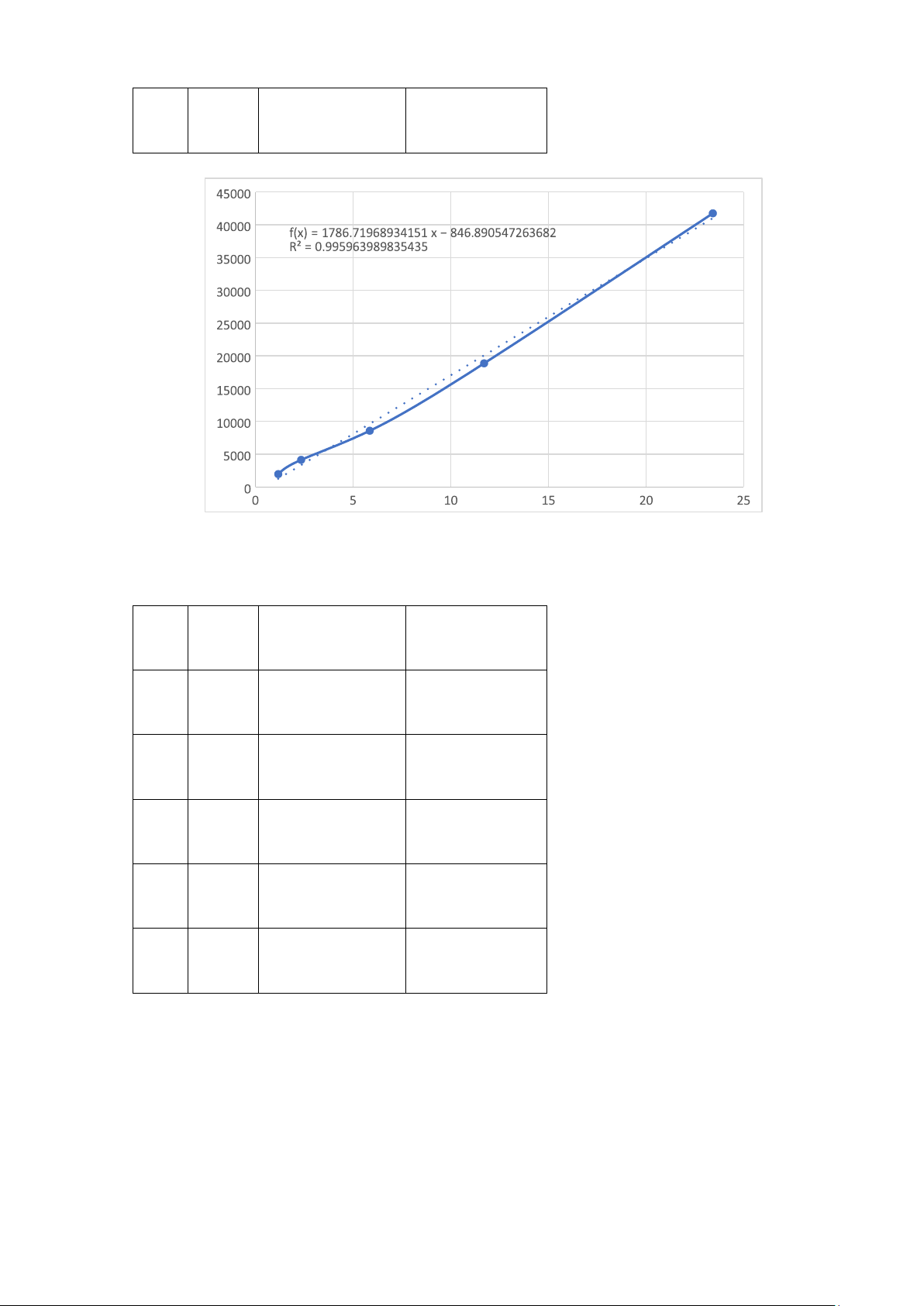
Hình 5. Đồ thị đường chuẩn S=f(C) của Caffein Nhận xét:
Với R2=0.9981>0.995 và R2=0.996>0.995: có sự tuyến tính giữa peak (S) và nồng độ C, ta thấy
đường chuẩn đã được xây dựng khá tốt.
Vậy diện tích peak phụ thuộc vào nồng độ chất phân tích tiêm vào cột. Nồng độ càng cao thì
diện tích peak càng lớn.
4. Kết quả đo mẫu thuốc
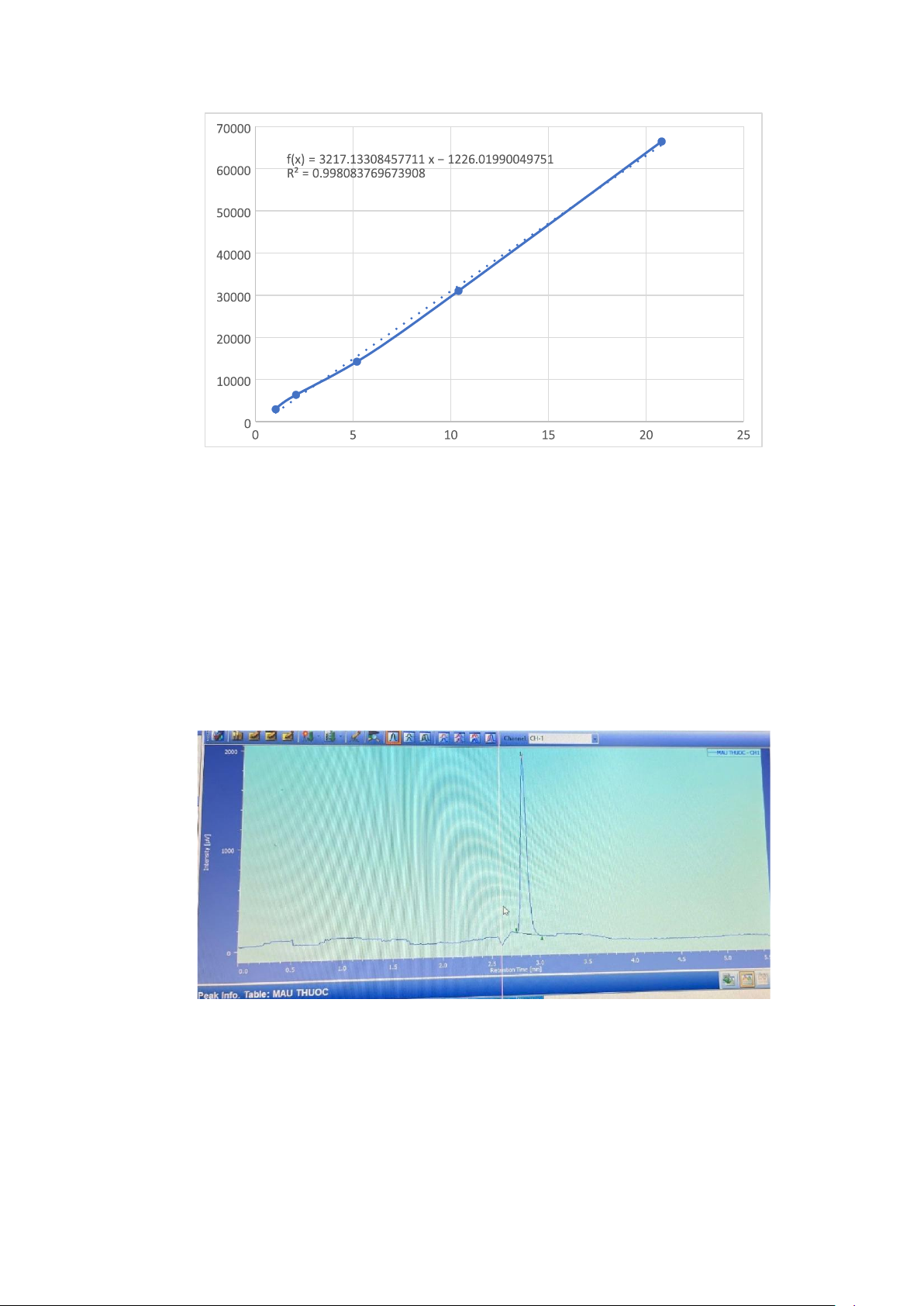
Hình 6. Kết quả đo thực tế của mẫu thuốc
Ta có thể thấy paracetamol ở trong mẫu thuốc có tR=2.842 phút và S=8064 và không có caffein.
Kết quả áp dụng đường chuẩn:
Phương trình đường chuẩn của paracetamol là: S=3217.1×C−1226 lOMoAR cPSD| 58794847
⇒Cpa=S3217.1+1226=8064+1226=2.8877 ppm
Nồng độ ban đầu của paracetamol trong mẫu chưa pha loãng: C=Cpa×1250=3609.62
ppm=3609.62 mg/l mpa=C×0.1×10−3=3609.62×10−4=0.361g 0.361
Tỉ lệ paracetamol trong mẫu thuốc là: %para= ×100%=71.705% 0.5034 V.
ĐÁNH GIÁ KẾT QUẢ PHÂN TÍCH
- Vậy từ kết quả tính ở trên thấy lượng paracetamol chiếm khoảng 71.705% trong một viên thuốc
vàphân còn lại là các tá dược khác.
- Qua đó, ta thấy nếu xây dựng đường chuẩn và viết phương trình hồi quy với dãy nồng độ chất chuẩn
từ thấp đến cao đưa ra kết quả ổn định và chính xác hơn.
+) Nguyên nhân gây ra sai số:
- Thao tác thí nghiệm của người làm có thể còn chưa hoàn toàn chính xác như cách pha hoặc tiêm mẫu.
- Sai số do dụng cụ đo. - Do còn lẫn tạp chất. VI. TRẢ LỜI CÂU HỎI



