





Preview text:
BÁO CÁO THÍ NGHIỆM
BÀI 3: ĐỘNG H A HỌC
Th nghiệm 1: Ảnh hưởng của nồng độ đến tốc độ phản ứng CÆch tiến h nh:
- Chuẩn bị 4 ống nghiệm c vẽ vạch sẵn trŒn th nh ống.
- Døng pipet lấy v o 4 ống nghiệm của mỗi ống 2ml dung dịch H2SO4 1M. -
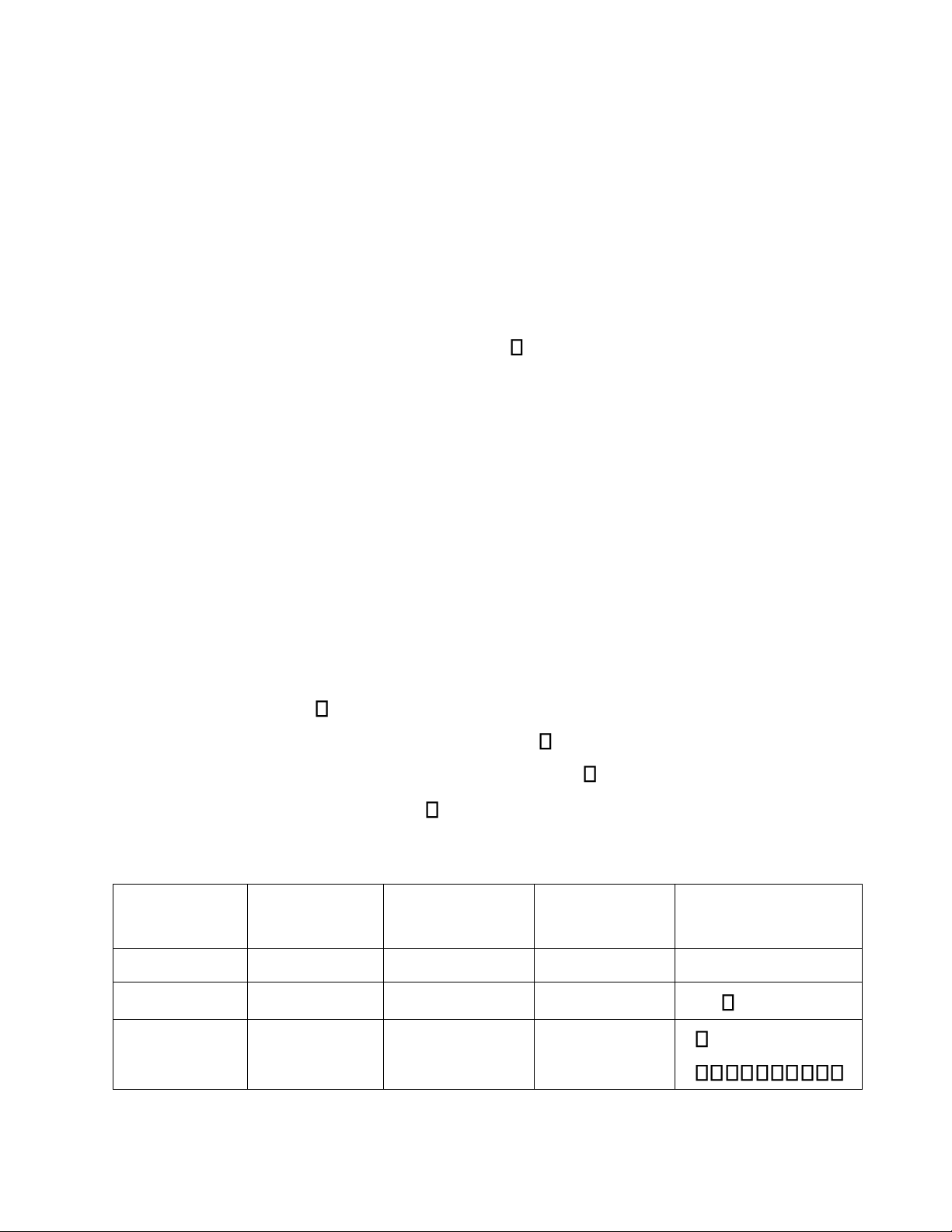
Døng pipet lấy v o 4 ống nghiệm khÆc hỗn hợp H2O v dung dịch Na2S2O3 0,1M theo tỉ lệ: TT 1 2 3 4 V(ml) 1 2 3 4 Na2S2O3 V(ml) 3 2 1 0 H2O
- Lần lượt tiến h nh cÆc th nghiệm bằng cÆch r t nhanh một ống được dung
dịch H2SO4 v o một ống đựng dung dịch Na2S2O3 đã chuẩn bị, lắc mạnh v nhanh.
- Dùng đồng hồ bấm gi y ghi lại thời gian mỗi th nghiệm từ lœc r t 2 dung
dịch v o với nhau cho đến khi bắt đầu xuất hiện kết tủa lưu huỳnh m u trắng sữa.
- Dùng đồng hồ bấm gi y theo dıi thời gian từ lúc đổ 2 dung dịch v o với nhau
cho tới khi bắt đầu xuất hiện kết tủa trắng. Kết quả:
- Sau khi 2 dung dịch được h a quyện lại với nhau:
+ Ống 1 mất 2:47s mới có tình trạng ục nước (màu trắng sữa) làm mờ i
vạch mực ã ược vẽ trên ống nghiệm.
+ Ống 2 mất 1:22s mới có tình trạng ục nước (màu trắng sữa) làm mờ i
vạch mực ã ược vẽ trên ống nghiệm.
+ Ống 3 mất 59s mới có tình trạng ục nước (màu trắng sữa) làm mờ i vạch
mực ã ược vẽ trên ống nghiệm.
+ Ống 4 mất 48s mới có tình trạng ục nước (màu trắng sữa) làm mờ i vạch
mực ã ược vẽ trên ống nghiệm.
- Để thŒm tầm 5 - 10 phœt th dung dịch của 4 ống nghiệm đều c hiện tượng
đục v v ng dần từ ống 1 – 4.
Giải th ch: Th nghiệm về ảnh hưởng của nồng độ đến tốc độ phản ứng xảy
ra vì tăng nồng độ của cÆc chất tham gia trong phản ứng làm tăng cơ hội va
chạm giữa chúng, làm tăng khả năng xảy ra cÆc va chạm hiệu quả và tăng
năng lượng hệ thống, từ đó làm tăng tốc độ phản ứng. PTPU:
Na2S2O3 + H2SO4 → Na2SO4 + H2O + SO2 + S
Th nghiệm 2: Ảnh hưởng của nhiệt độ đến tốc độ phản ứng.
CÆch tiến h nh:
- Lấy 8 ống nghiệm A, B, C, D v a, b, c, d chia th nh hai nh m để trŒn hai h ng
giÆ. Cho v o ống nghiệm A, B, C, D mỗi ống 2ml dung dịch Na2S2O3 1M v
cÆc ống a, b, c, d mỗi ống 2ml dung dịch H2SO4 1M
- Lấy 1/3 cốc nước lª, døng nhiệt kế khuấy nhẹ đo nhiệt độ t1. Đặt hai ống aA
v o cốc nước khoảng 2 phút để nhiệt độ của nước v dung dịch c n bằng. Đổ
ống A v o ống a v bấm đồng hồ bấm giây. Để nguyŒn ống a trong cốc nước,
quan sÆt khi dung dịch bắt đầu đục th bấm dừng đồng hồ.
- Cho từ từ nước s i v o cốc nước trŒn, døng nhiệt kế khuấy nhẹ đến khi
nhiệt độ tăng lên 10 C. Đặt hai ống b, B v o cốc trong 2 phút và cũng thao
tác như thế để xác định thời gian phản ứng t2 tương ứng với nhiệt độ t2. -
Cho nước s i v o cốc đến khi nhiệt độ tăng lên 10 C cũng tiến hành như
trên xác định thời gian phản ứng t3 ở nhiệt độ t3
- Làm tương tự như trên đối với th nghiệm 4. Kết quả: TN Nhiệt độ
Thời gian p/ư Tốc độ p/ư
hệ số nhiệt độ p/ư 1 25 49 0,020408163 2 35 40 0,025 1 = 1,225 3 45 39 0,025641026 2 = 4 55 35 0,028571429 3 = 1,114285714
Giải th ch: Th nghiệm về ảnh hưởng của nhiệt độ đến tốc độ phản ứng xảy
ra v nhiệt độ tăng làm tăng động năng của ph n tử, tăng tần số va chạm, tăng
khả năng tiếp xœc giữa cÆc ph n tử và thay đổi cơ chế phản ứng, tất cả đều
g p phần l m tăng tốc độ phản ứng.
Th nghiệm 3: Ảnh hưởng của xúc tác đến tốc độ phản ứng.
3.1. Xúc tác đồng thể CÆch tiến h nh:
- Lấy v o ống nghiệm 1 ml dung dịch H2O2 10%. Sau đó thêm vào dung dịch
trŒn v i giọt K2CrO4 bªo h a. Kết quả:
- Lœc mới nhỏ v i giọt K2CrO4 bªo h a v o th dung dịch chuyển sang m u nâu
đậm v c sự s i (thoÆt kh O2 ) rất nhanh v mªnh liệt.
- Đợi 1 lœc sau th dung dịch vẫn sôi nhưng chỉ lăn tăn như ga trong nước giải
khÆt v c sự chuyển m u từ nâu đậm sang m u dầu ăn neptune.
Giải th ch: Th nghiệm về ảnh hưởng của xúc tác đồng thể đến tốc độ phản
ứng xảy ra vì xúc tác đồng thể giœp giảm năng lượng hoạt h a, tạo điều kiện
thuận lợi cho phản ứng xảy ra và thúc đẩy cơ chế phản ứng phụ, từ đó tăng
tốc độ phản ứng m kh ng bị tiŒu hao trong quÆ tr nh phản ứng.
3.2. Xœc tÆc dị thể
CÆch tiến h nh:
- Lấy v o ống nghiệm 1 ml dung dịch H2O2 10%. Sau đó thêm vào 1 ít MnO2 v o. Kết quả:
- Sau khi thŒm MnO2 v o th c hiện tượng s i, sủi bọt trắng nhỏ rất nhiều làm
đục dung dịch, đọng lại xung quanh th nh ống nghiệm rất nhiều. - Đợi 1 lœc
th hiện tượng sôi đã không còn mạnh mẽ như lúc đầu nữa, nhờ vậy m dung
dịch đã trong hơn lúc đầu v cÆc bọt trắng li ti vẫn c n trŒn mặt dung dịch
xung quanh th nh ống nghiệm.
Giải th ch: Th nghiệm về ảnh hưởng của xœc tÆc dị thể đến tốc độ phản ứng
xảy ra v xœc tÆc n y tạo điều kiện tiếp xœc hiệu quả giữa cÆc ph n tử, giảm
năng lượng hoạt hóa, thúc đẩy các cơ chế phản ứng phụ, v tiết kiệm năng
lượng, tất cả đều giúp tăng tốc độ phản ứng m kh ng tiŒu hao xœc tÆc.



