






Preview text:
lOMoAR cPSD| 45740153 CHUYỂN HOÁ NĂNG LƯỢNG Mục tiêu
1. Trình bày được khái niệm về phản ứng oxy hoá Lâm Vĩnh Niên khửsinh học. Bộ môn Hoá sinh
2. Phân tích được các giai đoạn và vai trò của chu trình acid citric.
3. Phân tích được quá trình vận chuyển điện tử và
tổnghợp ATP trong ti thể. Nội dung 1. Oxy hoá khử sinh học •
Phản ứng oxy hoá khử, phản ứng oxy hoá khử sinh học • Nội dung Thế khử •
Liên hệ giữa biến thiên thế khử chuẩn và biến thiên năng lượng tự do chuẩn
3. Vận chuyển điện tử và tổng hợp ATP 2. Chu trình acid citric
• Các chất nhận điện tử chung • Các giai đoạn
• Các chất vận chuyển điện tử gắn màng • Vai trò
• Các phức hợp đa enzym • Điều hoà
• Năng lượng của sự vận chuyển điện tử • Tổng hợp ATP
• Điều hoà phosphoryl‐oxy hoá
• Các chất ức chế phosphoryl‐oxy hoá lOMoAR cPSD| 45740153 Phản ứng oxy hoá khử
• Vai trò trung tâm trong cung cấp năng lượng sinh học. PHẢN ỨNG OXY HOÁ KHỬ
• Điện tử được chuyển từ chất này sang chất khác. SINH HỌC
– Chấtkhử; chất oxy hoá – Sự oxy hoá; sự khử
Chuyển điện tử trong phản ứng oxy hoá khử sinh học Phản ứng oxy hoá khử
• Trựctiếplà điệntử . + • Fe 2+ + Cu 2+ Fe 3+ + Cu
Phản ứng oxy hoá và phản ứng khử luôn xảy ra cùng lúc với • nhau. Nguyêntửhydro .
– Enzymxúctác: dehydrogenase.
• Cặp oxy hoá khử liên hợp. AH 2 + B A + BH 2 • Bán phản ứng. • Ion hydrid (:H – )
• TD: sự oxy hoá sắt (II) bởi đồng (II)
• Gắntrựctiếpvớioxy . TD: oxy hoá Fe2+ + Cu2+ Fe3+ + Cu+ hydrocarbon thànhalcol: gồm 2 bán phản ứng: R—CH Fe 3 + O 2 R—CH 2 —OH Fe 3+
2++ e− Cu2++ e Cu+ − lOMoAR cPSD| 45740153 Đương lượng khử
Thế khử (thế oxy hoá khử)
• Một electron được vận chuyển (dù theo cách • Khuynh hướng nhận điện tử (bị khử) của một chất. thức nào). • Đơn vị: volt. • •
Quy ước đơn vị của phản ứng oxy hoá khử
Thế khử chuẩn, E°
sinh học là 2 đương lượng khử đi từ cơ chất đến oxy. • Echuẩn (H° của cặp oxh‐k: theo điện cực tham chiếu hydro +/H2). Quy ước:
▪ E° > 0 nếu cặp oxh‐k nhận e từ điện cực hydro chuẩn;
▪ E° <0 nếu cặp oxh‐k cho e đến điện cực hydro chuẩn.
Thếkhửchuẩnở mộtsốbánphảnứngsinhhọcquantrọng Bánphảnứngkhử
E ′ ° ( V ) Acetyl CoA+ CO e − 2 + H + + 2 →pyruvat+ CoA −0 ,48
Ferredoxin (Fe 3+ ) + e − →ferredoxin (Fe 2+ ) −0 ,43
2 H + + 2 e − → H 2 ( ở pH 7) −0 ,42 α- Ketoglutarat + CO →isocitrat −0, Thế khử 2 + 2H + + 2 e − 38
Lipoyl dehydrogenase (FAD) + 2H + + 2 e − →lipoyl dehydrogenase (FADH ) −0, • 2 34
Liên hệ giữa thế khử thực sự (E) với E°: phương trình NADP + + 2H + + 2 e − → NADPH + H + −0 , 32 Nernst : NAD + + 2H + + 2 e − → NADH + H + −0 , 32 Acid lipoic + 2H + + 2
e − → acid dihydrolipoic −0, 29
Glutathion(bịoxy hoá) + 2H + + 2 e − → 2 glutathion(bị • Ở 25 °C khử) −0 , 23
FAD + 2H + + 2 e − → FADH 2 −0 , 22
FMN + 2H + + 2 e − → FMNH 2 −0, 22
• Điều kiện chuẩn hiệu chỉnh: pH 7. → ký hiệu: E′°.
Acetaldehyd + 2H + + 2 e − → ethanol −0 ,20 • Pyruvat + 2H + + → lactat −0 18
Quy ước: ∆E′° = E′°chất oxy hoá – E′° chất khử. 2 e − ,
Oxaloacetat+ 2 H + + 2 e − → malat −0, 17 lOMoAR cPSD| 45740153
Thế khử chuẩn ở một số bán phản ứng sinh học quan trọng
Bán phản ứng khử E′° (V)
Cytochrom b5 (Fe3+) + e−→ cytochrom b5 (Fe2+) (vi thể) 0,02
Fumarat + 2H+ + 2e−→ succinat 0,03
Ubiquinone (Q) + 2H+ + 2e−→ ubiquinol (QH2) 0,04
Cytochrom b (Fe3+) + e−→ cytochrom b (Fe2+) (ti thể) 0,08
Cytochrom c1 (Fe3+) + e−→ cytochrom c1 (Fe2+) 0,22
Cytochrom c (Fe3+) + e−→ cytochrom c (Fe2+) 0,25
Cytochrom a (Fe3+) + e−→ cytochrom a (Fe2+) 0,29
O2 + + 2H+ + 2e−→ H2O2 0,30
Cytochrom a3 (Fe3+) + e−→ cytochrom a3 (Fe2+) 0,35
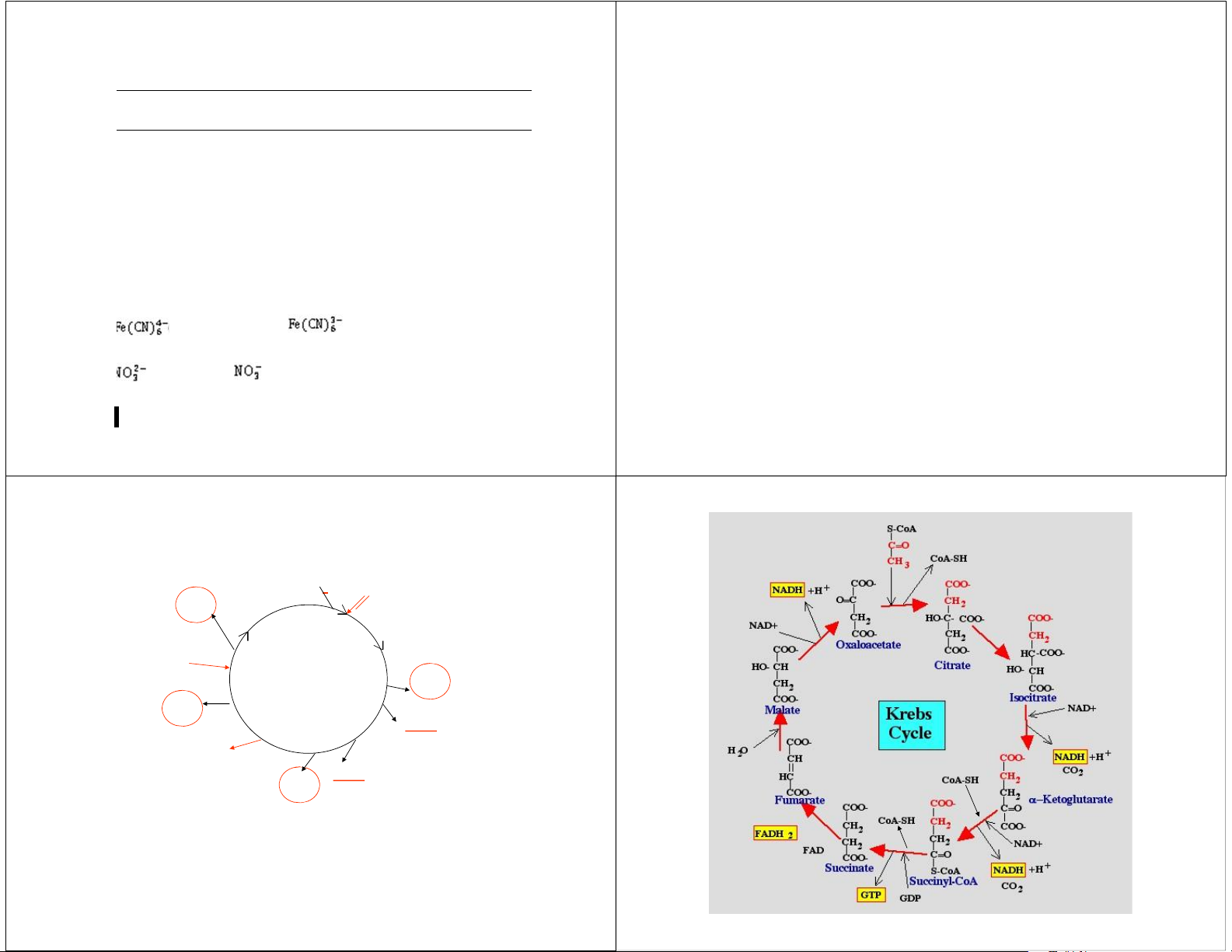
(ferricyanid) + e− → (ferrocyanid) 0,36
Cytochrom f (Fe3+) + e−→ cytochrom f (Fe2+) 0,36 + 2H+ + 2e−→ + H2O 0,42 Fe3+ + e−→ Fe2+ 0,77
O2 + 2H+ + 2e−→ H2O 0,82 CHU TRÌNH ACID CITRIC - Tên gọi khác:
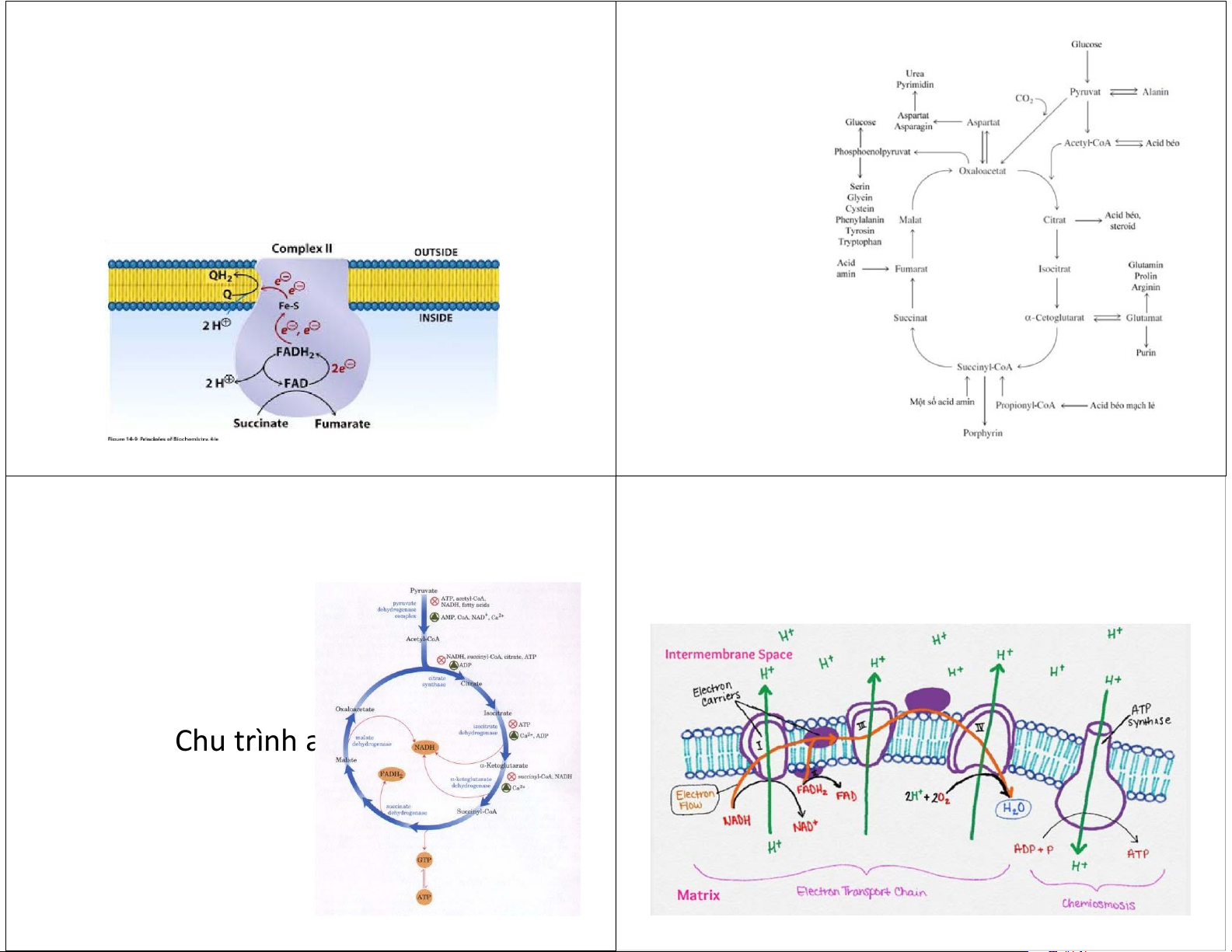
- Chu trình acid tricarboxylic (TCA) - Chu trình Krebs 8: malat DH 1: citrat synthase
- Quá trình “đốt cháy” oxh mạch 2C (Act~SCoA) giải phóng 2 phân 7: fumarase 2: aconitase tử CO 6: succinat DH 3: isocitrat DH
2, 4 cặp nguyên tử H (tạo thành H2O) và năng lượng. 5: succinyl-CoA synthetase 4: C α-cetoglutarat DH
2 H 2 O 2H C 1 4 C 6 2 C 8 H 6 2 O 2H 2 H C 3 4 CO 2 7 C 5 C 4 ATP CO 2 2 H CHU TRÌNH ACID CITRIC 4 6 5 lOMoAR cPSD| 45740153 lOMoAR cPSD| 45740153 Chu trình acid citric:
Vai trò chu trình acid citric
Tạo đương lượng khử, GTP (ATP), CO2
• Tạo các đương lượng khử, GTP (ATP) và CO2
Acetyl‐CoA + 3NAD+ +FAD + GDP (ADP) + Pi + 2H2O
• Tạo các chất trung gian sinh tổng hợp 2CO2 + 3NADH + FADH2 + GTP (ATP) +2H+ + CoA
• 2 C từ nhóm acetyl đi vào CT. 2 C rời CT ở dạng CO2.
• 4 cặp H rời chu trình trong 4 phản ứng oxy hoá khử. Chu trình acid citric:
Tạo đương lượng khử, GTP (ATP), CO 2
• Khảo sát dùng chất đồng vị: 2 C trong CO 2 Chu trình acid citric:
không cùng là 2 C trong nhóm acetyl đi vào CT.
• NADH và FADH 2 có thể được oxy hoá trong
chuỗi vận chuyển điện tử và tạo ATP. – 1 NADH tạo 2,5 ATP, – 1 FADH 2 tạo 1,5 ATP.
→ Oxy hoá hoàn toàn 1 acetyl‐CoA tạo 10 ATP. lOMoAR cPSD| 45740153
Tạo đương lượng khử, GTP (ATP), CO2
Acetyl‐CoA + 3NAD+ +FAD + GDP (ADP) + Pi + 2H2O
2CO2 + 3NADH + FADH2 + GTP (ATP) +2H+ + CoA
• Tạo thành ATP hoặc GTP.
• Hai phân tử nước bị tiêu thụ: lOMoAR cPSD| 45740153 Chu trình acid citric:
Tạo đương lượng khử, GTP (ATP), CO Tạo các chất trung 2 gian sinh tổng hợp
• CT acid citric chỉ xảy ra / hiếu khí.
• Trừ succinat DH gắn màng, các enzym khác được
xem là hoà tan trong chất nền ti thể. Tồn tại trong các
phức hợp đa enzym (metabolon). Vai trò trung tâm trong chuyển hoá: ngã ba đường cho các con đường chuyển hoá
VẬN CHUYỂN ĐIỆN TỬ VÀ TỔNG HỢP ATP
Điều hoà sự hình thành acetyl‐CoA
bởi phức hợp pyruvat dehydrogenase Điều hoà các Chu t phản ứn rình a g trong cid chu citric: Điều trình acid citric • Citrat synthase • Isocitrat dehydrogenase
• α‐Cetoglutarat dehydrogenase lOMoAR cPSD| 45740153 hoà chu trình acid citric lOMoAR cPSD| 45740153
Vận chuyển điện tử và tổng hợp ATP
• Điện tử tích trữ trong các coenzym bị khử
(NADH và FADH2) → vận chuyển qua chuỗi
các protein và coenzym có tổ chức cao và
phức tạp gắn ở màng trong ti thể (chuỗi vận
chuyển điện tử) → đến O2 (oxy phân tử).
• Trong quá trình vận chuyển điện tử, gradient
proton được hình thành xuyên qua màng
trong ti thể → cung cấp năng lượng tổng
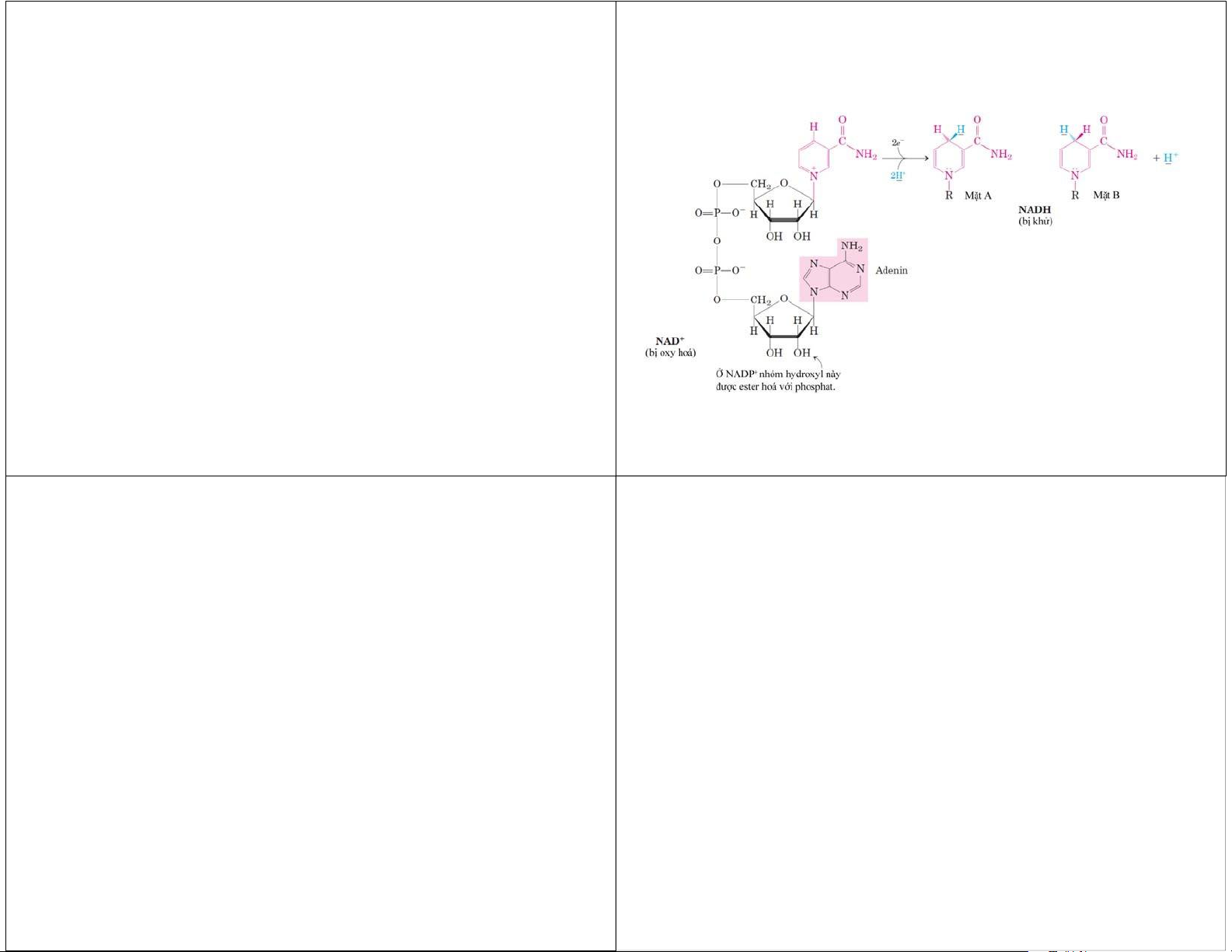
hợp ATP: phosphoryl oxy hoá hay hô hấp tế bào. NAD và NADP
• NADH mang e từdịhoávàochuỗiHHTB. NADPH
cungcấp e chođồnghoá. NAD và NADP
• NADH vàNADPH khôngqua đượcmàngtrongti thể.
(nicotinamid adenin dinucleotid [phosphat]) lOMoAR cPSD| 45740153
Các chất nhận điện tử chung
• Điện tử từ các phản ứng khử hydro được tích
trữ trong các chất nhận điện tử chung:
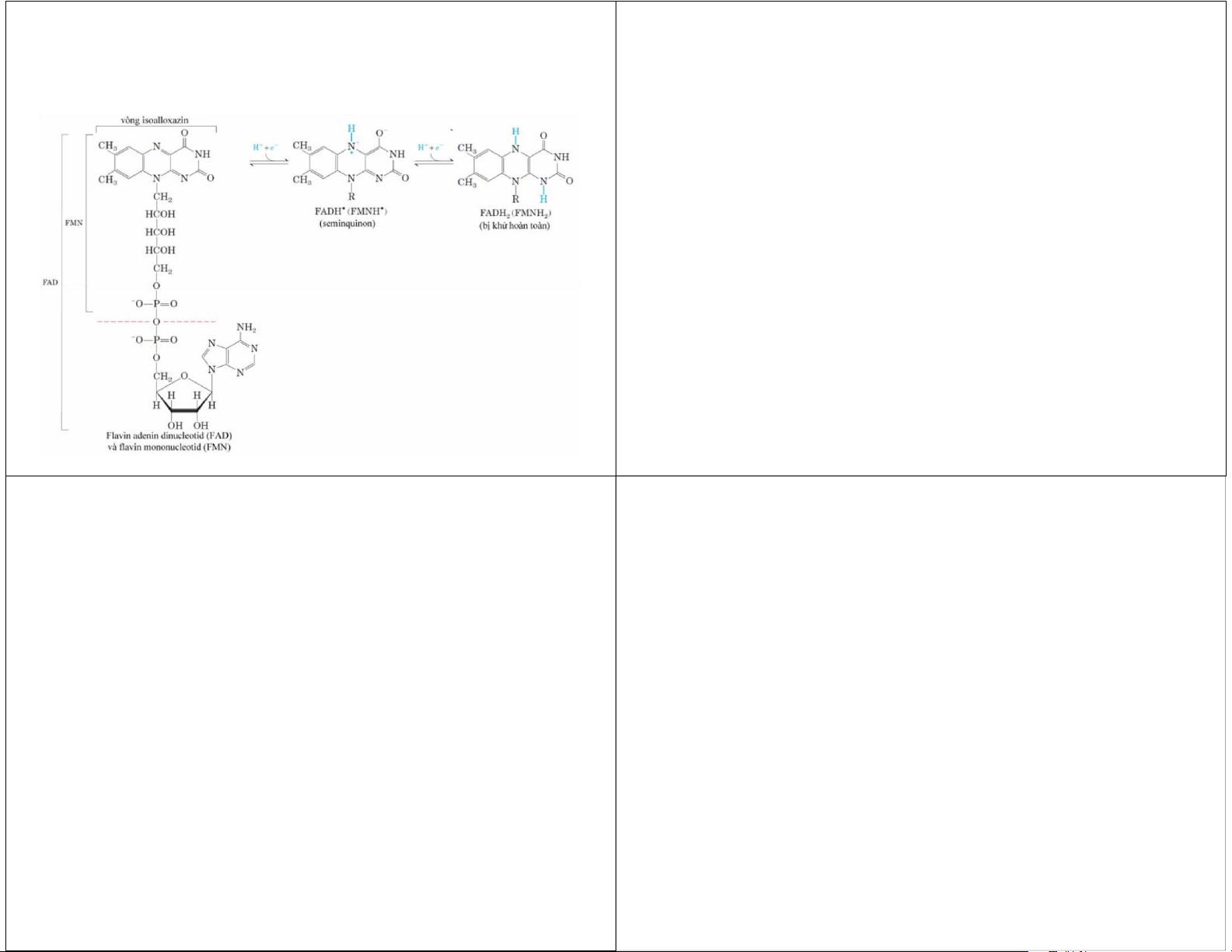
– nucleotid nicotinamid (NAD+, NADP+) – nucleotid flavin (FMN, FAD). lOMoAR cPSD| 45740153 FAD và FMN FAD và FMN
• Gắn rất chặt trong flavoprotein.
• Thế khử chuẩn phụ thuộc vào protein gắn với nó.
• Dạng bị khử có thể nhận 1 điện tử (tạo semiquinon)
hoặc 2 điện tử (tạo FADH2 hoặc FMNH2).
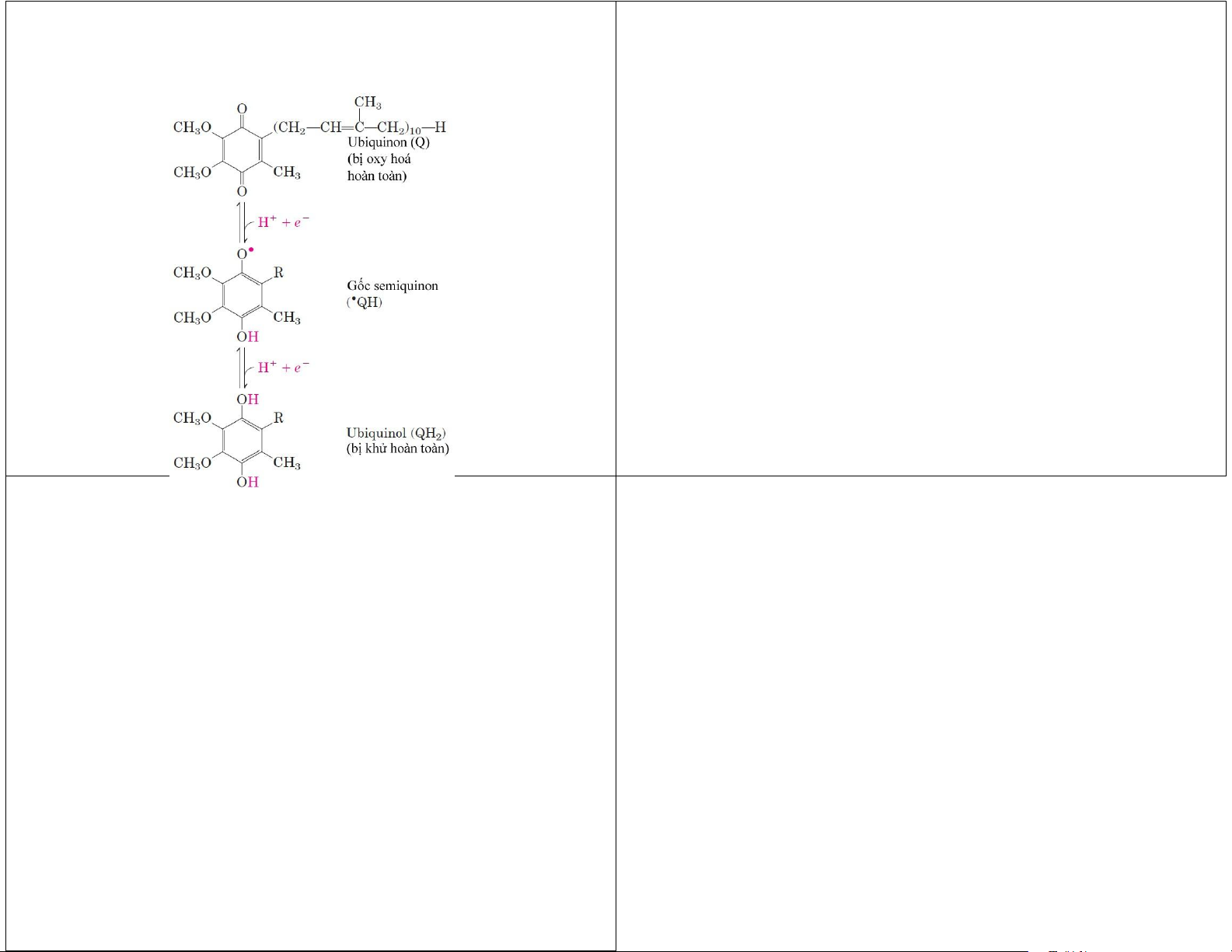
Các chất vận chuyển điện tử gắn Ubiquinon màng • • Coenzym Q, Q Ubiquinon
• Benozquinon có mạch bên isoprenoid dài. • Cytochrom
• Nhận 1 điện tử (tạo gốc semiquinon, • QH) hoặc 2
• Protein sắt‐lưu huỳnh
điện tử (tạo quinol, QH 2 ) .
• Phân tử nhỏ, kị nước → khuếch tán / lớp lipid kép
của màng trong ti thể → con thoi mang đương lượng khử.
• Mang được cả e và proton → vai trò trung tâm trong
ghép dòng e với sự di chuyển của proton. lOMoAR cPSD| 45740153 Cytochrom •
Các protein hấp thụ mạnh ánh sáng nhìn thấy được do nhóm phụ hem chứa sắt. lOMoAR cPSD| 45740153
• Ti thể chứa 3 lớp cytochrom, a, b và c, tuỳ theo phổ hấp thụ ánh sáng.
– Cytochrom loại a, b và một số loại c tích hợp ở màng trong ti thể.
– Cytochrom c: hoà tan, gắn với mặt ngoài màng trong.
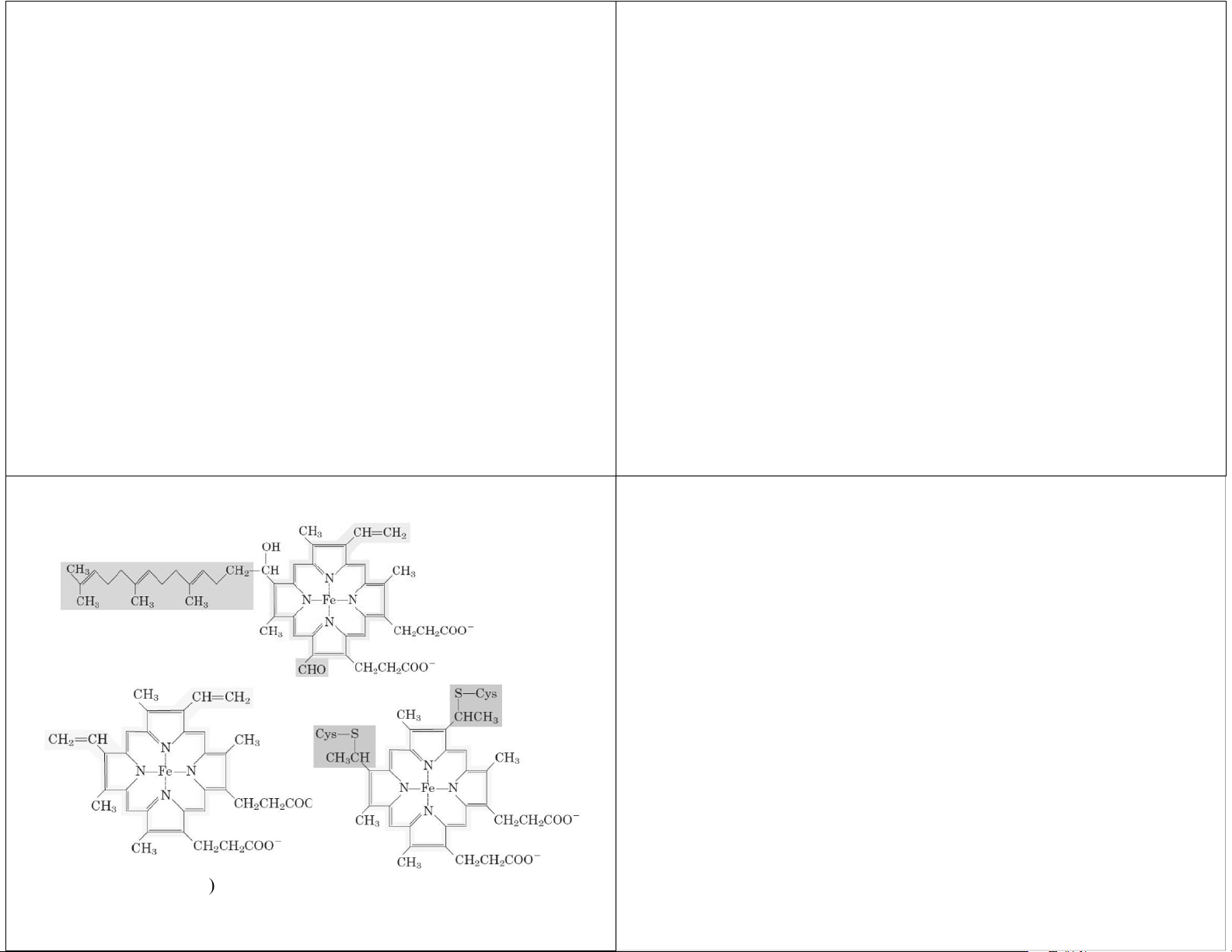
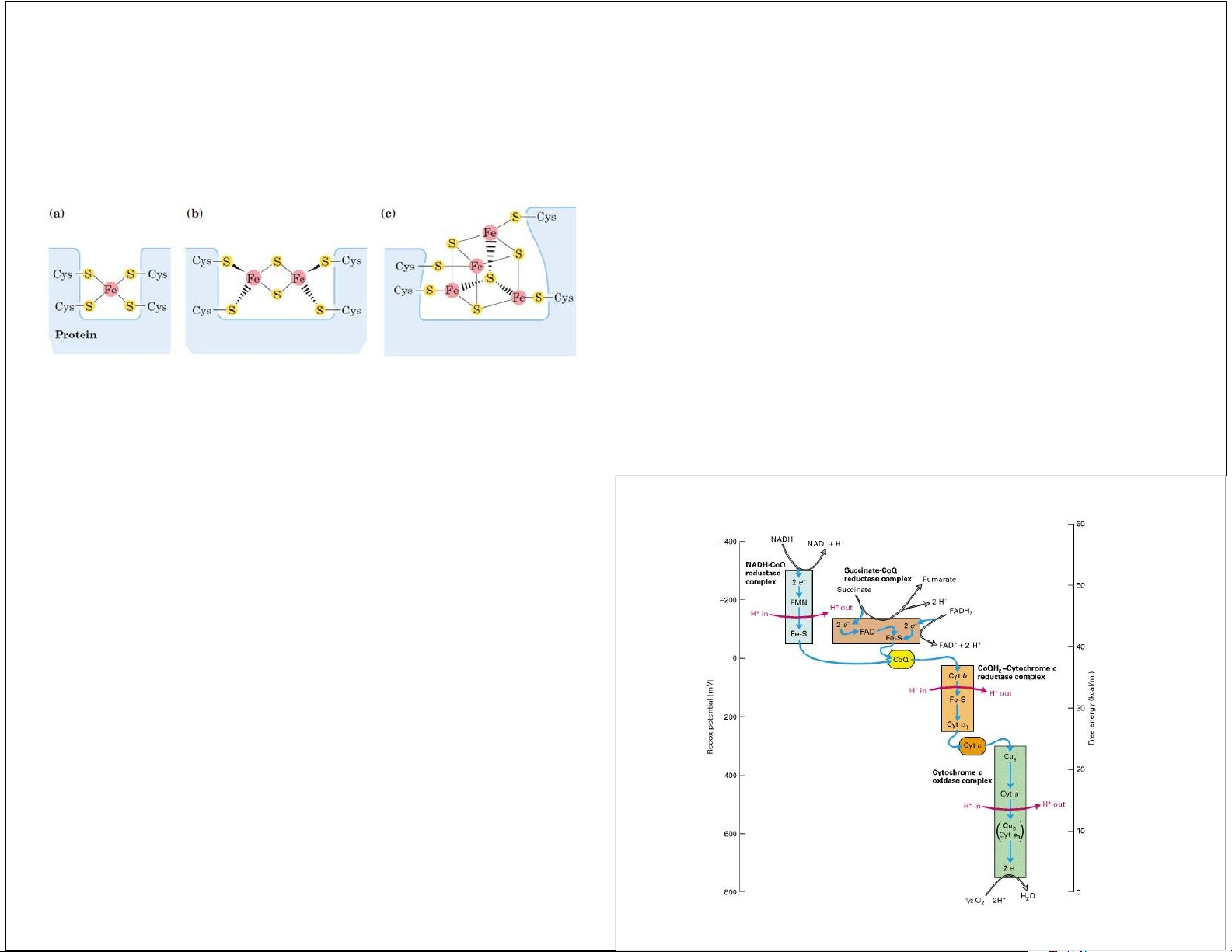
• Thế khử chuẩn của nguyên tử sắt trong hem khác nhau giữa các cytochrom. Hem A ( Protein sắt‐lưu huỳnh trong cytochrom loại a )
• Nguyên tử sắt nối với lưu huỳnh vô cơ
và/hoặc lưu huỳnh của Cys (protein).
• Protein sắt‐lưu huỳnh Rieske: sắt nối 2 gốc His.
• Vận chuyển 1 e (1 nguyên tử sắt của cụm Fe‐S bị oxy hoá hoặc khử). Hem B s ( ắt protoporphyrin IX) Hem C
(t rong cytochrom loại b )
( tron g cytochrom loại c ) lOMoAR cPSD| 45740153 Protein sắt‐lưu huỳnh
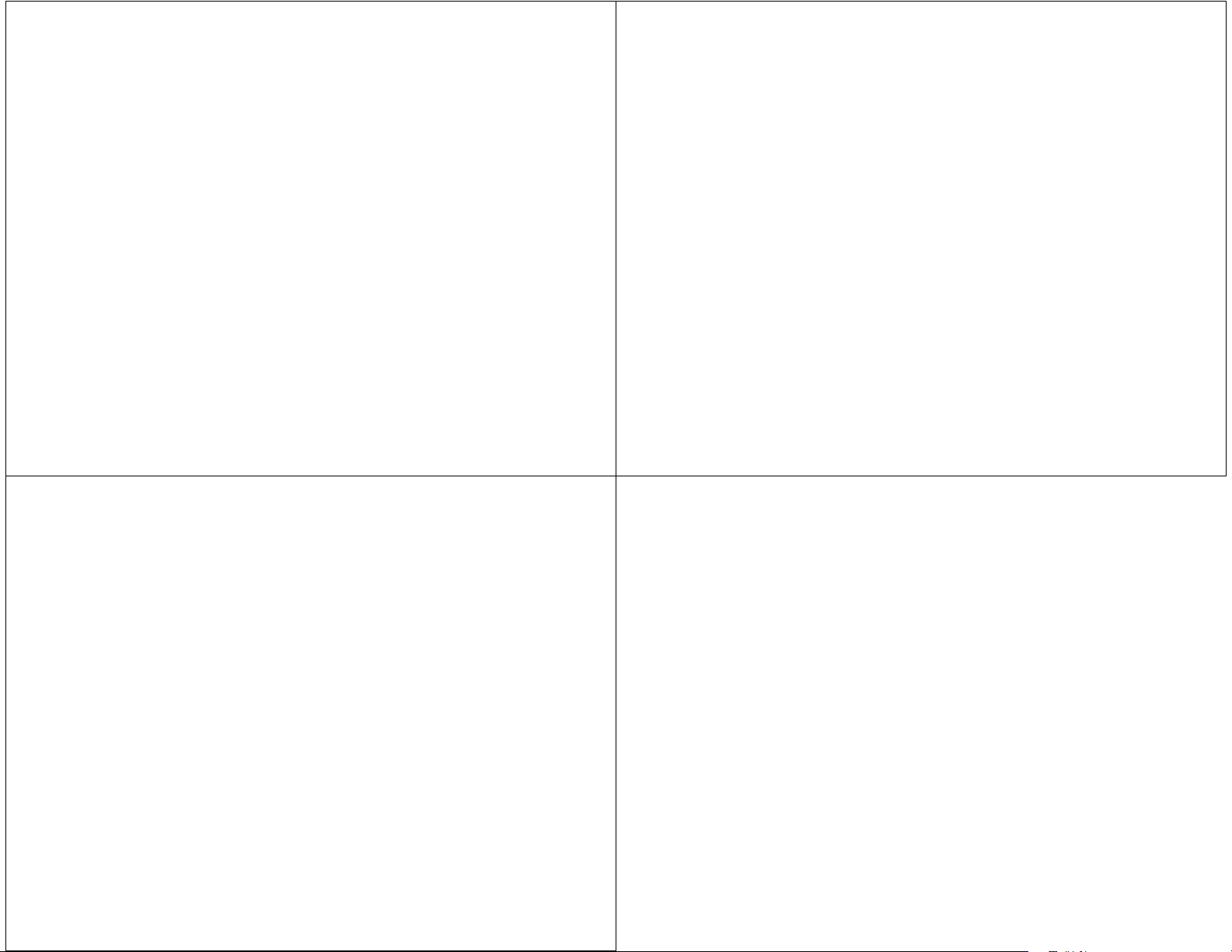
Các phức hợp vận chuyển điện tử
• Các chất vận chuyển điện tử của chuỗi hô hấp: tổ chức thành các phức hợp siêu phân tử gắn màng, có thể
tách rời về mặt vật lí.
• Mỗi phức hợp xúc tác một phần riêng biệt trong quá
trình dẫn truyền năng lượng.
• Đánh số từ I đến IV. Phức hợp V là ATP synthase. 1Fe 2Fe-2S 4Fe-4S • Dòng
điện tử: theo chiều tăng thế khử.
Các trung tâm sắt-lưu huỳnh
(chỉ tính số nguyên tử lưu huỳnh vô cơ). lOMoAR cPSD| 45740153 lOMoAR cPSD| 45740153 Phức hợp I: Phức hợp I: Từ NADH đến ubiquinon Từ NADH đến ubiquinon
• Tên khác: NADH:ubiquinon oxidoreductase
• NADH cung cấp e ở mặt trong của màng cho hay NADH
dehydrogenase. phức hợp I.
• Lớn, 42 chuỗi polypeptid khác nhau
• FMN nhận 2 e (dạng ion hydrid) từ NADH và 1 – Có flavoprotein chứa
FMN proton từ chất nền, tạo FMNH2.
– Ít nhất 6 trung tâm Fe‐S.
• FMNH2 được oxy hoá 2 bước, mỗi lần giải
• Cấu trúc hình L với một cánh tay trong màng phóng 1 điện tử lần lượt vào cụm Fe‐S.
và một cánh tay vươn vào chất nền.
• Fe‐S lần lượt chuyển từng e đến ubiquinon (Q) lOMoAR cPSD| 45740153 Phức hợp II:
(gắn với phức hợp I ở bên trong màng) → ubiquinol (QH2). Phức hợp I: Từ NADH đến ubiquinon
• Ứng với mỗi cặp e từ NADH đến QH → 2 4 proton
từ chất nền ra khoang gian màng.
(ETF : electron-transferring flavoprotein)
• Phản ứng tổng quát: Phức hợp II: NADH + 5 + Q NAD + + QH 2 + 4
P: phía tích điện dương của màng trong (khoảng
gian màng); N: phía tích điện âm (chất nền). lOMoAR cPSD| 45740153 Phức hợp III:
Từ succinat đến ubiquinon
Từ succinat đến ubiquinon
• Còn gọi succinat:ubiquinon oxidoreductase, • Năng lượng giải phóng từ phức hợp II rất ít hay succinat
dehydrogenase. →không kèm vận chuyển proton qua màng.
• Cũng là enzym xúc tác trong CT acid citric.
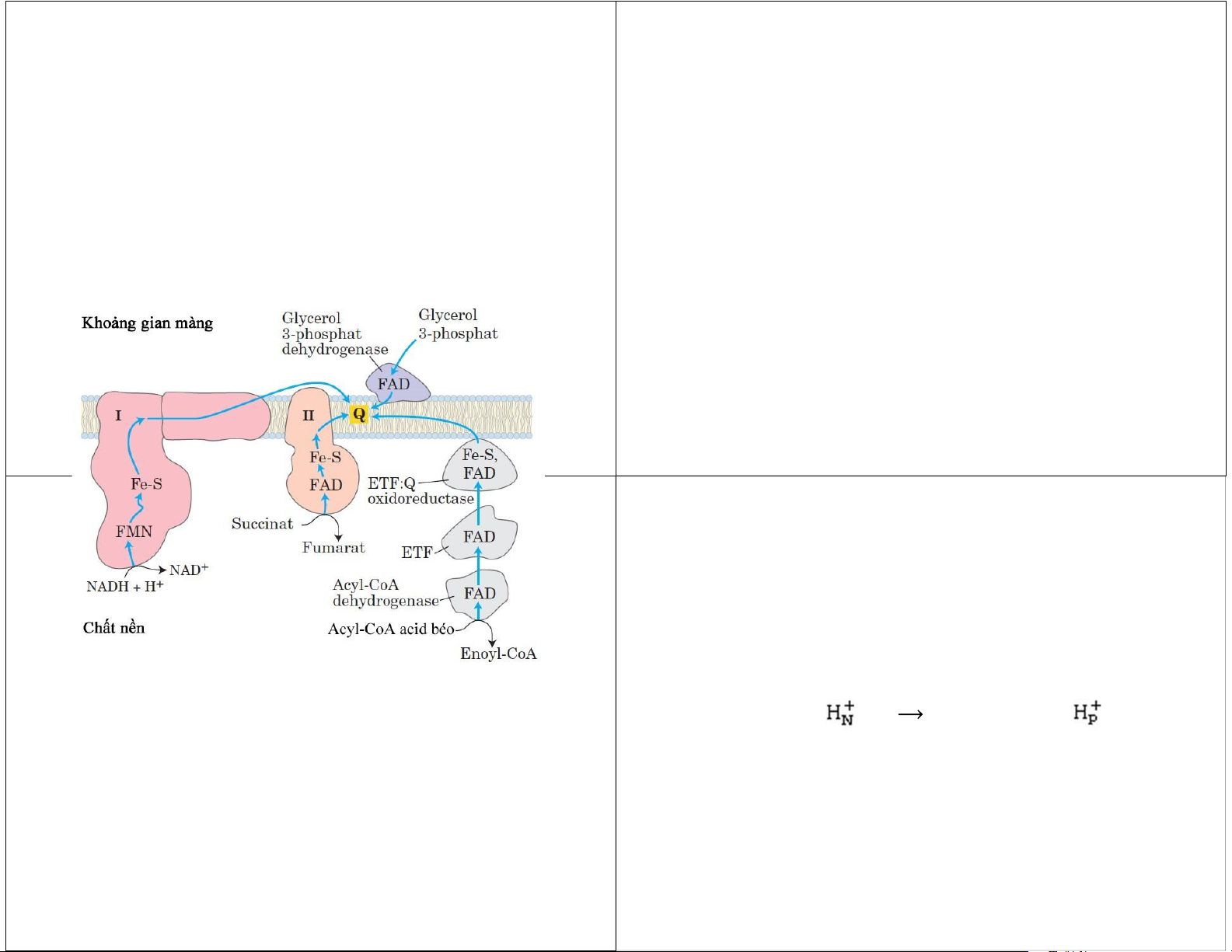
• Một số chất chuyển e trực tiếp vào chuỗi hô
• Nhỏ, đơn giản hơn phức hợp I. Chứa 5 nhóm hấp ở mức ubiquinon nhưng không qua phức phụ và 4 tiểu đơn vị protein. hợp II • –
Nhận điện tử từ succinat và khử Q thành QH Acid béo 2. – Glycerol 3‐phosphat
• Điện tử từ vị trí gắn succinat →FAD →các trung tâm Fe‐S →vị trí gắn Q. Phức hợp III:
Từ ubiquinon đến cytochrom c
Phức hợp III: Từ ubiquinon
• Có 3 hem trong 2 cytochrom: – ( b đến cytochrom c
hem b L L : ái lực thấp) và hem H ( H: ái lực cao) thuộc cytochrom b ,
• Còn gọi ubiquinol:cytochrom c oxidoreductase hay
– 1 hem thuộc cytochrom c 1 .
phức hợp cytochrom bc1.
• Chứa trung tâm 2Fe‐2S (protein sắt‐lưu huỳnh • Ghép Rieske).
– vận chuyển e từ ubiquinol sang cytochrom c với • Có 2 vị trí gắn Q:
– vận chuyển proton từ chất nền ra khoảng gian màng.
– Q N ( phía N của màng, gần b H )
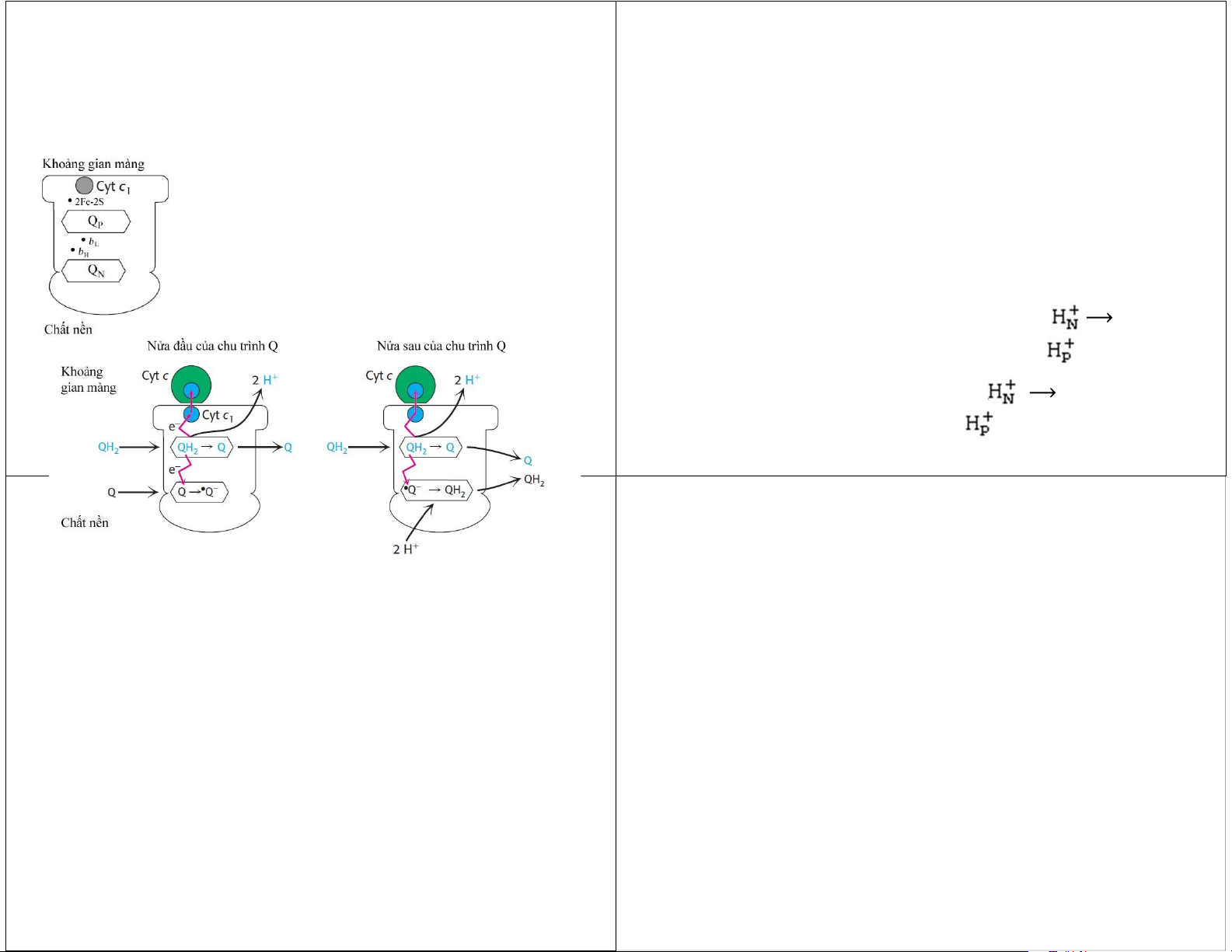
– Q P ( phía P, gần trung tâm 2Fe‐2S và b L ). lOMoAR cPSD| 45740153 Phức hợp IV:
• Homodimer, mỗi monomer có 11 tiểu đơn vị khác nhau. Chu trình Q của
Từ ubiquinon đến cytochrom c phức hợp III
• 2 proton được lấy từ chất nền. • Một chu trình Q:
2 QH2 + Q + 2 cyt c1 (bị oxy hoá) + 2
2 Q + QH2 + 2 cyt c1 (bị khử) + 4 hay:
QH2 + 2 cyt c1 (bị oxy hoá) + 2 Q + 2 cyt c1 (bị khử) + 4 Phức hợp IV:
Từ cytochrom c đến O 2
Phức hợp III: Từ ubiquinon
• Còn gọi là cytochrom c oxidase; gồm 13 tiểu đơn
vị, chứa 2 nhóm hem ( a và a đến cytochrom c 3 ) và 3 ion đồng.
– Hai ion đồng tạo trung tâm hai nhân Cu A .
• Chu trình Q → chuyển đổi từ chất vận chuyển 2
– Hem a 3 và ion đồng còn lại (Cu B ) → trung tâm hai
điện tử ubiquinon sang chất vận chuyển 1 điện tử. nhân thứ hai. • → Cytochrom c:
• Điện tử từ cytochrom c → trung tâm Cu hem A → –
a → trung tâm hem a O
protein hoà tan trong khoảng gian màng. 3 ‐Cu B 2
– nhận điện tử từ phức hợp III → di chuyển đến phức hợp IV.



