




Preview text:
lOMoAR cPSD| 45148588
CÂU 1) Tiến hành thí nghiệm : Pha va thử tính chất dung dịch đệm acetat Ph=4,75 Trả lời vấn đáp :
-Khái niệm : dung dịch đệm là dung dịch có Ph thay đổi không đáng kể khi ta thêm lượng nhỏ acid mạnh hoắc
base mạnh , hay pha loãng dung dịch
- Có hai loại dung dịch đêm + Hệ đệm acid : gồm một acid yếu và muối của nó với base mạnh
+Hệ đệm base : gồm một base yếu và muối của nó với acid mạnh -
Cơ chế tổng quát : trong dung dịch đệm tồn tại cân bằng :
+ khi thêm acid mạnh , ion H+ do acid mạnh phân li ra sẽ kết hợp với base tạo ra acid yếu liên hợp , lượng H+
tăng lên không đáng kể , và do đó Ph thay đổikhông đáng kể
+khi thêm base mạnh : ion OH- do base mạnh phân li ra sẽ kết hợp với ion H+ (do acid phân li ra) tạo ra nước
là chất điện li kém,lượng H+ bị hao hụt được bù lại nhờ cân bằng dịch chuyển về bên phải ,làm cho ph dung
dịch đệm thay đổi không đáng kể . -Vai trò :
+ Acid và độ kiềm đèu quan trọng đối với cơ thể
+ sự cân bằng độ ph của cơ thể con người có một tầm quan trọng to lớm cho sức khỏe , nhưng ít người biết về
nó và quan tâm đến sự cân bằng này
+thừa acid gây ra các bệnh như : thừa cân hoặc không giảm cân được, yếu xương, vấn đề răng miệng,thường
xuyên mệt mỏi, mất ngủ, tích tụ chất nhày, các vẫn đề về da ĐẶC BIỆT: -
Hệ đệm quan trọng trong máu người :
H2CO3/(Na+)HCO3- (Na+) H2PO4-/ (Na+)2HPO4 2- Hemoglobin/oxyhemoglobin -
Hệ đệm trong huyết tương :
Na2CO3 /NaHCO3 NaH2PO4/Na2HPO4 H- protein/Na- protein acid hữu cơ và muối của nó -
Hệ đệm trong hồng cầu :
Na2CO3/KHCO3 KH2PO4/ K2HPO4 HhbO2/KhbO2 HHb/KHb acid hữu cơ và muối kali của nó -Ứng
dụng :có nhiều ứng dụng
+ hóa học : dùng dung dịch đệm để tạo môi trường có ph ổn định dùng để tiến hành trong các phản ứng cần
môi trường ph không đổi
+ các cơ thể sinh vật chỉ tồn tại trong khoảng ph xác định
Các bước tiến hành pha dung dịch đệm ACETAT
Để pha 10ml dung dịch đệm acetat : cần 5ml dung dịch CH3COOH O,1 M và 5ml dung dịch CH3COONa 0,1M .
sau đó chia 3 ống -Thử tính chất : + ống 1 một giọt HCl 0,1M rồi đo ph
+ ống 2 một giọt dung dịch NaOH
+ ống 3 : 2 ml nước cất
CÂU 2 : Pha và thử tính chất của dung dịch đệm amoni ph=9,25
Các bước tiến hành : Để pha 10ml dung dịch đệm amoni có cần : 5ml NH3 0,1M VÀ 5ml NH4Cl 0,1M sau đó
chia 3 ống: + ống 1 : 2ml dung dịch đệm + 1 giọt HCl 0,1M
+ ống 2 : 2ml dung dịch đệm + 1 giọt NaOH 0,1 M
+ ống 3: 2ml dung dịch đệm + 2ml nước cất lOMoAR cPSD| 45148588
CÂU 3 : Nhận biệt các cation trong dung dịch ( có thể có : Ag+, Pb2+, Mg 2+, Ba 2+)
CÂU 4 : Nhận biết các anion trong hỗn hợp : (có thể có Cl-, CO3 2-, SO4 2-)
CÂU 5 : phản ứng của andehit fomic với thuốc thử Tollens ? lOMoAR cPSD| 45148588
Andehit và ceton :
-Là những hợp chất có chứa nhóm cacbonyl >C=O Andehit :
- liên kết với một phân tử H và một gốc hydrocacbon ta có hợp chất anđehit
( nhóm chức :-CHO : fomyl ) Ceton:
-Trườliên kết với 2 gốc hydrocacbon ta có ceton (nhóm chức : C=O :oxo) Ưng dụng :
+ andehit : thường sử dụng tẩy uế hay để bảo quản các mẫu sinh vật
+ceton :một lượng lớn được sử dụng để sản xuất tơ nhân tạo , thuốc sung skhông khói và là nguyên liệu tổng
hợp các chất hữu cơ quan trọng như cloroform , idoform, thuốc an thần, metylacrylat
Tiến hành thí nghiệm :
Lấy ống nghiệm sạch lần lượt cho vào ống nghiệm 1 ml dung dịch fomol và 3 giọt thuốc thử tollens Đun
cách thủy ống nghiệm 5p
Kq: xuất hiện lớp kim loại màu bạc bám trên thành ống nghiệm HCHO
+ 4 [Ag(NH3)3]OH -> (NH4)3CO3 + 4Ag + 6NH3 + 2H20
CÂU 6 : Phản ứng màu Biure và phản ứng HNO3 đặc của protein Protein :
KN : Protein là hợp chất cao phân tử có cấu trúc rất phức tạp. Thành phần gồm : C,H,O,N và 1 số nguyên tố
khác với lượng nhỏ PHÂN LOẠI:
-theo cấu tạo :+ protein đơn giản : khi thủy phân chỉ tạo một aminoacid như albumin ,colagen
+ protein phức tạp : khi thủy phân tạo các aminoacid và các thành phần khác như acid , lipd, glucid
-theo hình dạng :+ pr hình cầu +pr hình que
-theo chức năng sinh học : + enzym + pr vận chuyển +pr vận động
+ pr dinh dưỡng và dự trữ +pr cấu tạo + pr bảo vệ + pr điều hòa
CÁCH tiến hành thí nghiệm :
Cho 5 giọt lòng trắng trứng +5 giọt NaOH 0,2N . Thêm tiếp vào hỗn hợp 1 giọt dung dịch CuSO4 0,2 N
KQ : Xuất hiện kết tủa màu xanh lam sau khi lắc đều tạo phức xanh tím
CuSO4 + 2NaOH -> Cu(OH)2 kết tủa xanh + Na2SO4
Lòng trắng trứng + NaOH +CuSO4 -> phức xanh tím
CÂU 7 : PHÂN BIỆT Aldehit fomic (HCHO, fomol) ;Etanol (C2H5OH) ;Glyxerol (C3H5(OH)3) ; Glucose;NaOH lOMoAR cPSD| 45148588 ALDEHIT C2H5OH C3H5(OH)3 Glucose NaOH FOMIC (fomol) QUỲ −¿ −¿ −¿ −¿ XANH NaOH dư +CuSO4 Kết tủa Kết tủa ↓ Kết tủa ↓ Kết tủa ↓xanh × ↓xanh xanh xanh sau đó sau đó tan tan Bình ổn nhiệt Kết tủa −¿ −¿ Kết tủa ↓đỏ × (đun từng cặp ) ↓đỏ gạch gạch hoặc ↓ đồng
Chú thích áp dụng cho mọi bài về sau :
×:khôngxéttới
−:không hiệntượng
CÂU 8 : PHÂN BIỆT natri acetat (CH3COONa) ; acid acetic ( CH3COOH) ;glucose ;glyxerol ;aldehit fomic CH3COONa CH3COOH Glucose C3H5(OH)3 HCHO Đỏ NaOH dư + CuSO4 sau đó tan Đun (theo cặp) đỏ gạch Cu2O
Công thức cấu tạo của glu và fruc
CÂU 9 : PHÂN BIỆT : etanol ;aldehitfomic; lactose;saccarose; natri acetat lOMoAR cPSD| 45148588
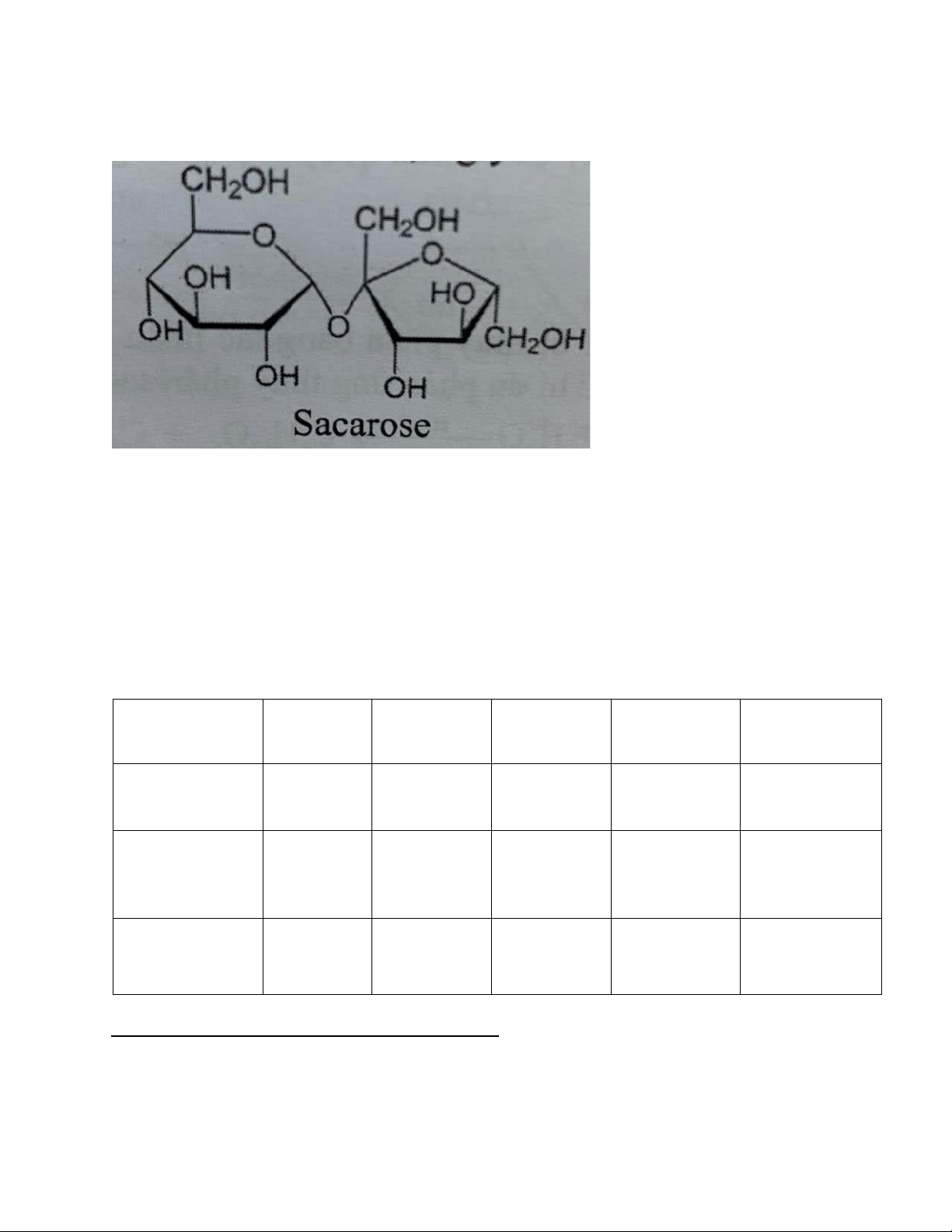
Phân tử saccarose gồm một gốc α–D – glucopyranose và một gốc β – D- fructofuranose liên kết với nhau nhờ liên kết 1,2- glycosid
Do không có nhóm –OH hemiacetal( nhóm OH ở C2 của gốc glu thứ 2) nên phân tử saccarose không còn khả
năng mở vòng, do đó saccarose là disaccasid không còn tính khử Laccarose là một disaccarit có tính khử
TRẠNG THÁI TỰ NHIÊN :
+ Glucose có hầu hết trong các bộ phận của thực vật ,trong mật ong chiếm trên 30%
+Fructose tự do có trong quả chín ngọt,trong mật ong chiếm khoảng 40%
+Saccarose tự do ( còn được gọi là đường mía, đường củ cải ) có nhiều trong cây mía, củ cải đường, quả thốt nốt....
+Lactose tự do ( còn đượcc gọi là đường sữa ) có trong sữa người và động vật có vú Tiến
hành thí nghiệm : C2H5OH HCHO Lactose Saccarose CH3COONa Quỳ −¿ −¿ −¿ −¿ Xanh NaOH dư + CuSO4 −¿ −¿ ↓sauđó↓tan ↓sauđó × ↓tan Đun −¿ ↓ đỏ gạch ↓ xám đen −¿ ×
Nếu cả 2 ống nghiệm đều xám đen thì cái nao ra trước là lactose cái nào ra sau là saccarose
CÂU 10 : PHÂN BIỆT : NaOH, NaCl, Na3PO4,NaCO3, NaI lOMoAR cPSD| 45148588 NaOH NaCO3 Na3PO4 NaCl NaI Qùy Xanh Xanh Xanh −¿ −¿ AgNO3 × × × ↓ trắng ↓ vàng HCl −¿ sủibọt khi,↑ −¿ × khí ko màu × AgNO3 ↓ xám −¿ ↓ trắng ×
CÂU 11 : PHÂN BIỆT : AgNO3 , MgCl2 , BaCl2 , Pb(CH3COO)2 , NaOH AgNO3 MgCl2 BaCl2 Pb(CH3COO)2 NaOH Quỳ −¿ −¿ −¿ Xanh Xanh HCl × × × ↓ trắng Ko hiện tượng HCl ↓ trắng −¿ −¿ × × Na2SO4 × −¿ ↓ trắng
CÂU 12 : PHÂN BIỆT : NaOH , HCl, BaCl2, Glyxerol, Glucose NaOH HCl BaCl2 Glyxerol Glucose lOMoAR cPSD| 45148588 Quỳ Xanh Đỏ −¿ −¿ −¿ Na2SO4 × × ↓ Trắng −¿ −¿ CuSO4 + NaOH × ↓sauđó ↓sauđó↓tan dư ↓ tan Đun −¿ ↓ đỏ gạch



