










Preview text:
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬
Bµi tËp ho¸ v« c¬ - phÇn I Ch¬ng 1
1. Dùa vµo ph¬ng ph¸p Slater h·y tÝnh n¨ng lîng tæng cña c¸c e trong nguyªn tö Li vµ ion
Li+ tõ ®ã tÝnh n¨ng lîng ion ho¸ thø nhÊt cña Li (I cña Li) 1 §¸p sè: -203eV; -196,8eV; 5,7eV (coi a = 0,31) i(1s)
2. Nguyªn tè Z = 19 cã thÓ viÕt cÊu h×nh e: 1s22s22p63s23p63d1 (I) hay 1s22s22p63s23p64s1 (II).
H·y chøng minh c«ng thøc II lµ hîp lý (dùa vµo viÖc tÝnh Z’ tõ ®ã tÝnh E (3d1) vµ E (4s1). e e
3. N¨ng lîng ion ho¸ I cña c¸c nguyªn tè chu kú 2 1 Li Be B C N O F Ne 5,4 9,32 8,32 11,26 14,53 13,6 17,42 21,5 eV
a. N¨ng lîng ion ho¸ t¨ng tõ ®Çu ®Õn cuèi chu kú. V× sao?
b. I cã gi¸ trÞ cùc ®¹i nhá ë Be, ë N; cùc tiÓu nhá ë B, ë O. Gi¶i thÝch. 1
c. TÝnh Z’ ®èi víi electron hãa trÞ cã n¨ng lîng cao nhÊt. §¸p sè:
c: 1,26; 1,66; 1,56; 1,82; 2,07; 2,00; 2,26; 2,52.
4. a. Ae(Si) = -134KJ.mol-1 P n»m bªn ph¶i Si nhng Ae(P) = -72 KJ.mol-1. H·y gi¶i thÝch sù bÊt thêng ®ã.
b. Nh÷ng yÕu tè g× ¶nh hëng lªn b¸n kÝnh nguyªn tö vµ ion? Cho vÝ dô minh ho¹.
d. §é t¨ng b¸n kÝnh ë nhãm IA (b¶ng 4): r = r - r (n + 1) n 0,2 0,42 0,1 0,12 Li Na K Rb Cs (1) (2) (3) (4)
Cã sù gi¶m m¹nh ë ®o¹n (3). T¹i sao?
5. a. TÝnh , biÕt D = 565; D = 151 kJ.mol-1; D = 432 kJ.mol-1 H HF F H 2 2
b. TÝnh n¨ng lîng liªn kÕt Cl – F, biÕt = 3,09; D = 239 kJ.mol-1 Cl Cl2 ch¬ng 2
1. Dùng công thức Lewis (giản đồ điểm electron Lewis); điện tích hình thức công thức cộng
hưởng, hãy xác định bậc liên kết của: a. OPCl - 2- 3 ; b. FSO3 ; c. SO4
2. a. Dự đoán cấu hình không gian của - NH -
3 , NH2 , NH4 ; so sánh góc liên kết giữa chúng.
- PCl5 và PCl6- ; so sánh góc liên kết giữa chúng.
b. Cho biết N trong 3 chất trên và P trong 2 chất dưới có thể có lai hóa gì?
3. Hãy dự đoán xem trong dãy hợp chất sau, góc liên kết tăng hay giảm a. NCl3, PCl3, AsCl3, SbCl3
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬ b. PF3, PCl3, PBr3
Từ đó hãy rút ra nhận xét về quan hệ giữa:
- Độ âm điện của nguyên tử trung tâm với góc liên kết
- Độ âm điện của nguyên tử bao quanh với góc liên kết
Hãy nêu nguyên nhân chính của hiện tượng trên.
5. a. Tính χH , biết DHF = 565; DF2 = 151, DH2(kJ.mol-1) , biết χF =4.
b. Tính năng lượng liên kết Cl-F, biết χCl =3.09, DCl2=239(kJ.mol-1)
a. TÝnh n¨ng lîng m¹ng líi NaCl theo ph¬ng ph¸p Born-LandÐ. BiÕt r = 0,95Ao; Na r = 1,81ACo; a = 1,7475. Cl NaCl
b. H·y so s¸nh víi kÕt qu¶ tÝnh theo ph¬ng ph¸p KapusTinsKÝi vµ víi kÕt qu¶ tÝnh theo chu
tr×nh Born-Haber, biÕt H o (NaCl) = -411,14 kJ.mol-1, H o (Na) = 108,44 kJ.mol-1, I (Na) = s nc 1 495,7 KJ.mol-1, E
= -240 kJ.mol-1, Ae(Cl) = -349kJ.mol-1. Cl-Cl
H·y cho nhËn xÐt vÒ 3 kÕt qu¶ tÝnh ®îc. §¸p sè:
BL: -768,63; K : -758,84; B-H: -756,28 p
6. ë thÓ h¬i vµ tr¹ng th¸i tan trong dung m«i h÷u c¬ nh«m clorua tån t¹i tr¹ng th¸i ë d¹ng
Al Cl . NghÜa lµ cã dime ho¸ 2 AlCl Al Cl . 2 6 3 2 6
H·y cho biÕt CHHH cña AlCl vµ Al Cl . 3 2 6
7. ViÕt c«ng thøc céng hëng cña NO ®Ó chøng minh nã còng cã hiÖn tîng dime ho¸ 2
2NO N O . BiÕt trong N O tån t¹i liªn kÕt N-N. 2 2 4 2 4
8. Dùa vµo qui t¾c Gillespie AX E , khi q = m + n = 4 vµ m = 4;3;2. th× hîp chÊt cã CHHH m n
thÕ nµo cho thÝ dô minh ho¹.
9. X¸c ®Þnh % ®Æc tÝnh ion vµ ®iÖn tÝch thùc cña liªn kÕt ë c¸cph©n tö sau: HF ( = 1,83D, l =
0,092 nm); HCl ( = 1,08D, l = 0,127 nm); HI ( = 0,44D, l = 0,161 nm). 6. Bµi tËp 3.4.
TÝnh n¨ng lîng trung b×nh cña liªn kÕt O – H vµ O – O trong ph©n tö H O dùa vµo c¸c sè 2 2 liÖu (kJ.mol-1) sau: Ho (H O, k) = -241,8; Ho (H, k) = 218; s 2 s Ho (H O, k) = 249,2; Ho (H O , k) = -136,3. s 2 s 2 2 §¸p sè: E = 463,5 kJ mol-; E = 143,7 kJ mol-1 O – H O – O 10) Bµi tËp 3.5.
TÝnh tæng entanpi hidrat ho¸ cña c¸c ion Mg2+ vµ Cl- theo ph¶n øng sau:
Mg2+(k) + 2Cl-(k) + aq Mg2+.aq + 2Cl-.aq
BiÕt r»ng entanpi hoµ tan vµ n¨ng lîng m¹ng ;íi ion cña MgCl (t.t) lÇn lît lµ -160 2 vµ 2480 kJ.mol-1.
§¸p sè: H = -2640 kJ. h 11) Bµi tËp 3.10.
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬
ë thÓ khÝ HF liªn hîp víi nhau b»ng liªn kÕt hidro t¹o thµnh vßng s¸u c¹nh (HF) theo 6 ph¶n øng sau: 6HF (HF) (k) 6 (k)
TÝnh n¨ng lîng liªn kÕt hidro trong (HF) , biÕt r»ng ë c¸c nhiÖt ®é 273K vµ 311K h»ng 6
sè K lÇn lît lµ 9,55.10-12 vµ 1,023.10-15. p §¸p sè: Kho¶ng 28302 J mol-1. Ch¬ng 3
1. trong dung dÞch c¸c axit HX (X = F … I), ®é m¹nh cña c¸c axit ®îc c¨n cø vµo ph¶n øng
sau: HX H+ + X- ë 25oC ®Ó tÝnh K th× ph¶i theo c«ng thøc Go = -RTlnK ; Go = aq aq aq a a Ho -TSo.
Cho b¶ng sè liÖu: (kJ.mol-1) Ho (HX) E (HX) I (H) Ae (X) Ho (H+) Ho (X-) TS h lk h h HF - 48,15 -563,54 1318,84 - 343,32 -1109,76 - 485,54 - 25 HCl -17,58 - 432 1315,84 -364,25 -1109,76 - 351,46 - 17,6
a. TÝnh pK cña HF vµ HCl (pK = -lgK ). a a a
b. Cho biÕt c¸c ®¹i lîng nµo cã ¶nh hëng m¹nh lªn tÝnh axit cña HX. 2. Bµi tËp 4.10.
C©n b»ng sau x¶y ra trong dung dÞch níc ë 25oC:
Pb(OH)2 + 2I- PbI2 + 2OH-
a. Hái chiÒu cña ph¶n øng ë ®iÒu kiÖn chuÈn?
b. Cã kÕt tña PbI kh«ng nÕu dung dÞch b·o hoµ Pb(OH) cã chøa KI 0,1M? 2 2
c. TÝnh nång ®é tèi thiÓu cña HNO ®Ó Pb(OH) b¾t ®Çu ph¶n øng víi H+theo ph¶n øng: 3 2 Pb(OH) + 2H+ Pb2+ + H O 2 2 15 9 Cho biÕt Tt . 4 10 Tt . 8 10 Pb(OH ) vµ 2 PbI 2
§¸p sè: a) ChiÒu nghÞch; b) Cã kÕt tña; c) [H+] > 5.10-10M. 3. a. TÝnh Go
cña ph¶n øng PbCl + 2I- PbI + 2Cl- 298 2 2
BiÕt TPbCl = 1,6.10-5; TPbI = 8.10-9. 2 2
b. Trong cèc cã s½n 0,16 mol PbCl . Cho vµo ®ã 1 lÝt dung dÞch KI 0,005M hái cã t¹o ra kÕt 2 tña PbI kh«ng? 2
4. C©n b»ng e cña c¸c ph¶n øng sau: a. Cu + HNO Cu(NO ) + NO + … 3 lo·ng 3 2
b. K Cr O + KNO + H SO Cr (SO ) + KNO + … 2 2 7 2 2 4 2 4 3 3 c. As S + HNO H AsO + H SO + NO + … 3 3 3 (d) 3 4 2 4
d. [Cr(OH) ]3- + H O CrO 2- + OH- 6 2 2 4
e. Al + HNO … + N O + … 3 2
g. Fe O + HNO Fe(NO ) + NO + … 3 4 3 3 3 5. Bµi tËp 4.4.
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬
C©n b»ng sau x¶y ra trong dung dÞch níc ë 25oC:
2Cr2+ + Cd2+ 2Cr3+ + Cd (t.t.) BiÕt: o(Cr3+/Cr2+) = -0,41V; o(Cd2+/Cd) = -0,40V;
a. ë ®iÒu kiÖn chuÈn ph¶n øng x¶y ra theo chiÒu nµo?
b. Trén 25cm3 dung dÞch Cr(NO ) 0,4M víi 50cm3 dung dÞch Cr(NO ) 0,02M; 25cm3 dung 3 3 3 2
dÞch Cd(NO ) 0,04M vµ bét Cd. Hái chiÒu ph¶n øng trªn trong ®iÒu kiÖn nµy? 3 2 §¸p sè:
a) ChiÒu thuËn: b) ChiÒu nghÞch 6. Bµi tËp 4.5.
ë 25oC cã o(H O /H O) = 1,77V; o(O /H O) = 1,23V 2 2 2 2 2
a. TÝnh o cña cÆp O /H O . 2 2 2
b. TÝnh h»ng sè c©n b»ng K cña ph¶n øng sau trong dung dÞch níc: 2H O 2H O + O 2 2 2 2 §¸p sè: a. o(O /H O ) = 0,69V 2 2 2 b. K 4,07.1036. 7. Bµi tËp 4.9.
Gi¶n ®å thÕ khö chuÈn cña mangan, s¾t vµ thiÕc nh sau: MnO - MnO 2- MnO Mn3+ Mn2+ Mn 4 4 2 0.56V 2,26V 0.95V 1.51V -1.18V Fe3+ Fe2+ Fe; Sn4+ Sn2+ Sn 0.77V -0.44V 0.15V -0.14V
H·y dù ®o¸n s¶n phÈm cña c¸c ph¶n øng sau:
a) MnO - + Fe2+ + H+ (kÓ c¶ khi d MnO -)
b) Sn + Fe3+ (kÓ c¶ khi d Sn) 4 4 §¸p sè:
a) Mn2+ + Fe3+ ; NÕu d MnO - th× s¶n phÈm lµ MnO vµ Fe3+. 4 2
b) Sn4+ + Fe2+ ; NÕu d Sn th× s¶n phÈm lµ Sn2+ + Fe2+. 8. 1,21V ClO - HClO 1,64V HClO 1,63V Cl 1,36V Cl- 3 2 2 oBr /Br- = 1,07. 2
a. Dù ®o¸n s¶n phÈm cña ph¶n øng: ClO - + Br- + H+ Br + … 3 2
b. ë pH b»ng mÊy th× ph¶n øng trªn kh«ng diÔn ra.
9. ThÕ khö chuÈn cña kim lo¹i kiÒm ®îc tÝnh theo c«ng thøc sau: o G G G M+/M = a I h ,
4 44 (Xem ho¸ häc v« c¬ - Lª MËu QuyÒn, trang 163) nF
Go = Go nguyªn tö ho¸; Go = Go ion ho¸; Go = Go hydrat ho¸, J.mol-1 a I h
TÝnh oNa+/Na vµ oLi+/Li vµ cho biÕt v× sao oLi+/Li < oNa+/Na CÆp M+/M Go (M) Go (M) Go (M+) a I h Li+/Li 128030 521745 - 509611 Na+/Na 77822 797477 -410032 §¸p sè:
oLi+/Li = - 2,99V; oNa+/Na = - 2,73V.
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬ ch¬ng 4
1. TÝnh nhiÖt hoµ tan cña tinh thÓ c¸c muèi sau: a. U H (M+) H (X-) h h LiF - 1021,58 - 531,36 - 485,34 KJ.mol-1 NaF - 904,35 - 422,59 - 485,34 KF - 808,00 - 338,9 - 485,34
Cho biÕt nÕu c¨n cø vµo nhiÖt hoµ tan th× theo chiÒu tõ LiF ®Õn KF ®é hoµ tan t¨ng hay gi¶m. b. U H (Ag+) H (X-) kJ.mol-1 h h AgF - 954,59 - 489,53 - 485,34 AgCl - 904,35 - 489,53 - 351,46 AgBr - 895,975 - 489,53 - 317,98
Cho biÕt nÕu c¨n cø vµo ®é hoµ tan th× theo chiÒu tõ AgF ®Õn AgBr ®é hoµ tan t¨ng hay gi¶m.
c. H·y so s¸nh kÕt qu¶ tÝnh to¸n víi thùc nghiÖm ®Ó rót ra c¸c nhËn xÐt vÒ c¸c yÕu tè ¶nh
hëng tÝnh tan cña hîp chÊt ion: Thùc nghiÖm cho biÕt: LiF NaF KF AgF AgCl AgBr §é hoµ tan 0,1mol/l 1,1mol/l 15,9mol/l Tan dÔ Tt = 10-10 Tt = 5.10-13
2. Bµi tËp 5.8 trang 33 s¸ch bµi tËp.
NhiÖt sinh chuÈn cña CaCl (t.t), CaCl .6H O (t.t) vµ H O(l) lÇn lît lµ -796,1; -2608,9 2 2 2 2 vµ -285,8 kJ.mol-1.
a. TÝnh entanpi chuÈn hidrat ho¸:
CaCl (t.t) + 6H O(l) CaCl .6H O(t.t) 2 2 2 2
b. TÝnh entanpi chuÈn hoµ tan CaCl (t.t) vµ CaCl .6H O(t.t) trong níc biÕt r»ng nhiÖt sinh 2 2 2
chuÈn cña Ca2+.aq vµ Cl-.aq lÇn lît lµ -543 vµ -167,1 kJ.mol-1. §¸p sè: a. -98kJ.mol-1.
b. Ho (CaCl , t.t) = -81,1 kJ.mol-1 ht 2
Ho (CaCl .6H O, t.t) = 16,9 kJ.mol-1 ht 2 2
4. Bµi tËp 5.6 trang 32 s¸ch bµi tËp.
ThÕ nµo lµ chÊt thuËn tõ, nghÞch tõ. Momen tõ cña CuSO .5H O vµ MnSO .4H O lÇn 4 2 4 2
lît lµ 1,95 vµ 5,86 . Hai chÊt ®ã lµ thuËn tõ hay nghÞch tõ? TÝnh sè electron ®éc th©n B B
trong ph©n tö mçi chÊt trªn.
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬ phÇn Ii
Ch¬ng 1: hydr« vµ h O 2
1. C¸c c©u hái 6.1 ; 6.2; 6.4; 6.5; 6.6 trang 34 s¸ch bµi tËp
6.1: Tr×nh bµy tÝnh chÊt ho¸ häc cña hidr«. LÊy vÝ dô chøng minh r»ng hidr« míi sinh
ho¹t ®éng ho¸ häc m¹nh h¬n hidr« thêng. Gi¶i thÝch.
6.2: Tr×nh bµy c¸c ph¬ng ph¸p ®iÒu chÕ hidr« trong c«ng nghiÖp vµ trong phßng thÝ
nghiÖm. T¹i sao ®iÒu chÕ hidr« trong phßng thÝ nghiÖm ngêi ta thêng dïng kÏm t¸c dông
víi dung dÞchH SO lo·ng vµ thªm vµo ®ã Ýt giät dung dÞch CuSO ? Cã thÓ thay thÕ H SO 2 4 4 2 4
lo·ng b»ng H SO ®Æc b»ng HNO hoÆc HCl kh«ng? T¹i sao? 2 4 3
6.4: Gi¶i thÝch tÝnh chÊt lÝ häc bÊt thêng cña níc so víi c¸c chÊt láng kh¸c: khèi
lîng riªng lín nhÊt ë 4oC, nhiÖt dung riªng cao bÊt thêng.
6.5: Gi¶i thÝch t¹i sao níc võa cã tÝnh chÊt «xi ho¸ võa cã tÝnh chÊt khö vµ c¸c tÝnh
chÊt nµy ®Òu phô thuéc vµo pH.
6.6: Nh÷ng muèi nµo khi tan trong níc bÞ thuû ph©n vµ m«i trêng cña dung dÞch c¸c
muèi ®ã lµ g×? LÊy vÝ dô minh häa.
2. Cho c¸c cÆp «xi ho¸ khö sau: a. MnO -
4 + 3e + 4H+ MnO2(r) + 2H2O (1) = 1,7V
LËp biÓu thøc - pH cña cÆp «xi ho¸ khö trªn khi [MnO -] = 10-2M vµ cho biÕt ë pH = 4
6 H O rÊt Ýt bÞ «xi ho¸ bëi MnO - t¹i sao? 2 4 b.
[Co(NH3)6]3+ + 1e [Co(NH3)6]2+ (2) = 0,1V
ViÕt ph¶n øng x¶y ra (nÕu cã) khi tån t¹i phøc [Co(NH ) ]2+ trong níc. NÕu ph¶n øng 3 6
x¶y ra th× H O ®ãng vai trß? 2
c. Co3+ + 1e Co2+ (3) = 1,8V
ViÕt ph¶n øng x¶y ra khi cho dung dÞch H SO lo·ng vµo Co(OH) ? Vai trß cña H O. 2 4 3 2
3. Bµi tËp 6.8 trang 36 s¸ch bµi tËp
TÝnh nhiÖt ®é nãng ch¶y cña níc ®¸ ë ¸p suÊt 1500atm, biÕt r»ng khèi lîng riªng cña
níc ®¸ lµ 917 kg.m-3 vµ nhiÖt nãng ch¶y cña nã lµ 319,7kJ.kg-1.
§¸p sè: T 261,65K hay -11,5oC.
4. Qu¸ tr×nh tan cña níc ®¸:
H2O(r) H2O(l) = 6,01kJ.mol-1 TÝnh Go
cña qu¸ tr×nh, cho biÕt nguyªn nh©n lµm cho qu¸ tr×nh tù x¶y ra. Coi Ho, 278K
So kh«ng ®æi theo T trong kho¶ng 0oC ®Õn 5oC.
5. Bµi tËp 6.11 trang 37 s¸ch bµi tËp TÝnh Go cña qu¸ tr×nh H 2 O ( l , - 1 0o C ) H 2 O ( t . t , - 1 0o C
) theo hai ph¬ng ph¸p sau:
a. TÝnh tõ Ho vµ So cña c¸c giai ®o¹n sau: H2O (l,-10oC) H2O (l, 0oC) H2O (l, 0oC) H2O (t.t, 0oC) H 2O (t.t, 0oC) H2O (t.t,-10oC)
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬
b. ThiÕt lËp ph¬ng tr×nh Ho = f(T) dùa vµo c«ng thøc o o
(H ) C vµ Go theo c«ng T p T o o G H thøc: T 2 T T T
Ho ®«ng ®Æc cña níc ë 0oC lµ -6kJ.mol-1, nhiÖt dung mol cña níc ®¸ Co = 75,5 JK-1.mol-1. P §¸p sè: a. Go -212,24 J.mol-1. 263 b. Go -211,92 J.mol-1. 263 Ch¬ng ii: halogen
1. V× sao ¸i lùc e cña F: Ae(F) = -328 kJ.mol-1 > Ae(Cl) = -342 kJ.mol-1 nhng thÕ khö chuÈn: o - -
F /F = 2,85V > o Cl /Cl = 1,36V ? 2 2
2. C©u 7.1 trang 39 s¸ch bµi tËp
T¹i sao Flo kh«ng cã sè «xi ho¸ d¬ng vµ chØ cã ho¸ trÞ mét, trong khi ®ã c¸c nguyªn
tè cßn l¹i trong nhãm l¹i cã c¶ sè «xi ho¸ d¬ng vµ cã nhiÒu ho¸ trÞ kh¸c nahu 1, 3, 5 vµ 7.
3. C©u 7.3 trang 39 s¸ch bµi tËp
LÊy c¸c vÝ dô minh ho¹ tÝnh «xi ho¸ m¹nh cña Halogen vµ tÝnh nµy gi¶m dÇn tõ trªn
xuèng trong nhãm, cßn tÝnh khö cña chóng l¹i t¨ng dÇn theo chiÒu trªn, trõ Flo.
4. ViÕt ph¶n øng x¶y ra khi ®iÖn ph©n dung dÞch NaCl trong c¸c trêng hîp sau: a. Cã mµng ng¨n b. Kh«ng cã mµng ng¨n
c. Dung dÞch NaCl nãng > 80oC, kh«ng cã mµng ng¨n.
5. C©u 7.5 trang 39 s¸ch bµi tËp
So s¸nh tÝnh chÊt cña HF víi c¸c HX kh¸c trong cïng nhãm. Th«ng thêng mét axit ph¶n øng
víi mét «xit baz¬, mµ kh«ng ph¶n øng víi mét «xit axit, nhng axit flohi®ric l¹i ph¶n øng
®îc víi c¶ «xit axit SiO . Gi¶i thÝch trêng hîp nµy. 2
6. C©u 7.8 trang 40 s¸ch bµi tËp
Sôc khÝ clo vµo dung dÞch NaOH, sau ®ã ®un nãng cho tíi kh«. TiÕp tôc ®un ®Õn khi ph©n huû
hoµn toµn. ViÕt c¸c ph¬ng tr×nh ph¶n øng x¶y ra.
7. C©u 7.9 trang 40 s¸ch bµi tËp
ViÕt c¸c ph¬ng tr×nh ph¶n øng sau díi d¹ng ion (nÕu cã) vµ ph©n tö, kÌm theo c¸ch
x¸c ®Þnh hÖ sè chÊt «xi ho¸ vµ chÊt khö:
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬
a. F2 + SiO2 i. Cl2 + KOH(nguéi vµ nãng)
b. X2 + H2O (X: halogen) k. NaOCl + KI + H2SO4(lo·ng)
c. Cl2 + HX (X: Br, I) l. CaOCl2 + HCl(®Æc)
d. MnO2(KMnO4;r) + HCl(®Æc, nãng) m. KClO3 + KI + H2SO4(lo·ng) e. H
2SO4(®Æc, nãng) + HX n. KClO3(r) (cã vµ kh«ng cã xóc t¸c MnO2)
g. Fe2(SO4)3 + KI(dd) o. KIO3 + KI + H2SO4(lo·ng) h. HF + SiO2 8. o - - -
NO /HNO = 0,94V; o I /I = 0,54V 3 2 3
a. ë ®iÒu kiÖn chuÈn, 25oC ph¶n øng sau diÔn ra theo chiÒu nµo? 2NO - -
3 + 9I- + 6H+ 3I3 + 2HNO2 + 2H2O
b. NÕu chØ thay ®æi pH th× ë pH b»ng mÊy ph¶n øng sÏ ®æi chiÒu?
c. ChØ ra gi¸ trÞ cña pH ë ®ã cïng tån t¹i c¶ 4 chÊt cña 2 cÆp «xi ho¸ khö trªn. 9. Cho o - -
I (r¾n)/I = 0,53V; o I (dd)/I = 0,62V 2 2
a. TÝnh ®é hoµ tan (S (mol/l)) cña I trong níc nguyªn chÊt vµ cho biÕt cã pha ®îc o 2 dung dÞch I 0,1M kh«ng. 2
b. TÝnh h»ng sè c©n b»ng cña ph¶n øng I - 2 + I- 3I3 BiÕt o - - I /I = 0,54V 3
d. TÝnh ®é hoµ tan (S) cña I trong dung dÞch KI 0,2M 2
10. Bµi tËp 7.14 trang s¸ch bµi tËp
Sôc khÝ clo (P = 1atm) vµo níc nguyªn chÊt ë 25oC x¶y ra ph¶n øng sau: Cl2(k) + H2O HClO + H+ + Cl-
a. TÝnh h»ng sè c©n b»ng K cña ph¶n øng, nång ®é c¸c ion, ph©n tö trong c©n b»ng vµ pH cña dung dÞch.
b. TÝnh nång ®é Cl .aq trong dung dÞch do ph¶n øng: 2 Cl2(k) + aq Cl2.aq
c. TÝnh ®é hoµ tan cña Cl (mol.l-1) trong níc. 2
d. TÝnh ®é hoµ tan cña Cl (mol.l-1) trong c¸c dung dÞch sau: 2 + NaCl 1M + HCl 1M Cho biÕt o - - -
(Cl (k)/Cl ) = 1,36V; o (Cl .aq/Cl ) = 1,40V; o (HClO/Cl ) = 1,49V 2 2
Ch¬ng iii: nhãm via
1. ViÕt cÊu h×nh e cña ph©n tö O theo ph¬ng ph¸p MO_LCAO vµ cÊu h×nh e cña nguyªn tö 2
¤xi díi d¹ng « lîng tö tõ ®ã h·y cho biÕt t¹i sao O thuËn tõ O nghÞch tõ. 2 3
2. a. N¨ng lîng ph¸ vì liªn kÕt cña O lµ 498,7kJ.mol-1. TÝnh (nm) cña ph«t«n cã thÓ 2 max
g©y ra sù ph©n ly O thµnh O, ®Ó nhê ®ã ¤z«n ®îc t¹o thµnh ë tÇng b×nh lu. 2
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬
b. ViÕt ph¶n øng t¹o thµnh vµ ph©n ly ¤z«n ë tÇng b×nh lu. Nã cã ý nghÜa g× cho cuéc
sèng cña sinh vËt trªn tr¸i ®Êt?
c. C¸c chÊt CFC (vÝ dô: FrÐon 12 - CF Cl ) cã t¸c dông g× lªn O ë tÇng b×nh lu? 2 2 3
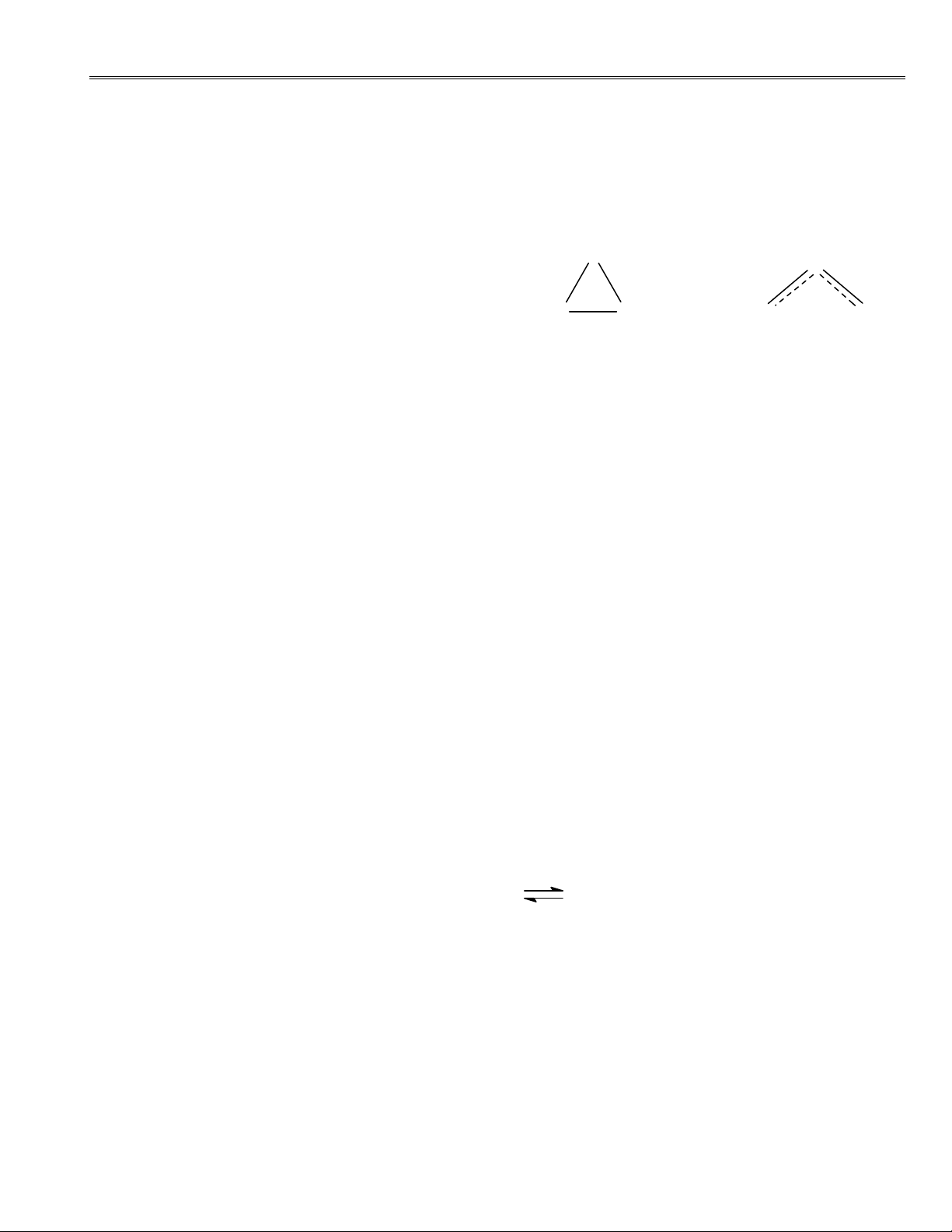
3. Tríc ®©y c«ng thøc cÊu t¹o cña ¤z«n ®îc viÕt lµ (1) sau nµy ngêi ta viÕt theo c«ng thøc cÊu t¹o (2)
a. C«ng thøc nµo ®óng? C¨n cø vµo ®©u ®Ó biÕt ®îc. O O
b. Tõ c«ng thøc (2) h·y viÕt c«ng thøc céng (1) (2)
hëng cña O vµ nhê ®ã tÝnh ®îc ®iÖn tÝch h×nh 3 O O O O
thøc cña tõng «xi; tÝnh ®îc bËc liªn kÕt trong O . 3
4. C©u 8.5 s¸ch bµi tËp trang 49.
Lùc axit cña hydr«xit axit phô thuéc vµo nh÷ngc yÕu tè g×? ViÕt c«ng thøc cÊu t¹o cña c¸c ph©n tö sau:
a. C¸c axit m¹nh H SeO vµ HClO . 2 4 4
b. C¸c axit trung b×nh H PO vµ H PO . 3 3 3 2
c. C¸c axit yÕu H TeO vµ H AsO . 6 6 3 3
5. ViÕt ph¶n øng minh ho¹ c¸c chÊt sau: H S; SO ; H SO thÓ hiÖn tÝnh khö, tÝnh «xi ho¸? Nªu 2 2 2 4
nhËn xÐt chung vÒ tÝnh «xi ho¸ khö cña mét nguyªn tè trong hîp chÊt.
6. C©u 8.12 s¸ch bµi tËp trang 50.
T¹i sao khi hoµ tan mét sufua tan ®îc trong axit (FeS, MnS, ZnS trong HCl) ngoµi H S 2
®îc t¹o thµnh ta thÊy lu«n cã mét lîng S kÕt tña.
7. C©u 8.13 s¸ch bµi tËp trang 50.
ViÕt c¸c ph¬ng tr×nh ph¶n øng sau díi d¹ng ion (nÕu cã) vµ ph©n tö: a. O + PbS g. PbS + H O (dd) 3 2 2 b. O + KI (dd) h. H O + KMnO + H SO (lo·ng) 3 2 2 4 2 4 c. O + KI + H SO (lo·ng) i. H S + O (ghi ®iÒu kiÖn) 3 2 4 2 2 d. H O + KI (dd) k. Fe + H+ + SO 2- 2 2 4 e. H O + KI + H SO (lo·ng) 2 2 2 4
8. ë 800K h»ng sè c©n b»ng cña ph¶n øng (1) lµ k = 1,21.105. p 2SO2(k) + O2(k) 2SO3(k)
§èt Pyrit FeS trong kh«ng khÝ ngêi ta thu ®îc hçn hîp khÝ (A) cã thµnh phÇn theo 2
thÓ tÝch: 7%SO ; 10%O ; 83%N . TiÕp theo SO ®îc «xi ho¸ thµnh SO (cã mÆt chÊt xóc 2 2 2 2 3
t¸c). NÕu xuÊt ph¸t tõ 100mol khÝ A th× ph¶n øng ®¹t c©n b»ng ë 800K, ®îc hçn hîp khÝ (B).
Cho toµn bé khÝ B hÊp thô vµo níc ®îc 69,2lÝt dung dÞch C.
TÝnh pH cña dung dÞch C, coi SO kh«ng bÞ hÊp thô bëi dung dÞch H SO . 2 2 4
9. Bµi tËp 8.21 s¸ch bµi tËp trang 57.
Mét b×nh cÇu dung tÝch 500cm3 chøa hçn hîp khÝ O vµ O ë ®iÒu kiÖn chuÈn (0oC vµ 2 3
1atm). Cho mét lîng d dung dÞch KI vµo b×nh cÇu vµ l¾c m¹nh, sau ®ã trung hoµ kiÒm b»ng
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬
dung dÞch H SO . Iot t¹o ra ph¶n øng võa ®ñ víi 37,6cm3 dung dÞch Na S O 0,1M. TÝnh phÇn 2 4 2 2 3
tr¨m sè mol O trong hçn hîp khÝ. 3
10. Bµi tËp 8.22 s¸ch bµi tËp trang 57.
TÝnh ®é hoµ tan (mol.l-1) cña ZnS trong dung dÞch HCl 0,1M vµ 2M, biÕt r»ng K vµ K 1 2
cña H S lµ 10-7 vµ 10-14, tÝch sè tan cña ZnS lµ 10-23 vµ nång ®é b·o hoµ cña H S trong dung 2 2 dÞch lµ 0,1M. Ch¬ng iv. Nhãm VA
1. C©u 9.12 s¸ch bài tập
T¹i sao m«i trêng cña dung dÞch Na HPO lµ kiÒm cßn dung dÞch NaH PO lµ axit? 2 4 2 4
Dïng c¸c sè liÖu h»ng sè ®iÖn ly axit cña H PO ®Ó gi¶i thÝch. 3 4
2. Cho 2,24l (đktc) khÝ NO hấp thụ hết vào 1l dung dịch NaOH 0,1M được dung dịch A. 2
TÝnh pH của dung dịch A. Coi thể tÝch kh«ng đổi. 3. C©u 9.13 s¸ch bµi tËp
ViÕt c¸c ph¬ng tr×nh ph¶n øng sau díi d¹ng ion (nÕu cã) vµ ph©n tö: to
a. NaNO + NH Cl (dd b·o hoµ) p. HNO ®Æc + S 2 4 3 d. CO + NH (d) s. Au + HNO + HCl 2 3 3 P, e. NH (k) + CO (k) t. NH HCO (r) 3 2 4 3 g. NH (k) + O (k)
z. HNO (lo·ng) + M (M: P, As, Sb, Bi) 3 2 3 Pt, 800oC h. NH (k) + O 3 2
. NaBiO (R) + MnSO + H SO (dd) 3 4 2 4 i. NH + Cl 3 2
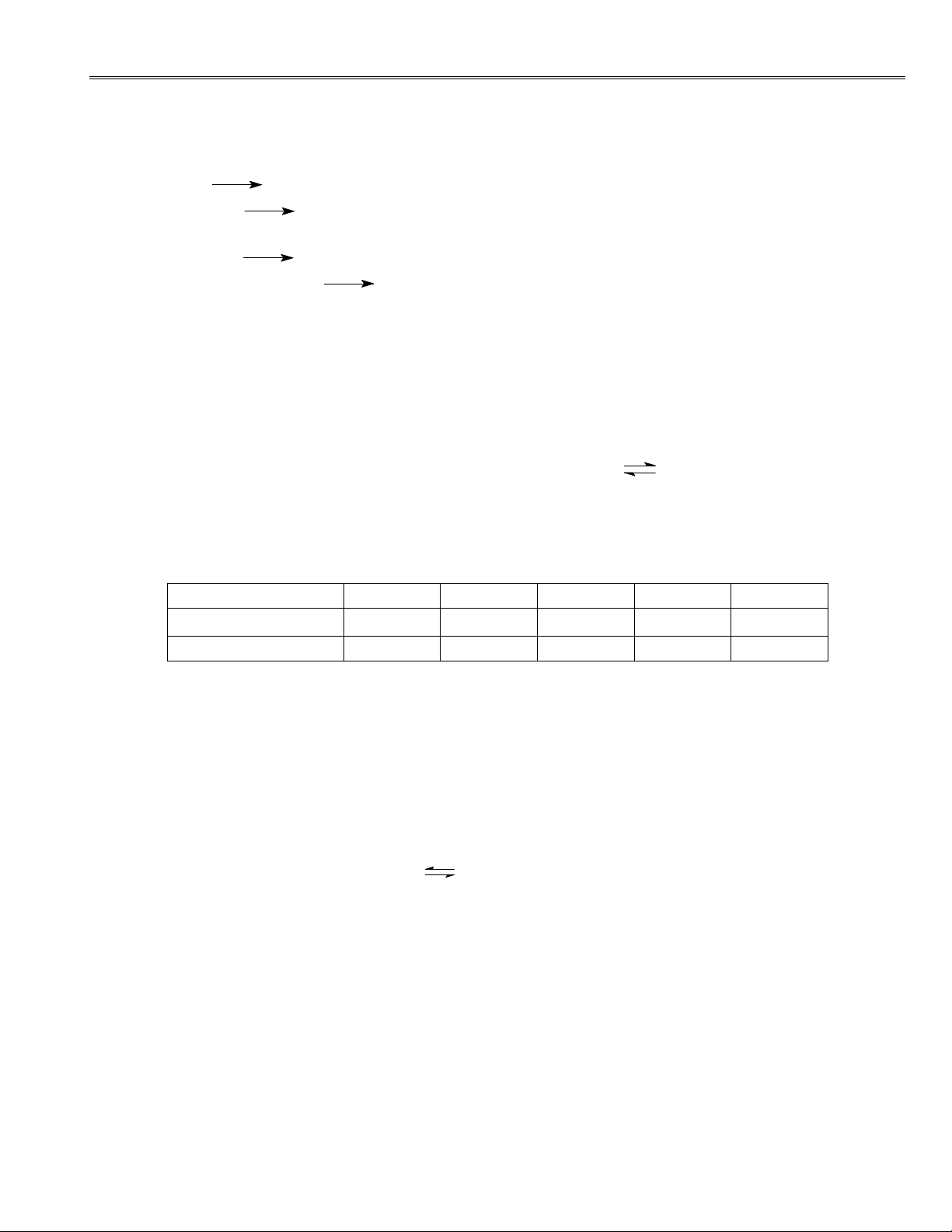
. Na AsO + KI + H SO lo·ng 3 4 2 4 k. NaNO + KI + H SO lo·ng 2 2 4 . SbCl + H O l. NaNO + KMnO + H SO lo·ng 3 2 2 4 2 4 . Bi(NO ) + H O m. HNO 3 3 2 2 n. HNO 3 4. N O - 3 H N O 2 N O (m«i trường axit) 0,94V 1,00V
a. Viết phản ứng ph©n huỷ của HNO và tÝnh hằng số c©n bằng của phản ứng. 2 - b. H N O 2 H+ + N
O 2 pK = 3,3. H·y cho biết ở pH bằng mấy th× trong a dung dịch - [HNO ] > [NO -] 2 2 - [NO -] > [HNO ] 2 2
c. Hợp chất N(III) cã thể tồn tại ở dạng HNO hay NO -. Nếu chỉ thay pH th× ở pH 2 2
bằng bao nhiªu hợp chất N(III) sẽ bền. Coi P = 1atm. Biết với cặp N(V)/N(III) = NO
NO -/HNO (NO -) người ta đã lập được quan hệ - pH như sau: 3 2 2
pH < 3,3 ’= 0,94 – 0,09 pH 1
pH > 3,3 ’= 0,84 – 0,06 pH. 2 o , 0 06 [Oxh]
Khi giải dïng c«ng thức lg n [Kh]
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬
5. Dung dịch b·o hoà Mg(OH) cã pH = 10,36 pK (NH ) = 4,744 2 b 3
a. Trộn 500ml dung dịch MgCl 0,1M với 500ml dung dịch NH 0,2M. Hỏi trong dung 2 3
dịch thu được cã tạo ra kết tủa Mg(OH) kh«ng? 2
b. Nếu cã kết tủa Mg(OH) th× phải thªm Ýt nhất mấy mol NH Cl để hoà tan hết lượng 2 4 kết tủa đã.
6. Bài tập 9.23 s¸ch bài tập
H»ng sè ®iÖn ly axit cña cÆp H PO -/HPO 2- lµ K = 6,2.10-8. 2 4 4 2
a. TÝnh pH cña dung dÞch chøa cïng sè mol Na HPO vµ NaH PO . 2 4 2 4
b. Muèn chuÈn bÞ mét dung dÞch ®Öm cã pH = 7,38 cÇn ph¶i hoµ tan bao nhiªu gam
NaH PO .H O trong 1 lÝt dung dÞch Na HPO 0,1M. 2 4 2 2 4
P = 31, O = 16, H = 1, Na = 23. §¸p sè: a. pH = 7,21 b. kho¶ng 9,33g
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬ Ch¬ng v. Nhãm iVA
1. C©u 10.10 s¸ch bài tập
ViÕt c¸c ph¬ng tr×nh ph¶n øng sau díi d¹ng ion (nÕu cã) vµ ph©n tö: b. CO (k) + Ca g. Na CO + H O 2 2 3 2 c. CO (k) + aq i. Si + HF + HNO (dd) 2 3 d. KHCO (r) k. Si + KOH (dd) 3 e. Mg(HCO ) l. SiO + HF 3 2 2 to
m. SiO + NaOH(n.c) hoÆc Na CO (n.c) 2 2 3
o. Pb(NO ) + NaOH (dd, thiÕu vµ d) hoÆc KI (dd, thiÕu vµ d) 3 2
s. Sn(OH) + HCl (dd, thiÕu vµ d) t. PbO + Mn(NO ) + HNO lo·ng 2 2 3 2 3
2. C¸cbon 14 ph©n r· phãng x¹ theo ph¶n øng sau: 14C 0e (h¹t ) + 14N 6 -1 7
Chu kú b¸n ph©n huû rÊt lín: t = 5730 n¨m. 1/2
N¨m 1960 nhµ Ho¸ häc Mü Williard Frank Libby ®· ®îc tÆng gi¶i thëng Nobel nhê
c«ng tr×nh “§Þnh niªn ®¹i b»ng c¸cbon phãng x¹” (Radiocarbon dating) (cho c¸c vËt kh¶o cæ cã nguån gèc h÷u c¬).
a. C¬ së khoa häc cña ph¬ng ph¸p: Radocarbon ®aling lµ g×?
b. H·y tÝnh tuæi cña mét mÈu gç kh¶o cæ cã ®é phãng x¹ b»ng 70% ®é phãng x¹ cña
mÈu gç hiÖn ®¹i (xem bµi tËp 10.12 s¸ch bµi tËp)
3. Quan s¸t gi¶n ®å pha cña H O vµ CO , h·y cho biÕt : 2 2
a. V× sao OB nghiªng sang tr¸i, OB’ nghiªng sang ph¶i.
b. HiÖn tîng g× x¶y ra khi níc ®¸ vµ tuyÕt CO ®îc ®Ó trong kh«ng khÝ (¸p suÊt b»ng 2 1atm). Gi¶i thÝch? B C B’ C’ t t suÊ p suÊ ¸ L p ¸ L R R 0,006atm 5,2atm O O H 1atm H A A’ 0,01oC -78oC -57oC NhiÖt ®é NhiÖt ®é Gi¶n ®å pha H O 2 Gi¶n ®å pha CO 2
4. Bµi tËp 10.20 s¸ch bµi tËp
Dù ®o¸n c¸c s¶n phÈm ph¶n øng sau: a. Sn + H+ b. Sn + Hg2+
BiÕt r»ng gi¶n ®å thÕ khö chuÈn cña c¸c chÊt nh sau:
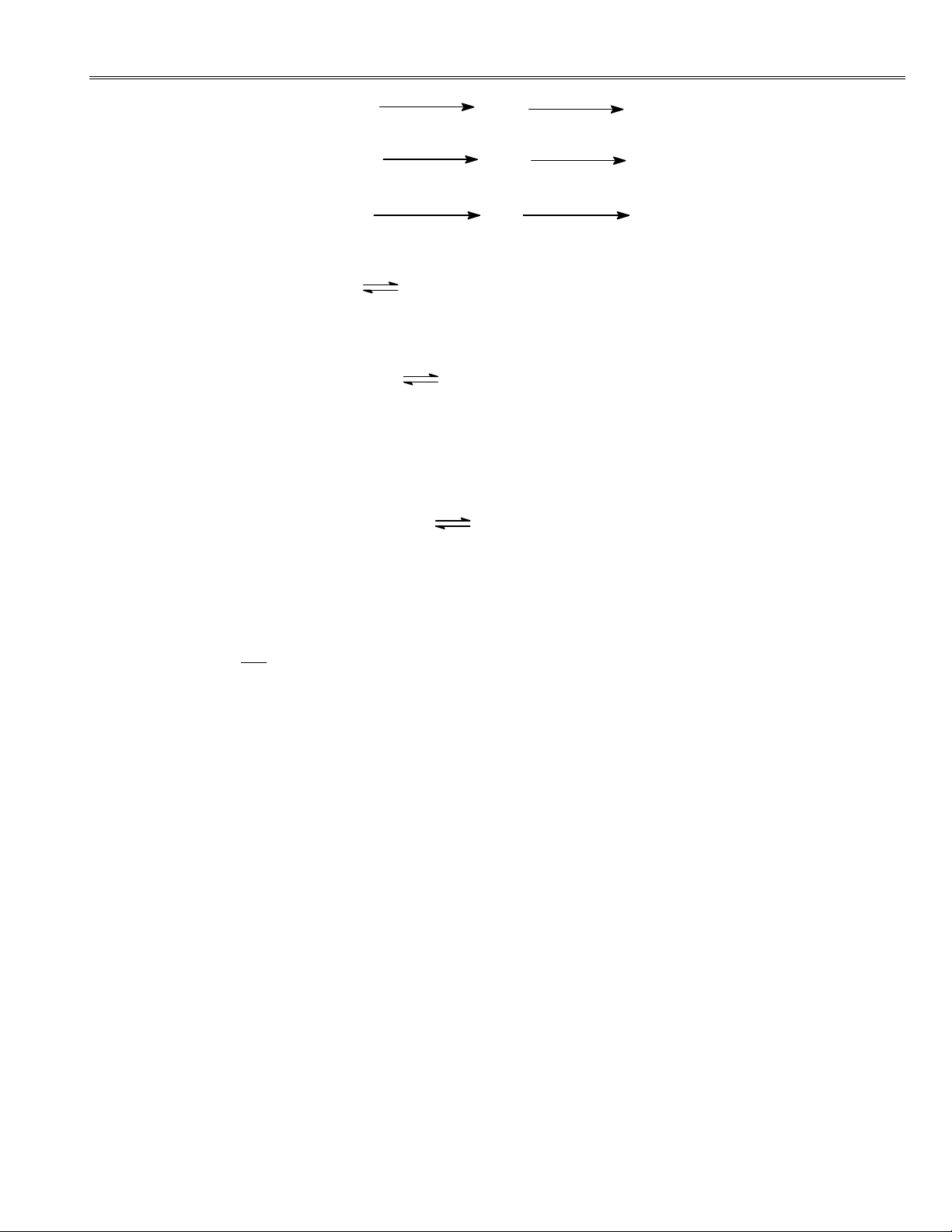
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬ Sn4+ 0 , 1 5 V Sn2+ 0 , 1 4 V Sn Hg2+ 0 , 9 2 V Hg 2+0,79V 2 Hg H+ 0 , 0 0 V H 2,25V 2 H- 5. Ge t¹o ra 2 oxyt GeO, GeO 2
2Ge(r) + O2(k) GeO (1) (1) Go = -510 1 0 0 0 + 130T
2GeO + O2(k) GeO2 (1) (2) Go = -594000 + 226T 2
H·y x¸c ®Þnh kho¶ng nhiÖt ®é GeO bÒn. (lu ý: cÇn lËp G o cña ph¶n øng (3) 3 2GeO Ge + GeO2 (3)
6.a. Dung dÞch CO ®îc chÕ ngù bëi khÝ CO díi ¸p suÊt 1atm. TÝnh pH cña dung dÞch. 2 2
b. Ngêi ta hoµ tan CaCO vµo dung dÞch trªn tíi khi b·o hoµ vµ gi÷ ¸p suÊt cña CO lu«n 3 2
b»ng 1atm. TÝnh pH vµ ®é hoµ tan cña CaCO trong dung dÞch thu ®îc. BiÕt axit yÕu CO .aq 3 2
cã pK = 6,4; pK = 10,2. Tt(CaCO ) = 10-8,3 1 2 3 CO2 + aq CO2.aq K = 0,024
7. Ngêi ta chuÈn ®é 10ml Na CO 0,01M b»ng HCl 0,1M. Cho biÕt axit yÕu CO .aq cã pK = 2 3 2 1 6,4; pK = 10,2. 2
a. TÝnh V (ml) lµ thÓ tÝch HCl cho vµo dung dÞch Na CO øng víi ®iÓm t¬ng ®¬ng e 2 3 thø nhÊt. V b. §Æt x =
; V lµ sè ml HCl cho vµo dung dÞch Na CO . LËp biÓu thøc pH = f(x) khi V 2 3 e
x = 0; 0 < x < 1; 1 < x < 2; x = 2 vµ x > 2.
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬
Ch¬ng vI. Nhãm iIIA
1. C©u 11.6 s¸ch bài tập
ViÕt c¸c ph¬ng tr×nh ph¶n øng sau díi d¹ng ion (nÕu cã) vµ ph©n tö:
a. M + O (M: c¸c ®¬n chÊt nhãm IIIA) 2 b. B O + Mg c. B + HNO (®Æc, nãng) 2 3 3 d. Na B O + H SO lo·ng e. H BO + NaOH (dd) 2 4 7 2 4 3 3 g. Al + Fe O h. Al + NaOH (dd) 3 4 i. Al O - + NaOH (r) k. Al O - + NaOH (dd) 2 3 2 3
2. S¶n xuÊt nh«m theo ph¬ng ph¸p ®iÖn ph©n Al O (trong cryolit Na [AlF ] nãng ch¶y) do 2 3 3 6
Hall (mü) vµ HÐroult (Ph¸p) ph¸t minh, ®iÖn cùc b»ng than bÞ mßn do ph¶n øng víi O 2
a. TÝnh lîng C bÞ mßn khi s¶n xuÊt 2,7 tÊn nh«m gi¶ sö lîng O sinh ra ®· ®èt 2
ch¸y C thµnh CO vµ CO trong ®ã CO chiÕm 60% thÓ tÝch. 2 2
b. NÕu coi qu¸ tr×nh ®iÖn ph©n thùc hiÖn ë 1000oC vµ khÝ t¹o thµnh lµ CO th× ph¶n
øng tæng cho qu¸ tr×nh Hall-Heroult ®îc biÓu diÔn lµ:
Al2O3 (trong cryolit nãng ch¶y) + 3C(r) 2Al(l) + 3CO(k)
cã Ho = 1340kJ vµ So = 586J.K-1. TÝnh ®iÖn thÕ tèi thiÓu ®Ó s¶n xuÊt 1mol Al ë
nhiÖt ®é trªn. NÕu ®iÖn thÕ thùc ®îc ¸p dông b»ng 3 lÇn gi¸ trÞ cña ®iÖn thÕ trªn th×
n¨ng lîng ®iÖn cÇn ®Ó s¶n xuÊt 1kg Al sÏ lµ bao nhiªu. 3. Cho d÷ kiÖn: O (k) Al(r) Al O (r) Si(r) SiO (r) 2 2 3 2 Ho (kJ.mol-1) - - -1673,2 - -877,4 298,S So (J.mol-1.K-1) 205,0 28,3 51,0 18,8 42,1 298
a. LËp biÓu thøc Go ph¶n øng cña Al víi 1 mol O vµ cña Si víi 1 mol O t¹o ra oxit T 2 2
t¬ng øng ë T < 1500K. BiÕt nhiÖt ®é nãng ch¶y cña Al lµ 930K víi Ho = 10,9 n.c
kJ.mol-1 cßn Si, SiO , Al O ®Òu cã T > 1500K. 2 2 3 n.c b. TÝnh Go cña ph¶n øng SiO 1000K 2 + 4/3Al = 3/2Al2O3 + Si (a)
Cho biÕt cã thÓ dïng chÐn sø (cã chøa SiO ) ®Ó nung ch¶y Al ®îc kh«ng? 2
4. Bµi tËp 11.12 s¸ch bµi tËp
Nång ®é H+ sinh ra trong dung dÞch Al3+ chñ yÕu do ph¶n øng sau:
Al3+ + HOH Al(OH)2+ + H+ ; Ka = 10-5
TÝnh nång ®é ban ®Çu cña Al3+ khi Al(OH) b¾t ®Çu kÕt tña vµ pH cña dung dÞch nµy, biÕt 3
r»ng tÝch sè tan cña Al(OH) lµ 10-32. 3 Nhãm IIA, IA
1. C©u 12.3 s¸ch bµi tËp
Cho bét Mg vµo níc nãng cã thuèc thö phenolphthalein thÊy cã mµu hång. Thªm vµo hçn
hîp nµy dung dÞch NH Cl ®Æc th× thÊy bät sñi lªn nhiÒu. Gi¶i thÝch. 4
2. Bµi tËp 12.12 s¸ch bµi tËp
Dung dÞch MgCl 10-2M ë 25oC b¾t ®Çu kÕt tña Mg(OH) ë pH = 9,5: 2 2
a. TÝnh tÝch sè tan cña Mg(OH) . 2
Bé m«n Ho¸ V« c¬ & §¹i c¬ng Bµi tËp Ho¸ v« c¬
b. TÝnh thÕ khö cña cÆp Mg2+/Mg khi pH = 11, biÕt r»ng thÕ khö chuÈn cña nã lµ -2,36V.
c. T¹i sao Mg ghÐp vµo c¸c thiÕt bÞ b»ng thÐp cã thÓ b¶o vÖ ®îc thÐp khái bÞ ¨n mßn ®iÖn ho¸?
3. Mét mÉu níc chøa 0,0045 mol CaCl vµ 0,005 mol NaHCO tÝnh cho mét lÝt níc. 2 3
a. X¸c ®Þnh xem mÉu níc trªn cã ph¶i níc cøng kh«ng? NÕu ph¶i th× cã ®é cøng g×?
b. Nªu ph¬ng ph¸p lµm mÒm. 4. C©u 13.7 s¸ch bµi tËp
ViÕt c¸c ph¬ng tr×nh ph¶n øng sau díi d¹ng ion (nÕu cã) vµ ph©n tö: a. Li + N (k) e. Na O + CO 2 2 2 2 b. Li + C g. KO + H O 2 2 c. M + H (M: kim lo¹i kiÒm) h. KO + CO 2 2 2 d. Na O + H O i. KO + CO + H O 2 2 2 2 2 2 k. NaOH (t.t) + SiO ; MOH + CO (thiÕu vµ d) 2 2



