


















Preview text:
CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC MỚI. Bài
1 THÀNH PHẦN CỦA NGUYÊN TỬ U
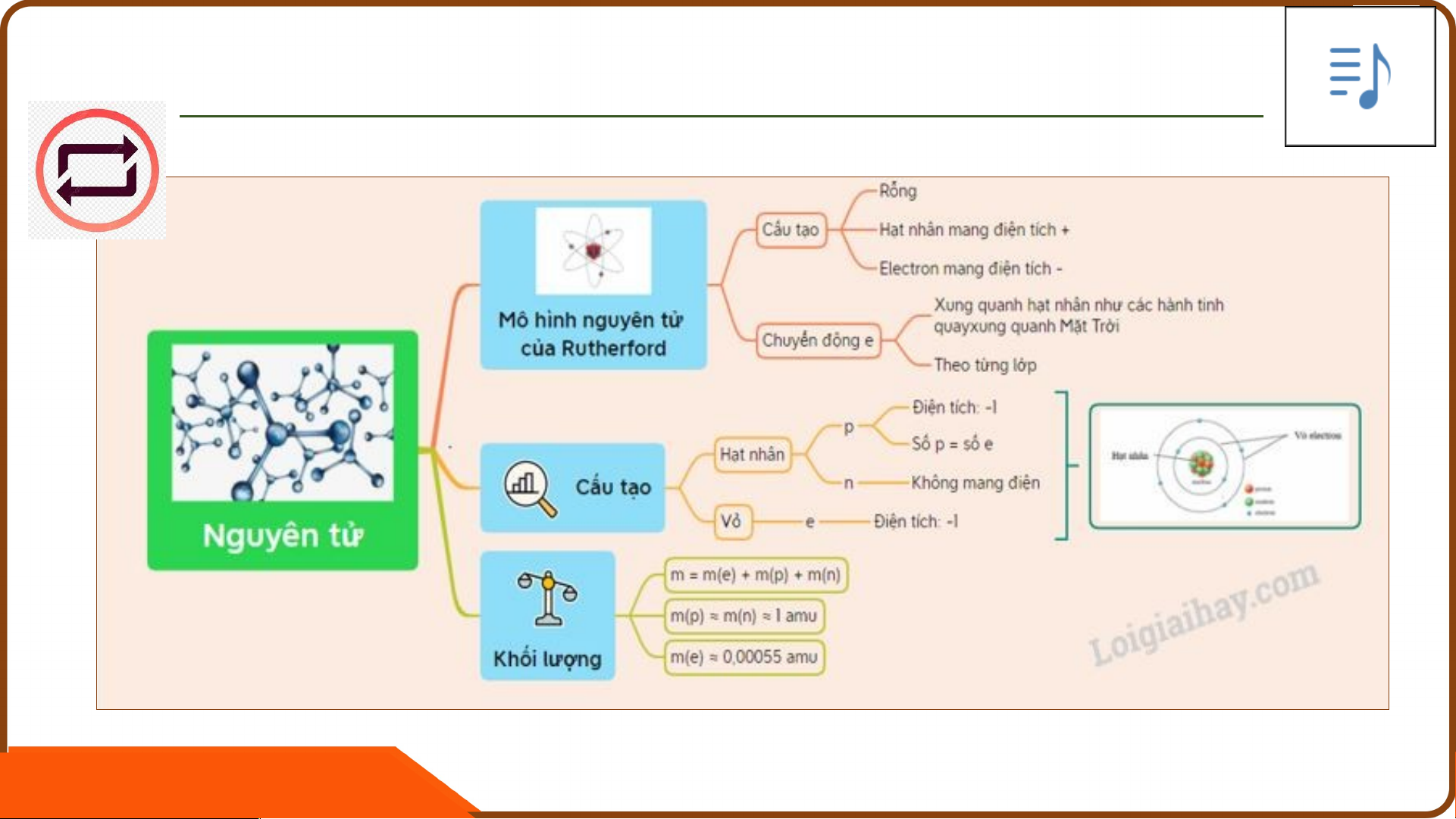
I CÁC LOẠI HẠT CẤU TẠO NÊN NGUYÊN TỬ.
II KÍCH THƯỚC VÀ KHỐI LƯỢNG CỦA NGUYÊN TỬ.
II ĐIỆN TÍCH HẠT NHÂN VÀ I SỐ KHỐI. Bài
1 THÀNH PHẦN CỦA NGUYÊN TỬ U
I CÁC LOẠI HẠT CẤU TẠO NÊN NGUYÊN TỬ. Năm 1897: J. J. Thomson phát hiện ra electron bằng thí nghiệm phóng điện qua không khí loãng. Bài
1 THÀNH PHẦN CỦA NGUYÊN TỬ U
I CÁC LOẠI HẠT CẤU TẠO NÊN NGUYÊN TỬ. - Năm 1911: E.
Rutherford phát hiện ra hạt nhân bằng thí nghiệm bắn phá lá vàng mỏng bằng hạt chùm alpha và sau đó phát hiện proton qua bắn phá nitrogen. Bài
1 THÀNH PHẦN CỦA NGUYÊN TỬ U
I CÁC LOẠI HẠT CẤU TẠO NÊN NGUYÊN TỬ.
Năm 1932, J. Chadwick phát hiện ra
neutron khi bắn phá beryllium bằng các hạt alpha. Bài
1 THÀNH PHẦN CỦA NGUYÊN TỬ U
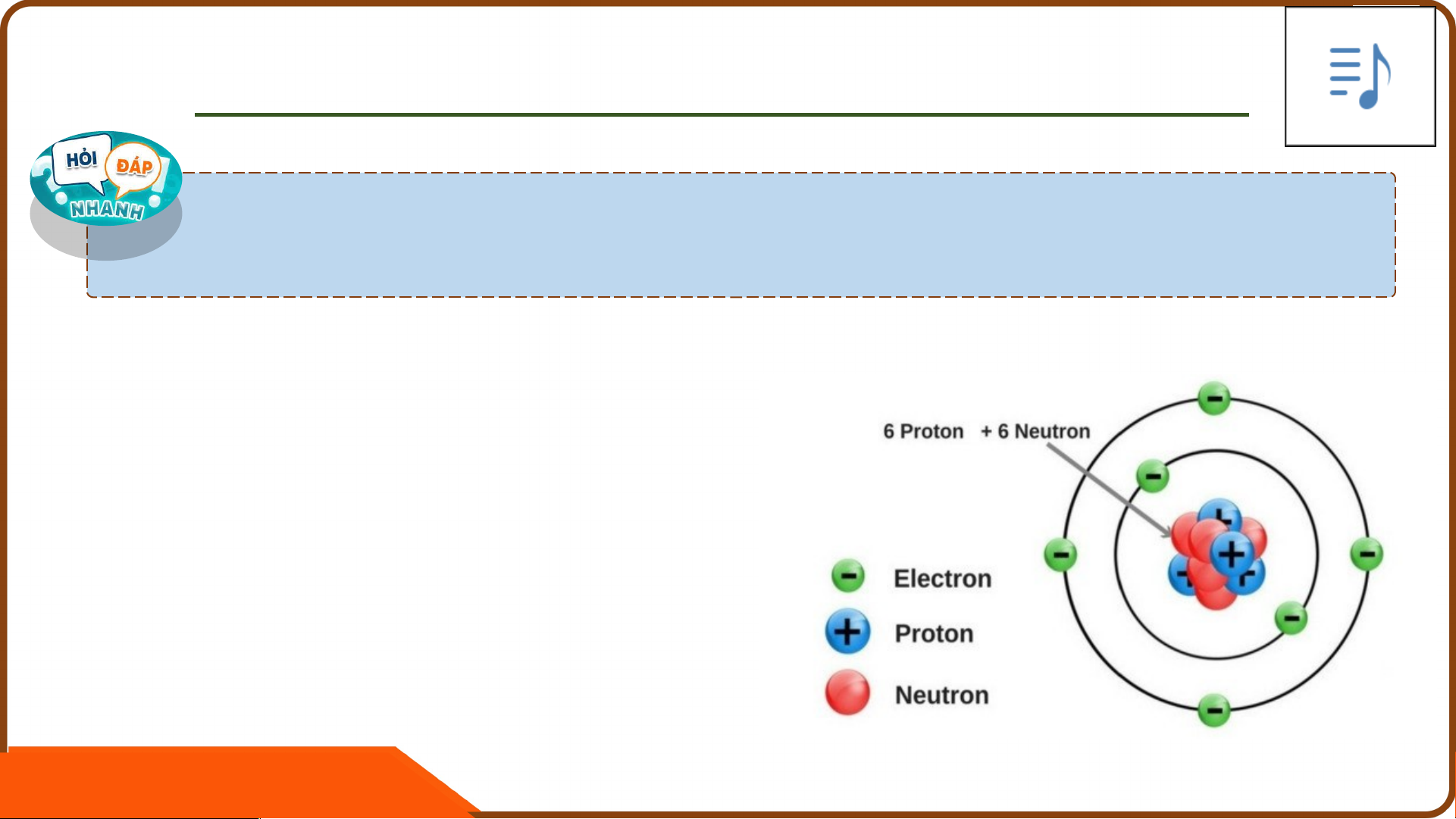
I CÁC LOẠI HẠT CẤU TẠO NÊN NGUYÊN TỬ. Khối Khối Điện tích Điện Hạt Kí lượng lượng (C) tích hiệu (Kg) (amu) tương Proto p 1,673. ≈ 1 +1,602.10−19 +1 đối nNeutro n 1,675. ≈ 1 0 0 n Electro e 9,109. ≈ −1,602.10−19 1 n 0,00055 LUYỆN TẬP U
Câu hỏi 1 (trang 14): Vẽ Mô hình biểu diễn thành phần cấu tạo của nguyên tử
KHTN 7 – KẾT NỐI TRI THỨC U KẾT LUẬN :
1. Khối lượng của nguyên tử tập trung ở hạt
nhân (Electron có khối lượng nhỏ hơn proton và neutron khoảng 1818 lần)
2. Nguyên tử trung hòa về điện là do số p(+) = số e(-). Q Select
Câu hỏi 2: Nguyên tử chứa những hạt mang điện là $1,000,000 $500,000 Q Right $250,000 $100,000 Q Wrong $50,000 $25,000 $16,000 $8,000 $4,000 $2,000 $1,000 $500 $300 A proton và α. B proton và neutron $200 $100 C proton và electron D electron và neutron Bắt đầu LUYỆN TẬP U
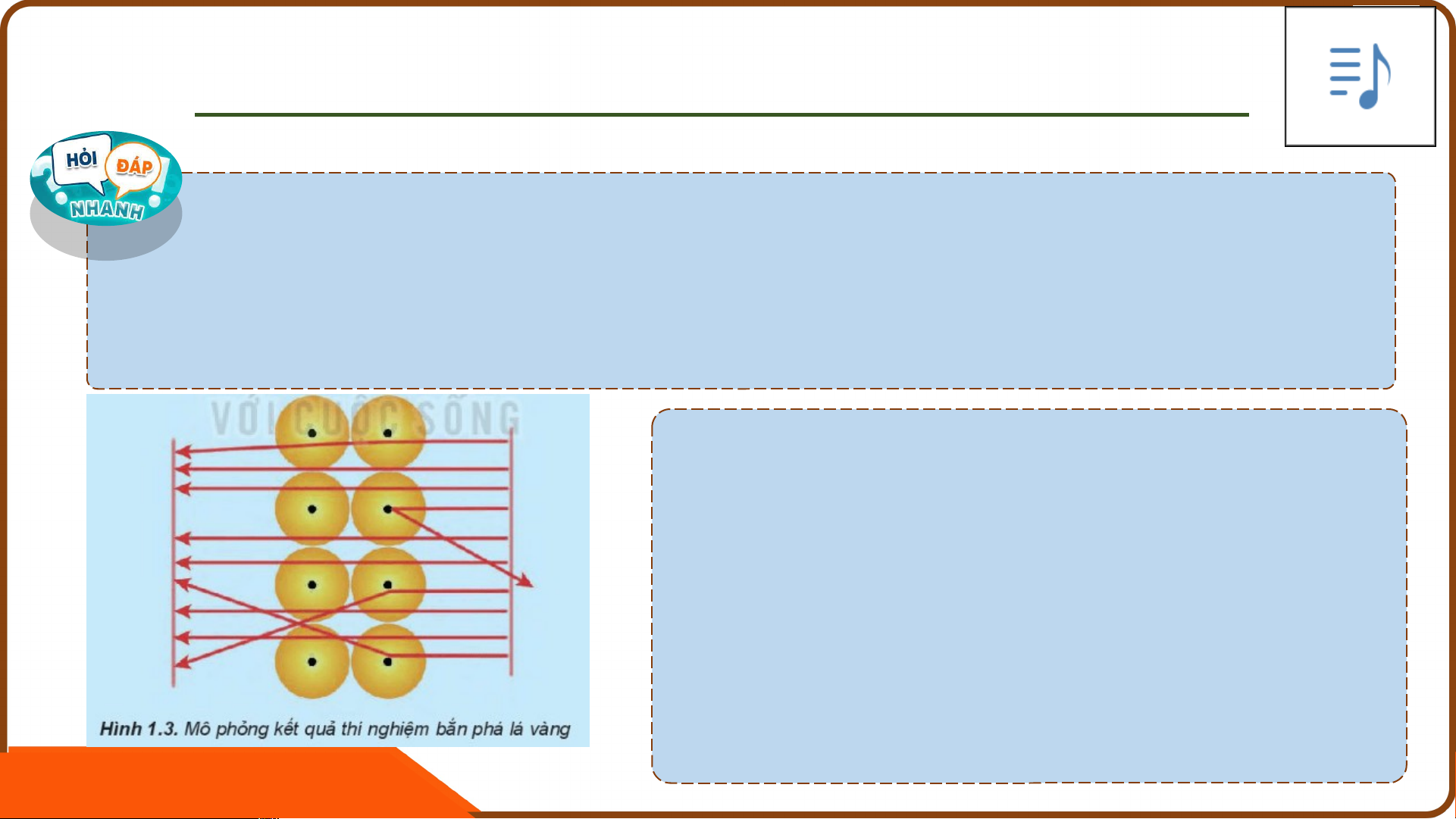
Câu hỏi 3 (trang 14): Quan sát hình ảnh mô phỏng kết
quả thí nghiệm bắn phá lá vàng thực hiện bởi Rutherford
(Hình 1.3) và nhận xét về đường đi của các hạt α. Rút ra kết
luận về một trong số các đặc điểm cấu tạo nguyên tử Đáp án:
• Đa số các trường hợp các hạt α
đi thẳng xuyên qua lá vàng
• Một số ít trường hợp bị lệch hoặc dội ngược lại
Rút ra kết luận nguyên tử có cấu tạo rỗng KẾT LUẬN:
1. Khối lượng của nguyên tử tập trung ở hạt
nhân (Electron có khối lượng nhỏ hơn proton và neutron khoảng 1818 lần)
2. Nguyên tử trung hòa về điện là do số p(+) = số e(-).
3. Nguyên tử có cấu tạo rỗng Bài
1 THÀNH PHẦN CỦA NGUYÊN TỬ U
II KÍCH THƯỚC VÀ KHỐI LƯỢNG CỦA NGUYÊN TỬ.
II KÍCH THƯỚC VÀ KHỐI LƯỢNG CỦA 1. N K GUY ÍCH ÊN THƯ T Ớ Ử C .CỦA NGUYÊN TỬ:
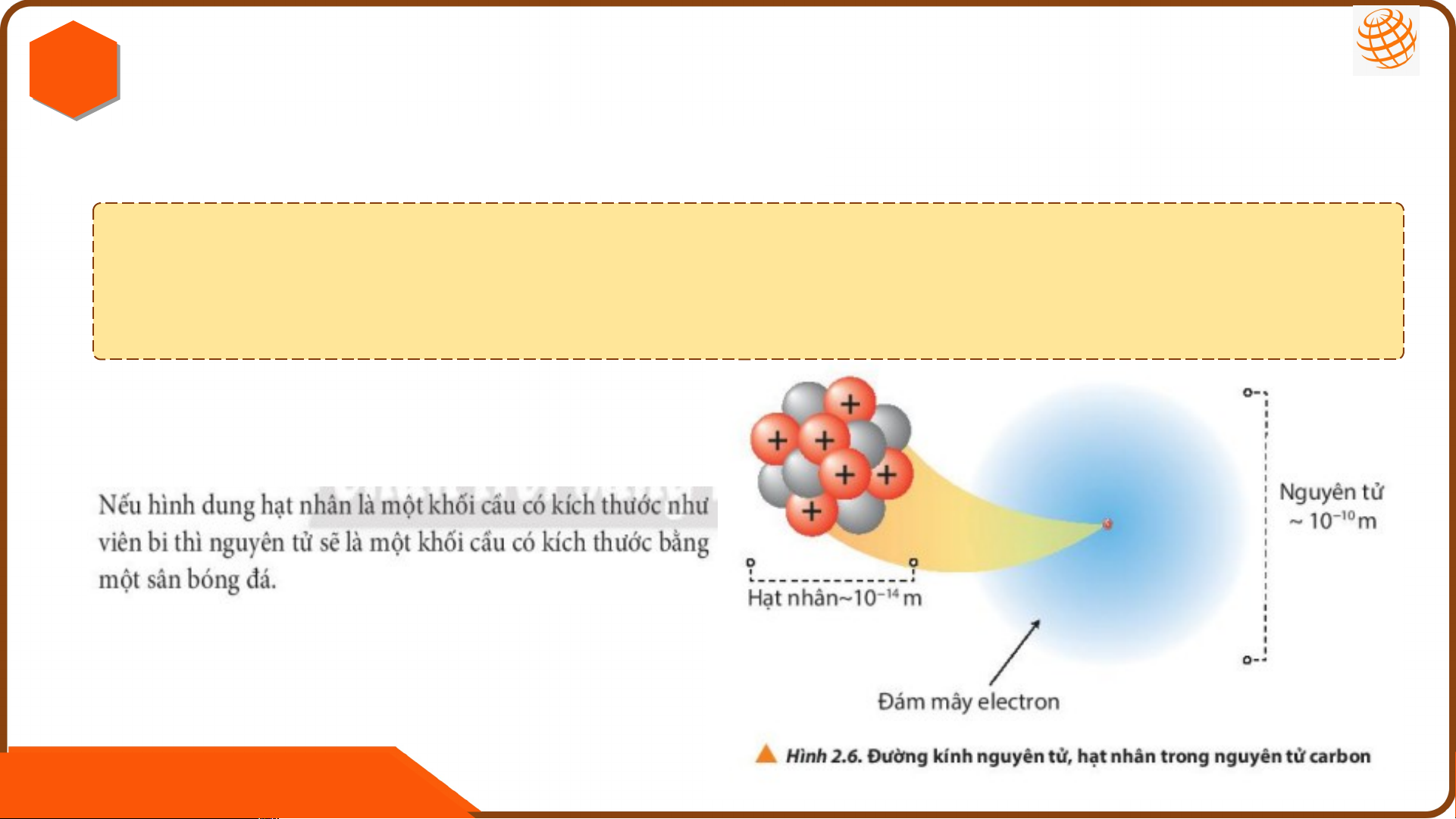
Kích thước của nguyên tử là khoảng không gian tạo
bởi sự chuyển động của các electron.
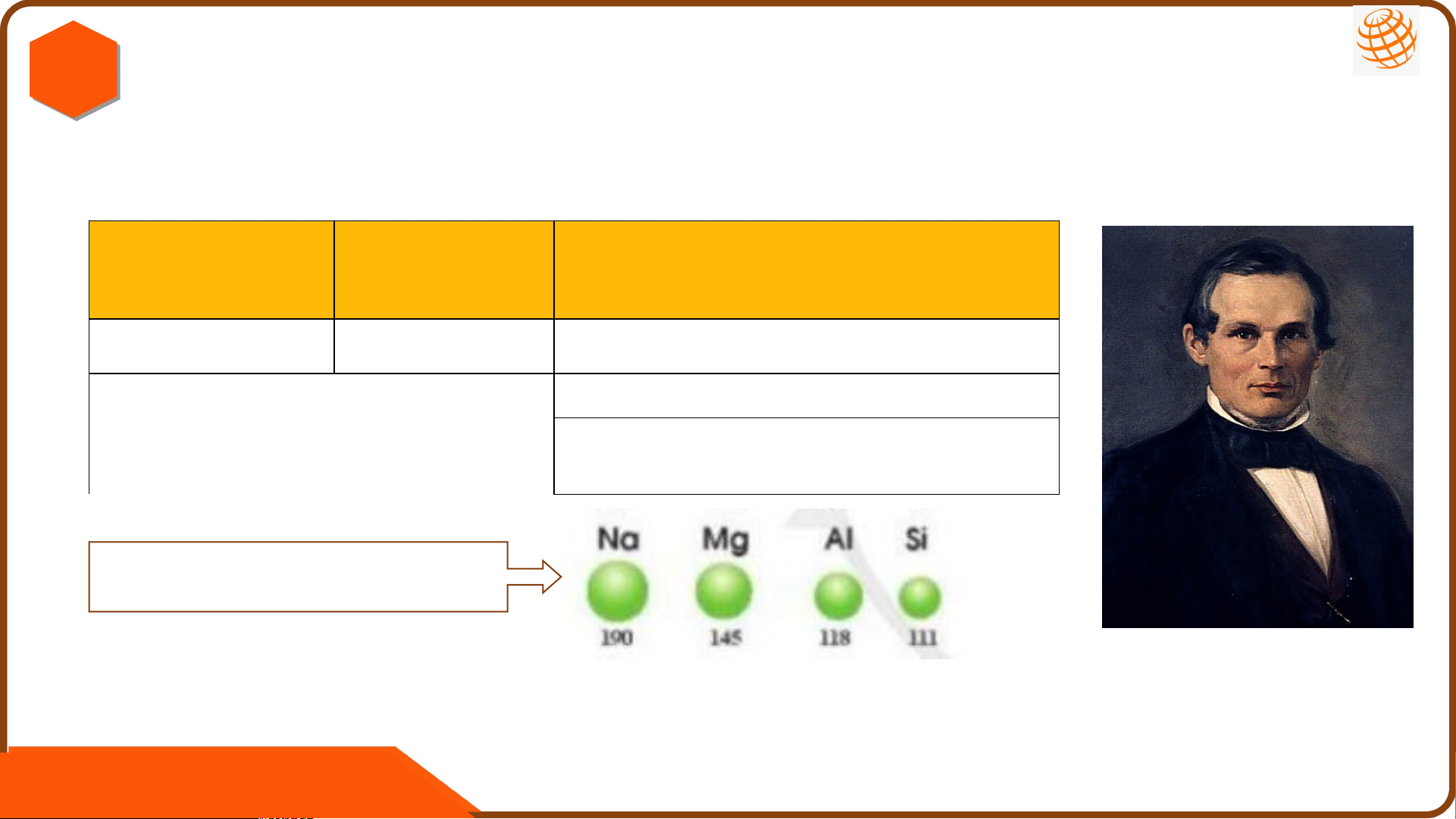
II KÍCH THƯỚC VÀ KHỐI LƯỢNG CỦA 1. N K GUY ÍCH ÊN THƯ T Ớ Ử C .CỦA NGUYÊN TỬ: Đường kính Đường kính Đơn vị đo nguyên tử hạt nhân 10-10 m 10-14 m 1pm (picomet) = 10-12 m
Đường kính nguyên tử lớn 1Å (Ångström)= 10-10 m
hơn hạt nhân bao nhiêu lần? 1nm (nanomet) = 10-9m
Bán kính một số nguyên tử (pm) Anders Jonas Ångström. LUYỆN TẬP U
Câu hỏi 4 (trang 15): Nếu phóng đại một nguyên tử
vàng lên 1 tỉ (109) lần thì kích thước của nó tương đương
một quả bóng rổ (có đường kính 30 cm) và kích thước của
hạt nhân tương đương một hạt cát (có đường kính 0,003
cm). Cho biết kích thước nguyên tử vàng lớn hơn so với hạt nhân bao nhiêu lần. Đáp án:
Kích thước nguyên tử vàng lớn
hơn so với hạt nhân là: 30: 0,003 = 10000 lần.
II KÍCH THƯỚC VÀ KHỐI LƯỢNG CỦA 2 N . G K UYÊN HỐI LƯ TỬ ỢN . G CỦA NGUYÊN TỬ:
Khối lượng của nguyên tử bằng tổng khối lượng các
hạt proton, neutron và electron có trong nguyên tử. LUYỆN TẬP U
Câu hỏi 5 (trang 15): Một loại nguyên tử nitrogen có 7
proton và 7 neutron trong hạt nhân. Dựa vào Bảng 1.1, hãy tính và so sánh:
a) Khối lượng hạt nhân với khối lượng nguyên tử.
b) Khối lượng hạt nhân với khối lượng vỏ nguyên tử Đáp án:
a) Khối lượng của hạt nhân là:
Khối lượng nguyên tử là: Vậy: LUYỆN TẬP U
Câu hỏi 5 (trang 15): Một loại nguyên tử nitrogen có 7
proton và 7 neutron trong hạt nhân. Dựa vào Bảng 1.1, hãy tính và so sánh:
a) Khối lượng hạt nhân với khối lượng nguyên tử.
b) Khối lượng hạt nhân với khối lượng vỏ nguyên tử Đáp án:
b) Khối lượng của hạt nhân là:
Khối lượng của vỏ nguyên tử là Vậy: KẾT LUẬN:
1. Khối lượng của nguyên tử tập trung ở hạt nhân
(Electron có khối lượng nhỏ hơn proton và neutron khoảng 1818 lần)
2. Nguyên tử trung hòa về điện là do số p(+) = số e(-).
3. Nguyên tử có cấu tạo rỗng: đường kính nguyên tử gấp
104 lần đường kính hạt nhân (phần không gian rỗng là chủ yếu)
4. Khối lượng của nguyên tử bằng tổng khối lượng các
hạt proton, neutron và electron trong nguyên tử
II ĐIỆN TÍCH HẠT NHÂN VÀ SỐ KHỐI.
I - Số proton trong hạt nhân nguyên tử bằng số đơn vị của
điện tích hạt nhân, kí hiệu là Z. Nếu gọi P là số proton thì P = Z
Vd: Nguyên tử C có 6 proton nên số đơn vị điện tích hạt nhân là Z=6
- Số khối (hay số nucleon) là tổng số proton và neuton
trong hạt nhân của một nguyên tử, kí hiệu là A. A= Z + N (gọi N là số neutron)
Vd: Nguyên tử O có số proton là 8, số neutron là 8 nên số
khối của hạt nhân nguyên tử O là: A=Z+N = 8+8=16. KẾT LUẬN:
1. Khối lượng của nguyên tử tập trung ở hạt nhân
(Electron có khối lượng nhỏ hơn proton và neutron khoảng 1818 lần)
2. Nguyên tử trung hòa về điện là do số p(+) = số e(-).
3. Nguyên tử có cấu tạo rỗng: đường kính nguyên tử gấp
104 lần đường kính hạt nhân (phần không gian rỗng là chủ yếu)
4. Khối lượng của nguyên tử bằng tổng khối lượng các
hạt proton, neutron và electron trong nguyên tử
5. Số khối A = Z + N (Z là số đơn vị điện tích hạt nhân,
P là số proton, N là số neutron) LUYỆN TẬP U
Câu hỏi 6 (trang 16): Aluminium là kim loại phổ biến
nhất trên vỏ Trái Đất, được sử dụng trong các ngành xây
dựng, ngành điện hoặc sản xuất đồ gia dụng. Hạt nhân của
nguyên tử aluminium có điện tích bằng +13 và số khối
bằng 27. Tính số proton, số neutron và số electron có trong nguyên tử aluminium. Đáp án:
A = Z + N = 27, mà điện tích bằng +13 nên Z = 13. Vậy số
proton P = 13, số neutron N = 27 – 13 = 14
Document Outline
- CHÀO MỪNG CÁC EM ĐẾN VỚI BÀI HỌC MỚI.
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24




