
















Preview text:
BÀI 17. BIẾN THIÊN ENTHALPY TRONG
CÁC PHẢN ỨNG HOÁ HỌC Ô 1 2 CỬA BÍ 5 MẬT 3 4
Ô cửa số 5: Một quá trình thường xảy ra trong tự nhiên
Ô số 1: Nguyên tố nào dưới đây là phi kim? kim A. Li (Z=3): 1s22s1. B. O (Z=8): 1s22s22p4.
C. Al (Z=13): 1s22s22p63s23p1.
D. Mg (Z=12): 1s22s22p63s2. back
Ô số 2: Khả năng phản ứng của các nguyên tố nhóm khí hiếm (VIIIA) là
A. dễ nhường electron.
B. dễ nhận electron. C. phản ứng chậm.
D. trơ về mặt hóa học (khó phản ứng).
Ô số 3: Khi tham gia các phản ứng hóa học kim loại có xu
hướng …. (1), phi kim có xu hướng ….(2)
Cụm từ còn thiếu trong các dấu … trên là
A. (1) nhận electron; (2) nhường electron.
B. (1) nhường electron; (2) nhận electron.
C. (1) nhận electron; (2) nhận electron.
D. (1) nhường electron; (2) nhường electron.
Ô số 4: C4H10 + O2 CO2 + H2O
Phản ứng oxi hoá khử trên có tổng hệ số (tối giản) các chất là A. 8. B. 22. C. 33. D. 28. kim
Năng lượng đóng vai trò quan trọng trong cuộc sống của con người.
a, Thực phẩm cung cấp năng lượng cho con người.
b, Quá trình đốt cháy xăng cung cấp năng lượng cho ô tô.
c, Than cốc cung cấp năng lượng cần thiết để chuyển hóa quặng sắt thành sắt.
Chương 5: NĂNG LƯỢNG HÓA HỌC
Năng lượng hóa học là tiềm năng của một
chất hóa học trải qua quá trình biến đổi thông qua
phản ứng hóa học để biến đổi các chất hóa học khác
(Bách khoa toàn thư mở Wikipedia)
Năng lượng hóa học thuộc dạng năng lượng tiềm năng
Năng lượng hóa học chứa trong thực phẩm được cơ thể con người biến thành
nhiệt và năng lượng cơ khí giúp bạn cử động tay chân. Động cơ nổ trong xe hơi
biến năng lượng hóa học trong dầu xăng thành năng lượng động và làm xe chạy được.
Nhiệt từ hóa năng chứa trong than đá hay dầu hỏa trong những nhà máy điện
làm hơi nước nóng và làm quay tua bin. Tua bin quay và làm ra điện năng. Hóa
năng trong bình điện hay pin điện qua quá trình điện phân biến thành điện năng.
Cây cối biến năng lượng mặt trời qua quá trình quang hợp thành năng lượng hóa
học chứa trong cây trái.
Năng lượng hoá học
2H + O → 2H O + Năng lượng 2 2 2
Chương 5: NĂNG LƯỢNG HÓA HỌC Bài 17:
BIẾN THIÊN ENTHALPY TRONG
CÁC PHẢN ỨNG HOÁ HỌC “Tình huống:
“Bạn Nam làm thí nghiệm:
(1) Thả thì vôi sống dạng bột (CaO) vào cốc 1 đựng nước cất.
(2) Thả C sủi vào cốc 2 chứa nước cất.
Nam thấy trước khi làm thí nghiệm, nhiệt độ của 2 cốc nước là 25oC.
Cốc 1, sau khi cho vôi sống, nhiệt độ tăng lên 75oC.
Cốc 2, sau khi thả C sủi, nhiệt độ giảm xuống 21oC.
- yêu cầu: Em hãy dự đoán thí nghiệm (1), (2) là phản ứng tỏa nhiệt hay thu nhiệt PHIẾU HỌC TẬP 1.
Đánh dấu “x” vào ô tương ứng để hoàn thiện bảng sau.
Phản ứng tỏa nhiệt
Phản ứng thu nhiệt
a, Quá trình pháo hoa cháy sáng trong không khí.
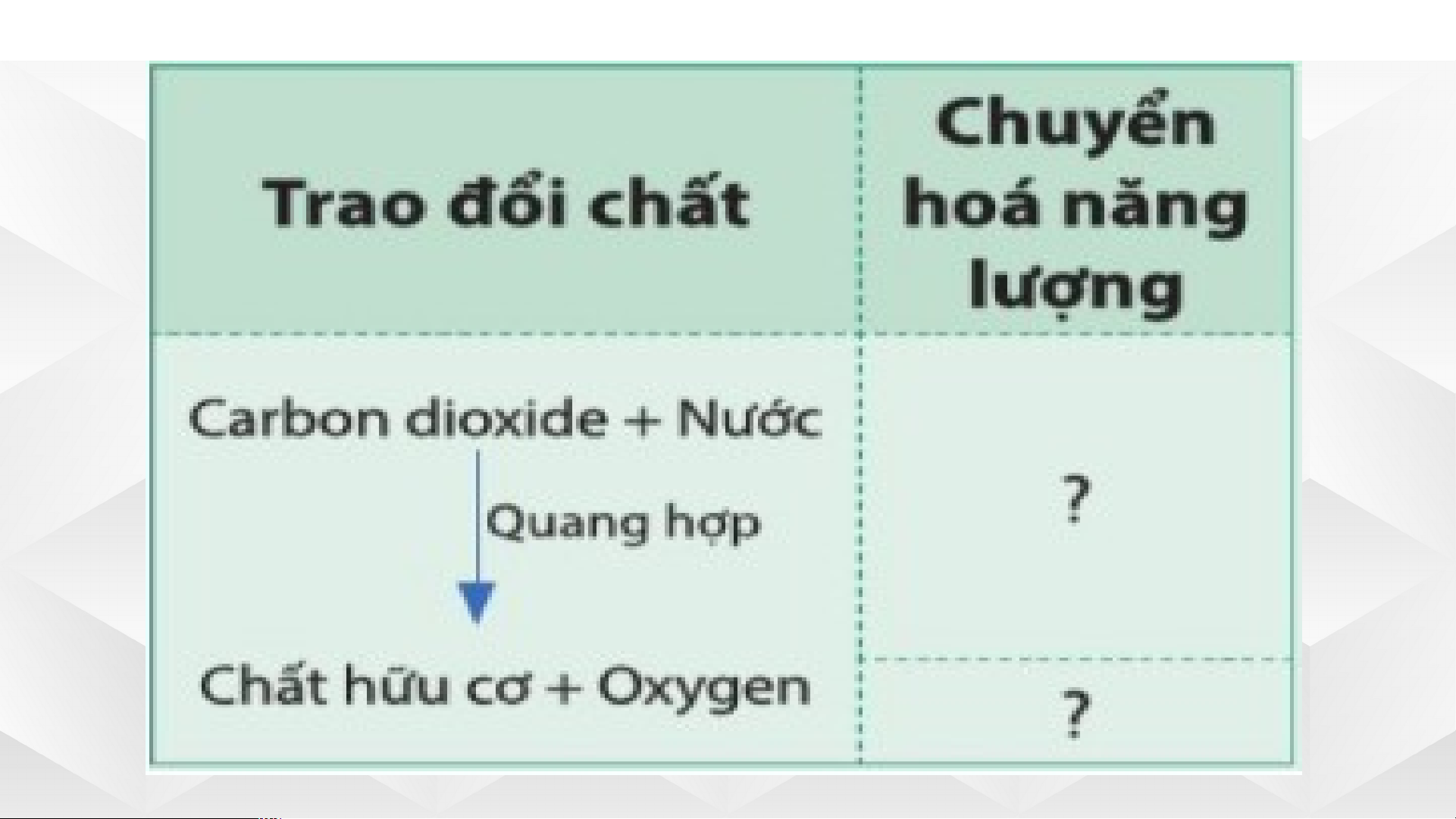
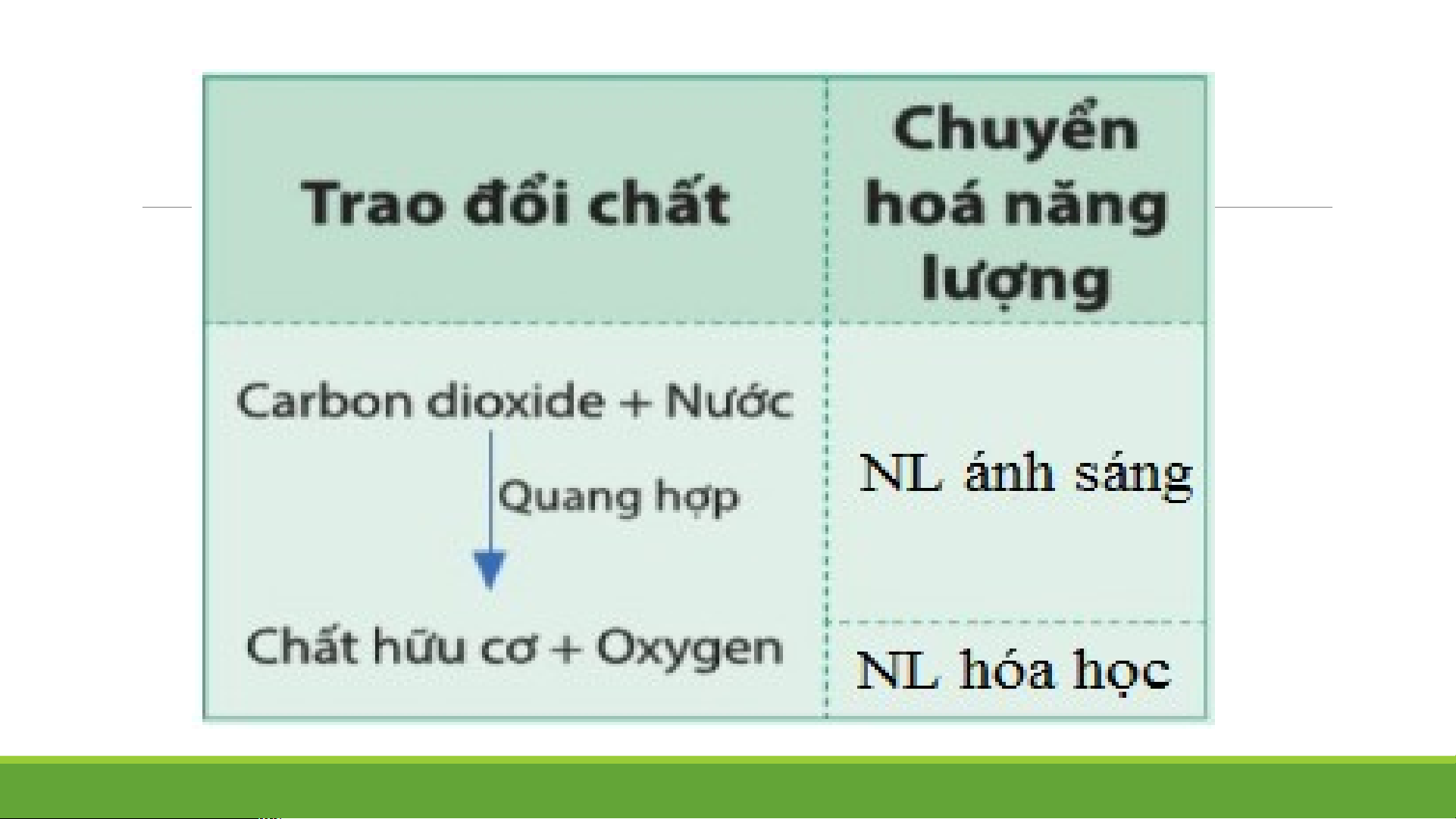
b, Quá trình quang hợp của thực vật.
c, Quá trình oxi hóa carbohydrate
trong cơ thể con người.
d, Đốt magnesium trong không khí.
e, Nhiệt phân magnesium nitrate. Mg(NO3)2
Phản ứng tỏa nhiệt
Phản ứng thu nhiệt
a, Quá trình pháo hoa cháy sáng x trong không khí.
b, Quá trình quang hợp của thực x vật.
c, Quá trình oxi hóa carbohydrate x
trong cơ thể con người.
d, Đốt magnesium trong không khí. x
e, Nhiệt phân magnesium nitrate. x Mg(NO3)2
PHẢN ỨNG TOẢ NHIỆT PHẢN ỨNG HOÁ HỌC
PHẢN ỨNG THU NHIỆT
Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
Phản ứng thu nhiệt là phản ứng hấp thu năng lượng dưới dạng nhiệt.
Phiếu học tập số 2: Cho các phản ứng sau, phản ứng nào là phản ứng thu
nhiệt, phản ứng nào là phản ứng tỏa nhiệt?
1. Cho dung dịch silver nitrate (AgNO3)phản ứng
với sodium chloride NaCl (thấy nhiệt độ tăng).
3.Calcium (Ca) tác dụng với nước.
2. Cho dung dịch X phản ứng với dung dịch Y
thấy xuất hiện kết tủa trắng, dưới đáy cốc có
hiện tượng đóng đá.
4.Nhiệt phân Cu(OH)2. PHIẾU HỌC TẬP 3
“Theo dõi sự thay đổi sự thay đổi nhiệt độ của phản ứng trung hòa”.
Làm thí nghiệm và trả lời câu hỏi
1. Nhiệt độ thay đổi như thế nào? Phản ứng trung hòa là phản ứng tỏa nhiệt hay thu nhiệt?
2. Trong thí nghiệm trên, nếu thay các dung dịch HCl và NaOH bằng các dung dịch
loãng hơn thì nhiệt độ thay đổi như thế nào so với thí nghiệm trên.
3. Thay acid khác (HNO3, H2SO4, HCOOH…) và base khác ( KOH, Ba(OH)2. thì
hiện tượng thay đổi không
Câu1: Phản ứng nào sau đây toả nhiệt
A. Phản ứng nhiệt phân CaCO3.
B. Phản ứng phân huỷ AgCl.
C. Phản ứng oxi hoá glucozose.
D. Hoà tan NH4Cl vào nước.
Câu 2: Phản ứng nào sau đây có thể tự xảy ra ở điều kiện thường ?
A. Phản ứng nhiệt phân Cu(OH)2.
B. Phản ứng giữa Zn và dd HCl.
C. Phản ứng giữa H2 và O2.
D. Phản ứng đốt cháy khí ga.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Năng lượng hóa học thuộc dạng năng lượng tiềm năng
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23





