









Preview text:
CHƯƠNG 4: HYDROCARBON BÀI 15: ALKANE
CHÀO MỪNG CẢ LỚP
QUAY TRỞ LẠI VỚI MÔN HỌC! KHỞI ĐỘNG
Quan sát video và cho biết khí
thiên nhiên thuộc loại hợp chất
hữu cơ nào? Trong video cung
cấp cho các em thông tin gì về khí thiên nhiên? CHƯƠNG 4: HYDROCARBON BÀI 15: ALKANE NỘI DUNG BÀI HỌC
1 Khái niệm, danh pháp
2 Đặc điểm cấu tạo
3 Tính chất vật lí
4 Tính chất hóa học 5 Ứng dụng 6 Điều chế
7 Ô nhiễm không khí do phương tiện giao thông I. KHÁI NIỆM, DANH PHÁP
1. Khái niệm và công thức chung của alkane
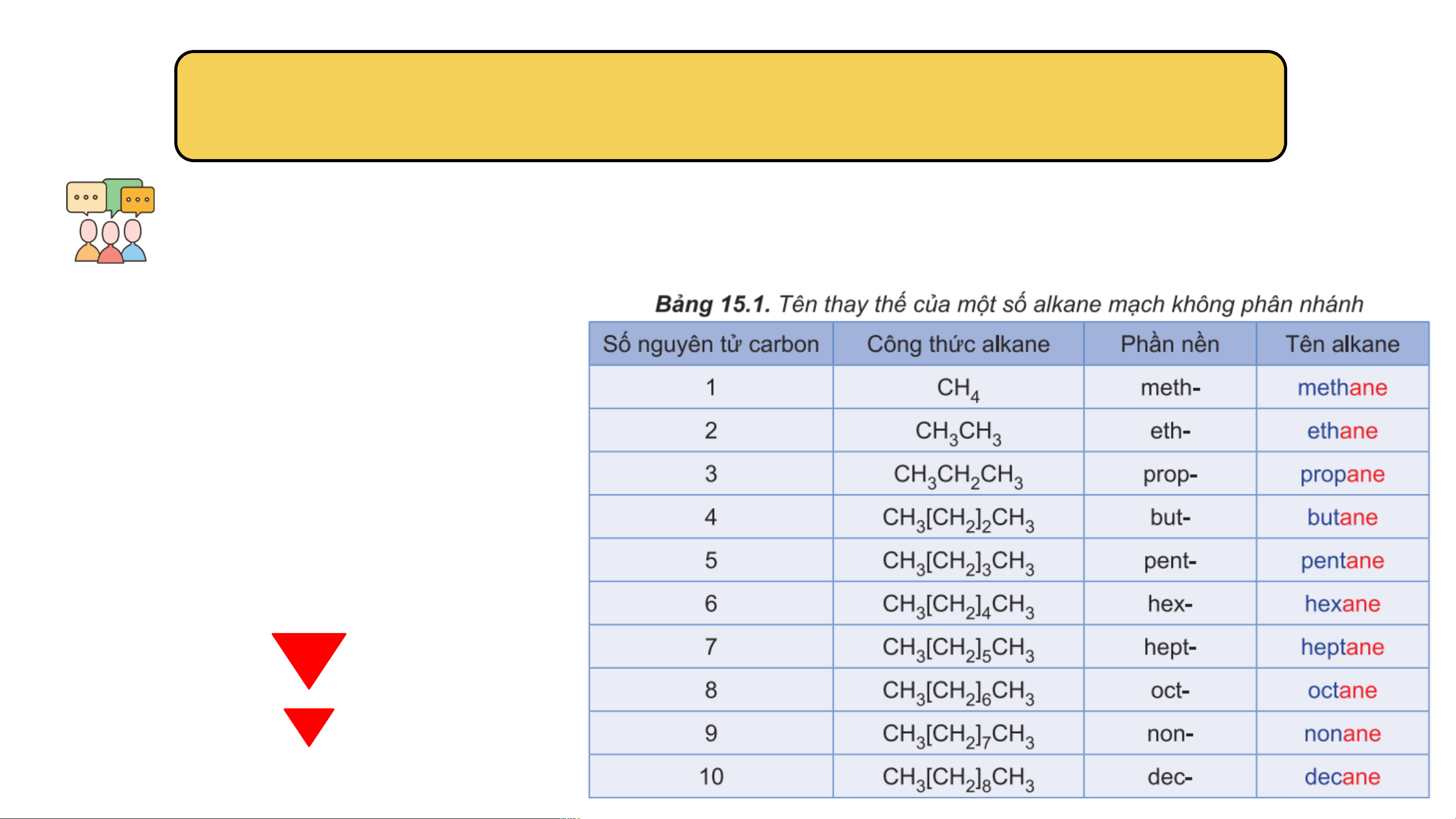
Chia lớp thành 4 nhóm, hoàn thành nhiệm vụ: Hãy quan sát dãy đồng đẳng của methane (Bảng
15.1, SGK), thực hiện các yêu cầu:
1. Nhận xét về thành phần nguyên tố của các chất trong dãy đồng đẳng của methane.
2. Sự khác nhau về số lượng nguyên tử H và C tuân theo quy luật nào?
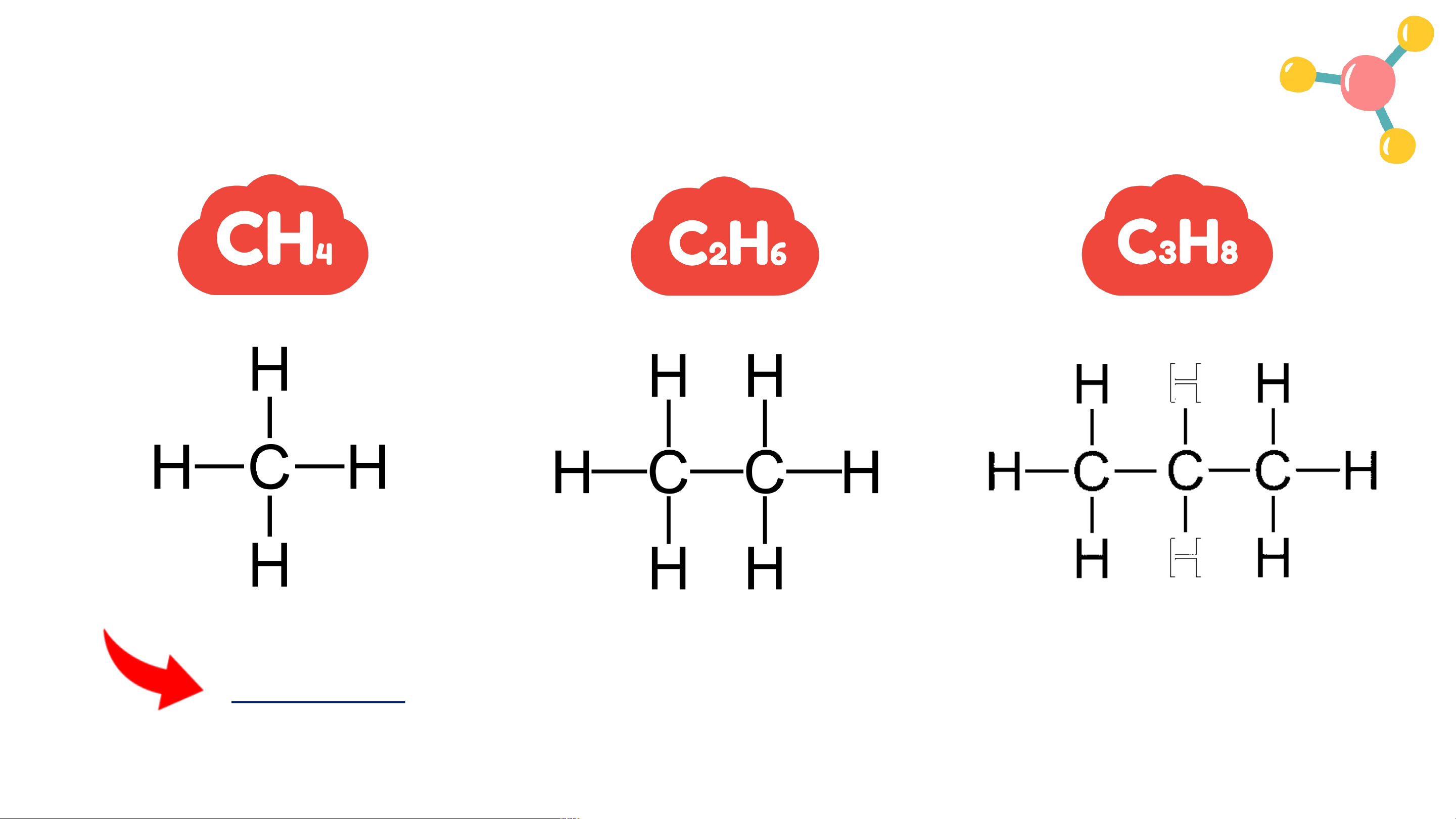
3. Viết công thức cấu tạo đầy đủ của CH , C H , C H ,...; từ đó 4 2 6 3 8
rút ra đặc điểm cấu tạo phân tử.
4. Trong các hợp chất hữu cơ, carbon có hoá trị IV và
hydrogen có hoá trị I, hãy lập công thức chung của alkane. 1. Thành phần nguyên tử chỉ có carbon và hydrogen.
2. Các chất trong dãy đồng đẳng của methane hơn kém nhau 1 hay nhiều nhóm CH . 2
3. Viết công thức cấu tạo đầy đủ của:
Nhận xét: Phân tử chỉ có liên kết đơn (liên kết σ). Đặc điểm
là liên kết cộng hóa trị.
4. Lập công thức hóa học chung của alkane: Bư B ớc ư ớc 1: 1
Công thức hóa học của alkane là C H . n m
Nguyên tử carbon có hoá trị IV nên tổng số liên kết xung Bư B ớ ư c 2 c : 2
quanh n nguyên tử carbon là 4n. Bư B ớ ư c 3 c : 3
Nguyên tử carbon có thể liên kết với nhau tạo thành mạch
nên nC sẽ có (n - 1) liên kết C-C
⇒ số nguyên tử H liên kết
với các nguyền từ carbon sẽ là: 4n - 2.(n - 1) = 2n + 2.
Công thức chung của alkane là C H (n ≥ 1). n 2n+2
4. Lập công thức hóa học chung của alkane: Cách khác
Lập công thức chung của alkane dựa vào
định nghĩa dãy đồng đẳng:
Công thức của alkane là CH [CH ] hay C H 4 2 k 1+k 4+2k
Đặt 1 + k = n thì 4 + 2k = 2n +2
Công thức chung của alkane là C H (n ≥ 1). n 2n+2 GHI NHỚ
Alkane là các hydrocarbon no, mạch hở chỉ
có liên kết đơn C - H và C - C trong phân tử. Công thức chung: C H (n ≥ 1). n 2n+2 2. Danh pháp
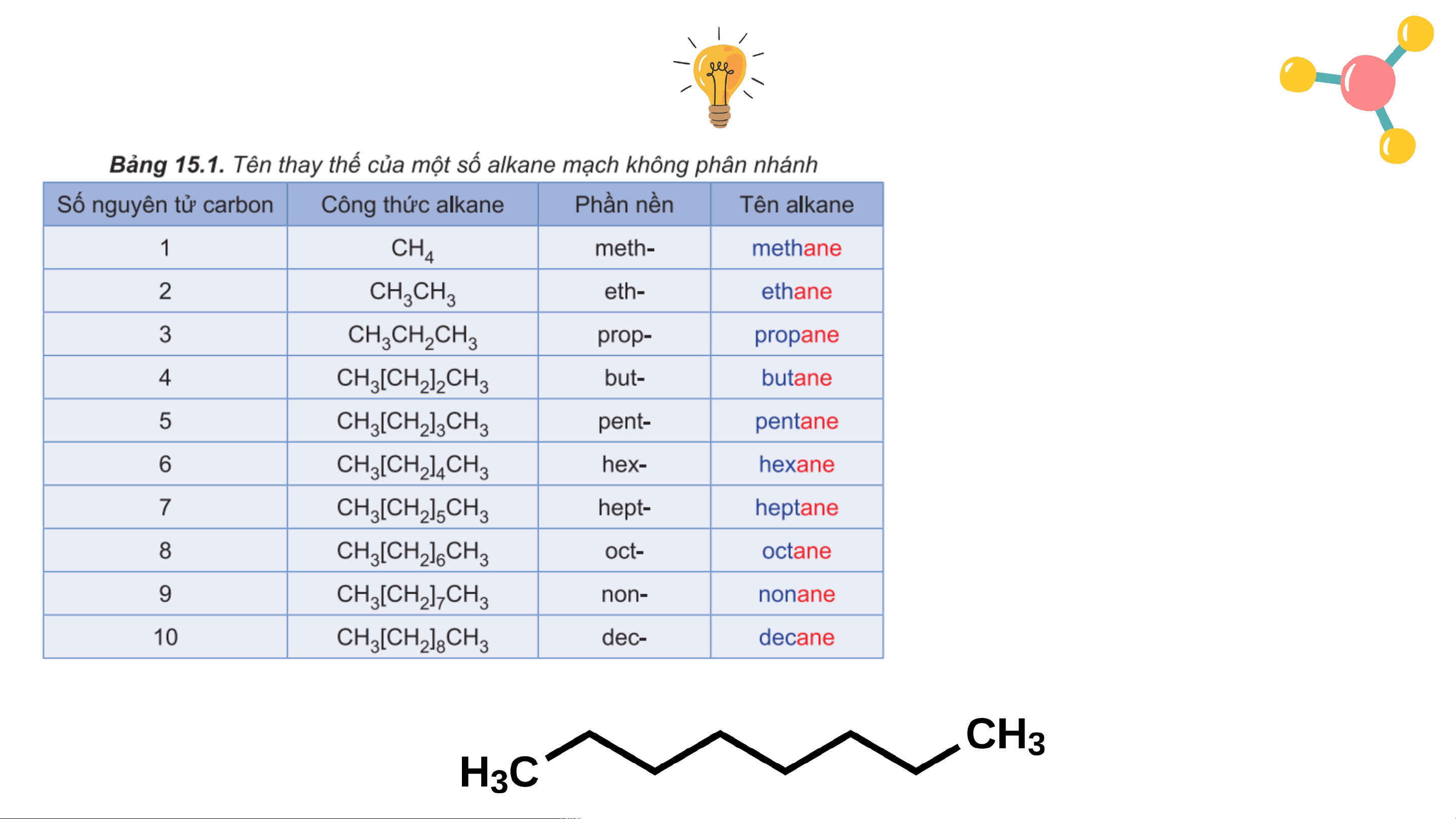
Tên theo danh pháp thay thế của các alkane không phân nhánh:
Phần nền (chỉ số lượng nguyên tử C) ane
Tên theo danh pháp thay thế của gốc alkyl:
Phần nền (chỉ số lượng nguyên tử C) yl
Tên theo danh pháp thay thế của các alkane phân nhánh:
Số chỉ vị trí mạch nhánh – tên nhánh tên alkane mạch chính Lưu ý cách gọi tên
Chọn mạch dài nhất, nhiều nhánh nhất là alkane mạch chính.
Đánh số nguyên tử C mạch chính sao cho
mạch nhánh có số chỉ vị trí là nhỏ nhất.
Dùng chữ số (1, 2, 3, ...) và gạch nối (-)
để chỉ vị trí nhánh, nhóm cuối cùng viết
liền với tên mạch chính.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15




