











Preview text:
CHÀO MỪNG CÁC EM
QUAY TRỞ LẠI VỚI MÔN HỌC! BÀI 17: PHENOL KHỞI ĐỘNG
Những lợi ích của chè xanh đối với sức khỏe
Trò chơi: Trí nhớ siêu phàm
• Lớp chia làm 4 nhóm, các nhóm quan sát video.
• Các nhóm có 60 giây để liệt kê ra những lợi ích của chè xanh.
• Nhóm nào liệt kê được nhiều nhất, chính xác nhất
sẽ chiến thắng và nhận được phần thưởng. Đáp án
• Chống oxy hóa làm giảm quá trình lão hóa,
• Thanh nhiệt, giải khát, giải độc. làm đẹp da.
• Tác dụng tốt giúp ổn định huyết áp.
• Giảm buồn ngủ, giúp tinh thần sảng khoái.
• Tác dụng giảm nguy cơ ung thư.
• Chống sâu răng, bảo vệ răng lợi khỏe
• Chữa bệnh da liễu ngoài da, mẩn ngứa. mạnh.
• Dạng cholesterol và hỗ trợ giảm cân.
• Tăng cường sức đề kháng cho cơ thể,
• Ngăn ngừa các bệnh về tim mạch. chữa cảm cúm.
• Tác dụng tăng cường trí nhớ.
• Giúp xương chắc khỏe, hỗ trợ bệnh viêm
• Bảo vệ gan giúp gan khỏe mạnh. khớp dạng thấp.
• Hỗ trợ điều trị bệnh tiểu đường.
• Tác dụng làm đẹp với bột trà xanh.
• Tăng cường hệ miễn dịch.
• Công dụng chữa bệnh lỵ.
• Giảm nguy cơ hen suyễn. BÀI 17: PHENOL NỘI DUNG BÀI HỌC
1. Khái niệm và cấu trúc
2. Tính chất vật lí
3. Tính chất hóa học
4. Ứng dụng và điều chế
1. KHÁI NIỆM VÀ CẤU TRÚC
Tìm hiểu các khái niệm của phenol
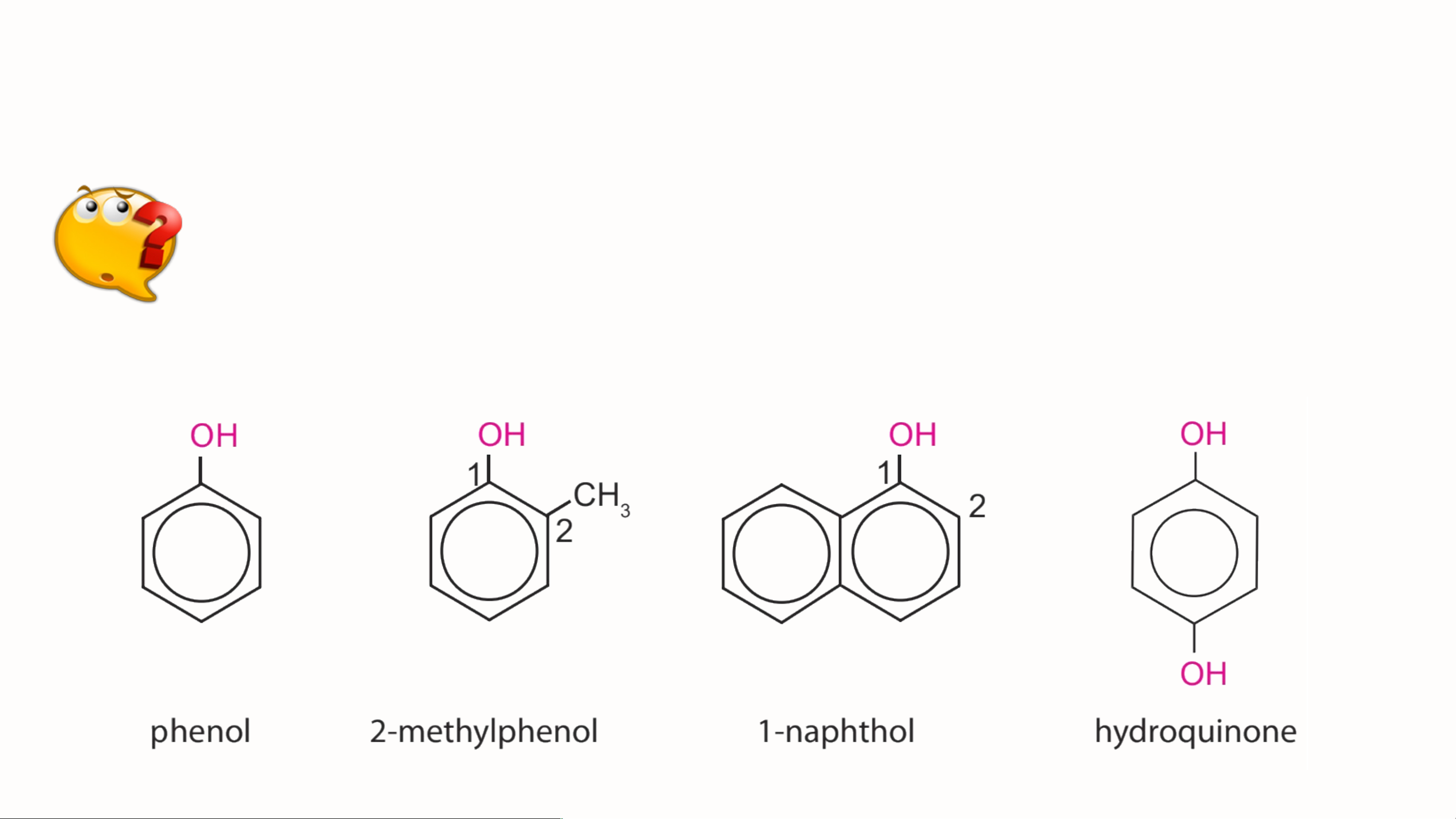
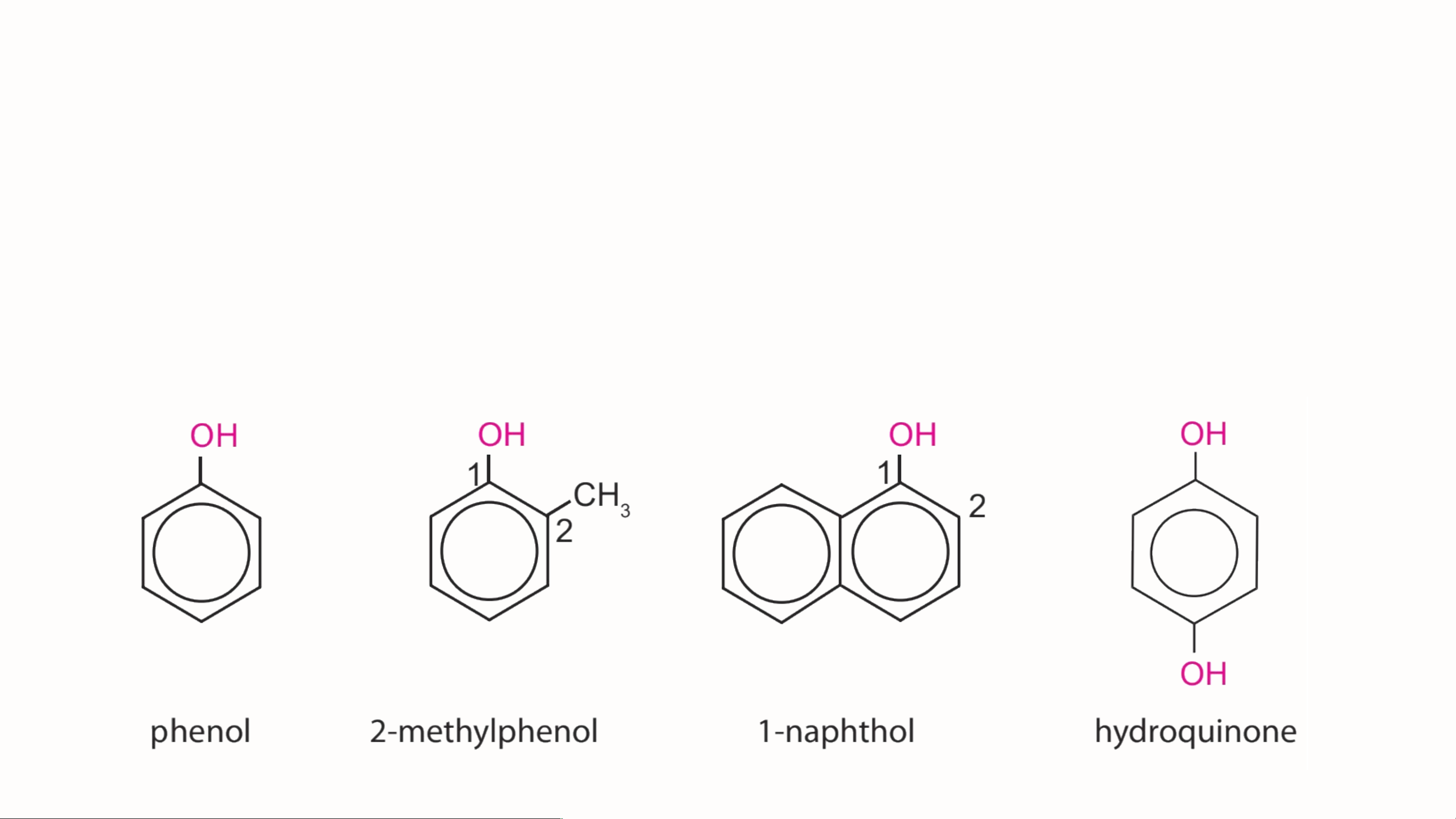
Quan sát các hợp chất phenol, cho biết đặc điểm của nhóm OH
giống và khác nhóm OH trong phân tử alcohol như thế nào?
Giống nhau: có nhóm - OH gắn trực tiếp với nguyên tử carbon trong phân tử. Khác nhau:
• Alcohol: Nhóm - OH không gắn trực tiếp vào vòng benzene.
• Phenol: Nhóm - OH gắn trực tiếp vào vòng benzene. Kết luận
Phenol là những hợp chất hữu cơ
trong phân tử có chứa nhóm -OH
liên kết trực tiếp với nguyên tử carbon của vòng benzene.
Tìm hiểu đặc điểm cấu tạo và hình dạng phân tử phenol
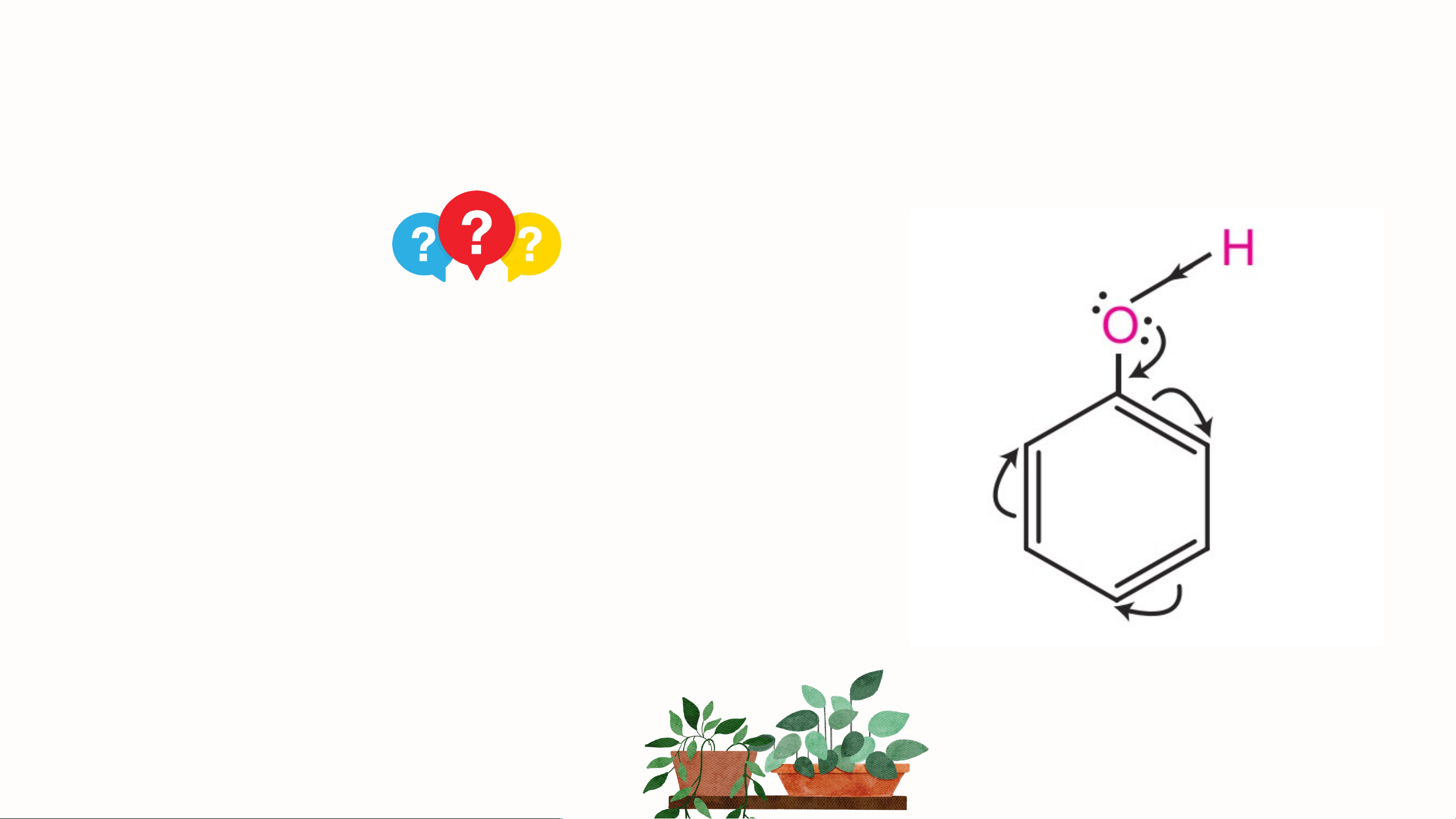
Quan sát công thức cấu tạo của
phenol, cho biết các vị trí giàu mật độ
electron trong vòng benzene. Nhóm
phenyl hút electron, làm ảnh hưởng
như thế nào đến liên kết O - H? Đáp án
• Cặp electron trên nguyên tử O dịch chuyển một phần
vào vòng benzene → tăng mật độ e của vòng benzen
(nhiều nhất ở các vị trí ortho và para) đồng thời làm
giảm mật độ electron trên nguyên tử O.
• Nhóm phenyl hút electron và liên kết - OH phân cực
mạnh về phía nguyên tử H → tăng độ linh động của nguyên tử H.
• Độ linh động của H mạnh hơn nguyên tử H của nhóm OH trong alcohol. Kết luận
Phenol có nhóm phenyl hút electron, làm mật độ electron trên nguyên tử O giảm.
→ Liên kết –O-H phân cực mạnh, đồng thời làm tăng mật độ
electron trong vòng benzene, nhiều nhất ở ortho, para.
2. TÍNH CHẤT VẬT LÍ
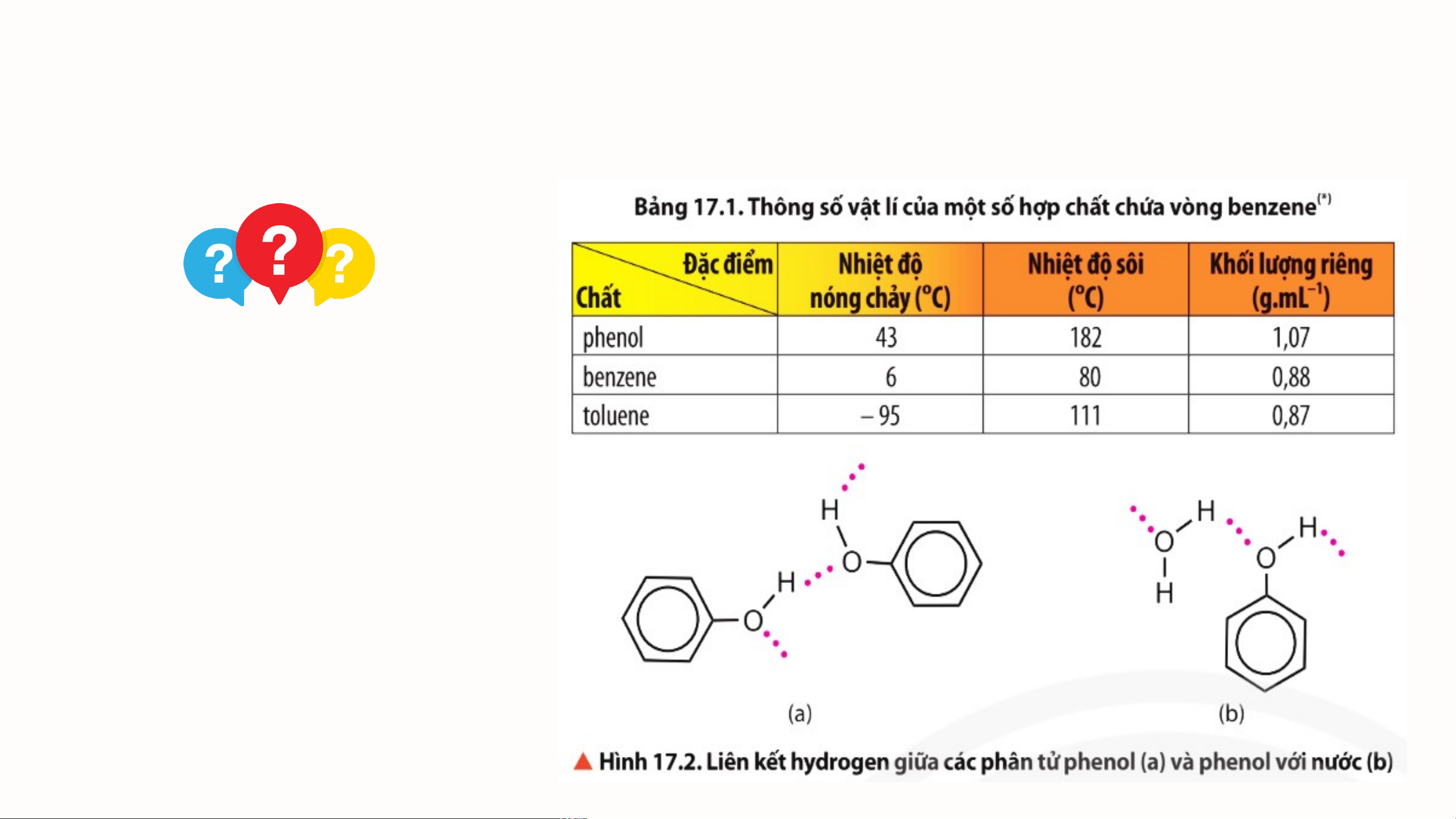
Tìm hiểu tính chất vật lí phenol Đọc thông tin trong bảng 17.1 và hình 17.2, so sánh nhiệt độ nóng chảy của phenol và các
chất còn lại. Giải thích. Đáp án
• Do phân tử phenol có liên kết hydrogen liên phân tử nên khả
năng kết tinh tốt hơn các chất không tạo liên kết hydrogen.
→ Nhiệt độ nóng chảy của phenol cao nhất trong ba chất.
• Benzene có cấu trúc vòng đối xứng bền vững.
→ Nhiệt độ nóng chảy cao hơn các chất cùng dãy đồng đẳng. Nhiệt độ nóng chảy: tol o ue u n e e < benzene benz < phenol Kết luận
• Ở điều kiện thường: phenol là chất rắn, không màu.
• Dễ chảy rữa, để lâu trong không khí bị oxi hóa chậm và hóa màu hồng. • Độc, gây bỏng da.
• Ít tan trong nước lạnh, tan vô hạn trong nước ở 66oC và tan tốt trong ethanol.
• Các phenol có nhiệt độ nóng chảy nhiệt độ sôi cao hơn các
hydrocarbon thơm có khối lượng phân tử tương đương. Lưu ý
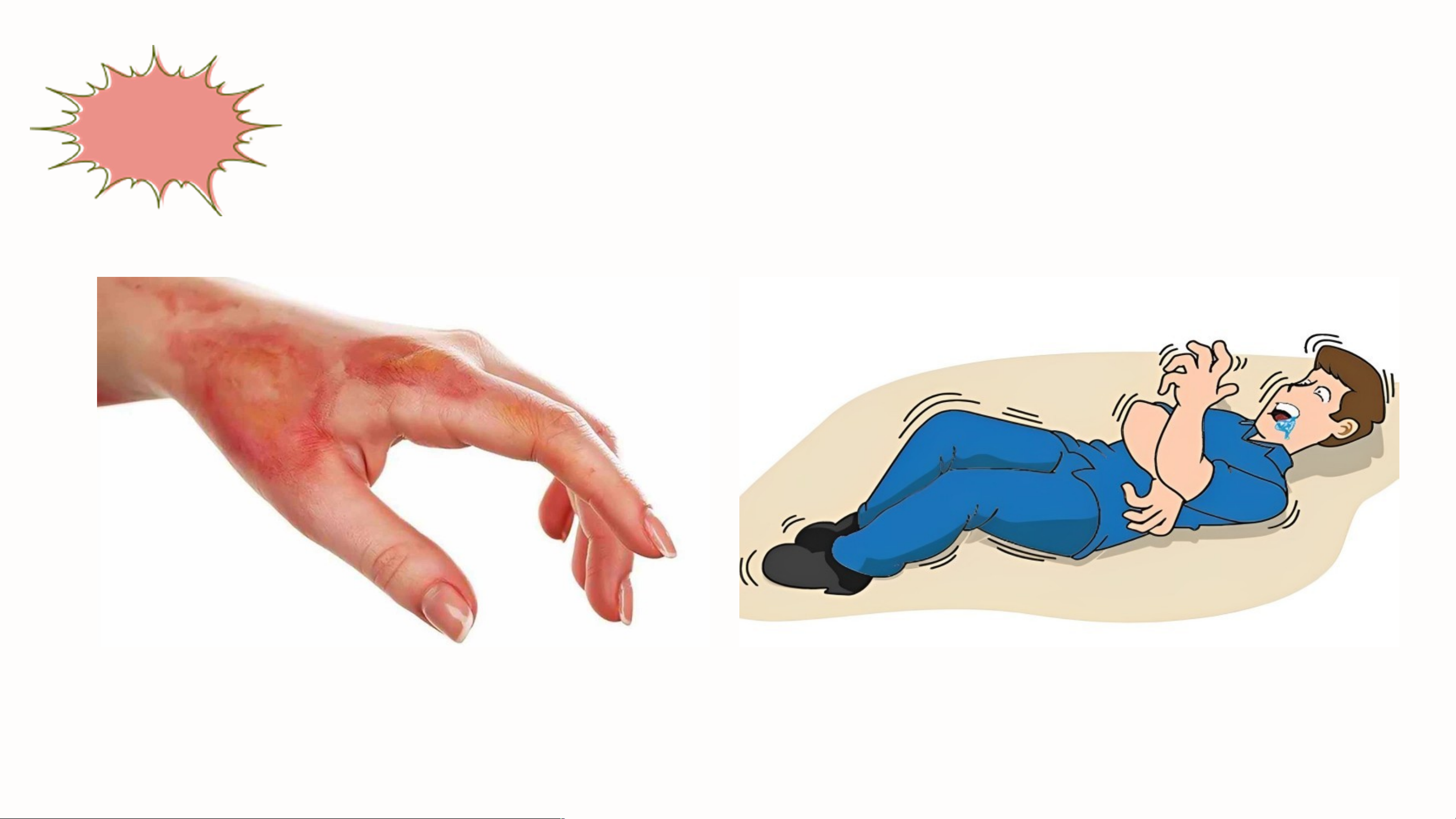
Phenol rất độc. Do đó, phải rất cẩn thận khi làm các thí nghiệm với phenol.
Bàn tay bị bỏng do tiếp xúc với
Ngộ độc do hít phải phenol trong thời phenol
gian dài gây co giật
3. TÍNH CHẤT HOÁ HỌC
1. Phản ứng thế nguyên tử hydrogen của nhóm - OH: Tính acid
Thí nghiệm 1: Phenol phản ứng với dung dịch NaOH
So sánh khả năng phản ứng của phenol với ethanol khi tác dụng với NaOH. Đáp án
Phenol phản ứng với dung dịch NaOH, ethanol không
phản ứng với dung dịch NaOH.
⇒ Phenol có tính acid mạnh hơn ethanol.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23




