

























Preview text:
GV:NGUYỄN THỊ THU HẰNG Hoạt độn Ho g 1: ạt độ Mở ng 1. đ M ầu ở đầu
HS thảo luận cặp đôi, trả lời: Nêu N cách để nhận biết bi một m chất ấ là axit 1 trong thực hự tế Kể K tên t các acid có t rong cơ ơ thể động thực hự 2 vật hoặc thực hự phẩm phẩm mà m à em em biết Tr
T ong nọc độc của ong, kiến có axit gì? 3 Hoạt độn Ho g 1: ạt độ Mở ng 1. đ M ầu ở đầu Báo cáo, thảo luận: Cá C ch nhận biết bi một m chất l à axit trong r thực hự tế: có vị chua hu , dd d axit axi làm àm quỳ qu tím m hóa đỏ 1 acetic acid tro r ng ng giấm gi ấm ăn, cit ci ric acid trong r 2 quả chanh, mal m ei e c acid trong quả táo… Tr T ong r nọc độc Ong, O kiến, muỗi m … uỗi có acid 3 fomi om c (HC H O C O O H) H . Ng N oài oà ra, a còn có acid chlohydric (H ( C H l C ), ) acid phospho ph rirc (H PO4). 3 O4). 3 Hoạt độn Ho g 1: ạt độ Mở ng 1. đ M ầu ở đầu BASE Hoạt độn Ho g 1: ạt độ Mở ng 1. đ M ầu ở đầu Tại sao khi bị ong hoặc kiến đốt, người ta thường bôi vôi vào vết đốt? Hoạt độn Ho g 1: ạt độ Mở ng 1. đ M ầu ở đầu ACID BASE
Tại sao bôi vôi vào vết cắn có thể làm cho vết phồng
xẹp xuống và không còn cảm giác rát ngứa nữa? Bài 9 : BASE. THANG PH H Hoạ oạt đ t độn ộng 2: g 1: Hình t Mở hàn đ h kiầu ến thức mới I. KHÁI NIỆM BASE
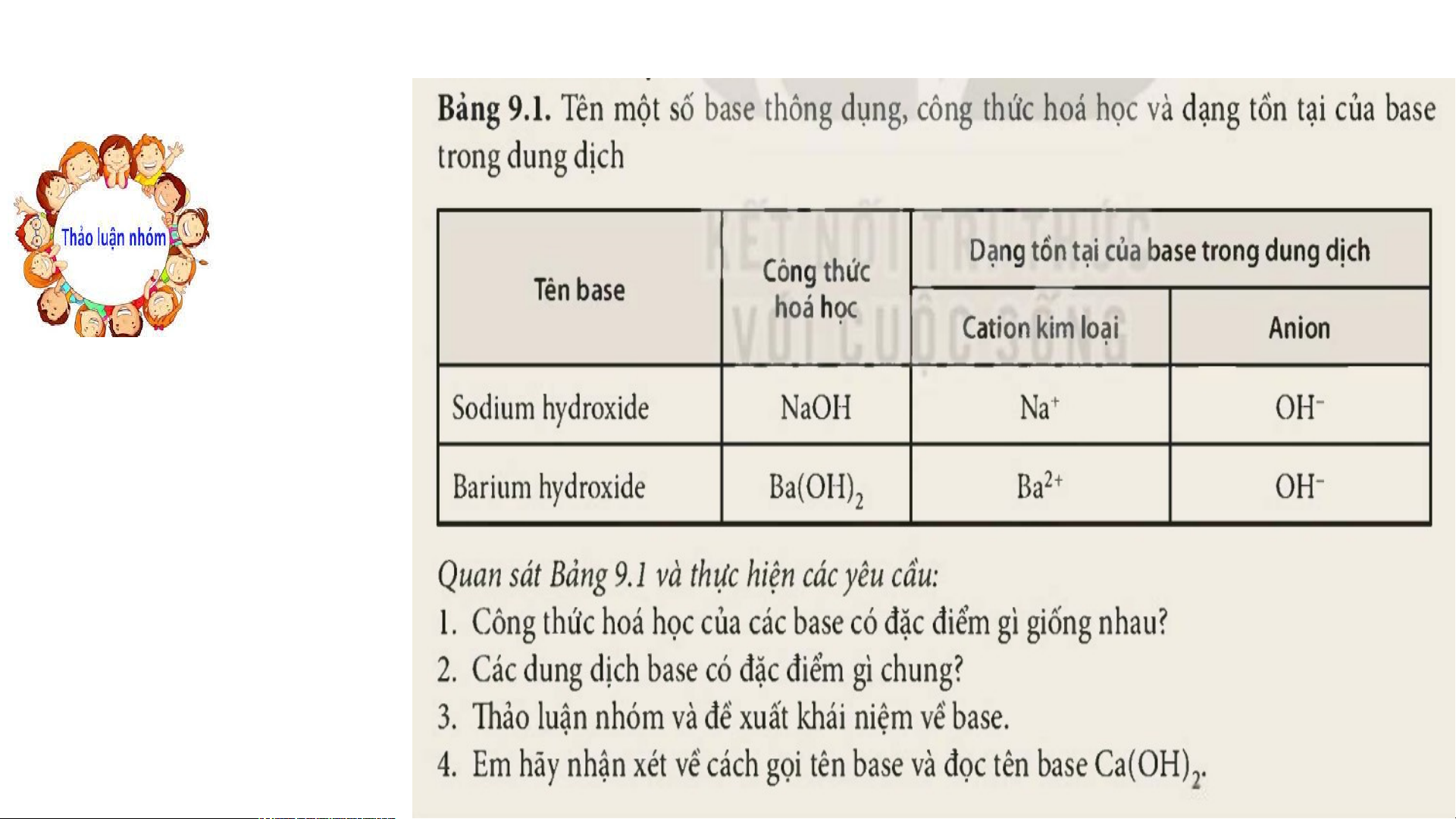
Vòng 1: Nhóm chuyên gia Quan sát bảng 9.1 Thảo luận nhóm (5’): Nhóm 1: CH1 Nhóm 2: CH2 Nhóm 3: CH3 Nhóm 4: CH4
Vòng 2: Nhóm mảnh ghép:
NV1: Thảo luận nhóm (5 phút), trả lời 4 câu hỏi:
1.Công thức hoá học của các base đều có nhóm -OH
2. Dạng tồn tại của base trong dung dịch có chứa
cation kim loại và anion OH- Báo cáo,
3. Base là những hợp chất trong phân tử có nguyên tử thảo
kim loại liên kết với nhóm hydroxide. Khi tan trong nước, luận base tạo ra ion OH-
4.Tên Base = tên kim loại + hóa trị (nếu KL có nhiều hóa trị) + hydroxide Ca(OH) : Calcium hydroxide 2 KẾT LUẬN I. KHÁI NIỆM BASE 1. K . hái K ni ệm ệm : Ba B se l se à những hợp chấ những hợp t t t r t ong r p hâ h n t n ử có ử c ng uyên t uyên ử ki ử m l m oại l iên kết ên v ới ớ nhóm hyd m ro r xide. K de. hi K ta t n t n rong nước, r base ong nước, t base ạo ra o i on O n H O - H . 2. C . ông t C h ông t ức c ứ hung c c - Dạn D g t g ổng qu át: át M(O M( H) H n + n: + l n: à hóa t rị r của ki m m l oại M 3. .T ên T g ên ọi: Tên T B ên a B se = se t ên ki ên m l m oại + hó a trị a t (nếu ( K nếu L K c L ó c nhi ều hó ều a trị r ) + hy drox dr ide i
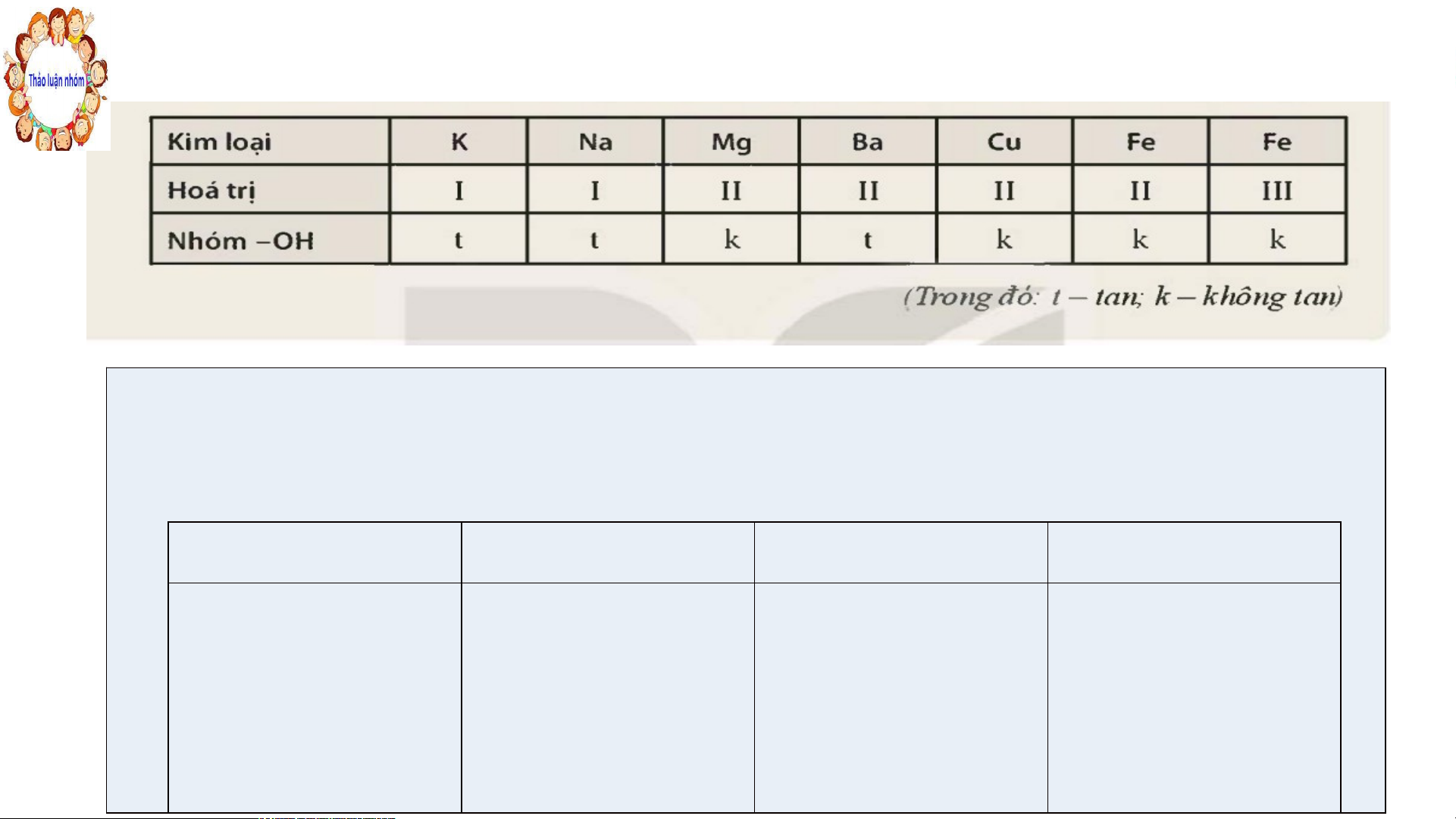
NV2: Quan sát bảng tính tan dưới đây, hoàn thành bài tập : PHT 1
Dựa vào bảng tính tan, em hãy viết công thức hóa học của các base có trong bảng, sau
đó xếp các base vào cột thích hợp và gọi tên Base không tan Tên gọi Base kiềm Tên gọi
Báo cáo, thảo luận PHT 1
Dựa vào bảng tính tan, em hãy viết công thức hóa học của các base có trong
bảng, sau đó xếp các base vào cột thích hợp và gọi tên Base không Tên gọi Base kiềm Tên gọi tan Mg(OH) Magnesiumhydroxide KOH Potassium hydroxide 2 Cu(OH) Copper (II) hydroxide NaOH Sodium hydroxide 2 Fe(OH) Iron (II) hydroxide Ba(OH) . Barium hydroxide 2 2 Fe(OH) Iron (III) hydroxide 3 KẾT LUẬN I. KHÁI NIỆM BASE 1. K 1. hái K niệm : ệm Bas B e l
e à những hợp chất à những hợp t rong r phâ n t n ử có ử ng uy u ên t ên ử ki ử m l m oại l i iên kết ên với kết nhóm hydr m ox hydr ide. K de. hi K t an t n rong nước r , base ong nước t , base ạo ra i on OH on O - H . 2. Cô 2. C ng thức c ng t hung hức c - D ạng D t ổng quá t: t M( M OH O )n + n: l n: à hóa t rị r củ a củ kim l m oại M 3. T 3. ên T g ên ọi: : Tên T B ên a B se = se t ên ki ê m m l oại + hó a trị a t ( nếu nế K L K L có nhi ều hó ều a trị a t ) + hy dro dr xide 4.Phâ 4.Ph n l n oại: + B a B se t se an được t an đượ r c t on r g nước g nướ g c ọi là kiềm ề : m NaO N H aO , K H O , K H O , H C , a( C OH O ) H ,... ,2 + B a B se khô se ng n tan t t rong nước r : ong nước Fe ( Fe OH O ) H Cu C ( u OH O ) 2, 2,…. … . II. TÍNH CHẤT HÓA HỌC:
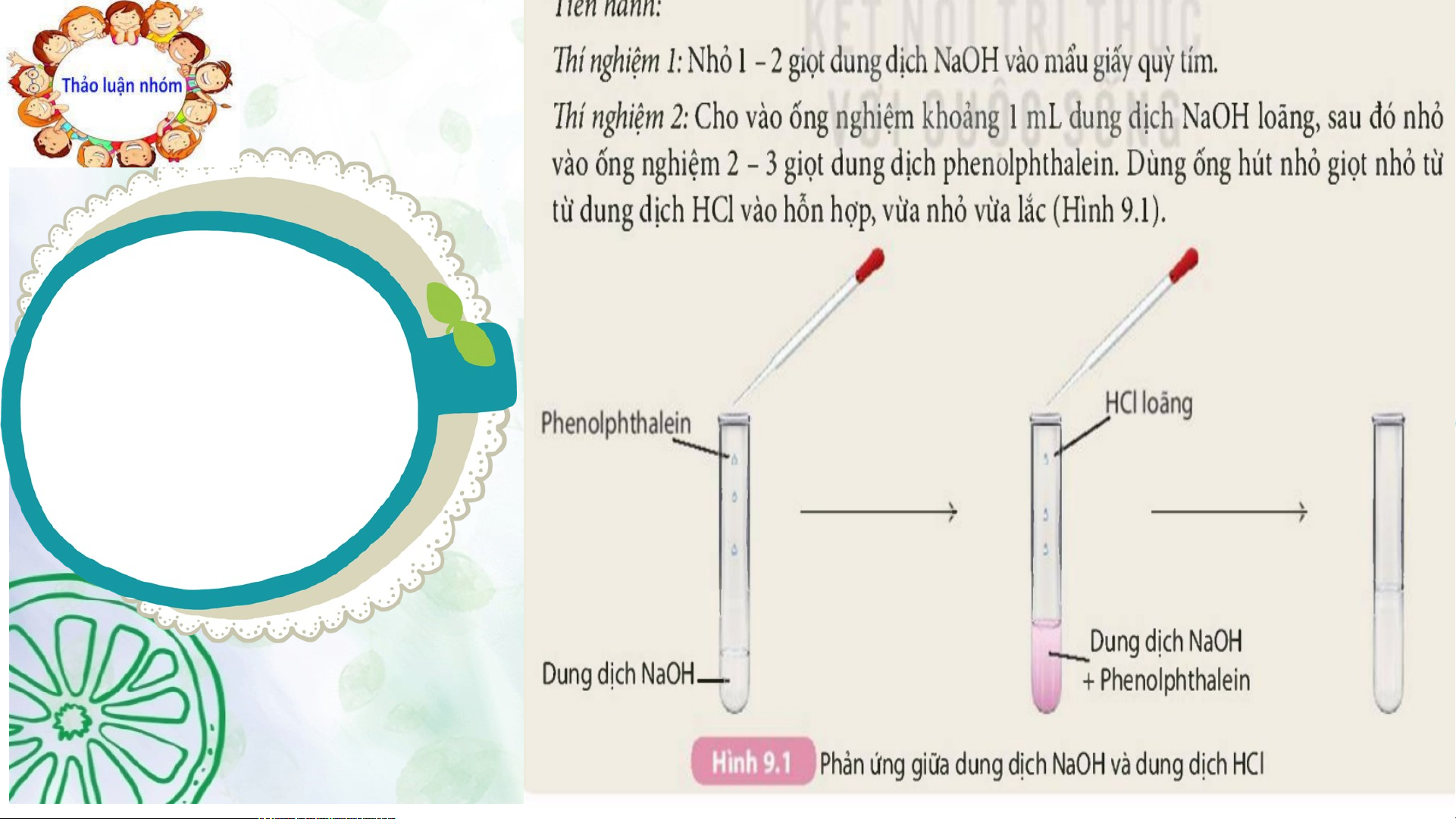
Hoạt động 1: Mở đầu Tiến hành thí nghiệm, ghi kết quả vào PHT 2 PHT 2
Tiến hành thí nghiệm tìm hiểu tính chất của base và hoàn thành bảng sau: STT Thí nghiệm Hiện tượng
Kết luận. Viết PTHH(nếu có) 1 Nhỏ 1-2 giọt dd NaOH và - D
ung dịch base làm đổi màu mẩu giấy quỳ tím Quỳ tím thành màu chất chỉ thị: xanh. +Quì tím-> xanh 2 -Cho vào ống nghiệm - Dung dịch +DD phenolphtalein không khoảng 1ml dung dịch
phenolphtalein không màu-> hồng
NaOH, sau đó nhỏ vài giọt màu -> màu hồng. dd phenolphthalein
- Nhỏ từ từ dung dịch HCl - Dung dịch màu hồng -Base tác dụng với dd acid vào hỗn hợp
chuyển sang không màu NaOH + HCl-> NaCl + H O 2 KẾT LUẬN
II. TÍNH CHẤT HÓA HỌC: - C ác C dun u g dị g d ch b h as a e (ki (k ềm ề ) làm đổi m đ màu à chất c h hỉ h thị h : + Quỳ t u ím thàn h h àn m h àu xan àu h xan . h + Du D n u g d n ị g d ch c p h he h nol n ph p talein k n h k ông màu ôn t g màu hàn h h àn m àu h àu ồn h g ồn . - Bas B e e tác dụ d n ụ g ac n id tạo thàn tạo th h mu h ối ố và nước và n ( phản h ứn ản g tr ứn ung h n òa) g h
Hoạt động 1: Mở đầu Tại sao khi bị ong hoặc kiến đốt, người ta thường bôi vôi vào vết đốt?
Hoạt động 1: Mở đầu
?1. Có hai ống nghiệm mất nhãn đựng
hai dung dịch riêng biệt không màu:
NaOH, HCl. Nêu cách nhận biết hai dung dịch trên?
Hoạt động 1: Mở đầu
?2. Ở nông thôn, người ta dùng vôi bột để
rắc lên ruộng để khử chua cho đất. Biết
rằng thành phần chính của vôi bột là CaO,
CaO tác dụng với H O tạo thành Ca(OH) . 2 2
Giải thích tác dụng của vôi bột? III. THANG PH:
Hoạt động 1: Mở đầu Tiến hành thí nghiệm, ghi kết quả vào Phiếu học tập 3 Phiếu học tập 3
Nhỏ lên mỗi mẩu giấy PH một loại dung dịch rồi ghi kết quả vào cột thích hợp: Dung dịch Nước lọc Nước Nước ngọt có nước xà Giấm ăn Dung dịch chanh gas phòng baking soda Màu giấy PH Giá trị PH
1. Từ kết quả trên, kết luận:
Dung dịch có tính axit là:………………………………………………………..
Dung dịch có tính base là: ……………………………………………………….
2. Dung dịch các chất có giá trị PH<7 có tính chất……………………
Dung dịch các chất có giá trị PH>7 có tính chất…………………… Phiếu học tập 3
Nhỏ lên mỗi mẩu giấy PH một loại dung dịch rồi ghi kết quả vào cột thích hợp: Dung dịch Nước lọc Nước Nước ngọt có nước xà Giấm ăn Dung dịch chanh gas phòng baking soda Màu giấy PH Không đổi Đỏ Đỏ Xanh Đỏ Xanh Giá trị PH 7 2 3 10 4 9
1. Từ kết quả trên, kết luận:
Dung dịch có tính acid là:………………………………………………………..
Nước chanh, nước ngọt có gas, Giấm ăn
Dung dịch có tính base là: ……………………………………………………….
Nước xà phòng, dung dịch Baking soda
2.Dung dịch các chất có giá trị PH<7 có tính chất…………………… Acid
Dung dịch các chất có giá trị PH>7 có tính chất…………………… Base KẾT LUẬN III. THANG PH: Than Th g P an H được đ dù d n ù g để g đ ể bi b ểu th u ị độ ac đ id, b d as , b e củ c a du a d n u g d n ịch. h + PH P < 7 : < Mô M i trường ac ườn id; pH ; p càng n àn hỏ th h ì ỏ th độ ac đ id c d ủa d ủ u a d n u g g dị d ch c h àng l àn ớn + PH P = 7: = Môi trường t ườn ru r ng tí n nh n (k h hôn h g c ôn ó tính n acid và k d h và k ôn h g g có t c ính n b h as a e). + PH P > 7: > Môi trường b ườn as a e; pH p cà c ng l n ớn t ớn hì h độ đ b as a e của d ủ u a d ng n d ịch c h àng l àn ớn Phiếu học tập 4
Câu 2: Em hãy nêu cách để kiểm tra đất trồng có bị chua hay không?
Lấy mẫu đất hòa vào cốc nước cất rồi dùng giấy PH hoặc thiết bị đo PH. Nếu giá trị PH đo được là <7 thì đất trồng bị chua
Câu 3: Em hãy tìm hiểu và cho biết giá trị PH trong máu, trong dịch dạ dày của người, trong nước mưa,
trong đất. Nếu giá trị PH trong máu và trong dịch dạ dày của người ngoài khoảng chuẩn sẽ gây nguy hiểm
cho sức khỏe của người như thế nào?
- PH bình thường của máu nằm trong khoảng 7,35-7,45 có nghĩa là máu có tính base yếu. KHi PH< 7,35 có thể bị các
bệnh: đau đầu, lú lẫn, mệt mỏi, ho và khó thở ; nhịp tim không đều, đau bụng, co giật; hôn mê….Khi PH> 7,45 có thể bị
các bệnh: lú lẫn và chóng mặt; run tay; tê ngứa bàn chân, mặt; co thắt cơ; buồn nôn; hôn mê;…
- Dịch ở dạ dày thường có PH khoảng 3-5,5. PH thấp sẽ giúp việc tiêu hóa thức ăn và tiêu diệt vi khuẩn trong dạ dày dễ
dàng hơn. PH>5,5 có thể do cơ thể mắc các bệnh: ung thư dạ dày, nhiễm trùng dạ dày tái phát, ; hội chứng kém hấp thu;
sự phát triển quá mức vi khuẩn đường ruột;…PH<3 ( lượng các chất tiết dạ dày cao hơn bình thường): viêm dạ dày; loét
dạ dày; hội chứng kém hấp thu; trào ngược dạ dày..
- PH của đất và nước mưa tùy thuộc từng vùng, nước mưa bình thường mà chúng ta hay sử dụng có giá trị pH rơi vào
khoảng 5,6. Cụ thể hơn, tại thành phố, giá trị pH nước mưa dao động từ 4,67 – 7,5. Và tại các khu công nghiệp, nước
mưa có giá trị pH trung bình khoảng 4,72, thường dao động từ 3,8 – 5,3.
Hoạt động 1: Mở đầu
HOẠT ĐỘNG 3: LUYỆN TẬP 单 M 击此处添加文字标题
Mỗi nhóm đều phải vượt qua 4 trạm, ở mỗi trạm sẽ có 1 gói câu hỏi
tương ứng, trả lời hết câu hỏi ở trạm này mới được sang trạm tiếp
theo, nhóm về đích trước nhất và có số câu trả lời đúng nhiều nhất là thắng TRẠM 1 TRẠM 2 TRẠM 3 TRẠM 4 ĐÍC H T Hoạ
RẠM 1 t động 1: Mở đầu
1. Dãy các base làm phenolphtalein hoá hồng A A .. N N a a O O H H ;; C C a a ( ( O O H H ) ) ;; KO KO H H 2 2 B. NaOH; Ca(OH) ; Zn(OH) 2 2 C. Ba(OH) ; KOH; Al(OH) 2 3 D. Ba(OH) ; Ca(OH) ; Fe(OH) 2 2 3
2. Trong các base dưới đây, base nào tan tốt trong nước? A. Fe(OH) . 3 B. KOH B. KOH. C. Fe(OH) . 2 D. Cu(OH) . 2 3.D A u . ng N a d Oịch H, nào KO Hsa , u C a đ ( â O y H l)à.m
quỳ tím chuyển sang màu xanh? 2 A. NaOH, KOH, Ca(OH) . 2 B. HCl, NaCl, NaOH C. HNO , Ba(OH) , NaOH 3 2 D. H SO , Ca(OH) , KOH. 2 4 2 Hoạ TRẠM t độn 2 g 1: 4. Sodiu m Mở hydroxi dđ e ầu công thức là A. NOH B. N a O B. H NaOH C.Ba(OH) 2 D.KOH.
5.Tên gọi của Mg(OH) 2 A. Potassium hydroxide C. Magnesium hydroxide B. Calcium hydroxide C. Magnesium hydroxide D. Aluminium hydroxide
A. dung dịch có môi trường base thì pH >
6. Điều khẳng định đúng là: 7.
A. dung dịch có môi trường base thì pH > 7.
B. dung dịch có môi trường trung tính thì pH < 7.
C. dung dịch có môi trường acid thì pH = 7.
D. dung dịch có môi trường trung tính thì pH > 7. Hoạ TRẠM t độn 3 7. g 1: Dung dịch Mở
nào sau đây có pH = 7 A. NaOH. B . B .N a N Cl C đ .l ầu C. H2SO4. D. HCl.
8. Dung dịch nào sau đây có pH < 7
A. NaOH. B. KCl. C.H SO . 2 4 D. KOH. 2 4
9. Ở những vùng đất phèn người ta bón vôi để làm
A. Giảm khoáng chất cho đất B. Tăng khoáng chất cho đất.
C. Giảm PH của đất. D D.. Đ Đểể ttrung rung hòa hòa đđộ ộ PPH H..
10. Dịch vị dạ dày thường có pH trong khoảng từ 2-3. Những người bị
mắc bệnh viêm loét dạ dày, tá tràng thường có pH < 2. Để chữa căn bệnh
này, người bệnh thường uống trước bữa ăn chất nào sau đây?
A. Nước đường saccharozo. B . B .D u D ng un dị g d cịh ch N aHCO .3 NaHCO . 3
C. Nước đun sôi để nguội.
D. Một ít giấm ăn. TRẠM 4
Câu 2: Một loại thuốc dành cho bệnh nhân đau dạ dày có chứa
Al(OH)3 và Mg(OH)2. Viết phương trình hoá học xảy ra giữa acid HCl có
trong dạ dày với các chất trên.
Câu 2: Các phương trình hoá học xảy ra:
Al(OH) + 3HCl → AlCl + 3H O 3 3 2
Mg(OH) + 2HCl → MgCl + 2H O. 2 2 2 1 2 KẾT QUẢ 3 4
Hoạt động 1: Mở đầu HOẠT ĐỘNG 4: - L VẬ ớp chi N a th D ành Ụ 8 n NG hóm
- Tìm hiểu sự thay đổi màu PH các loại nước ngọt
hay sử dụng, từ đó kết luận ảnh hưởng của các loại
nước ngọt đó đến sức khỏe nếu sử dụng quá nhiều.
- Chụp hình và thực hiện bài báo cáo dưới dạng
Power Point vào tiết sau
Hoạt động 1: Mở đầu HOẠT ĐỘNG 4: VẬN DỤNG
BÁO CÁO, THẢO LUẬN KẾT LUẬN Các lo ại ạ th i ứ th c ứ u ố u ng n tr g on tr g th g ị th tr ị ư tr ờ ư ng n , gầ g n ầ gũ i gũ v i ới v c á c c em p h p ầ h n l ớ l n n đ ều c ó c m ôi tr ôi ư tr ờn ư g ờn a x a it. x it. Nếu ếu u ống n g h n iề i u u s ẽ kh ẽ ông ôn tố t t t c ho s o ức ứ kh ỏ kh e n e ếu ếu k hôn h g b g iế b t iế s t ử ử d ụn ụ g m g ột c t á c ch h đ iều iều đ ộ chưa ư k ể k đến đ c òn c òn ả nh n h ư h ởn ư g đ g ến ến k inh in h t ế t v ế à v n ạ n p v à v o cơ c th ể mộ ể t h t à h m l ư l ợ ư ng n đ g ườn ư g ờn k g há h ca c o a c ó c th ó ể th g â g y â r a r ti ểu ểu đ ườn ư g. ờn 1 5 2 6 KẾT QUẢ 3 7 4 8
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- II. TÍNH CHẤT HÓA HỌC:
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- III. THANG PH:
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40




