



























Preview text:
NHẬP MÔN HÓA HỌC
Thời gian thực hiện: 01 tiết I. MỤC TIÊU 1) Kiến thức
Học xong bài này, học sinh có thể:
- Nêu được đối tượng nghiên cứu của hóa học.
- Trình bày được phương pháp học tập và nghiên cứu hóa học.
- Nêu được vai trò của hóa học đối với đời sống, sản xuất, ... 2) Năng lực a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và
điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm
vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/nhóm, trách nhiệm của bản thân, đề
xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
- Năng lực giải quyết vấn đề và sáng tạo: đề xuất được một số giải thích về các hiện tượng xảy ra
là hiện tượng vật lý hay hiện tượng hóa học.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học: hiểu được bản chất của hóa học là nghiên cứu về chất và sự biến đổi của chất.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: phân biệt được các hiện tượng hóa học
hay hiện tượng vật lý xảy ra trong tự nhiên.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được các hiện tượng hóa học hay hiện
tượng vật lý xảy ra trong tự nhiên. 3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU Giáo viên Học sinh
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV trình bày vấn đề, HS lắng nghe, dựa vào hiểu biết của bản thân trả lời.
c) Sản phẩm: HS biết được những vấn đề liên quan đến hóa học.
d) Tổ chức thực hiện: GV yêu cầu HS đọc SGK và trả lời các câu hỏi trong SGK.
Nội dung nào dưới đây thuộc đối tượng nghiên cứu của hóa học?
(1) Sự hình thành hệ Mặt Trời.
(2) Cấu tạo chất và sự biến đổi của chất.
(3) Quá trình phát triển của loài người.
(4) Tốc độ của ánh sáng trong chân không.
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Đối tượng nghiên cứu của hóa học
a) Mục tiêu: HS biết đối tượng nghiên cứu của hóa học là chất và sự biến đổi của chất.
b) Nội dung: HS đọc SGK, dựa vào sự hiểu biết bản thân để trả lời.
c) Sản phẩm: HS nêu được một số ví dụ về chất và phân tích được một số quá trình biến đổi của chất.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, đồng thời tự lấy các ví dụ về chất và sự biến đổi của chất.
(1) Hãy kể tên một số chất thông dụng xung quanh em và cho biết, chúng được tạo ra từ
những nguyên tố hóa học nào?
(2) Hãy nêu một số phản ứng hóa học xảy ra trong tự nhiên và trong sản xuất hóa học? Vai trò
và ứng dụng của chúng là gì? Bư
ớc 2: Thực hiện nhiệm vụ
HS đọc SGK; HS lấy các ví dụ về chất và sự biến đổi của chất.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ nêu ví dụ và phân tích.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 2: Phương pháp học tập và nghiên cứu hóa học
a) Mục tiêu: HS hiểu được các phương pháp học tập và nghiên cứu hóa học.
b) Nội dung: HS đọc SGK, dựa vào sự hiểu biết bản thân để trả lời.
c) Sản phẩm: HS trình bày được phương pháp học tập và nghiên cứu hóa học:
- Nắm vững nội dung chính của các vấn đề lý thuyết hóa học.
- Chủ động tìm hiểu thế giới tự nhiên.
- Vận dụng kiến thức đã học vào việc giải thích các hiện tượng hóa học xảy ra trong tự nhiên.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, đồng thời tóm tắt những điểm chính.
Vì sao cần liên hệ nội dung bài học hóa học với nội dung những môn học khác cũng như
các thí nghiệm, quá trình thực tiễn có liên quan? Nêu một ví dụ. Bư
ớc 2: Thực hiện nhiệm vụ
HS đọc SGK; trả lời câu hỏi và lấy ví dụ.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 3: Vai trò của hóa học trong thực tiễn
a) Mục tiêu: HS hiểu được vai trò của hóa học trong thực tiễn.
b) Nội dung: HS đọc SGK, dựa vào sự hiểu biết bản thân để trả lời.
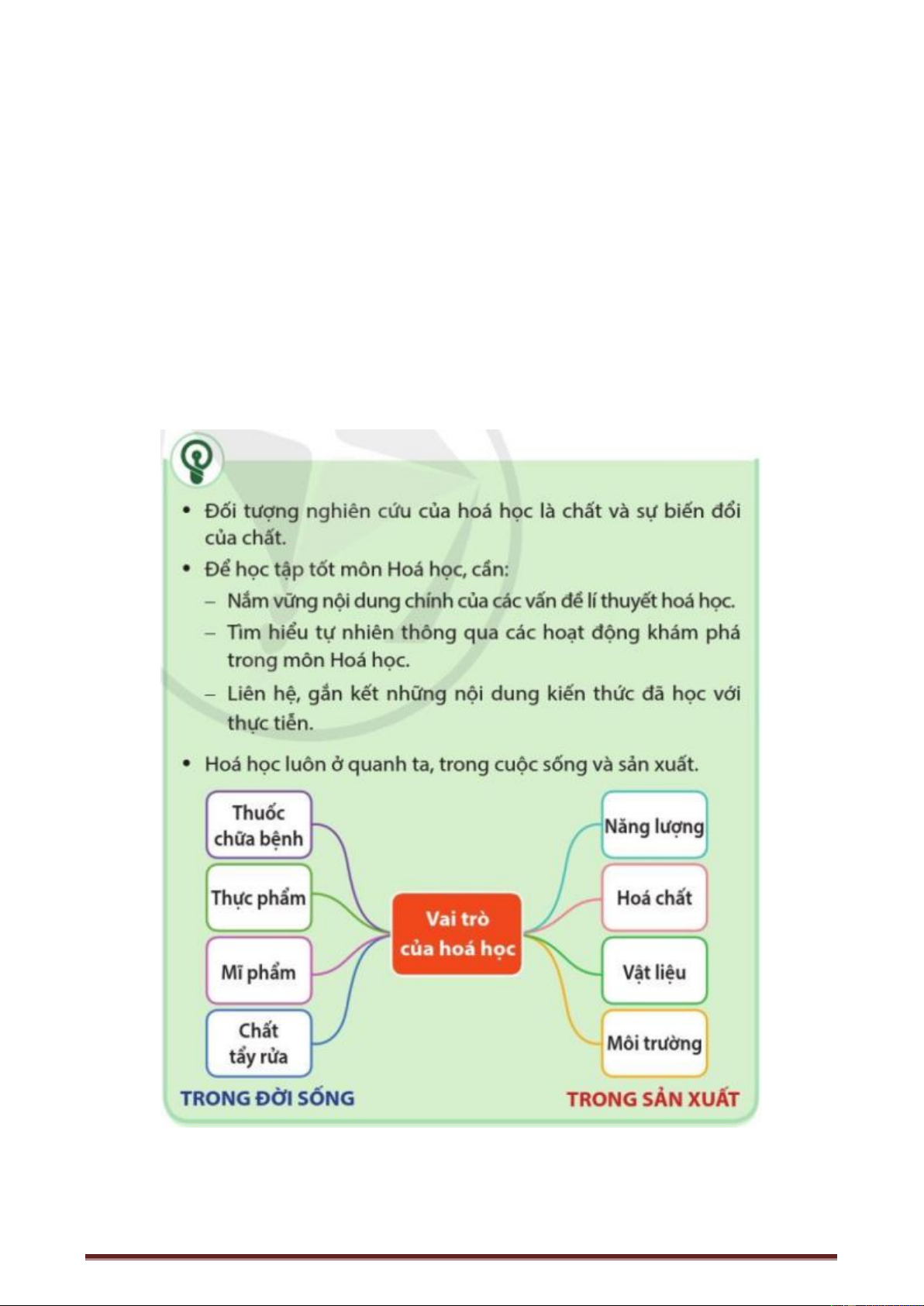
c) Sản phẩm: HS trình bày được vai trò của hóa học trong đời sống và trong sản xuất:
- Trong đời sống: Hóa học về thực phẩm, hóa học về thuốc, hóa học về mĩ phẩm, hóa học về chất tẩy rửa, ...
- Trong sản xuất: hóa học về năng lượng, hóa học về sản xuất hóa chất, hóa học về vật liệu, hóa
học về môi trường, ...
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, đồng thời tóm tắt những điểm chính.
Yêu cầu HS trả lời các câu hỏi trong tuyến phụ.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; trả lời các câu hỏi và lấy ví dụ.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu: Luyện tập, củng cố kiến thức đã học trong bài.
b) Nội dung: HS tổng kết những nội dung đã học.
c) Sản phẩm: HS sơ đồ hóa nội dung kiến thức.
d) Tổ chức thực hiện:
GV vấn đáp HS những nội dung chính của bài học. HS tự tổng kết.
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b) Nội dung: HS đưa ra các ví dụ và phân tích ví dụ.
c) Sản phẩm: Kỹ năng vận dụng vào giải thích các vấn đề đặt ra.
d) Tổ chức thực hiện:
GV yêu cầu HS nêu ra các ví dụ và phân tích ví dụ.
GV yêu cầu HS khác nhận xét. GV kết luận, đánh giá. CHỦ ĐỀ 1
CẤU TẠO NGUYÊN TỬ
THÀNH PHẦN CỦA NGUYÊN TỬ
Thời gian thực hiện: 01 tiết I. MỤC TIÊU 1) Kiến thức
Học xong bài này, học sinh có thể:
- Trình bày được thành phần của nguyên tử.
- So sánh được khối lượng của electron với proton và với neutron.
- So sánh được kích thước của hạt nhân với nguyên tử. 2) Năng lực a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và
điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm
vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/nhóm, trách nhiệm của bản thân, đề
xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
- Năng lực giải quyết vấn đề và sáng tạo: đề xuất cách giải quyết một số bài toán xác định các hạt
cơ bản của nguyên tử
- Năng lực nhận thức hóa học: hiểu được bản chất của nguyên tử gồm các hạt cơ bản là p, n, e.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: hiểu được sự đa dạng của các nguyên
tử, tạo nên sự đa dạng của vật chất trong tự nhiên.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được sự đa dạng của vật chất trong tự nhiên. 3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU Giáo viên Học sinh Các mô hình nguyên tử Chuẩn bị bài ở nhà
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV trình bày vấn đề, HS lắng nghe.
c) Sản phẩm: HS trả lời các câu hỏi của GV, cùng dẫn dắt vào nội dung vấn đề.
d) Tổ chức thực hiện: GV yêu cầu HS:
- Ở bài học trước, chúng ta tìm hiểu được, đối tượng nghiên cứu của hóa học là gì?
- Vậy chất được cấu tạo bởi những yếu tố nào?
Hôm nay, bài học 2, sẽ giúp chúng ta cùng tìm hiểu về vấn đề đó.
GV yêu cầu HS đọc phần giới thiệu ở đầu bài học. GV có thể trình chiếu nội dung lên màn hình.
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Thành phần cấu trúc của nguyên tử - Thành phần nguyên tử
a) Mục tiêu: HS biết thành phần của nguyên tử gồm các hạt p, n, e.
b) Nội dung: HS đọc SGK, trả lời câu hỏi.
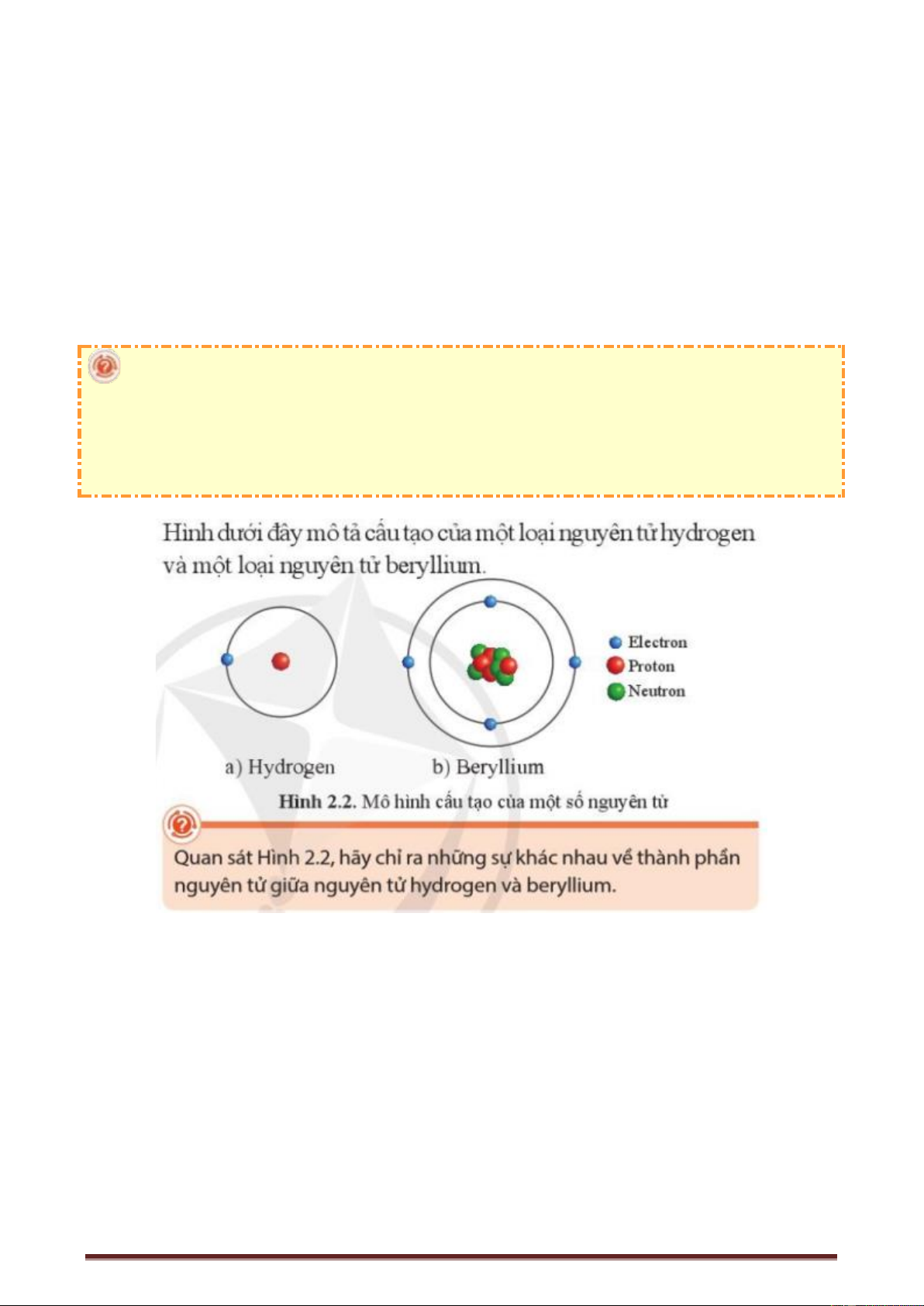
(1) Nguyên tử được cấu tạo bởi những thành phần nào? Cho biết, khối lượng và điện tích của các thành phần đó?
(2) Các nguyên tử trung hòa về điện. Dựa vào Bảng 2.1, em hãy lập luận để chứng minh rằng: trong
một nguyên tử, số proton và số electron luôn bằng nhau.
(3) Hạt proton, neutron nặng hơn hạt electron bao nhiêu lần?
(4) Hãy cho biết, bao nhiêu hạt proton thì có tổng khối lượng bằng 1 gam.
c) Sản phẩm: HS nêu được thành phần nguyên tử, khối lượng và điện tích của các hạt cơ bản.
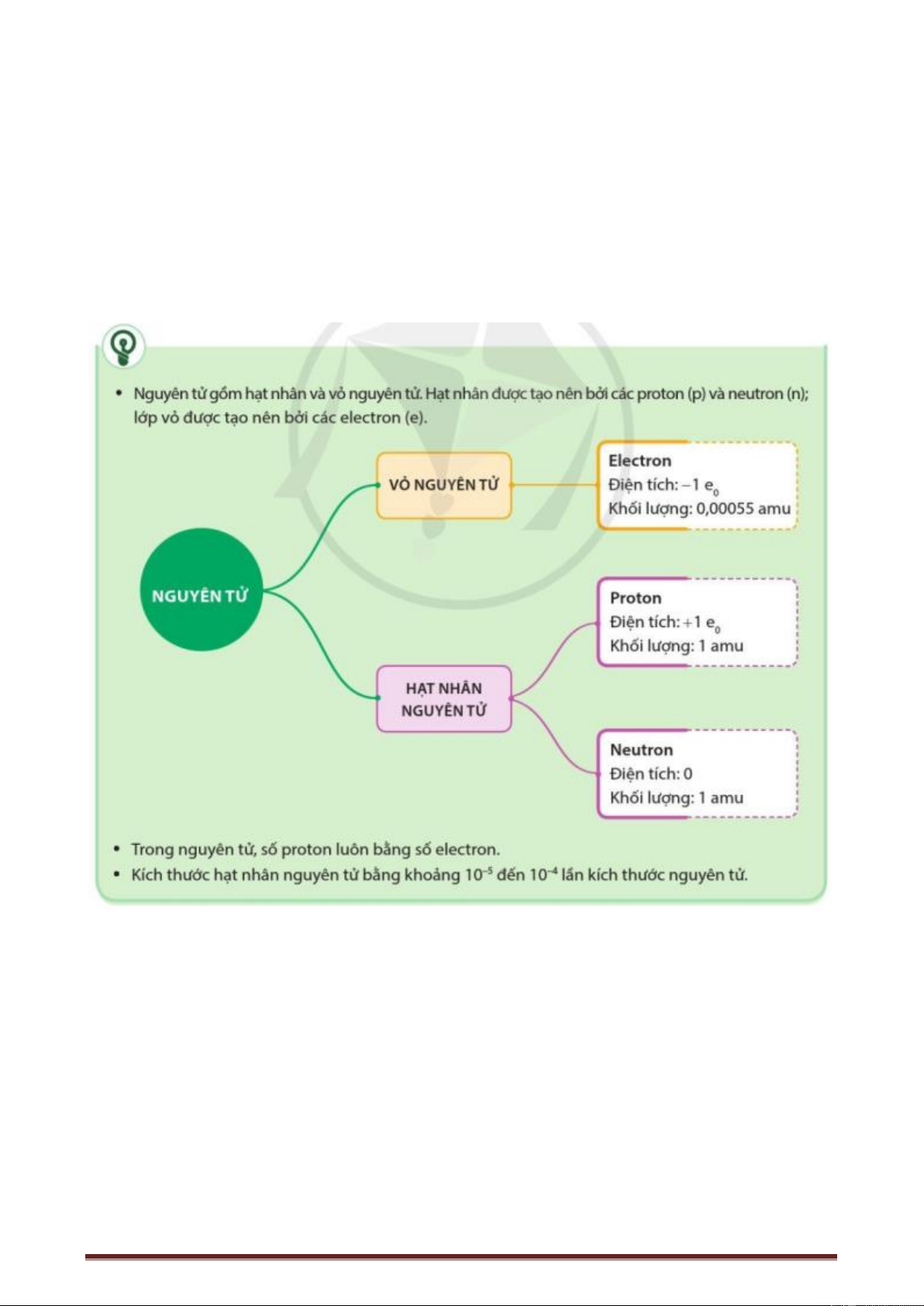
(1) Nguyên tử được cấu tạo từ các hạt cơ bản proton, neutron và electron.
(2) Vì electron mang điện tích 1-, còn proton mang điện tích 1+ và neutron không mang điện nên
để nguyên tử trung hòa điện thì tổng số điện tích (-) bằng tổng số điện tích (+), suy ra số proton luôn bằng số electron. m m 1 (amu) (3) p n = = = 1818,18 m m 0, 00055 (amu) e e
(4) Với 1 hạt proton: mp = 1 amu = 1,6605.10-27 kg = 1,6605.10-24 g → 1 23
trong 1 gam proton cã sè h¹t proton = = 6,0223.10 (h¹t) 24 1, 6605.10−
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, trả lời câu hỏi (tuyến chính và tuyến phụ):
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trả lời.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 2: Cấu trúc của nguyên tử
a) Mục tiêu: HS biết cấu trúc của nguyên tử.
b) Nội dung: HS đọc SGK, trả lời câu hỏi.
(1) Nguyên tử được cấu tạo bởi mấy phần? Thành phần của mỗi phần là gì?
(2) Khi các nguyên tử tiến lại gần nhau để hình thành liên kết hóa học, sự tiếp xúc đầu tiên giữa hai
nguyên tử sẽ xảy ra giữa
A. lớp vỏ với lớp vỏ.
B. lớp vỏ với hạt nhân.
C. hạt nhân với hạt nhân.
c) Sản phẩm: HS nêu được:
(1) Nguyên tử gồm lớp vỏ tạo nên bởi các hạt electron và hạt nhân tạo nên bởi các hạt proton và neutron.
(2) Đáp án A - lớp vỏ với lớp vỏ.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, trả lời câu hỏi (tuyến chính và tuyến phụ):
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trả lời.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 3: Khối lượng của nguyên tử
a) Mục tiêu: HS biết đơn vị đo khối lượng nguyên tử.
b) Nội dung: HS đọc SGK, trả lời câu hỏi.
c) Sản phẩm: HS nêu được:
Khối lượng nguyên tử vô cùng nhỏ, đơn vị tính là amu.
Một cách gần đúng, coi khối lượng nguyên tử bằng khối lượng hạt nhân.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, trả lời câu hỏi (tuyến chính và tuyến phụ):
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trả lời.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 4: Kích thước của nguyên tử
a) Mục tiêu: HS biết đơn vị đo kích thước nguyên tử.
b) Nội dung: HS đọc SGK, trả lời câu hỏi.
c) Sản phẩm: HS nêu được:
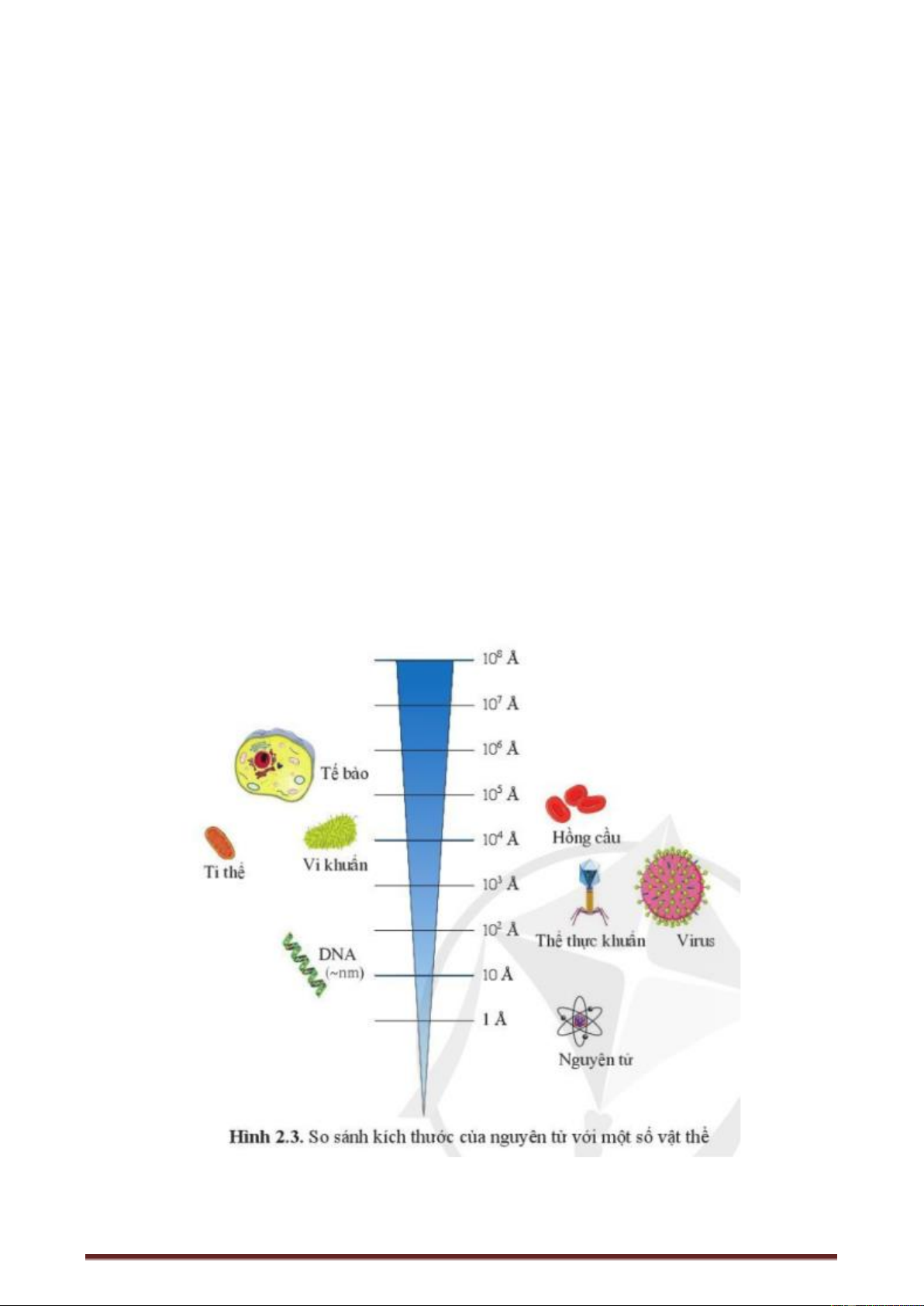
- Kích thước của nguyên tử vô cùng nhỏ bé. o o
- Đơn vị đo là Angstrom (kí hiệu là A ), 2 10 1A 10 pm 10− = = m .
- Kích thước của hạt nhân rất nhỏ so với kích thước nguyên tử, bằng từ 10-5 đến 10-4 lần kích thước nguyên tử.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, trả lời câu hỏi (tuyến chính và tuyến phụ):
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trả lời.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu: Củng cố kiến thức đã học trong bài.
b) Nội dung: HS trả lời câu hỏi, tự tổng kết kiến thức.
c) Sản phẩm: HS tổng kết kiến thức.
d) Tổ chức thực hiện: GV vấn đáp HS.
HS trả lời, tự tổng kết kiến thức theo sơ đồ.
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b) Nội dung: HS tìm hiểu thêm các mô hình nguyên tử khác.
c) Sản phẩm: HS vẽ được mô hình một số nguyên tử khác.
d) Tổ chức thực hiện:
GV yêu cầu HS thực hiện: Hãy tìm hiểu thêm về mô hình một số nguyên tử khác (nguồn: sách, tài liệu, internet, ...). CHỦ ĐỀ 1
CẤU TẠO NGUYÊN TỬ
NGUYÊN TỐ HÓA HỌC
Thời gian thực hiện: 01 tiết I. MỤC TIÊU 1) Kiến thức
Học xong bài này, học sinh có thể:
- Trình bày được khái niệm về nguyên tố hóa học, số hiệu nguyên tử, số khối và kí hiệu nguyên tử.
- Phát biểu được khái niệm đồng vị, nguyên tử khối.
- Tính được nguyên tử khối trung bình (theo amu) dựa vào khối lượng nguyên tử và phần trăm số
nguyên tử của các đồng vị theo phổ khối lượng được cung cấp. 2) Năng lực a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và
điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm
vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/nhóm, trách nhiệm của bản thân, đề
xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
- Năng lực giải quyết vấn đề và sáng tạo: đề xuất được cách giải một số bài toán liên quan đến đồng vị.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học: cách sử dụng các khái niệm hóa học về nguyên tố hóa học, số hiệu
nguyên tử, số khối và kí hiệu nguyên tử.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: xác định được nguyên tố hóa học có
trong mọt số hợp chất có trong tự nhiên xung quanh.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được các ứng dụng khác nhau của các
dạng đồng vị khác nhau. 3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU Giáo viên Học sinh
Các mô hình, hình vẽ mô phỏng. Chuẩn bị bài ở nhà.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV trình bày vấn đề, HS lắng nghe.
c) Sản phẩm: HS nắm được vấn đề của bài học mới.
d) Tổ chức thực hiện: GV yêu cầu HS đọc mục đầu bài trong SGK và trả lời các câu hỏi.
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Nguyên tố hóa học - Khái niệm về nguyên tố hóa học
a) Mục tiêu: HS biết khái niệm về nguyên tố hóa học.
b) Nội dung: HS đọc SGK, dựa vào sự hiểu biết bản thân để trả lời.
(1) Nêu khái niệm về nguyên tố hóa học? Cho ví dụ.
(2) Nguyên tử lithium (Li) có 3 proton trong hạt nhân. Khi cho Li tác dụng với khí chlorine (Cl2) sẽ
thu được muối lithium chloride (LiCl), trong đó, Li tồn tại ở dạng Li+. Ion Li+ có bao nhiêu proton trong hạt nhân.
c) Sản phẩm: HS nêu được khái niệm về nguyên tố hóa học, đưa ra được một số ví dụ về nguyên tố hóa học.
Nguyên tố hóa học là tập hợp các nguyên tử có cùng số hạt proton.
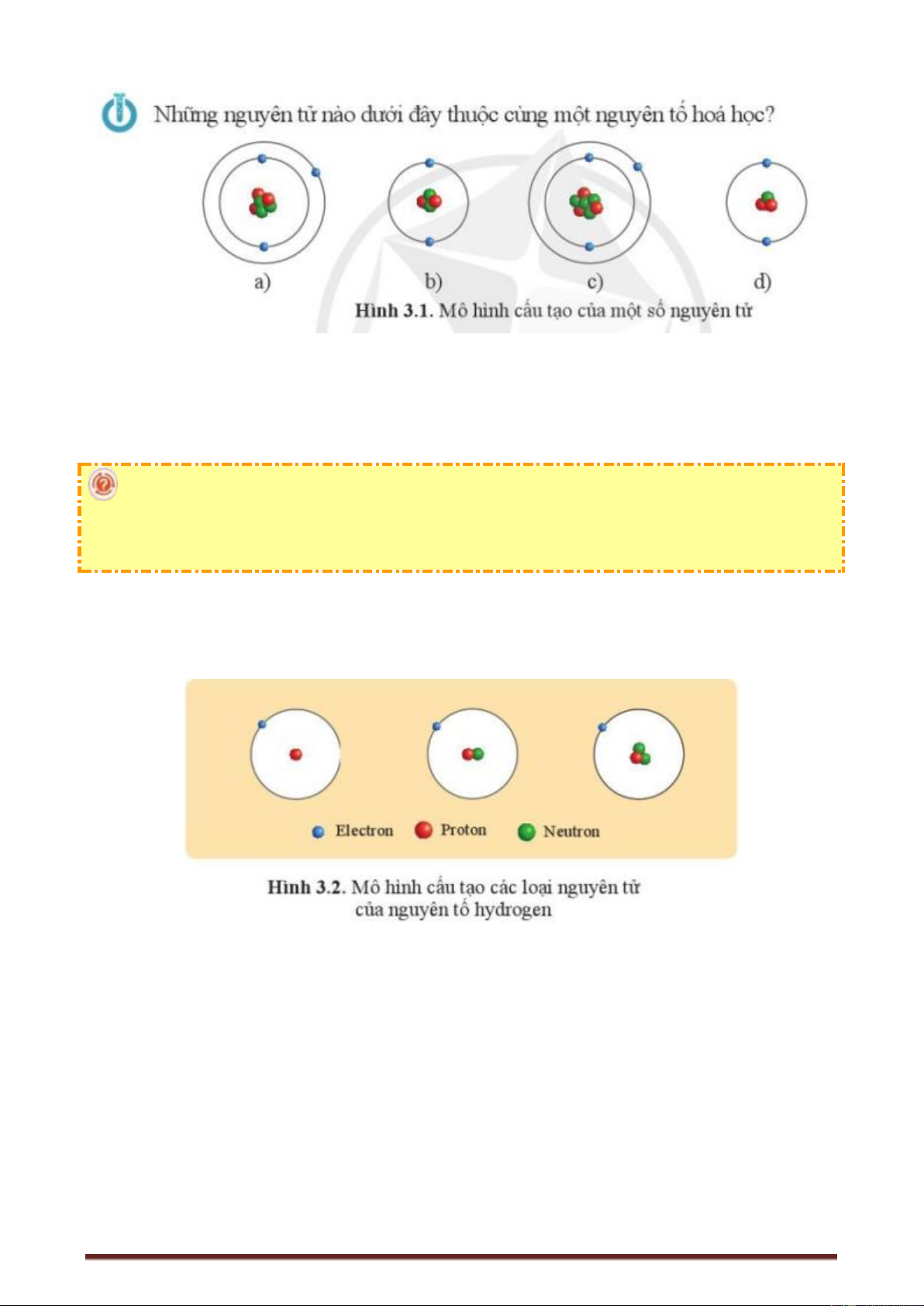
Ví dụ: Ba loại nguyên tử H đều có cùng 1 proton trong hạt nhân nên đều thuộc nguyên tố H.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK và trả lời các câu hỏi.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ nêu khái niệm, cho ví dụ.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 2: Nguyên tố hóa học - Số hiệu nguyên tử, số khối, kí hiệu nguyên tử
a) Mục tiêu: HS biết khái niệm về số hiệu nguyên tử, số khối, kí hiệu nguyên tử.
b) Nội dung: HS đọc SGK, dựa vào sự hiểu biết bản thân để trả lời các câu hỏi. Nhóm 1 Nhóm 2 Nhóm 3
(1) Nêu khái niệm về số hiệu (4) Nêu khái niệm về số khối? (6) Nêu khái niệm về kí hiệu nguyên tử?
Công thức tính số khối? nguyên tử. Cho ví dụ.
(2) Hạt nhân nguyên tử He có (5) Một nguyên tử có chứa Z (7) Nguyên tử lithium (Li) có 3
chứa 2 proton. Vậy số hiệu hạt proton, Z hạt electron và proton và 4 neutron. Viết kí hiệu
nguyên tử của He là bao N hạt neutron. Tính khối nguyên tử của nguyên tố này. nhiêu?
lượng (gần đúng theo amu) và (8) Hoàn thành bảng sau:
(3) Phân tử S8 có 128 số khối của nguyên tử này. Nguyên số p số Kí hiệu
electron. Hỏi số hiệu nguyên Nhận xét về kết quả thu được. tử n nguyên tử
tử của (S) là bao nhiêu? C 6 6 ? ? ? ? 23 X 11
c) Sản phẩm: HS nêu được các khái niệm về số hiệu nguyên tử, số khối, kí hiệu nguyên tử; HS áp
dụng xác định các yêu cầu của đề bài đưa ra.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK và chia 3 nhóm HS thực hiện 3 nhiệm vụ nêu trên.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự thảo luận nhóm và trả lời.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đại diện nhóm trình bày phần nội dung đã được chuẩn bị.
GV yêu cầu HS nhóm khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 3: Đồng vị, nguyên tử khối trung bình - Đồng vị
a) Mục tiêu: HS biết khái niệm về đồng vị.
b) Nội dung: HS đọc SGK, dựa vào sự hiểu biết bản thân để trả lời các câu hỏi.
c) Sản phẩm: HS hoàn thành các câu hỏi như đã được gợi ý.
(1) Nêu khái niệm đồng vị.
(2) Cho các nguyên tử sau: 5 7 9 11 12
X; R; Z; M; T . Những nguyên tử nào là đồng vị của nhau? 2 3 4 5 5
(3) a) Nguyên tố oxygen có 17 đồng vị, bắt đầu từ 12 O và kết thúc là 28O . Các đồng vị oxygen có tỉ 8 8 N
lệ giữa số hạt neutron (N) và số hiệu nguyên tử thỏa mãn 1
1,5 thì bền vững. Hòi trong tự Z
nhiên, thường gặp những đồng vị nào của oxygen?
b) Em hãy tìm hiểu đồng vị nào của oxygen chiếm tỉ lệ lớn nhất trong tự nhiên?
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK và hoàn thành nhiệm vụ học tập.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đúng tại chỗ trình bày.
GV yêu cầu HS nhóm khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 4: Đồng vị, nguyên tử khối trung bình - Nguyên tử khối trung bình
a) Mục tiêu: HS biết khái niệm về nguyên tử khối trung bình.
b) Nội dung: HS đọc SGK, dựa vào sự hiểu biết bản thân để trả lời các câu hỏi.
(1) Nêu khái niệm về nguyên tử khối trung bình? Công thức tính nguyên tử khối trung bình?
(2) Trong tự nhiên, argon có các đồng vị 40Ar, 38Ar, 36Ar chiếm tương ứng khoảng 99,604%,
0,063%, 0,333% số nguyên tử. Tính nguyên tử khối trung bình của Ar.
(3) Chlorine có hai đồng vị bền là 35Cl và 37Cl. Nguyên tử khối trung bình của Chlorine là 35,45.
Tính tỉ lệ phần trăm số nguyên tử mỗi đồng vị của chlorine trong tự nhiên.
c) Sản phẩm: HS nêu được khái niệm và tính được nguyên tử khối trung bình.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK và hoàn thành nhiệm vụ học tập.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đúng tại chỗ trình bày.
GV yêu cầu HS nhóm khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu: Luyện tập, củng cố kiến thức đã học trong bài.
b) Nội dung: HS tự tổng kết kiến thức.
c) Sản phẩm: Hệ thống hóa kiến thức trọng tâm của bài học.
d) Tổ chức thực hiện: GV yêu cầu vấn đáp HS.
HS trả lời và tự tổng kết kiến thức.
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b) Nội dung: HS tìm hiểu thêm về lịch sử tìm ra các nguyên tố hóa học.
c) Sản phẩm: Kỹ năng tìm hiểu, khai thác và sử dụng thông tin.
d) Tổ chức thực hiện: GV yêu cầu HS về nhà tìm hiểu thêm về lịch sử tìm ra các nguyên tố hóa
học và những ứng dụng của chúng trong đời sống và trong sản xuất. CHỦ ĐỀ 1
CẤU TẠO NGUYÊN TỬ
MÔ HÌNH NGUYÊN TỬ VÀ ORBITAL NGUYÊN TỬ
Thời gian thực hiện: 01 tiết I. MỤC TIÊU 1) Kiến thức
Học xong bài này, học sinh có thể:
- Trình bày và so sánh được mô hình nguyên tử theo Rutherford-Bohr và mô hình hiện đại.
- Nêu được khái niệm orbital nguyên tử (AO), mô tả được hình dạng của AO (s, p), số lượng electron trong một AO. 2) Năng lực a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và
điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm
vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/nhóm, trách nhiệm của bản thân, đề
xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
- Năng lực giải quyết vấn đề và sáng tạo: giải một số bài tập liên quan đến xác định dạng AO.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học: hiểu được bản chất của mô hình nguyên tử, quỹ đạo chuyển động của các electron.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: sự tương tác giữa các nguyên tử để hình thành chất.
- Năng lực vận dụng kiến thức, kỹ năng đã học: ứng dụng mô hình nguyên tử để giải thích sự hình thành các chất. 3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU Giáo viên Học sinh
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV trình bày vấn đề, HS lắng nghe.
c) Sản phẩm: HS nắm được những vấn đề liên quan đến bài học mới.
d) Tổ chức thực hiện:
GV yêu cầu HS đọc phần đầu trong SGK.
GV đặt vấn đề dẫn dắt vào bài học.
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
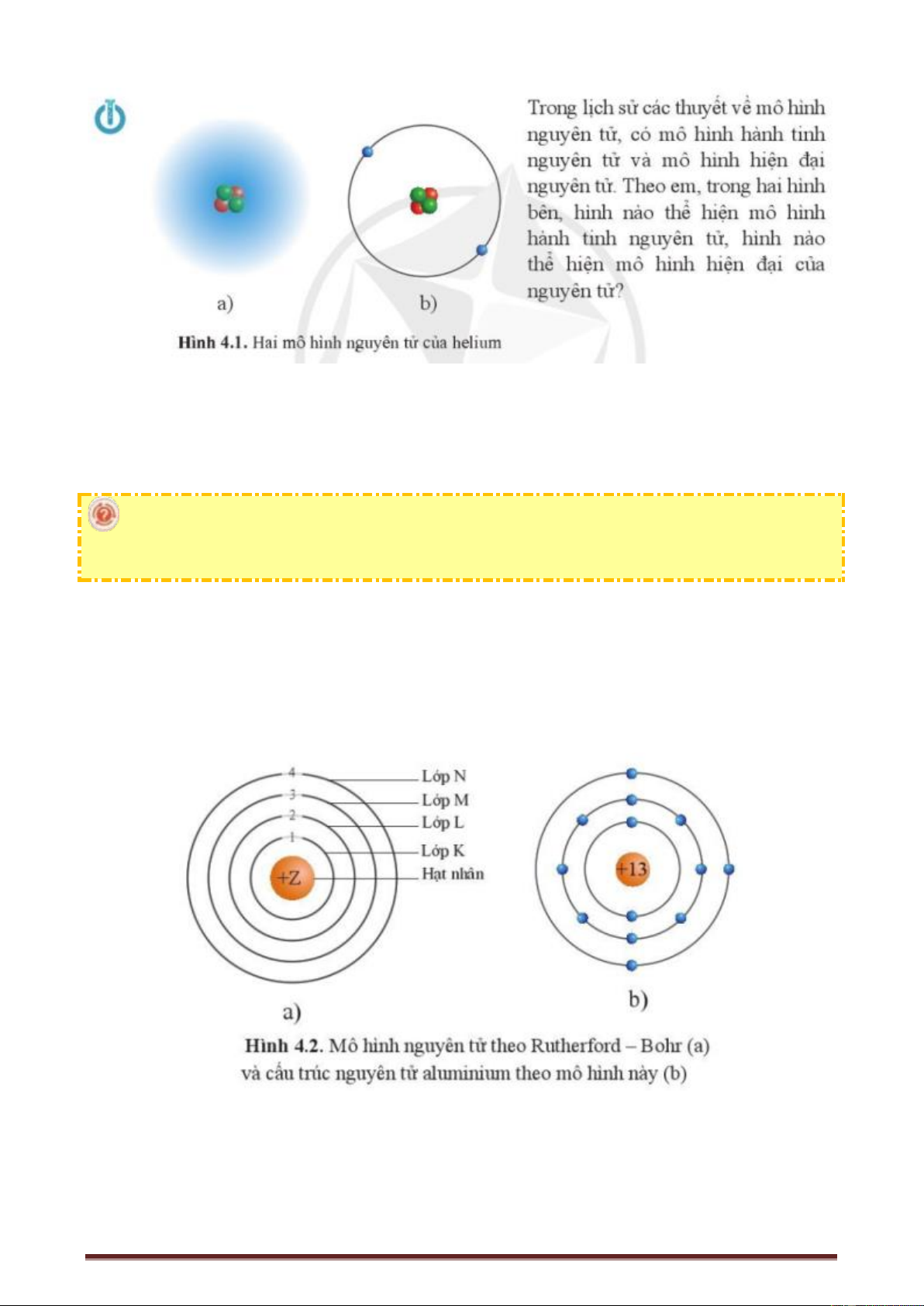
Hoạt động 1: Mô hình nguyên tử - Mô hình Rutherford-Bohr
a) Mục tiêu: HS biết mô hình nguyên tử Rutherford-Bohr.
b) Nội dung: HS đọc SGK.
(1) Nêu những điểm chính trong mô hình Rutherford-Bohr?
(2) Dựa theo mô hình nguyên tử của Rutherford-Bohr, hãy vẽ mô hình nguyên tử của các nguyên tố có Z từ 1 đến 11.
c) Sản phẩm: HS trình bày được những điểm chính trong mô hình Rutherford-Bohr, vẽ được mô
hình của một số nguyên tử đơn giản.
- Khối lượng nguyên tử tập trung chủ yếu ở hạt nhân.
- Electron quay xung quanh hạt nhân theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời.
- Năng lượng của electron phụ thuộc vào khoảng từ electron đó tới hạt nhân nguyên tử. Electron ở
càng xa hạt nhân thì năng lượng càng cao.
Các electron được phân bố vào lớp gần hạt nhân trước.
Số electron tối đa trong mỗi lớp là 2n2 (với n là số thứ tự của lớp electron, n ≤ 4).
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, chuẩn bị các nhiệm vụ học tập.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày; gọi HS lên bảng trình bày bài.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 2: Mô hình nguyên tử - Mô hình hiện đại về nguyên tử
a) Mục tiêu: HS biết mô hình hiện đại về nguyên tử.
b) Nội dung: HS đọc SGK.
(1) Nêu điểm khác biệt giữa mô hình Rutherford-Bohr và mô hình hiện đại về nguyên tử.
(2) Đám mây electron là gì?
c) Sản phẩm: HS so sánh được mô hình Rutherford-Bohr và mô hình hiện đại.
Điểm khác biệt là quỹ đạo chuyển động của các electron: mô hình Rutherford-Bohr có quỹ đạo là
những hình tròn; còn mô hình hiện đại thì sự chuyển động của electron không có quỹ đạo xác định.
Các electron chuyển động rất nhanh trong cả khu vực không gian xung quanh hạt nhân với xác
suất tìm thầy hạt khác nhau. Sự chuyển động này tạo nên một hình ảnh giống như đám mây electron.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, chuẩn bị các nhiệm vụ học tập.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày; gọi HS lên bảng trình bày bài.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 3: Orbital nguyên tử - Khái niệm
a) Mục tiêu: HS biết khái niệm orbital nguyên tử.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được khái niệm orbital nguyên tử, trình bày được các dạng của AO (s, p).
Orbital nguyên tử (kí hiệu là AO) là khu vực không gian xung quanh hạt nhân nguyên tử mà xác
suất tìm thấy electron trong khu vực đó là lớn nhất (khoảng 90%).
Orbital nguyên tử có một số hình dạng khác nhau. Ví dụ: AO hình cầu còn gọi là AO s, AO hình
số tám nổi còn gọi là AO p (tùy theo vị trí của AO p trên hệ trục tọa độ Descartes (Đề-các), sẽ còn
gọi là AO px, AO py, AO pz).
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, chuẩn bị các nhiệm vụ học tập.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày; gọi HS lên bảng trình bày bài.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 4: Orbital nguyên tử - Số lượng electron trong một AO
a) Mục tiêu: HS biết khái niệm, cách xác định số lượng electron trong một AO.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS xác định được số lượng electron trong các AO.
Một AO chỉ chứa tối đa 2 electron, 2 electron này được gọi là electron ghép đôi.
Nếu AO chỉ chứa 1 electron, 1 electron này được gọi là electron độc thân.
Nếu AO không chứa electron nào, được gọi là AO trống.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK, chuẩn bị các nhiệm vụ học tập.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự trả lời các câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày; gọi HS lên bảng trình bày bài.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu: Luyện tập, củng cố kiến thức đã học trong bài.
b) Nội dung: HS tổng kết lại nội dung kiến thức.
c) Sản phẩm: HS hệ thống hóa nội dung kiến thức.
d) Tổ chức thực hiện:
GV yêu cầu HS tổng kết và hệ thống hóa nội dung kiến thức trong bài.
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b) Nội dung: HS tìm hiểu thêm qua internet.
c) Sản phẩm: Kỹ năng khai thác và xử lý thông tin.
d) Tổ chức thực hiện:
GV yêu cầu HS về nhà tìm hiểu thêm các thông tin về: hình dạng của các AO d, f. CHỦ ĐỀ 1
CẤU TẠO NGUYÊN TỬ
LỚP, PHÂN LỚP VÀ CẤU HÌNH ELECTRON NGUYÊN TỬ
Thời gian thực hiện: 01 tiết I. MỤC TIÊU 1) Kiến thức
Học xong bài này, học sinh có thể:
- Trình bày được khái niệm lớp, phân lớp electron và mối quan hệ về số lượng phân lớp trong một
lớp. Liên hệ được về số lượng AO trong một phân lớp, trong một lớp.
- Viết được cấu hình electron nguyên tử theo lớp, phân lớp electron và theo ô orbital khi biết số
hiệu nguyên tử Z của 20 nguyên tố đầu tiên trong bảng tuần hoàn.
- Dựa vào đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử, dự đoán được tính chất hóa
học cơ bản (kim loại hay phi kim) của nguyên tố tương ứng. 2) Năng lực a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và
điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm
vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/nhóm, trách nhiệm của bản thân, đề
xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
- Năng lực giải quyết vấn đề và sáng tạo: đề xuất được một số giải thích về các hiện tượng xảy ra
trong tự nhiên về mặt hóa học.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học: hiểu được bản chất của lớp, phân lớp, cấu hình electron nguyên tử.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: phân biệt được các hiện tượng hóa học
hay hiện tượng vật lý xảy ra trong tự nhiên.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được các hiện tượng hóa học xảy ra trong tự nhiên. 3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU Giáo viên Học sinh Mô hình, hình vẽ Chuẩn bị bài ở nhà
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV trình bày vấn đề, HS lắng nghe, dựa vào hiểu biết của bản thân trả lời.
c) Sản phẩm: HS biết được những vấn đề liên quan đến bài học mới.
d) Tổ chức thực hiện: GV yêu cầu HS đọc SGK và trả lời các câu hỏi trong SGK:
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Lớp và phân lớp electron - Lớp electron
a) Mục tiêu: HS biết khái niệm lớp electron.
b) Nội dung: HS đọc SGK, dựa vào sự hiểu biết bản thân để trả lời.
c) Sản phẩm: HS nêu được khái niệm lớp electron và xác định được số thứ tự của lớp.
- Các electron trong cùng một lớp có năng lượng gần bằng nhau.
- Số electron và số AO trong lớp electron thứ n (n ≤ 4) được ghi nhớ theo quy tắc sau: Lớp thứ n có n2 AO
Lớp thứ n có tối đa 2n2 electron.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 2: Lớp và phân lớp electron - Phân lớp electron
a) Mục tiêu: HS biết khái niệm phân lớp electron.
b) Nội dung: HS đọc SGK, trả lời các câu hỏi:
(1) Nêu khái niệm phân lớp.
(2) Xác định số lượng và kí hiệu các phân lớp trong một lớp.
(3) Xác định số lượng AO trong mỗi phân lớp
c) Sản phẩm: HS nêu được khái niệm phân lớp electron và xác định được số phân lớp trong một
lớp; số electron tối đa trong một phân lớp, kí hiệu điền số electron vào phân lớp.
- Các electron trong cùng một phân lớp có năng lượng bằng nhau.
- Số lượng và kí hiệu các phân lớp trong một lớp:
Lớp K, n = 1, có một phân lớp, kí hiệu 1s.
Lớp L, n = 2, có hai phân lớp, kí hiệu 2s, 2p.
Lớp M, n = 3, có ba phân lớp, kí hiệu 3s, 3p, 3d.
- Số lượng AO trong mỗi phân lớp: Phân lớp ns có 1 AO. Phân lớp np có 3 AO. Phân lớp nd có 5 AO. Phân lớp nf có 7 AO.
- Kí hiệu số electron trong mỗi phân lớp. Ví dụ: 2s1, 3p4, ...
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 3: Cấu hình electron nguyên tử - Cách viết cấu hình electron nguyên tử
a) Mục tiêu: HS biết cách viết cấu hình electron nguyên tử.
b) Nội dung: HS đọc SGK, trả lời các câu hỏi.
c) Sản phẩm: HS nêu được khái niệm cấu hình electron nguyên tử, các bước viết cấu hình electron nguyên tử.
- Cấu hình electron biểu diễn sự phân bố electron vào lớp vỏ nguyên tử theo các lớp và phân lớp.
- Các bước viết cấu hình electron nguyên tử:
Quy tắc 1: Điền electron theo thứ tự các mức năng lượng từ thấp đến cao: (dãy Klechkovski) 1s2s2p3s3p4s3d4p5s4d5p6s ...
Quy tắc 2: Đổi lại vị trí các phân lớp sao cho số thứ tự lớp (n) tăng dần từ trái qua phải, các phân
lớp trong cùng một lớp theo thứ tự s, p, d, f. Ví dụ: Li (Z = 3): 1s22s1
K (Z = 19): 1s22s22p63s23p64s1
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày; gọi HS lên bảng biểu diễn.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 4: Cấu hình electron nguyên tử - Biểu diễn cấu hình electron theo ô orbital
a) Mục tiêu: HS biết cách viết cấu hình electron theo ô obital.
b) Nội dung: HS đọc SGK, trả lời các câu hỏi.
c) Sản phẩm: HS nêu được quy tắc biểu diễn cấu hình electron theo ô obital, viết được cấu hình electron theo ô orbital.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày; gọi HS lên bảng biểu diễn.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 5: Dự đoán tính chất hóa học cơ bản của nguyên tố dựa theo cấu hình electron nguyên tử
a) Mục tiêu: HS biết cách dự đoán tính chất hóa học của nguyên tố dựa theo cấu hình electron nguyên tử.
b) Nội dung: HS đọc SGK, trả lời các câu hỏi.
c) Sản phẩm: HS dự đoán được tính chất hóa học cơ bản của nguyên tố dựa theo cấu hình electron nguyên tử.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu: Luyện tập, củng cố kiến thức đã học trong bài.
b) Nội dung: HS tự tổng kết kiến thức trong bài.
c) Sản phẩm: HS hệ thống hóa kiến thức trong bài.
d) Tổ chức thực hiện: GV vấn đáp HS để gợi ý HS tổng kết.
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b) Nội dung: HS về nhà tìm hiểu.
c) Sản phẩm: Kỹ năng xử lý vấn đề
d) Tổ chức thực hiện:
GV yêu cầu HS: Tìm hiểu tính chất hóa học của một số nguyên tố dựa vào cấu hình electron nguyên tử của nguyên tố đó. BẢNG TUẦN HOÀN CHỦ ĐỀ 2
CÁC NGUYÊN TỐ HÓA HỌC
CẤU TẠO CỦA BẢNG TUẦN HOÀN
CÁC NGUYÊN TỐ HÓA HỌC
Thời gian thực hiện: 01 tiết I. MỤC TIÊU 1) Kiến thức
Học xong bài này, học sinh có thể:
- Nêu được lịch sử phát minh định luật tuần hoàn và bảng tuần hoàn các nguyên tố hóa học.
- Mô tả được cấu tạo của bảng tuần hoàn các nguyên tố hóa học và nêu được khái niệm liên quan: ô, chu kì, nhóm.
- Nêu được nguyên tắc sắp xếp của bảng tuần hoàn các nguyên tố hóa học.
- Phân loại được nguyên tố hóa học. 2) Năng lực a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và
điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm
vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/nhóm, trách nhiệm của bản thân, đề
xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
- Năng lực giải quyết vấn đề và sáng tạo: đề xuất được một số giải thích về các hiện tượng xảy ra
trong tự nhiên về mặt hóa học.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học: hiểu được bản chất của hóa học là nghiên cứu về chất và sự biến đổi của chất.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: phân biệt được các hiện tượng hóa học
hay hiện tượng vật lý xảy ra trong tự nhiên.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được các hiện tượng hóa học xảy ra trong tự nhiên. 3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU Giáo viên Học sinh Bảng tuần hoàn Chuẩn bị bài ở nhà
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV kiểm tra bài cũ.
c) Sản phẩm: HS hoàn thành nhiệm vụ học tập
d) Tổ chức thực hiện: GV yêu cầu HS:
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Lịch sử phát minh
a) Mục tiêu: HS biết lịch sử phát minh ra bảng hệ thống tuần hoàn.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được lịch sử phát minh ra bảng hệ thống tuần hoàn.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK và trả lời các câu hỏi.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 2: Nguyên tắc sắp xếp
a) Mục tiêu: HS biết nguyên tắc sắp xếp của bảng hệ thống tuần hoàn.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được các nguyên tắc sắp xếp của bảng hệ thống tuần hoàn.
- Các nguyên tố hóa học được sắp xếp từ trái sang phải và từ trên xuống dưới theo chiều tăng dần
của điện tích hạt nhân của nguyên tử.
- Các nguyên tố mà nguyên tử có cùng số lớp electron được xếp vào cùng một hàng.
- Các nguyên tố mà nguyên tử có cùng số electron hóa trị như nhau được xếp vào cùng một cột.
(Electron hóa trị là những electron có khả năng tham gia hình thành liên kết hóa học - thường là
những electron ở lớp ngoài cùng).
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 3: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
a) Mục tiêu: HS biết cấu tạo của bảng hệ thống tuần hoàn.
b) Nội dung: HS đọc SGK, hoàn thành nhiệm vụ học tập. Nhóm 1 Nhóm 2 Nhóm 3
- Mỗi nguyên tố hóa học được - Chu kì là tập hợp các nguyên - Nhóm là tập hợp các nguyên
xếp vào một o trong bảng tuần tố hóa học mà nguyên tử của tố hóa học mà nguyên tử có .....
hoàn, gọi là ............................... chúng có cùng .......................... ...................................................
- Số thứ tự của ô nguyên tố được xếp theo chiều tăng dần ... được xếp thành cột theo chiều
bằng .......................................... ................................................... ...................................................
................................................... - Số thứ tự của chu kì bằng ...... - Bảng tuần hoàn chia thánh 8
................................................... nhóm .... và 8 nhóm .....
c) Sản phẩm: HS nêu được khái niệm ô, chu kì, nhóm.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV chia 3 nhóm HS, yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS thảo luận, hoàn thành câu hỏi.
Bước 3: Báo cáo kết quả
GV yêu cầu đại diện HS trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 4: Liên hệ giữa cấu hình electron nguyên tử với vị trí của nguyên tố trong bảng tuần hoàn
a) Mục tiêu: HS biết mối liên hệ giữa cấu hình electron với vị trí nguyên tố trong bảng tuần hoàn.
b) Nội dung: HS đọc SGK, hoàn thành nhiệm vụ học tập.
c) Sản phẩm: HS nêu được mối liên hệ giữa cấu hình electron với vị trí nguyên tố trong bảng tuần hoàn.
- Số thứ tự của ô nguyên tố bằng số hiệu nguyên tử của nguyên tố đó.
- Số thứ tự của chu kì bằng số lớp electron trong nguyên tử của nguyên tố thuộc chu kì đó.
- Nguyên tố nhóm A có cấu hình electron lớp ngoài cùng dạng ns1-2 hoặc ns2np1-6
(Với nguyên tố nhóm A, số thứ tự của nhóm bằng số electron lớp ngoài cùng của nguyên tử
nguyên tố đó - trừ He).
Nguyên tố nhóm B* có cấu hình electron phân lớp ngoài cùng và phân lớp sát lớp ngoài cùng dạng (n - 1)d1-10ns1-2.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ HS đọc SGK.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng lên tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 5: Phân loại nguyên tố hóa học - Dựa theo cấu hình electron
a) Mục tiêu: HS biết cách phân loại nguyên tố hóa học dựa theo cấu hình electron.
b) Nội dung: HS đọc SGK, hoàn thành nhiệm vụ học tập.
c) Sản phẩm: HS phân loại được nguyên tố hóa học dựa theo cấu hình electron.
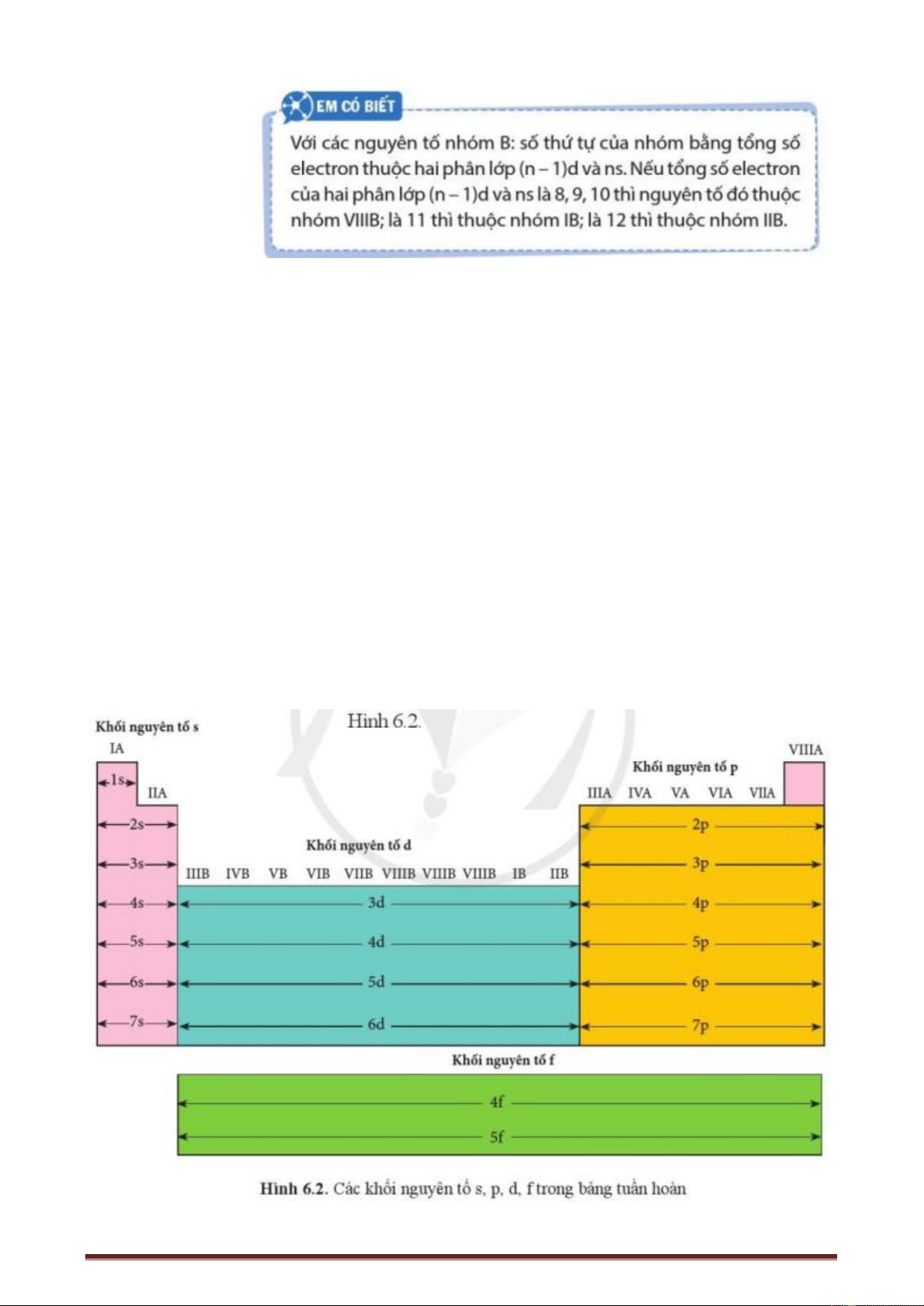
Dựa theo cấu hình, có thể phân loại thành các nguyên tố s, p, d, f.
- Nguyên tố s → nhóm A → cấu hình electron lớp ngoài cùng: ns1-2.
- Nguyên tố p → nhóm A → cấu hình electron lớp ngoài cùng: ns2np1-6.
- Nguyên tố d → nhóm B → cấu hình electron lớp ngoài cùng: (n - 1)d1-10ns2.
- Nguyên tố f → nhóm B → cấu hình electron lớp ngoài cùng: (n - 2)f0-14(n - 1)d0-2ns2.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ HS đọc SGK.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng lên tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 6: Phân loại nguyên tố hóa học - Dựa theo tính chất
a) Mục tiêu: HS biết cách phân loại nguyên tố hóa học dựa theo tính chất.
b) Nội dung: HS đọc SGK, hoàn thành nhiệm vụ học tập.
c) Sản phẩm: HS phân loại được nguyên tố hóa học dựa theo tính chất.
Các nguyên tố hóa học còn có thể được phân loại dựa theo tính chất hóa học cơ bản. Dựa theo
cách này, các nguyên tố hóa học được phân loại thành: kim loại, phi kim và khí hiếm.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ HS đọc SGK.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng lên tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu: Luyện tập, củng cố kiến thức đã học trong bài.
b) Nội dung: HS tổng kết kiến thức; HS làm các bài tập 1, 2, 3/tr.37.
c) Sản phẩm: HS hệ thống hóa được kiến thức trong bài học.
d) Tổ chức thực hiện: GV vấn đáp để HS tự tổng kết và hệ thống hóa kiến thức.
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b) Nội dung: HS tìm hiểu thêm ở nhà.
c) Sản phẩm: Kỹ năng tìm hiểu, khai thác và xử lý thông tin.
d) Tổ chức thực hiện: GV yêu cầu HS: BẢNG TUẦN HOÀN CHỦ ĐỀ 2
CÁC NGUYÊN TỐ HÓA HỌC
XU HƯỚNG BIẾN ĐỔI MỘT SỐ TÍNH CHẤT CỦA
ĐƠN CHẤT, BIẾN ĐỔI THÀNH PHẦN VÀ TÍNH
CHẤT CỦA HỢP CHẤT TRONG MỘT CHU KÌ VÀ TRONG MỘT NHÓM
Thời gian thực hiện: 01 tiết I. MỤC TIÊU 1) Kiến thức
Học xong bài này, học sinh có thể:
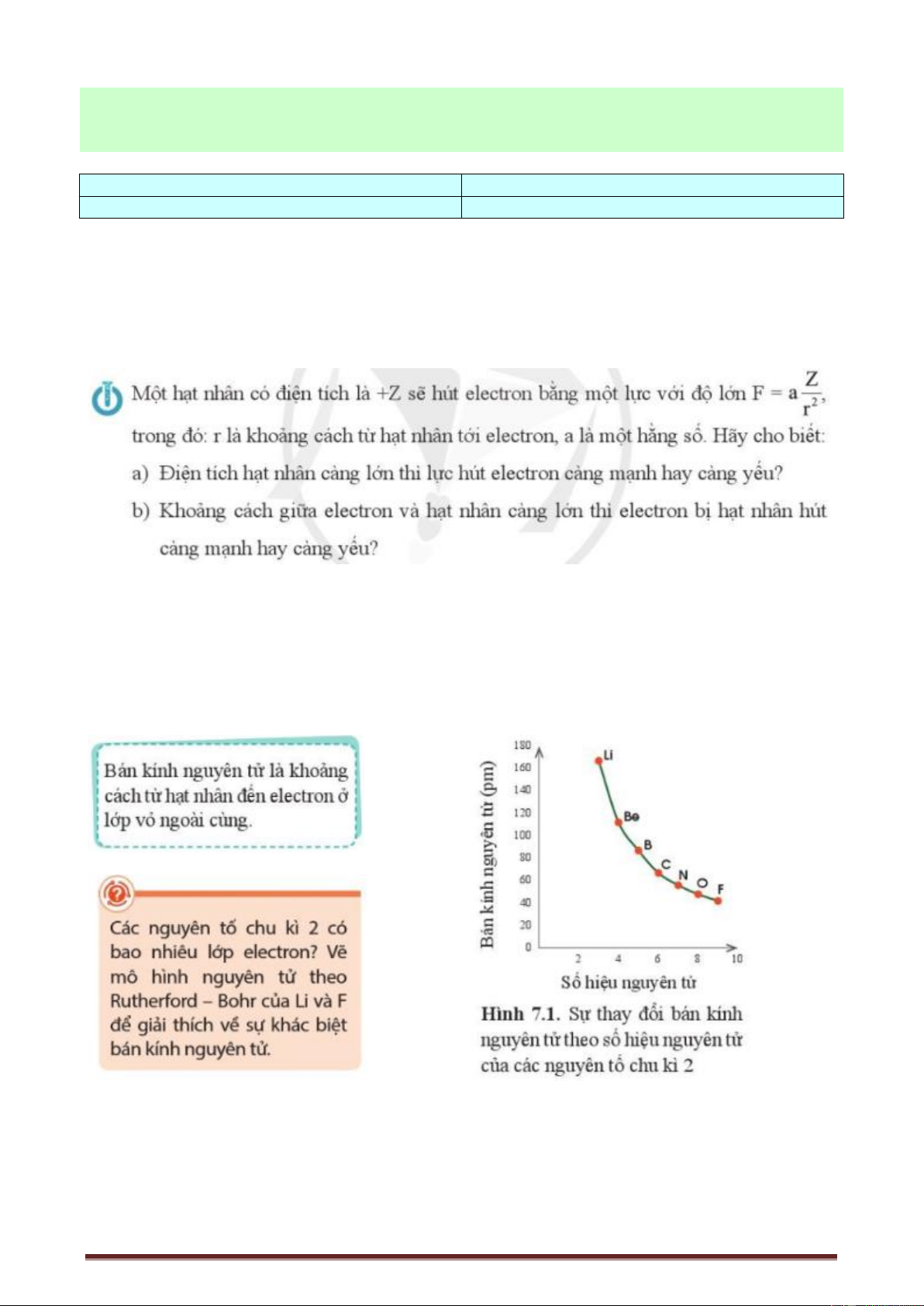
- Giải thích được xu hướng biến đổi bán kính nguyên tử trong một chu kì, trong một nhóm (các nguyên tố nhóm A).
- Nhận xét và giải thích được xu hướng biến đổi độ âm điện và tính kim loại, phi kim của nguyên
tử các nguyên tố trong một chu kì, trong một nhóm (nhóm A).
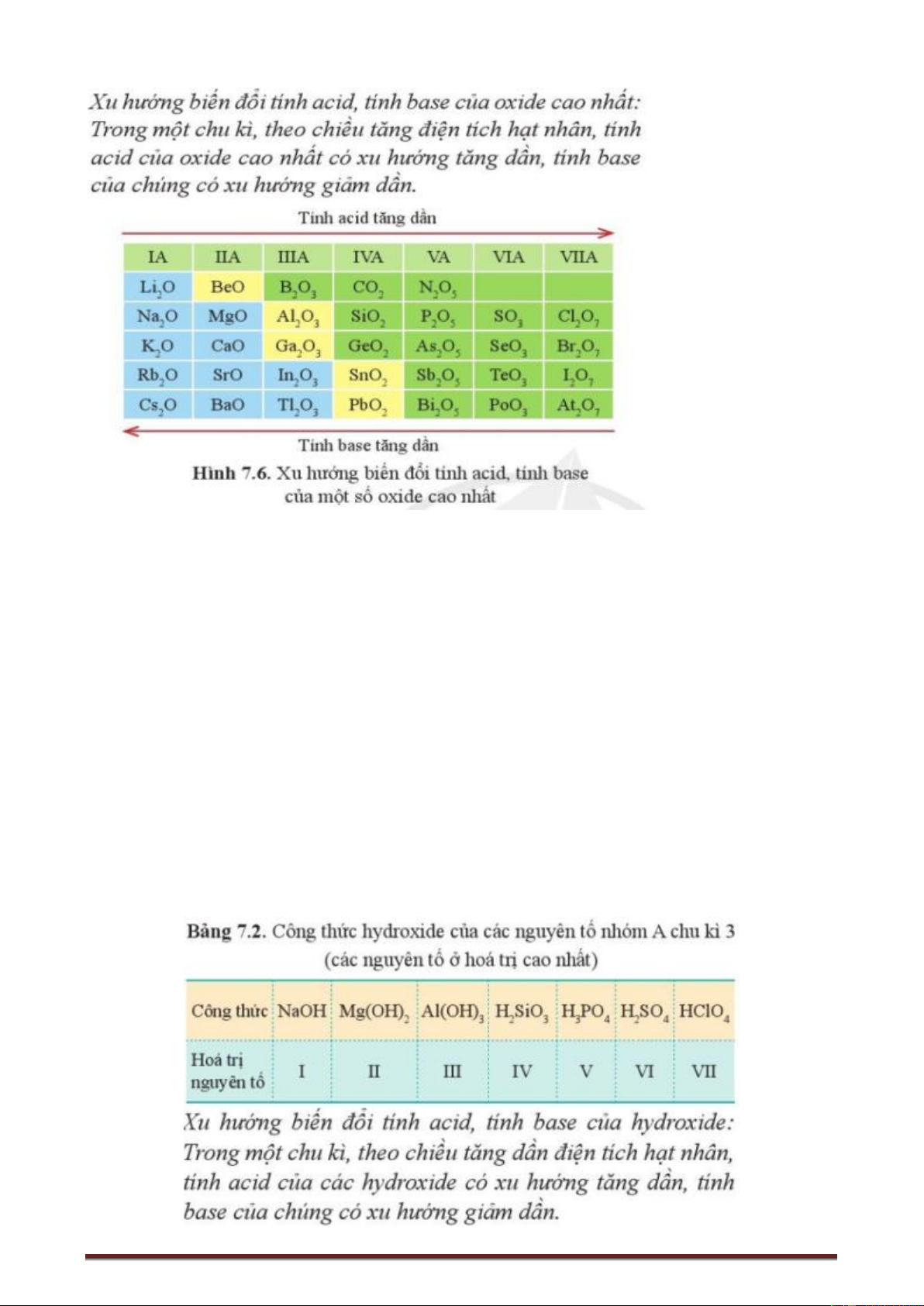
- Nhận xét được xu hướng biến đổi thành phần và tính acid, tính base của các oxide và các
hydroxide theo chu kì. Viết được phương trình hóa học minh họa. 2) Năng lực a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và
điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm
vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/nhóm, trách nhiệm của bản thân, đề
xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
- Năng lực giải quyết vấn đề và sáng tạo: đề xuất được một số giải thích về các hiện tượng xảy ra
trong tự nhiên về mặt hóa học.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học: hiểu được bản chất xu hướng biến đổi tính chất theo chu kì, nhóm.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: nhận biết được các nhóm chất có tính chất tương tự nhau.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được các hiện tượng hóa học xảy ra trong tự nhiên. 3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU Giáo viên Học sinh Bảng tuần hoàn Chuẩn bị bài ở nhà
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV trình bày vấn đề, HS lắng nghe.
c) Sản phẩm: HS biết được những vấn đề liên quan đến bài học mới.
d) Tổ chức thực hiện: GV yêu cầu HS đọc SGK và trả lời các câu hỏi trong SGK:
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Xu hướng biến đổi bán kính nguyên tử - Trong một chu kì
a) Mục tiêu: HS biết xu hướng biến đổi bán kính nguyên tử trong một chu kì.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được xu hướng biến đổi bán kính nguyên tử trong một chu kì.
Quy luật chung đối với các nguyên tố nhóm A: Trong một chu kì, theo chiều tăng dần điện tích
hạt nhân, bán kính các nguyên tử có xu hướng giảm dần.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 2: Xu hướng biến đổi bán kính nguyên tử - Trong một nhóm A
a) Mục tiêu: HS biết xu hướng biến đổi bán kính nguyên tử trong một nhóm A.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được xu hướng biến đổi bán kính nguyên tử trong một nhóm A.
Quy luật chung đối với các nguyên tố nhóm A: Trong một nhóm, theo chiều tăng điện tích hạt
nhân, bán kính của nguyên tử có xu hướng tăng dần.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
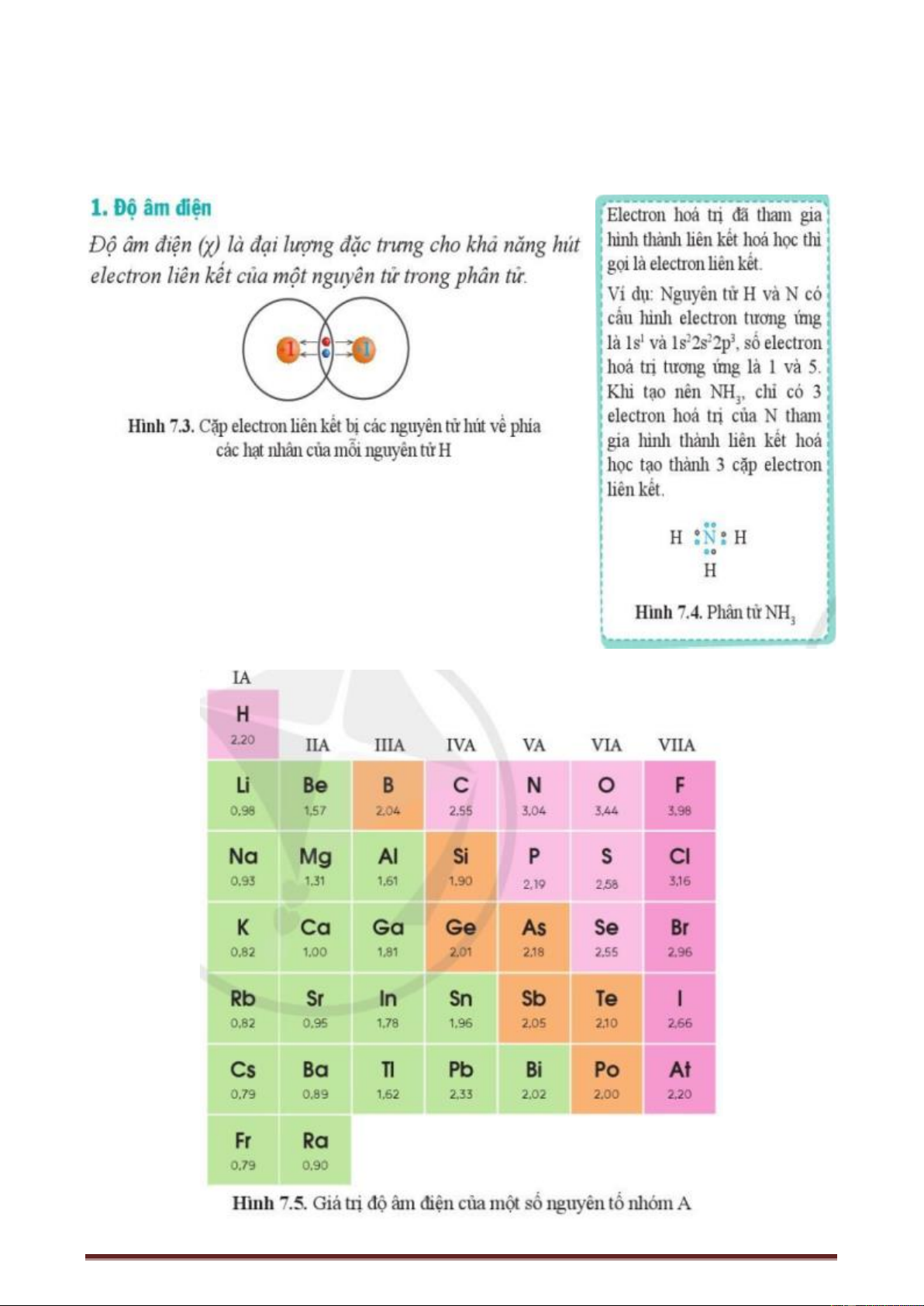
Hoạt động 3: Xu hướng biến đổi độ âm điện, tính kim loại, tính phi kim - Độ âm điện
a) Mục tiêu: HS biết khái niệm độ âm điện và xu hướng biến đổi theo chu kì, theo nhóm A.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được khái niệm độ âm điện và xu hướng biến đổi theo chu kì, theo nhóm A.
Quy luật chung đối với các nguyên tố nhóm A:
- Trong một chu kì, theo chiều tăng điện tích hạt nhân, độ
âm điện của các nguyên tử nguyên tố có xu hướng tăng dần.
- Trong một nhóm, theo chiều tăng điện tích hạt nhân, độ âm
điện của các nguyên tử nguyên tố có xu hướng giảm dần.
Độ âm điện cũng phụ thuộc điện tích hạt nhân và bán kính nguyên tử.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 4: Xu hướng biến đổi độ âm điện, tính kim loại, tính phi kim - Tính kim loại, tính phi kim
a) Mục tiêu: HS biết khái niệm tính kim loại và tính phi kim và xu hướng biến đổi theo chu kì, theo nhóm A.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được khái niệm tính kim loại và tính phi kim và xu hướng biến đổi theo chu kì, theo nhóm A.
- Tính kim loại đặc trưng bởi khả năng nhường electron của nguyên tử.
- Tính phi kim đặc trưng bởi khả năng nhận electron của nguyên tử.
Quy luật chung đối với các nguyên tố nhóm A:
- Trong một chu kì, theo chiều tăng điện tích hạt nhân, tính
kim loại của các nguyên tố có xu hướng giảm dần, tính phi
kim của các nguyên tố có xu hướng tăng dần.
- Trong một nhóm, theo chiều tăng điện tích hạt nhân, tính
kim loại của các nguyên tố có xu hướng tăng dần, tính phi
kim của các nguyên tố có xu hướng giảm dần.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 5: Xu hướng biến đổi thành phần và tính acid, tính base của các oxide và các
hydroxide theo chu kì - Thành phần và tính acid, tính base của các oxide cao nhất trong một chu kì
a) Mục tiêu: HS biết thành phần và tính acid, tính base của các oxide cao nhất trong một chu kì.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được thành phần và tính acid, tính base của các oxide cao nhất trong một chu kì.
Oxide cao nhất của một nguyên tố là oxide mà nguyên tố trong đó có hóa trị cao nhất. Các
nguyên tố thuộc nhóm IA đến VIIA (trừ fluorine) có hóa trị cao nhất đúng bằng số thứ tự của nhóm.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 6: Xu hướng biến đổi thành phần và tính acid, tính base của các oxide và các
hydroxide theo chu kì - Thành phần và tính acid, tính base của các hydroxide trong một chu kì
a) Mục tiêu: HS biết thành phần và tính acid, tính base của các hydroxide trong một chu kì.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được thành phần và tính acid, tính base của các hydroxide trong một chu kì.
Hydroxide của nguyên tố kim loại M hóa trị n có dạng M(OH)n.
Đối với nguyên tố phi kim, hydroxide của nó ở dạng acid.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu: Luyện tập, củng cố kiến thức đã học trong bài.
b) Nội dung: HS tổng kết kiến thức.
c) Sản phẩm: HS hệ thống hóa kiến thức trong bài học.
d) Tổ chức thực hiện: GV vấn đáp HS trả lời, gợi ý tổng kết.
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b) Nội dung: HS tìm hiểu ở nhà.
c) Sản phẩm: Kỹ năng khai thác và xử lý thông tin.
d) Tổ chức thực hiện:
GV yêu cầu HS: Tìm hiểu về mối liên hệ trong xu hướng biến đổi tính kim loại, tính phi kim với
các đại lượng: bán kính nguyên tử, độ âm điện, điện tích hạt nhân. BẢNG TUẦN HOÀN CHỦ ĐỀ 2
CÁC NGUYÊN TỐ HÓA HỌC
ĐỊNH LUẬT TUẦN HOÀN VÀ Ý NGHĨA CỦA BẢNG
TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
Thời gian thực hiện: 01 tiết I. MỤC TIÊU 1) Kiến thức
Học xong bài này, học sinh có thể:
- Phát biểu được định luật tuần hoàn các nguyên tố hóa học.
- Trình bày được ý nghĩa của bảng tuần hoàn các nguyên tố hóa học: Mối liên hệ giữa vị trí (trong
bảng tuần hoàn các nguyên tố hóa học) với tính chất và ngược lại. 2) Năng lực a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và
điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm
vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/nhóm, trách nhiệm của bản thân, đề
xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
- Năng lực giải quyết vấn đề và sáng tạo: đề xuất được một số giải thích về các hiện tượng xảy ra
trong tự nhiên về mặt hóa học.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học: hiểu được bản chất của định luật tuần hoàn.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: bản chất tuần hoàn của một số hiện
tượng hóa học xảy ra trong tự nhiên.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được các hiện tượng hóa học xảy ra trong tự nhiên. 3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU Giáo viên Học sinh Bảng tuần hoàn Chuẩn bị bài ở nhà
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV trình bày vấn đề, HS lắng nghe.
c) Sản phẩm: HS biết được những vấn đề liên quan đến bài học mới.
d) Tổ chức thực hiện: GV yêu cầu HS đọc SGK và trả lời các câu hỏi trong SGK:
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Định luật tuần hoàn các nguyên tố hóa học
a) Mục tiêu: HS biết định luật tuần hoàn các nguyên tố hóa học.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được định luật tuần hoàn các nguyên tố hóa học.
Tính chất của các nguyên tố và đơn chất cũng như thành phần và tính chất của hợp chất tạo nên tử
các nguyên tố đó biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 2: Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
a) Mục tiêu: HS biết ý nghĩa của bảng tuần hoàn các nguyên tố hóa học.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS áp dụng được ý nghĩa của bảng tuần hoàn các nguyên tố hóa học.
Khi biết vị trí của một nguyên tố trong bảng tuần hoàn, có thể đưa ra dự đoán về tính chất của đơn
chất cũng như hợp chất của nó.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu: Luyện tập, củng cố kiến thức đã học trong bài.
b) Nội dung: HS tự tổng kết kiến thức.
c) Sản phẩm: HS hệ thống hóa kiến thức trong bài học.
d) Tổ chức thực hiện: GV vấn đáp HS, gợi ý để tổng kết kiến thức.
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b) Nội dung: HS tìm hiểu ở nhà.
c) Sản phẩm: Kỹ năng khai thác, xử lý thông tin.
d) Tổ chức thực hiện:
GV yêu cầu HS: Vận dụng giải thích tính chất acid, tính chất base của oxide và hydroxide tương
ứng của các nguyên tố thuộc cùng chu kì 2. CHỦ ĐỀ 3 LIÊN KẾT HÓA HỌC QUY TẮC OCTET
Thời gian thực hiện: 01 tiết I. MỤC TIÊU 1) Kiến thức
Học xong bài này, học sinh có thể:
- Trình bày được quy tắc octet với các nguyên tố nhóm A.
- Vận dụng được quy tắc octet trong quá trình hình thành liên kết hóa học ở các nguyên tố nhóm A. 2) Năng lực a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và
điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm
vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/nhóm, trách nhiệm của bản thân, đề
xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
- Năng lực giải quyết vấn đề và sáng tạo: đề xuất được một số giải thích về các hiện tượng xảy ra
trong tự nhiên về mặt hóa học.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học: hiểu được bản chất của quy tắc octet.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: phân biệt được các hiện tượng hóa học
hay hiện tượng vật lý xảy ra trong tự nhiên.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được các hiện tượng hóa học xảy ra trong tự nhiên. 3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU Giáo viên Học sinh Tranh ảnh, mô hình Chuẩn bị bài ở nhà
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV trình bày vấn đề, HS lắng nghe.
c) Sản phẩm: HS biết được những vấn đề liên quan đến bài học mới.
d) Tổ chức thực hiện: GV yêu cầu HS đọc SGK và trả lời các câu hỏi trong SGK:
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Quy tắc octet
a) Mục tiêu: HS biết quy tắc octet.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được quy tắc octet.
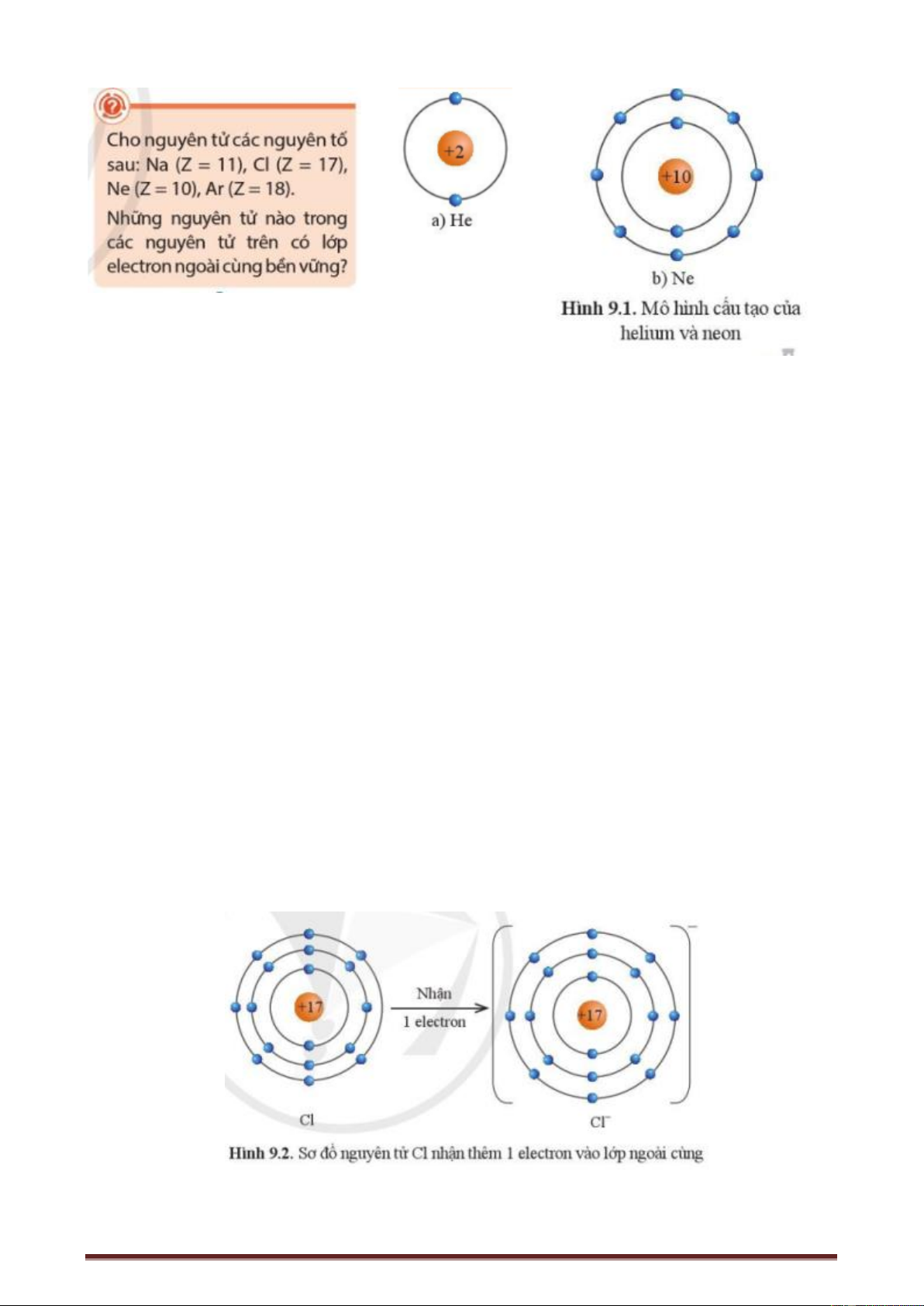
Trong phản ứng hóa học, các nguyên tử có xu hướng hình thành lớp vỏ bền vững như của khí hiếm.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 2: Vận dụng quy tắc octet trong quá trình hình thành liên kết hóa học của các nguyên tố nhóm A
a) Mục tiêu: HS biết cách vận dụng quy tắc octet.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS vận dụng được octet giải thích sự hình thành liên kết hóa học của một số nguyên tố thuộc nhóm A.
Trong quá trình hình thành liên kết hóa học, các nguyên tử có xu hướng nhường, nhận hoặc góp
chung electron để đạt được cấu hình bền vững như của khí hiếm với 8 electron ở lớp ngoài cùng
(hoặc 2 electrong ở lớp ngoài cùng như của helium). Ví dụ 1: Ví dụ 2: Ví dụ 3:
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu: Luyện tập, củng cố kiến thức đã học trong bài.
b) Nội dung: HS tự tổng kết kiến thức trong bài học.
c) Sản phẩm: HS tổng kết, hệ thống hóa kiến thức.
d) Tổ chức thực hiện: GV vấn đáp HS để dẫn dẵn HS tổng kết kiến thức.
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b) Nội dung: HS làm bài tập trong SGK trang 52.
c) Sản phẩm: Bài làm của HS, kỹ năng tính toán hóa học.
d) Tổ chức thực hiện: GV yêu cầu HS làm các bài tập trong SGK trang 52. CHỦ ĐỀ 3 LIÊN KẾT HÓA HỌC LIÊN KẾT ION
Thời gian thực hiện: 01 tiết I. MỤC TIÊU 1) Kiến thức
Học xong bài này, học sinh có thể:
- Trình bày được khái niệm và sự hình thành liên kết ion.
- Nêu được cấu tạo tinh thể NaCl. Giải thích được vì sao các hợp chất ion thường ở trạng thái rắn
trong điều kiện thường (dạng tinh thể ion).
- Lắp được mô hình tinh thể NaCl (theo mô hình có sẵn). 2) Năng lực a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và
điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm
vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/nhóm, trách nhiệm của bản thân, đề
xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
- Năng lực giải quyết vấn đề và sáng tạo: đề xuất được một số giải thích về các hiện tượng xảy ra
trong tự nhiên về mặt hóa học.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học: hiểu được bản chất của của liên kết ion.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: phân biệt được các hiện tượng hóa học
hay hiện tượng vật lý xảy ra trong tự nhiên.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được các hiện tượng hóa học xảy ra trong tự nhiên. 3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU Giáo viên Học sinh Tranh ảnh, mô hình Chuẩn bị bài ở nhà
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: GV trình bày vấn đề, HS lắng nghe.
c) Sản phẩm: HS biết được những vấn đề liên quan đến bài học mới.
d) Tổ chức thực hiện: GV yêu cầu HS đọc SGK và trả lời các câu hỏi trong SGK:
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Khái niệm và sự hình thành liên kết ion - Khái niệm
a) Mục tiêu: HS biết khái niệm liên kết ion.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS nêu được khái niệm liên kết ion.
Liên kết ion được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
Ví dụ: Liên kết ion trong hợp chất NaCl tạo bởi lực hút tĩnh điện giữa ion dương Na+ và ion âm Cl-: Na+ + Cl- → NaCl
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày, nêu ví dụ.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 2: Khái niệm và sự hình thành liên kết ion - Sự hình thành liên kết ion từ phản ứng giữa các nguyên tử
a) Mục tiêu: HS hiểu được quá trình hình thành liên kết ion.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS trình bày được sự hình thành liên kết ion.
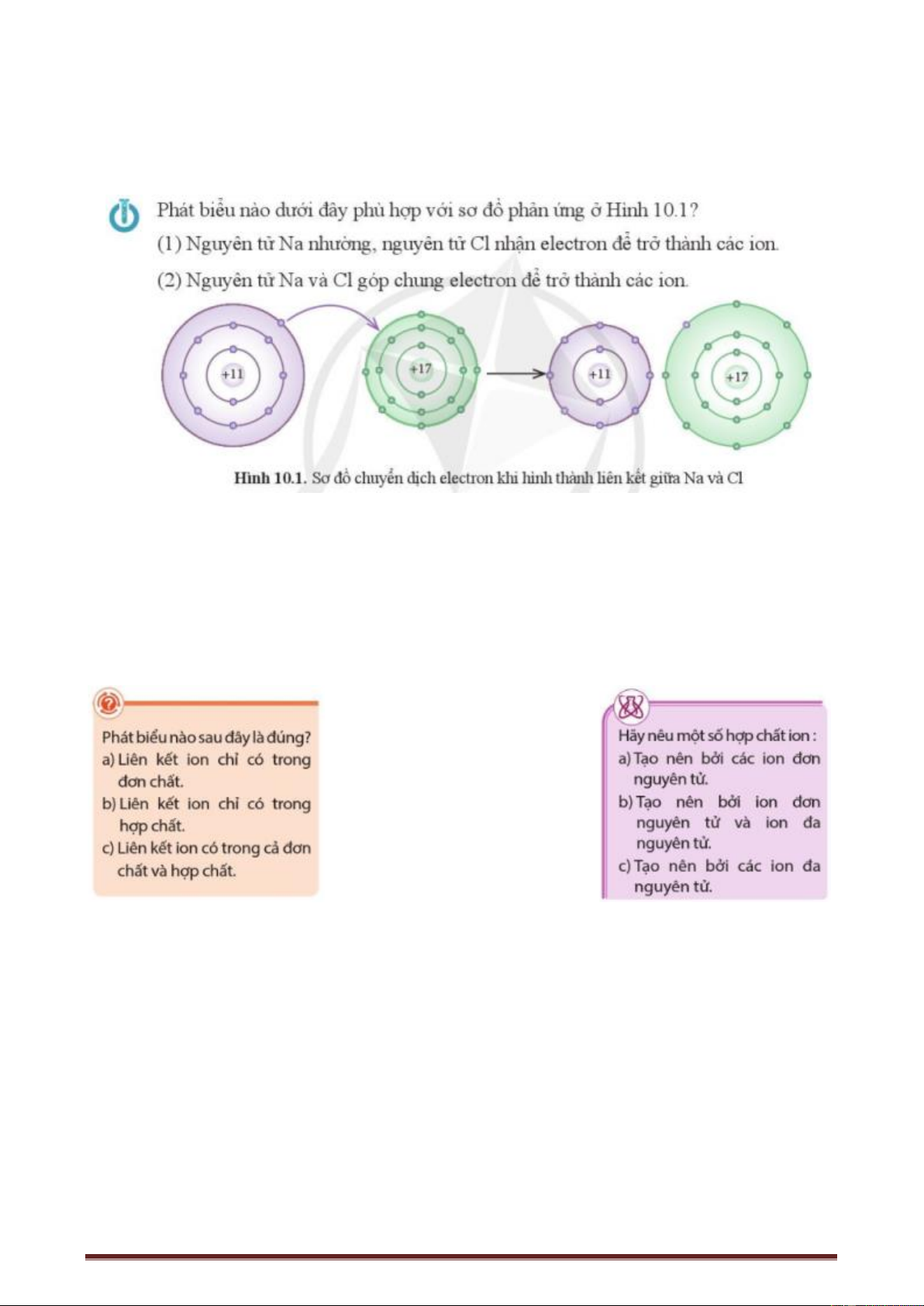
Quá trình hình thành liên kết ion như sau:
- Hình thành các ion trái dầu từ các quá trình nguyên tử kim loại nhường electron và nguyên tử
phi kim nhận electron theo quy tắc octet.
- Các ion trái dấu hút nhau bằng lực hút tĩnh điện tạo nên hợp chất ion. Các ion trái dấu kết hợp
với nhau theo tỉ lệ sao cho, tổng điện tích của các ion trong hợp chất phải bằng không.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 3: Tinh thể ion - khái niệm
a) Mục tiêu: HS biết khái niệm tinh thể ion.
b) Nội dung: HS đọc SGK.
(1) Lắp ráp mô hình tinh thể NaCl. Quan sát Hình 10.2b để lắp ráp mô hình tinh thể NaCl từ
các quả cầu minh họa cho ion Na+, Cl- và que nối.
(2) Từ mô hình NaCl, hãy cho biết xung quanh mỗi ion Na+ có bao nhiêu ion Cl- (ở gần nhất với Na+).
c) Sản phẩm: HS trình bày được khái niệm tinh thể ion.
Tinh thể ion là loại tinht hể được tạo nên bởi các cation và anion.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
Hoạt động 4: Tinh thể ion - Đặc điểm của hợp chất ion
a) Mục tiêu: HS biết đặc điểm của hợp chất ion.
b) Nội dung: HS đọc SGK.
c) Sản phẩm: HS trình bày được đặc điểm của hợp chất ion.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ
GV yêu cầu HS đọc SGK.
Bước 2: Thực hiện nhiệm vụ
HS đọc SGK; HS tự tóm tắt các nội dung chính.
Bước 3: Báo cáo kết quả
GV yêu cầu HS đứng tại chỗ trình bày.
GV yêu cầu HS khác nhận xét về câu trả lời.
Bước 4: Kết luận, nhận định
GV đánh giá, kết luận và chốt kiến thức và chuyển sang nội dung mới.
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu: Luyện tập, củng cố kiến thức đã học trong bài.
b) Nội dung: HS tự tổng kết kiến thức trong bài học.
c) Sản phẩm: HS tổng kết, hệ thống hóa kiến thức.
d) Tổ chức thực hiện: GV vấn đáp HS để dẫn dẵn HS tổng kết kiến thức.
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b) Nội dung: HS nuôi tinh thể NaCl.
c) Sản phẩm: Kỹ năng thực hành.
d) Tổ chức thực hiện: GV yêu cầu HS: Thực hành nuôi tinh thể NaCl.




