













Preview text:
Tính chất hóa học của Oxide Acid Base Muối
CHUYÊN ĐỀ KHOA HỌC TỰ NHIÊN 8
Tính chất hóa học của Oxide Acid Base Muối
A. Tóm tắt nội dung kiến thức trọng tâm
1. Tính chất hóa học của acid, base Acid Base Chất chỉ thị
Đổi màu quỳ tím → đỏ
đổi màu quỳ tím → xanh
Đổi màu dung dịch phenolphatalein từ
không màu thành màu hồng Tác dụng với kim loại Acid (HCl và H 2 SO 4 loãng) +
kim loại (đứng trước H trong
dãy hoạt động hóa học) → muối + H 2 Fe + 2HCl → FeCl 2 + H 2
Một số nguyên tố lưỡng tính như Zn, Al, Cr, … 2Al + 2NaOH + 2H 2 O → 2NaAlO 2 + 3H 2 Tác dụng với base
Base + acid → muối + nước NaOH + HCl → NaCl + H 2 O
Một số base lưỡng tính (Zn(OH) 2 , Al(OH) 3 , …) + dung dịch kiềm Al(OH) 3 + NaOH → NaAlO 2 + 2H 2 O Tác dụng với acid/base
Base + acid → muối + nước H 2 SO 4 + NaOH → Na 2 SO 4 + H 2 O Tác dụng với oxide acid Không phản ứng
Base + oxide acid → muối acid hoặc muối trung hòa + nước SO 2 + NaOH → Na 2 SO 3 + H 2 O SO 2 + NaOH → Na 2 HSO 3 + H 2 O Tác dụng với oxide base
Acid + oxide base → muối + nước CaO + H 2 SO 4 → CaSO 4 + H 2 O
Một số oxide lưỡng tính như ZnO, Al 2 O 3 , Cr 2 O 3
,… tác dụng với dung dịch base Tác dụng với muối
Acid + muối → muối mới + acid mới HCl + AgNO 3 → AgCl + HNO 3
Base + muối → Base mới + muối mới KOH + CuSO 4 → K 2 SO 4 + Cu(OH) 2 Phản ứng nhiệt phân Một số acid o t oxide acid + nước H 2 SO 4 o t SO 3 + H 2 O Base không tan o t oxide base + nước Cu(OH) 2 o t CuO + H 2 O
2. Tính chất hóa học của oxide Oxide acid Oxide base Tác dụng với nước Một số oxide acid + H 2 O →
dung dịch axit (đổi màu quỳ tím → đỏ) CO 2 + H 2 O → H 2 CO 3
Oxide acid tác dụng được với nước: SO 2 , SO 3 , N 2 O 5 , P 2 O 5 …
Không tác dụng với nước: SiO 2 ,… Một số oxide base + H 2 O → dung
dịch kiềm (đổi màu quỳ tím → xanh) CaO + H 2 O → Ca(OH) 2
Oxide base tác dụng được với nước: Na 2 O, K 2 O, BaO,..
Không tác dụng với nước: FeO, CuO, Fe 2 O 3 ,… Tác dụng với acid Không phản ứng
Acid + Oxide base → muối + H 2 O FeO + H 2 SO 4 (loãng) → FeSO 4 + H 2 O Tác dụng base kiềm Base + Oxide acid → muối
(muối trung hòa, hoặc axit) + H 2 O CO 2 + 2NaOH → Na 2 CO 3 + H 2 O CO 2 + NaOH → NaHCO 3 Không phản ứng Tác dụng oxide acid Không phản ứng
Oxide acid + Oxide base (tan) → muối CaO + CO 2 → CaCO 3 Tác dụng oxide base
Oxide acid + Oxide base (tan) → muối MgO + SO 3 → MgSO 4 Không phản ứng Oxie lưỡng tính (ZnO, Al 2 O 3 , Cr 2 O 3 )
Oxide trung tính (oxide không tạo muối) NO, CO,… Tác dụng với nước Không phản ứng Không phản ứng Tác dụng với acid Al 2 O 3 + 6HCl → 2AlCl 3 + 3H 2 O Không phản ứng Tác dụng với base Al 2 O 3 + 2NaOH → 2NaAlO 2 + 3H 2 O Không phản ứng Phản ứng oxi hóa khử Không phản ứng
Tham gia phản ứng oxi hóa khử 2NO + O 2 o t 2NO 2
3. Tính chất hóa học của muối Tính chất hóa học Muối Tác dụng với kim loại
Kim loại + muối → muối mới + kim loại mới Cu + 2AgNO 3 → Cu(NO 3 ) 2 + 2Ag
Điều kiện: Kim loại đứng trước (trừ Na, K, Ca,…) đẩy kim loại đứng
sau (trong dãy hoạt động hóa học) ra khỏi dung dịch muối của chúng.
Kim loại Na, K, Ca… khi tác dụng với dung dịch muối thì không cho kim loại mới vì: Na + CuSO 4 → 2Na + H 2 O → NaOH + H 2 CuSO 4 + 2NaOH → Cu(OH) 2 ↓+ Na 2 SO 4 Tác dụng với base
Muối + base → muối mới + base mới FeCl 3 + 3NaOH → Fe(OH) 3 + 3NaCl Tác dụng với acid
Muối + acid → muối mới + acid mới BaCl 2 + AgNO 3 → Ba(NO 3 ) 2 + AgCl Tác dụng với muối
Muối + muối → 2 muối mới BaCl 2 + Na 2 SO 4 → BaSO 4 + NaCl Nhiệt phân muối
Một số muối bị nhiệt phân hủy ở nhiệt độ cao CaCO 3 o t CaO + CO 2 2KMnO 4 o t K 2 MnO 4 + MnO 2 + O 2
Mối quan hệ giữa các hợp chất vô cơ
Bảng tính tan trong nước của một số chất Nhóm Hydrogen và các kim loại 3/11Xem thêm
Tính chất hóa học của oxide acid base muối
Tính chất hóa học của Oxide Acid Base Muối giúp các bạn hệ thống lại kiến thức được
học về tính chất hóa học của oxide, acid, base và muối, dễ dàng ghi nhớ các tính chất
hóa học, cũng như so sánh đối chiếu tính chất hóa học của các chất.
A. Tóm tắt nội dung kiến thức trọng tâm
1. Tính chất hóa học của Acid - Base Acid Base
Chất chỉ thị Đổi màu quỳ tím → đỏ
đổi màu quỳ tím → xanh
Đổi màu dung dịch phenolphatalein từ không màu thành màu hồng
Tác dụng với Acid (HCl và H
Một số nguyên tố lưỡng tính như Zn, Al, Cr, …
2SO4 loãng) + kim loại (đứng kim loại
trước H trong dãy hoạt động hóa học) → muối 2Al + 2NaOH + 2H O → 2NaAlO 2 2 + 3H2 + H2 Fe + 2HCl → FeCl2 + H2
Tác dụng với Base + acid → muối + nước
Một số base lưỡng tính (Zn(OH) , …) + dung dịch 2, Al(OH)3 base NaOH + HCl → NaCl + H kiềm 2O
Al(OH)3 + NaOH → NaAlO2 + 2H2O Tác dụng với
Base + acid → muối + nước acid/base H2SO4 + NaOH → Na2SO4 + H2O
Tác dụng với Không phản ứng
Base + oxide acid → muối acid hoặc muối trung hòa + nước oxide acid SO2 + NaOH → Na2SO3 + H2O SO2 + NaOH → Na2HSO3 + H2O
Tác dụng với Acid + oxide base → muối + nước
Một số oxide lưỡng tính như ZnO, Al ,… tác dụng 2O3, Cr2O3 oxide base CaO + H với dung dịch base 2SO4 → CaSO4 + H2O
Tác dụng với Acid + muối → muối mới + acid mới
Base + muối → Base mới + muối mới muối HCl + AgNO3 → AgCl + HNO3
KOH + CuSO4 → K2SO4 + Cu(OH)2
Phản ứng Một số acid oxide acid + nước
Base không tan oxide base + nước
nhiệt phân H2SO4 →toSO3 + H2O Cu(OH)2 →to CuO + H2O
2. Tính chất hóa học của oxide Oxide acid Oxide base Tác dụng với
Một số oxide acid + H O → dung dịch acid (đổi
Một số oxide base + H O → dung dịch kiềm (đổi màu 2 2 nước màu quỳ tím → đỏ) quỳ tím → xanh) CO O → H O → Ca(OH) 2 + H2 2CO3 CaO + H2 2
Oxide acid tác dụng được với nước: SO
Oxide base tác dụng được với nước: Na 2, SO3, 2O, K2O, BaO,.. N …
Không tác dụng với nước: FeO, CuO, Fe ,… 2O5, P2O5 2O3
Không tác dụng với nước: SiO ,… 2 Tác dụng với Không phản ứng
Acid + Oxide base → muối + H2O acid
FeO + H2SO4 (loãng) → FeSO4 + H2O
Tác dụng base Base + Oxide acid → muối (muối trung hòa, hoặc Không phản ứng kiềm acid) + H2O CO2 + 2NaOH → Na2CO3 + H2O CO2 + NaOH → NaHCO3 Tác dụng Không phản ứng
Oxide acid + Oxide base (tan) → muối oxide acid CaO + CO2 → CaCO3 Tác dụng
Oxide acid + Oxide base (tan) → muối Không phản ứng oxide base MgO + SO3 → MgSO4 Oxie lưỡng tính
Oxide trung tính (oxide không tạo muối) (ZnO, Al2O3, Cr2O3) NO, CO,…
Tác dụng với nước Không phản ứng Không phản ứng
Tác dụng với acid Al2O3 + 6HCl → 2AlCl3 + 3H2O Không phản ứng
Tác dụng với base Al2O3 + 2NaOH → 2NaAlO2 + 3H2O Không phản ứng
Phản ứng oxi hóa Không phản ứng
Tham gia phản ứng oxi hóa khử khử 2NO + O2 →to 2NO2
3. Tính chất hóa học của muối
Tính chất hóa học Muối
Tác dụng với kim loại Kim loại + muối → muối mới + kim loại mới
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Điều kiện: Kim loại đứng trước (trừ Na, K, Ca,…) đẩy kim loại đứng sau (trong dãy hoạt động hóa
học) ra khỏi dung dịch muối của chúng.
Kim loại Na, K, Ca… khi tác dụng với dung dịch muối thì không cho kim loại mới vì: Na + CuSO O → NaOH + H 4 → 2Na + H2 2
CuSO4 + 2NaOH → Cu(OH)2 ↓+ Na2SO4 Tác dụng với base
Muối + base → muối mới + base mới
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl Tác dụng với acid
Muối + acid → muối mới + acid mới
BaCl2 + AgNO3 → Ba(NO3)2 + AgCl
Tác dụng với muối
Muối + muối → 2 muối mới
BaCl2 + Na2SO4 → BaSO4 + NaCl Nhiệt phân muối
Một số muối bị nhiệt phân hủy ở nhiệt độ cao CaCO3 →toCaO + CO2 2KMnO4 →to K2MnO4 + MnO2 + O2
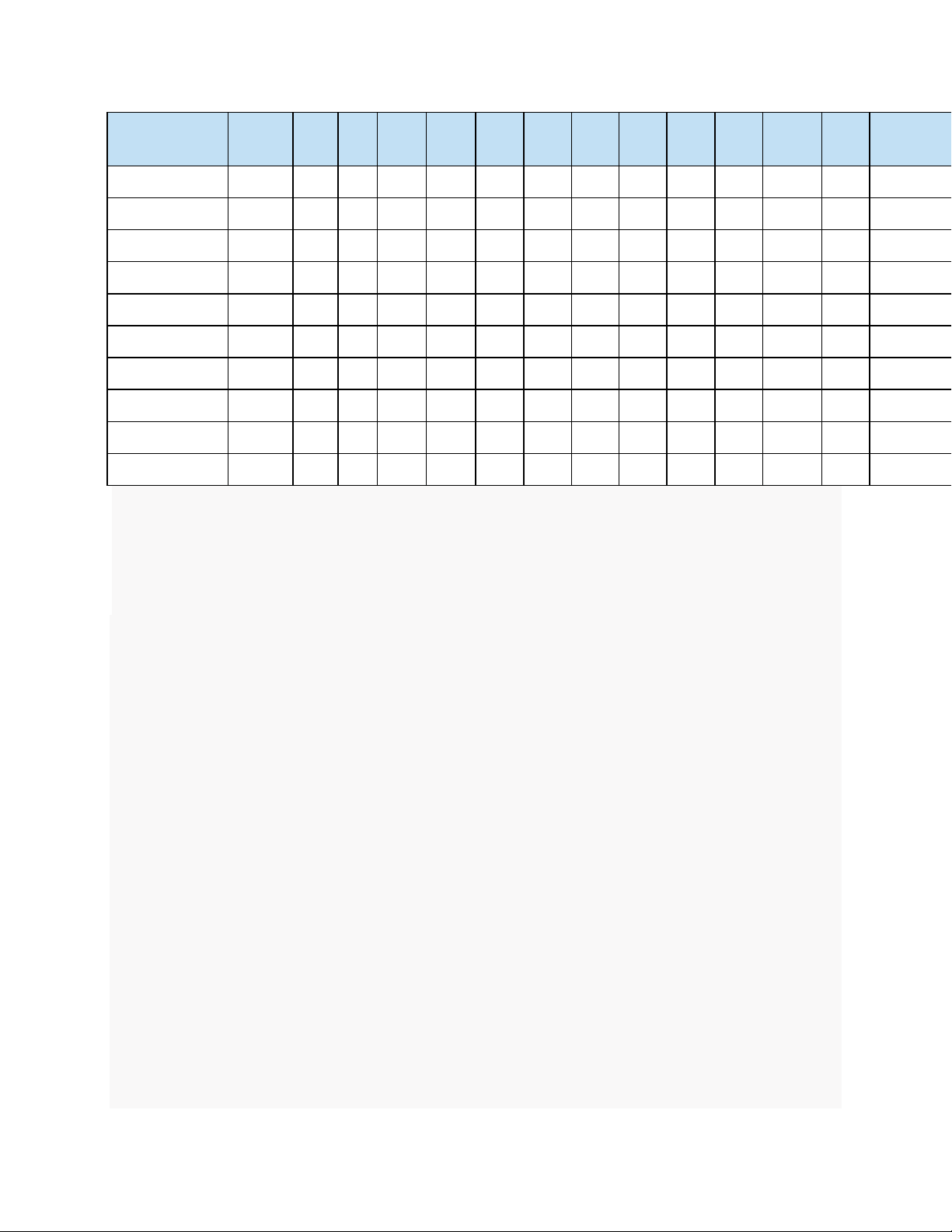
Bảng tính tan trong nước của một số chất Nhóm
Hydrogen và các kim loại hydroxide và H K Na Ag Mg Ca Ba Zn Hg Pb Cu Fe Fe Al gốc acid I I I I II II II II II II II II III III –OH T/B T T – K I K K – K K K K K –Cl T/B T T K T T T T T I T T T T –NO3 T/B T T T T T T T T T T T T T CH3COO- T/B T T T T T T T T T T T – I =S T/B T T T – T T K K K K K K – =SO3 T/B T T T K K K K K K K K – – =SO4 T/Kb T T I K I K T – K T T T T =CO3 T/B T T K K K K K – K – K – – =SiO3 K/Kb T T – K K K K – K – K K K ≡PO4 T/Kb T T T K K K K K K K K K K
T: Hợp chất dễ tan trong nước I: Hợp chất ít tan
K: Hợp chất thực tế không tan
"–": Hợp chất không tồn tại hoặc bị phân hủy trong nước
B: Hợp chất bay hơi hoặc dễ phân hủy thành khí bay lên
Kb: Hợp chất không bay hơi
B. Bài tập vận dụng liên quan 1. Câu hỏi tự luận
Câu 1. Có các oxide sau: CaO, Al2O3, Fe2O3, P2O5, CuO, SO3, CO2. Oxide nào có thể tác dụng được với: a) Nước b) Hydrochloric acid c) Sodium hydroxide
Câu 2. Tìm các chất kí hiệu bằng chữ cái trong sơ đồ sau và hoàn thành sơ đồ bằng phương trình phản ứng:
a) FeS2 → M → N → D → CuSO4
b) CuSO4 → B → C → D → Cu
Câu 3. Viết các phương trình phản ứng theo sơ đồ chuyển hóa sau:
a) Ca → CaO → Ca(OH)2 → CaCl2 → CaCO3
b) CaCO3 → CO2 → NaHCO3 → Na2CO3 → Na2SO4
c) Al → Al2O3 → NaAlO2 → Al(OH)3→ Al2(SO4)3 → AlCl3→ Al(NO3)3
2. Câu hỏi trắc nghiệm
Câu 1. Dung dịch H2SO4 tác dụng với dãy chất là: A. Fe, CaO, HCl. B.Cu, BaO, NaOH. C. Mg, CuO, HCl. D. Zn, BaO, NaOH.
Câu 2. Để phân biệt 2 dung dịch HCl và H2SO4. Người ta dùng thuốc thử là: A. Quỳ tím . B. Zn. C. dung dịch NaOH. D. dung dịch BaCl2.
Câu 3. Chất gây ô nhiễm và mưa acid là A. Khí O2. B. Khí SO2. C. Khí N2. D. Khí H2.
Câu 4. Cặp chất tạo ra chất kết tủa trắng là A. CuO và H2SO4. B. ZnO và HCl. C. NaOH và HNO3. D. BaCl2 và H2SO4
Câu 5. Các khí ẩm được làm khô bằng CaO là: A. H2; O2; N2 . B. H2; CO2; N2. C. H2; O2; SO2. D. CO2; SO2; HCl.
C. Đáp án bài tập vận dụng liên quan 1. Câu hỏi tự luận Câu 1. a) Tác dụng với H2O CaO + H2O → Ca(OH)2 P2O5 + H2O → H3PO4 SO3 + H2O → H2SO4 CO2 + H2O → CaCO3 b) Tác dụng HCl CaO + 2HCl → CaCl2 + H2O Al2O3+ 6HCl → 2AlCl3 + 3H2O
Fe2O3 + 6HCl → 2FeCl3 + 3H2O CuO + 2HCl → CuCl2 + H2O c) Tác dụng NaOH
2P2O5 + 3NaOH → Na3PO4 + H2O SO3 + 2NaOH → Na2SO3 + H2O CO2 + 2NaOH → Na2CO3 + H2O Câu 2.
a) FeS2 → M → N → D → CuSO4 FeS2 + O2 → SO2 + Fe2O3 SO2+ O2→ SO3 SO3 + H2O → H2SO4
H2SO4 + Cu(OH)2 → CuSO4+ H2O
b) CuSO4 → B → C → D → Cu
CuSO4 + NaOH → Cu(OH)2 + Na2SO4 Cu(OH)2 → CuO + H2O CuO + H2 → Cu + H2O Câu 3.
a) Ca → CaO → Ca(OH)2 → CaCl2 → CaCO3 1) 2Ca + O2→ 2CaO 2) CaO + H2O →Ca(OH)2
3) Ca(OH)2 + HCl → CaCl2 + H2O
4) CaCl2 + H2CO3 → CaCO3+ HCl
b) CaCO3 → CO2 → NaHCO3 → Na2CO3 → Na2SO4 (1)CaCO3 →toCaO + CO2 (2) CO2+ NaOH → NaHCO3
(3) NaHCO3 + NaOH → Na2CO3 + H2O
(4) Na2CO3 + H2SO4 → Na2CO3 + CO2 + H2O
c) Al → Al2O3 → NaAlO2 → Al(OH)3 → Al2(SO4)3 → AlCl3→ Al(NO3)3 1) 4Al + 3O2 → 2Al2O3
2) Al2O3+ 2NaOH → 2NaAlO2 + H2O
3) NaAlO2 + 2H2O → NaOH + Al(OH)3
4) 2Al(OH)3 + 3ZnSO4→ Al2(SO4)3 + 3Zn(OH)2
5) Al2(SO4)3 + 3BaCl2 → 2AlCl3 + 3BaSO4
6) AlCl3 + 3AgNO3 → Al(NO3)3+ 3AgCl Câu 4. SO3+ Na2O → Na2SO4 SO3+ BaO → BaSO4 SO3 + 2KOH → K2SO4 + H2O CO2 + Na2O → Na2CO3 CO2 + BaO → BaCO3 CO2 + 2KOH → K2CO3+ H2O Na2O + H2SO4→ Na2SO4 + H2O BaO + H2SO4 → BaSO4 + H2O KOH + H2SO4→ K2SO4 + H2O
Fe2O3 + 3H2SO4 → Fe2(SO4)3+ 3H2O