Preview text:
Tổng hợp nhiều thứ của Hóa Hữu Cơ
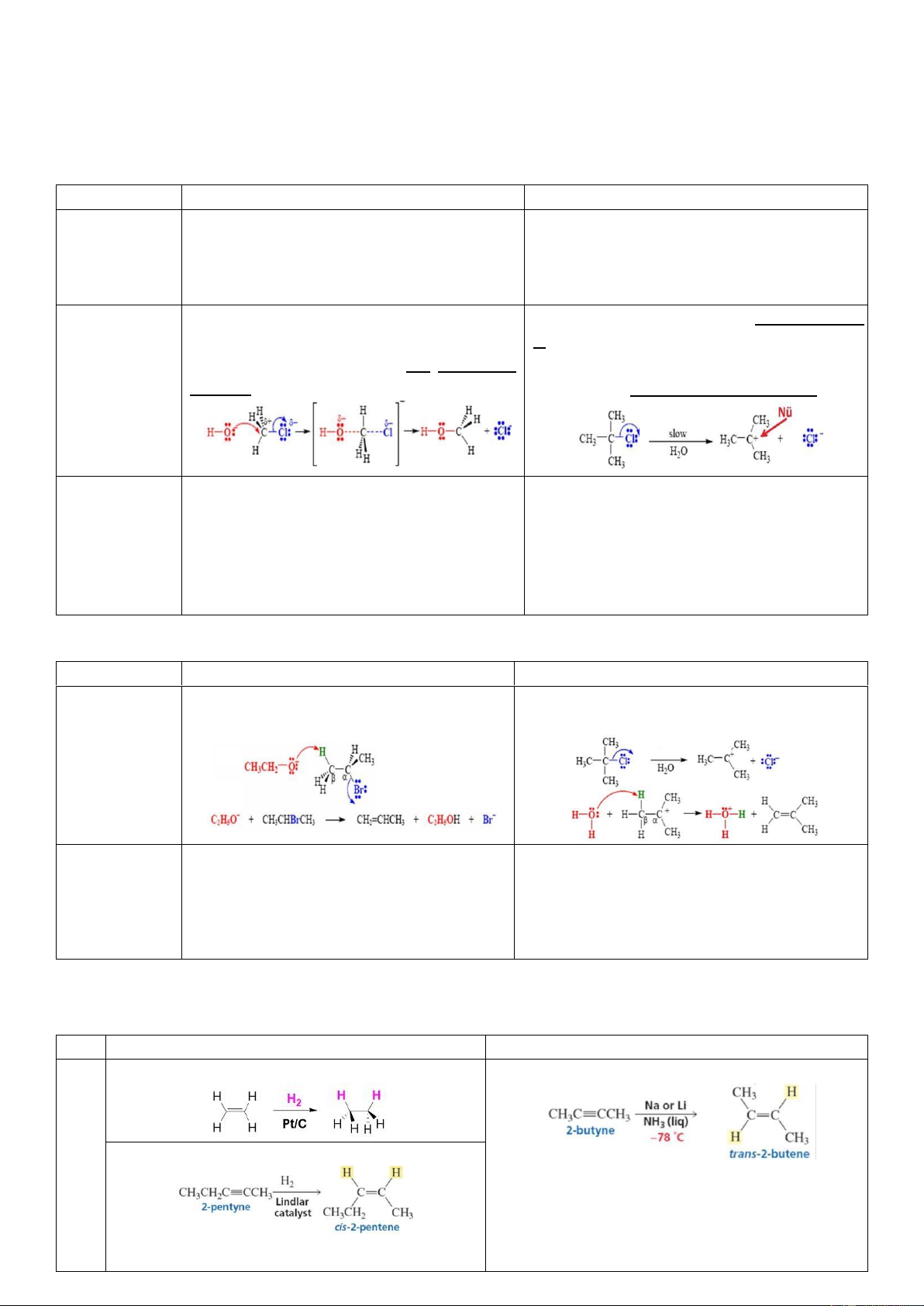
1. Phản ứng thế SN2 và SN1
Đề bài có thể cho biết trước ó là phản ứng SN2 hoặc SN1 hoặc không. Nếu không cho và không biết thì chúc may mắn. Đặc iểm SN2 SN1 Dấu hiệu
+ Dung môi không phân cực (DMSO,
+ Dung môi phân cực (H2O, alcohol, H+,...) DMF,...)
+ Dễ xảy ra với C bậc cao
+ Dễ xảy ra với C bậc thấp
(Tham khảo slide, giáo trình thêm)
(Tham khảo slide, giáo trình thêm) Cơ chế
Bước 1: Gắn Nucleophile vào vị trí thế Bước 1: Tạo carbocation và có thể chuyển
nhưng ở ối phía với nhóm ược thế Bước 2: vị
Tách nhóm ược thế ra → tạo thành sản Bước 2: Gắn Nucleophile vào carbocation ở phẩm ối
cả 2 phía → tạo hai sản phẩm lập thể Một số phản
+ Alcohol tác dụng SOCl2, pyridine
+ Alcohol tác dụng HX thành alkyl halide
ứng tiêu biểu + Alcohol tác dụng PBr3 hoặc PCl3
+ Muối carboxylate tác dụng RX tạo thành ester
+ Muối phenolate tác dụng RX tạo ether có nối mạch vòng
2. Phản ứng tách E2 và E1
Phản ứng tách trong môi trường base (kiềm, alcohol, muối alcoholate như RONa) ể tạo nối ôi. Đặc iểm E2 E1 Cơ chế
Tách hai nhóm ở trái phía với nhau (ở vị Tạo carbocation và có thể chuyển vị trước khi trí anti) tách thành nối ôi Sản phẩm
Sản phầm chính là alkene bền hơn và ưu Sản phẩm chính là alkene bền hơn ( ồng tiên liên hợp
phân trans) và ưu tiên liên hợp. Nếu phản
ứng tách trong trường hợp alcohol hay muối
alcoholate cồng kềnh (4C trở lên) thì tạo nối ôi ầu mạch.
Đề bài thường sẽ cho biết trước là phản ứng E2 hay E1 hoặc không. Nếu
không cho và không biết thì chúc may mắn.
3. Một số phản ứng dạng syn và anti STT Kiểu syn Kiểu anti 1.
Alkene với H2, Pt/C hoặc Pd/C, Ni
Alkyne với Na hoặc Li, NH3 liquid, -78oC
Alkyne với H2, Lindlar catalyst 2.
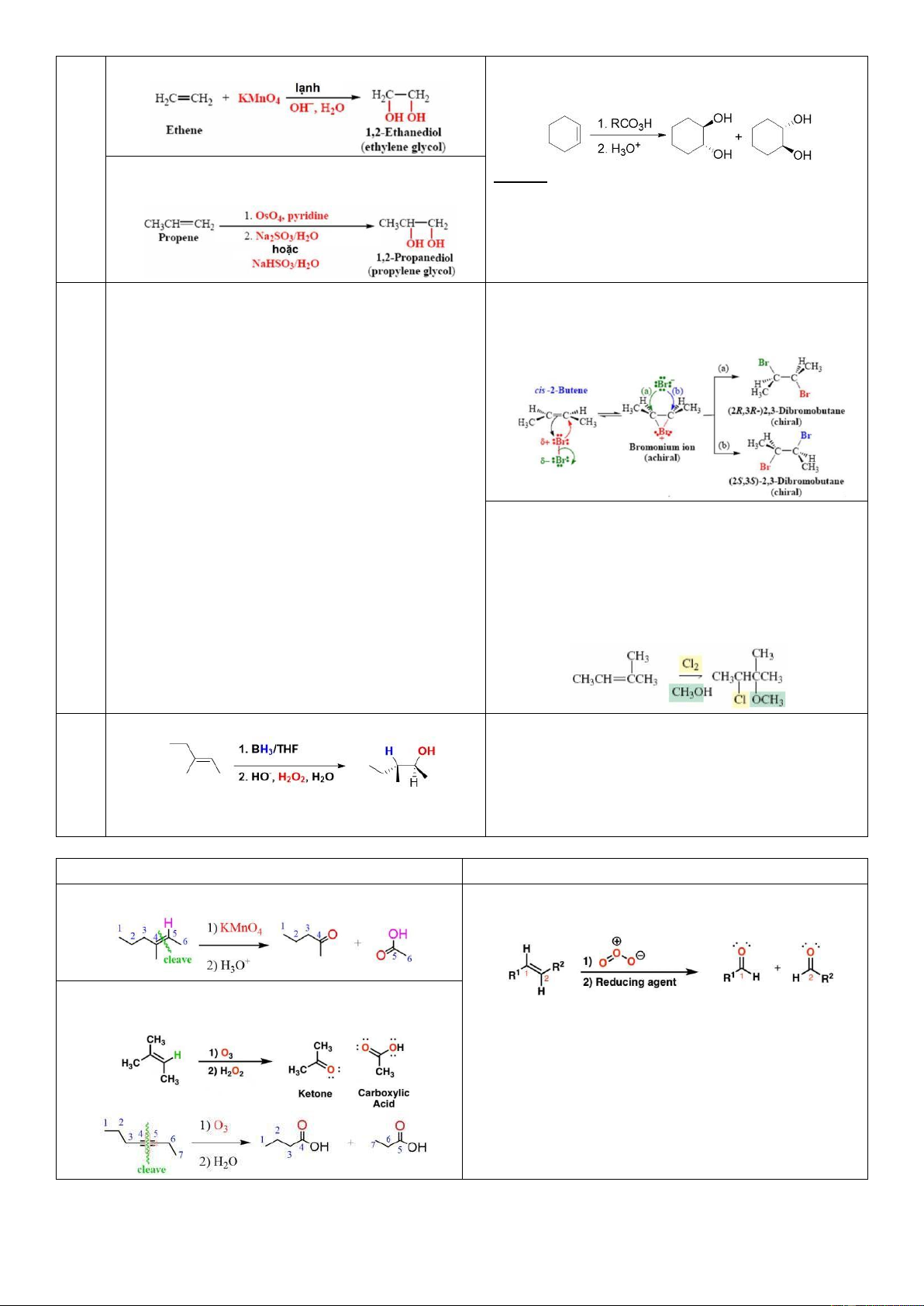
Alkene với KMnO4, cold, OH–, H2O
Alkene với 1. RCO3H hoặc mCPBA 2. HA, H2O
Alkene với 1. OsO4, pyridine
Lưu ý: Nếu không có HA, H2O thì phản ứng chỉ 2. Na2SO3 hoặc NaHSO3/H2O tạo ra epoxy 3.
Alkene/Alkyne với X2 (các halogen )/dung môi trơ (CH2Cl2 hoặc CCl4)
Tạo cặp ồng phân ối quang
Alkene/Alkyne với X2 (các halogen )/dung môi
phân cực (H2O hoặc CH3OH, NaCl,...)
Tạo cặp ồng phân ối quang
(Giống với phản ứng ở trên nhưng X gắn với vị
trí C bậc thấp hơn còn anion từ dung môi sẽ gắn với C bậc cao) 4. Alkene với BH3/THF
(Có thể thay BH3 bằng alkylborane hoặc disiamyl borane)
4. Phản ứng cắt mạch nối ôi
Tạo acid (CO2 nếu chỉ có 1C), ketone
Tạo aldehyde, ketone
KMnO4, to/H+ hoặc K2Cr2O7/H+ 1. O3, CH2Cl2
2. Zn/CH3COOH, H2O hoặc (CH3)2S (DMS) 1. O3
2. H2O2 (alkene) hoặc H2O (alkyne)
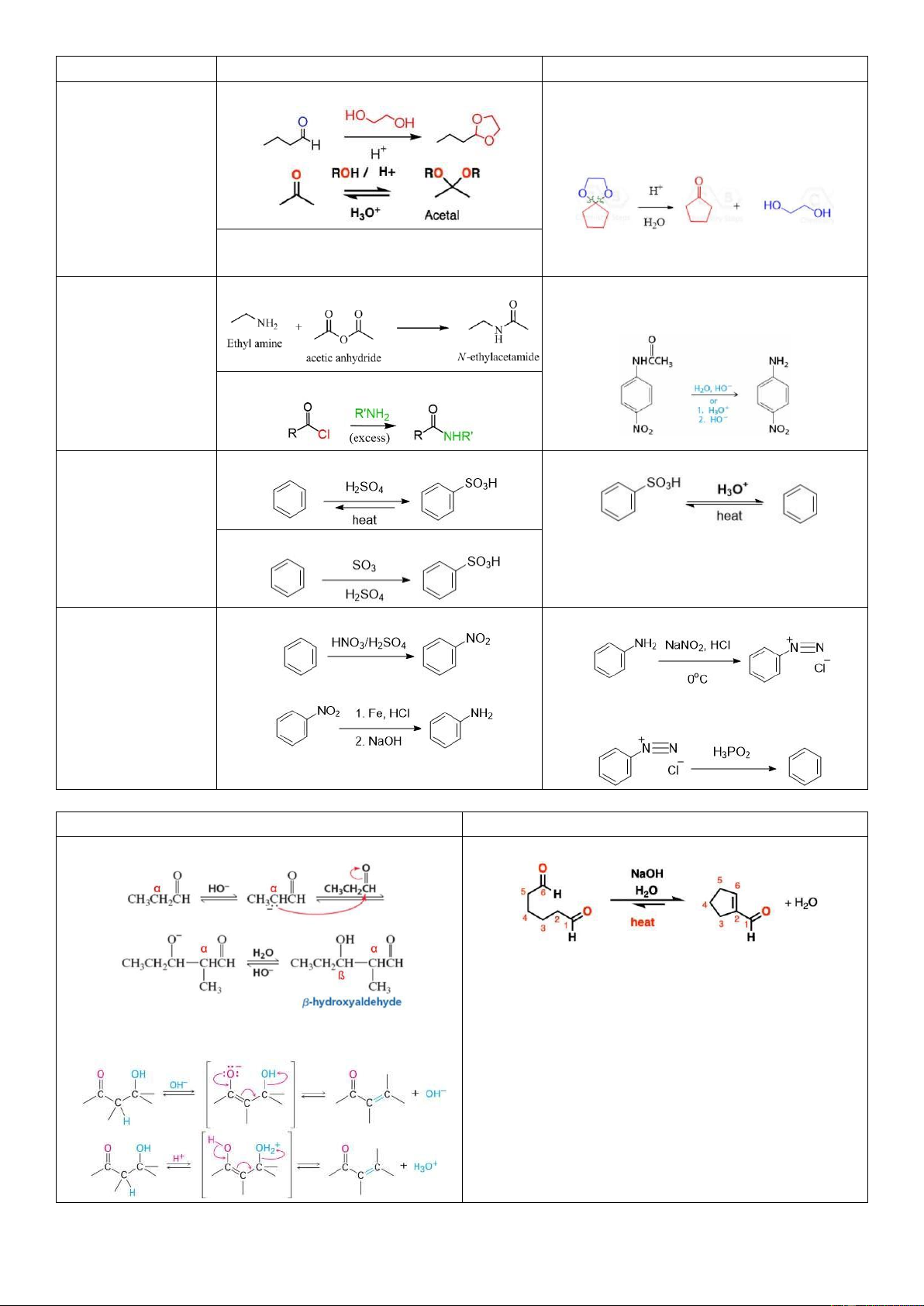
5. Một số cách bảo vệ nhóm chức Nhóm chức Bảo vệ Chuyển lại Aldehyde/Ketone
Diol (Vd: HO-[CH2]2-OH) hoặc alcohol, H+ (Cách chuyển giống nhau) H+, H2O hoặc H3O+
Tương tự với dithiol (Vd: HS-[CH2]3-SH) hoặc thiol, H+ Amine Acid anhydride, pyridine (Cách chuyển giống nhau)
H2O, HO– hoặc 1. H3O+, 2. HO– Acyl chlodride
Thêm và loại bỏ H2SO4, heat Khử i bằng acid, heat SO3H ở benzene SO3/H2SO4 fuming
Thêm và loại bỏ + Benzene tác dụng HNO3/H2SO4 ( ặc)
+ Chuyển thành muối diazonium NH2 ở benzene + Khử NO 2 thành NH2 + Khử i bằng H3PO2
(hoặc NaBH4 hoặc C2H5OH ngậm nước)
(Có thể thay bằng H2/Pd; Sn/HCl, NaOH)
6. Phản ứng Aldol hóa Giữa 2 phân tử Nội phân tử
Phản ứng của ketone chậm hơn aldehyde
Ưu tiên tạo thành vòng 5-6 cạnh
Sản phẩm aldol dễ tách nước ở iều kiện phản ứng
cũng như trong môi trường acid
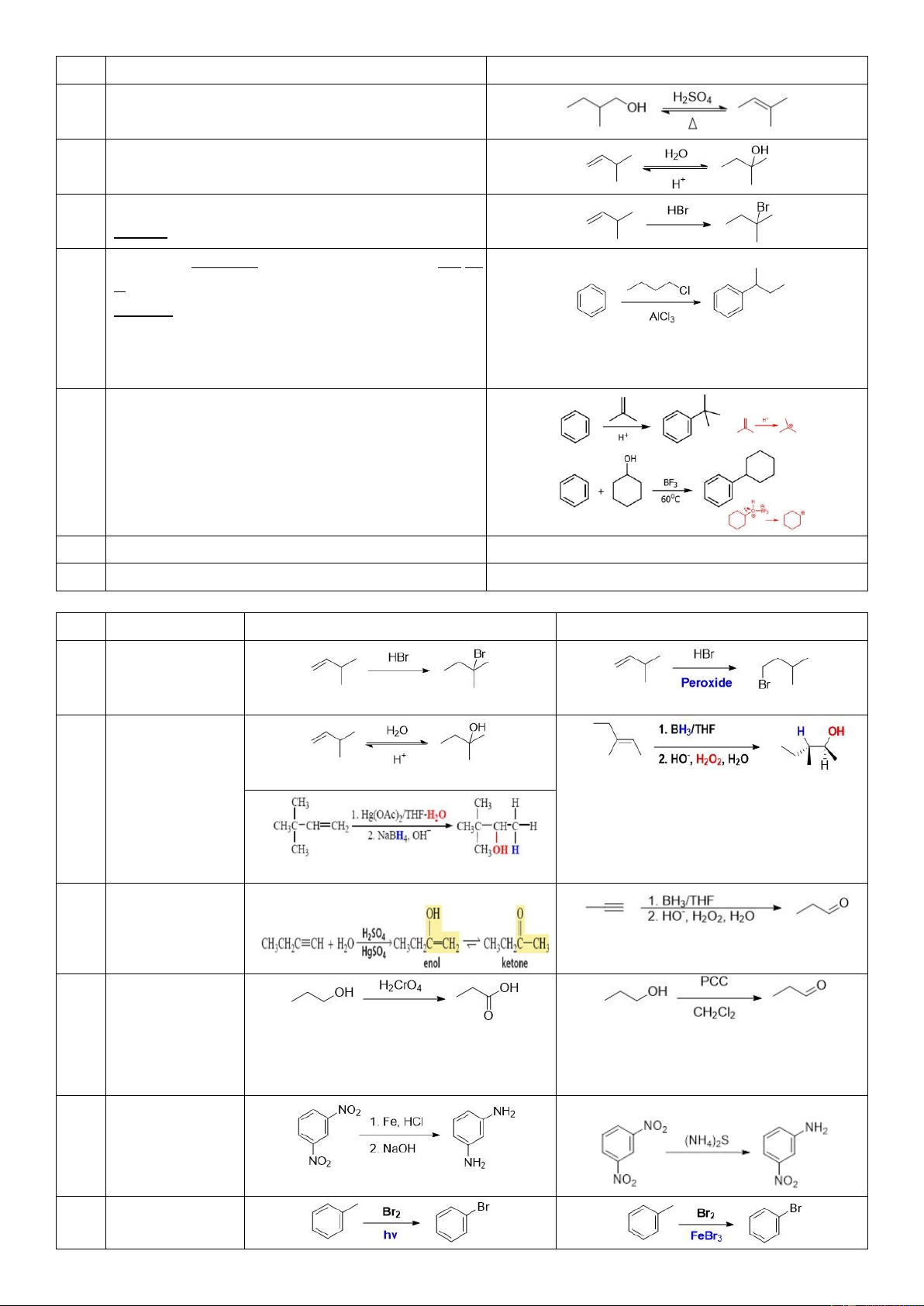
7. Một số phản ứng có chuyển vị
Chuyển vị H ể tạo hợp chất bền hơn, C-α. Nếu không còn H thì chuyển vị CH3. STT Loại phản ứng Ví dụ 1.
Tách nước từ alcohol tạo alkene bằng H+, nhiệt ộ 2.
Alkene cộng nước: H2O, H+ (Markovnikov’s rule) 3.
Alkene cộng HX (Markovnikov’s rule)
Lưu ý: Tạo ồng phân lập thể ngẫu nhiên 4.
Phản ứng alkyl hóa Friedel-Crafts benzene với R- X bằng xúc tác Lewis acid
Lưu ý: các loại phản ứng Friedel-Crafts sẽ
không xảy ra nếu trên benzene có các nhóm hút Xúc tác Lewis acid thường thấy: AlCl3, FeCl3,
mạnh h n (COOH, NO2, SO3H,...) hoặc phản ứng FeBr3, Al, Fe,...
với aniline (C6H5NH2) và các dẫn xuất aniline 5.
Phản ứng alkyl hóa benzene bằng alkene hoặc alcohol 6. Phản ứng thế SN1 mục 1 7.
Phản ứng tách E1 (tùy trường hợp) mục 2
.8. Một số cặp phản ứng this that (gọi ngược cho vui)
STT Loại phản ứng This That 1. Alkene/Alkyne cộng HX (có chuyển vị)
(Peroxide có thể ghi là ROOR) 2. Alkene → Alcohol (có chuyển vị)
(Có thể thay BH3 bằng alkyl borane hoặc disiamylborane) (không chuyển vị) 3. Alkyne → Aldehyde hoặc Ketone
(Có thể thay BH3 bằng alkyl borane
hoặc disiamylborane) 4. Oxi hóa R-OH
(Có thể thay H2CrO4 bằng tác nhân oxi PCC: Pyridinium chlorochromate
hóa như CrO3/H+, Na2Cr2O7/H+, KMnO4/H+) 5. Khử NO2 thành NH2
(Có thể thay bằng H2/Pd; Sn/HCl, OH–) 6. Halogen hóa 7. Phản ứng Friedel-Crafts của phenol 8. Halogen hóa Dung môi trơ Dung môi phân cực phenol (Không cần dùng xúc tác Lewis acid)
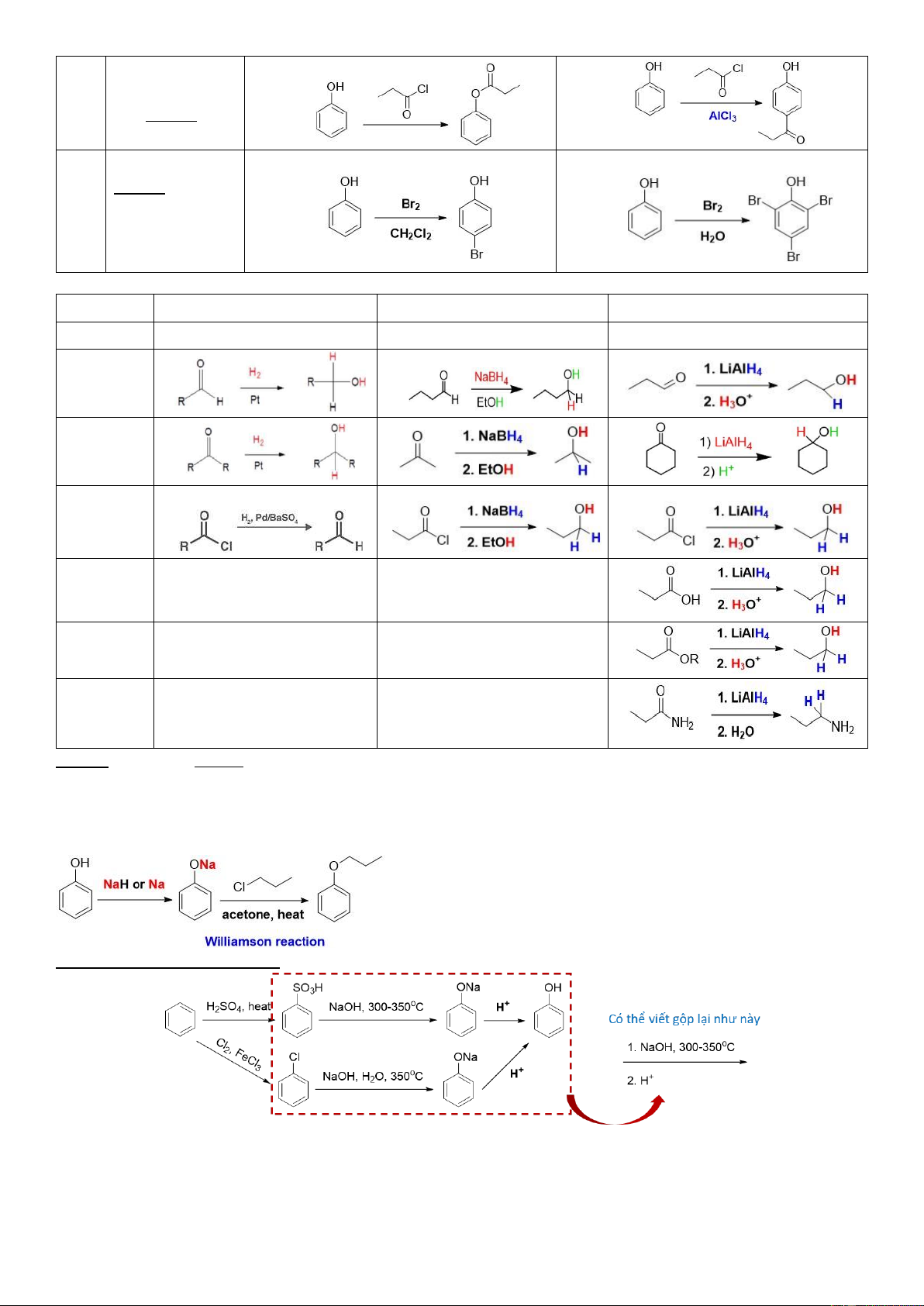
9. Tác dụng với hợp chất hydride hoặc H2 Loại chất
H2 với xt kim loại NaBH4/EtOH (H2O, H+) LiAlH4 C=C, C≡C
Thành liên kết ơn C–C - - Aldehyde Ketone Acyl (Tìm hiểu thêm) halide Acid - - Ester - - Amide - -
Lưu ý: Chú ý các vị trí H. Áp dụng tư ng tự nếu ề bài thay H bằng ồng vị D hoặc T
10. Phản ứng tạo ether của phenol
Không thể tạo ether trực tiếp từ phenol với alcohol khác bằng xúc tác H+. Ta nên chuyển thành muối
phenolate rồi tác dụng với alkyl halide theo phản ứng Williamson.
Điều chế phenol (tham khảo):




