
















Preview text:
PHƯƠNG PHÁP QUANG PHỔ Mục tiêu học tập
• Trình bày được một số khái niệm cơ bản:
độ hấp thụ ánh sáng, đường cong hấp thụ phổ, phổ UV-VIS
• Trình bày phát biểu định luật Lambert- Beer và công thức
• Trình bày được ứng dụng định lượng của phương pháp quang phổ
Một số khái niệm cơ bản
Nhiều kỹ thuật phân tích trong các phòng thí nghiệm hóa học và sinh
học, hóa sinh dựa trên việc đo năng lượng bức xạ điện từ phát đi,
truyền đi, hấp thụ, tán xạ hoặc khuyêch xạ trong các điều kiện được
kiểm soát.Các kỹ thật này được gọi là Kỹ thuật quang học (optical techniques).
Các kỹ thuật quang học bao gồm:
• Phương pháp quang phổ(spectrophotometry)
• Phương pháp đo quang phản xạ( reflectance photometry)
• Phương pháp quang phổ ngọn lửa( Flame emission spectrophotometry)
• Phương pháp quang phổ hấp thụ nguyên tử (atomic absorption spectrophotometry)
• Phương pháp huỳnh quang (Fluorometry)
• Phương pháp lân quang(phosphorescence)
• Hóa phát quang (Chemiluminescence), sinh phát quang
(bioluminescence), và điện hóa phát quang (electrochemiluminescence)
• Đo độ đục (Nephelometry and turbidimetry)
Một số khái niệm cơ bản
1. Đặc điểm của ánh sáng:
-Bức xạ điện từ bao gồm năng lượng bức xạ
của tia vũ trụ hay tia gama (bước sóng ngắn ở
mức 10-9 nm), tia X, tia cực tím, khả kiến, hồng
ngoại, sóng siêu âm,sóng radio (dài hơn 1000 km)
-Trong bài này, thuật ngữ ánh sáng dùng mô
tả năng lượng bức xạ của ánh sáng nhìn thấy
(visible) và tia cực tím (ultraviolet).
Một số khái niệm cơ bản
• Ánh sáng có tính chất sóng: Bước sóng (Wavelength): Là khoảng
cách giữa 2 đỉnh (peak) liên tiếp của sóng ánh sáng, đơn vị quốc tế là nm. Ký hiệu:.
Số sóng/giây: Tần số ánh sáng. Kí hiệu: v
• Ánh sáng có tính chất hạt: Ánh sáng gồm các hạt có năng lượng, gọi là photon.
• Mối liên hệ giữa năng lượng photon và tần số ánh sáng: E=hv (1)
(E: năng lượng, h: hằng số Planck 6.62x 1027,v: tần số ánh sáng/giây) v= c/ (2)
(c: tốc độ ánh sáng trong chân không 3X1010 cm/s)
Kết hợp (1) và (2): E= hc/ .
• Năng lượng ánh sáng tỷ lệ nghịch với bước sóng. Bước sóng càng
ngắn, năng lượng càng cao và ngược lại. VD: UV 200nm có năng
lượng lớn hơn hồng ngoại (infrared) 750 nm.
Một số khái niệm cơ bản
• Các đặc điểm của phổ UV, khả kiến(visible) và hồng ngoại (infrared) (nm) Tên của vùng Màu sắc quan sát được < 380 UV Không nhìn thấy 380- 440 Khả kiến Tím 440- 500 Khả kiến Xanh da trời 500- 580 Khả kiến Xanh lục 580- 600 Khả kiến Vàng 600- 620 Khả kiến Da cam 620- 750 Khả kiến Đỏ 800- 2500 IR gần Không nhìn thấy 2500-15000 IR trung gian Không nhìn thấy 15000- IR xa Không nhìn thấy 1.000.000
Một số khái niệm cơ bản
• Phổ UV và khả kiến thường được dùng
nhiều nhất trong các phòng XN hóa sinh lâm sàng.
• Phổ hồng ngoại đôi khi được dùng trong
phòng XN độc chất để xác định các thuốc hay chất độc.
• Tia gamma được dùng trong miễn dịch
phóng xạ (radioimmunoassay counters)
Một số khái niệm cơ bản • Phổ UV: < 380 nm
+Phổ này thu được bởi sự dịch chuyển năng lượng của
các điện tử hóa trị trong phân tử.
+ Năng lượng rất cao, có thể gây tổn thương mắt, da.
+ Các hợp chất chứa các liên kết đôi, ba, peptid, chứa
nhân thơm, nhóm carbonyl hay dị vòng có độ hấp thụ
ánh sáng cực đại tại phổ UV
+ Các yếu tố: pH, nồng độ muối, điện tích dung môi làm
tăng hay giảm điện tích phân tử sẽ gây dịch chuyển phổ UV
+ Phổ UV có vai trò quan trọng trong định tính và định
lượng các hợp chất hữu cơ
Một số khái niệm cơ bản • Phổ khả kiến:
+ Bước sóng từ 380- 750 nm
+ Màu của dung dịch tương ứng với bước sóng ánh sáng truyền qua.
+ Muốn đo sự hấp thụ ánh sáng phải chọn bước
sóng tại đấy dung dịch hấp thụ ánh sáng.
+ Cả dung dịch có màu và dung dịch không màu
có thể chuyển thành các sản phẩm có màu nhờ
các phản ứng thích hợp có thể phân tích được trong vùng này.
Một số khái niệm cơ bản
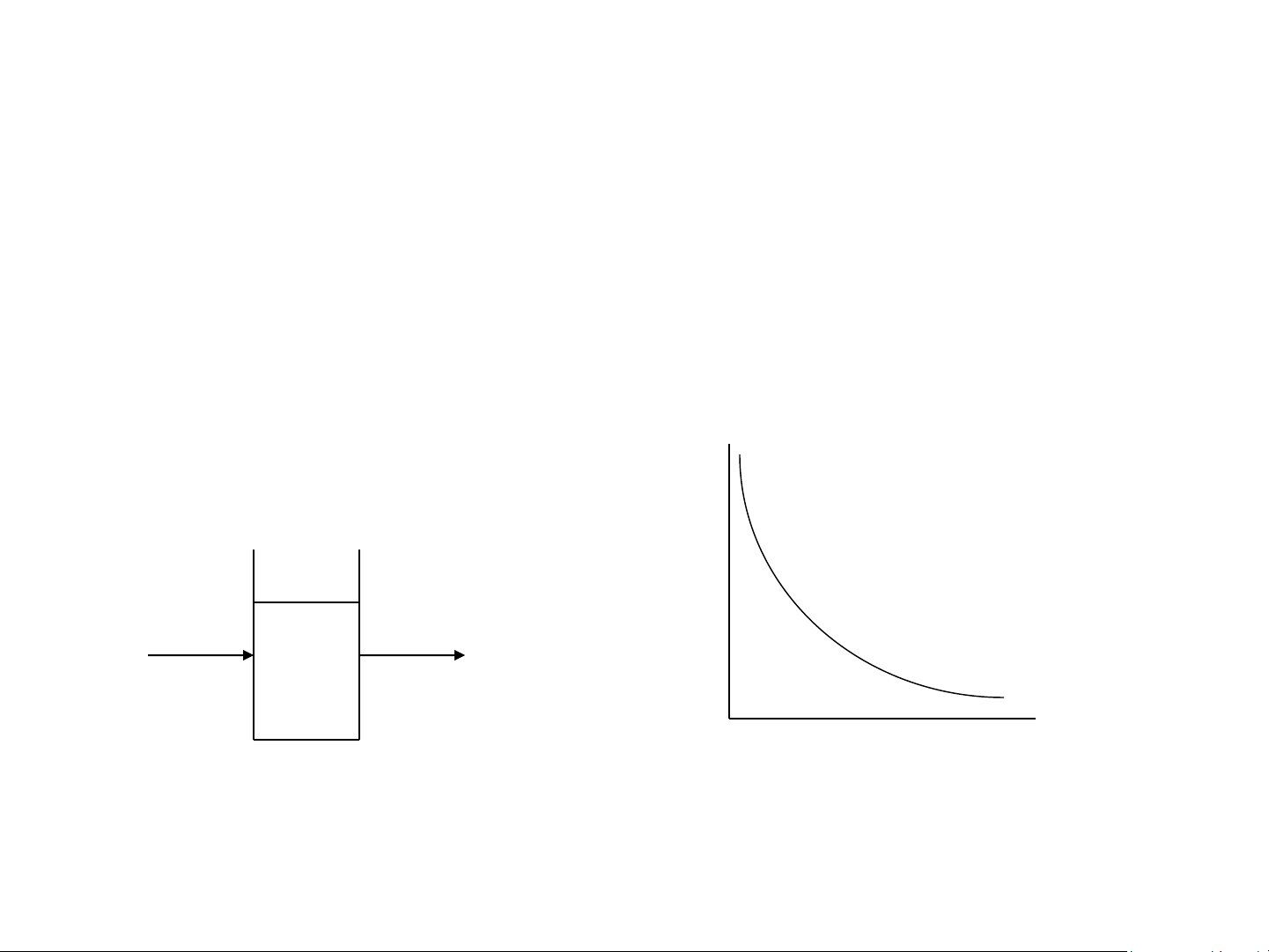
• Độ thấu quang T(Transmittance): T= It/Io
- T thường được biểu diễn dưới dạng %: - %T= It/Io x 100%
Io: Cường độ của tia tới
It: Cường độ của tia ló %T Io It Nồng độ C
- %T và nồng độ C có mối tương quan logarit ngược
Một số khái niệm cơ bản
• Độ hấp thụ ánh sáng A (Absorbance) hay
mật độ quang OD (optical density): A = log1/T= -logT= -log It/Io A C Mối quan hệ giữa A và C
Một số khái niệm cơ bản
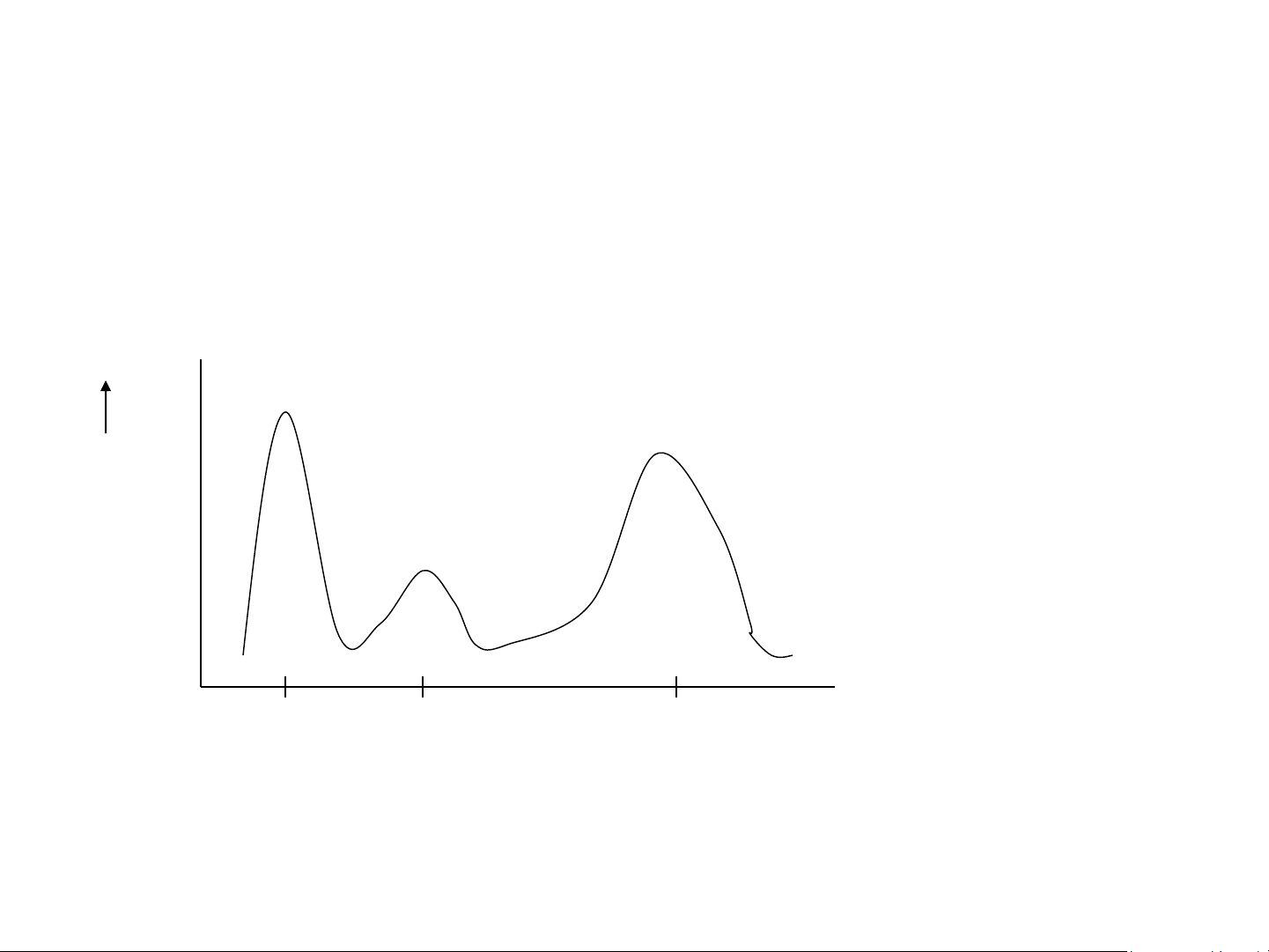
• Đường cong hấp thụ phổ (Spectral absorbance
curves): Khi độ hấp thụ ánh sáng A của 1 chất được
đo ở nhiều bước sóng liên tục, ta được đường cong
hấp thụ phổ hay phổ hấp thụ (absorbance spectrum)
hay phổ quét (spectral scan).
+ Mỗi chất có phổ hấp thụ đặc trưng, được dùng xác
định bước sóng tại đấy chất hấp thụ ánh sáng mạnh
nhất ( max) và bước sóng tại đấy chất hấp thụ ánh sáng ít nhất ( min).
+ Để có độ nhạy lớn nhất, người ta thường lựa chọn
max trong phân tích định lượng. Ngoài ra cần tính
đến độ nhọn của peak, sự xuất hiện các yếu tố
nhiễu, đặc tính dung môi
Một số khái niệm cơ bản PHỔ HẤP THỤ A 255 300 480 Bước sóng nm
Một số khái niệm cơ bản
2. Định luật Lambert- Beer:
• Theo Bouger và Lambert, ánh sáng truyền
qua dung dịch trong cuvet giảm theo hàm
số mũ với sự tăng đường kính cuvet.
• Theo Bernard và Beer, độ hấp thụ ánh
sáng của dung dịch tỷ lệ thuận với nồng độ dung dịch
Một số khái niệm cơ bản
2. Định luật Lambert- Beer:
• Định luật Lambert- Beer: Nồng độ của chất tan
trong dung dịch tỷ lệ thuận với lượng ánh sáng
hấp thụ hay tỷ lệ nghịch với logarit của ánh sáng truyền qua.
• Về toán học, định luật này được thể hiện bằng công thức: It=Io. 10-aCl A= -log1/T= -log10-aCl =aCl
A là mật độ quang, a là hệ số hấp thụ phân tử
(Absorptivity), l là chiều dày lớp dung dịch (cm), C
là nồng độ dung dịch chất hấp thụ (g/L)
• Khi C có đơn vị mol/L thì a gọi là (hệ số hấp thụ phân tử gam) A=Cl
Ứng dụng của phương pháp quang phổ 1. Định tính:
-Xác định độ tinh khiết của 1 chất
-Phân tích định tính các chất 2. Định lượng:
2.1. Sử dụng hệ số hấp thụ:
Hệ số hấp thụ được dùng trong định lượng và đo hoạt
độ enzym, xác định độ tinh khiết của 1 chất trong dung dịch. A= lC C= A/l
Ví dụ: của NADH tại 340 nm là 6.22 x 103. Mật độ quang
của dung dịch NADH tại 340 nm là 0.38. Vậy nồng dộ dung dịch NADH là:
A= Cl C=A/ l= 0.38/ 6.22 x 103 x1=6.11x10-5 (mol/L)
Ứng dụng của phương pháp quang phổ
2.2. Sử dụng các dung dịch chuẩn: •
Mật độ quang của dung dịch chưa biết nồng
độ (Ax) và dung dịch chuẩn (As) được đo ở
cùng 1 điều kiện:Ax=alCx và As=alCs. •
Vì dung dịch chuẩn và dung dịch chưa biết
của cùng 1 chất, đo cùng 1 điều kiện nên a và l như nhau. Ta có:
As/Cs= Ax/Cx Cx = Ax x Cs/As hay Cx= Ax x K với K = Cs/As
K: Hệ số chuẩn(calibration constant)
• Thận trọng khi sử dụng K:
+ Khi Ax hay As vượt quá vùng tuyến tính
của đường chuẩn, không sử dụng K
+ Ít nhất 2 dung dịch chuẩn hoặc nhiều hơn
được sử dụng để tính K vì sự thay đổi về
thuốc thử, điều kiện thí nghiệm, đường
kính cuvet, sự biến chất hay sự thay đổi
của máy móc có thể dẫn đến sự thay đổi
A của các dung dịch chuẩn.
• Đường chuẩn không tuyến tính có thể dùng nếu
số lượng các dung dịch chuẩn với các nồng độ
khác nhau bao phủ toàn bộ khoảng nồng độ của các dung dịch chưa biết
• Trong một số trường hợp không có dung dịch
chuẩn, có thể dùng K nêu ra trong tài liệu nếu:
+Phương pháp được tiến hành theo đúng hướng dẫn
+ Quang phổ kế có khả năng cung cấp ánh sáng
với phổ có độ tinh khiết cao ở 1 bước sóng nhất định
• Định luật Lambert- Beer chỉ đúng khi các điều
kiện sau đây được thỏa mãn:
+ Ánh sáng tới là đơn sắc
+ Sự hấp thụ ánh sáng của dung môi là không có ý nghĩa so với chất tan
+Nồng độ chất tan trong giới hạn nhất định
+Không có yếu tố nhiễu về quang học
+Không có phản ứng hóa học giữa chất cần định
lượng với các chất tan khác hay với dung môi



