










Preview text:
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
Chương I – Những cơ sở của thuyết động học phân tử của chất khí ..... 2
I. Tóm tắt lí thuyết chương I ................................................................... 2
II. Phương pháp giải ................................................................................ 4
III. Bài tập mẫu ....................................................................................... 5
IV. Bài tập ............................................................................................... 9
Chương II- Các hiện tượng truyền nhiệt trong chất khí .......................... 17
I. Tóm tắt lí thuyết chương II .................................................................. 17
II. Phương pháp giải ................................................................................ 19
III. Bài tập mẫu ....................................................................................... 19
IV. Bài tập ............................................................................................... 20
Chương III- Các nguyên lý cơ bản của nhiệt động lực học ..................... 23
I. Tóm tắt lí thuyết chương III ................................................................ 23
II. Phương pháp giải ................................................................................ 31
III. Bài tập mẫu ....................................................................................... 32
IV. Bài tập ............................................................................................... 35
Chương IV- Khí thực .................................................................................... 48
Chương V- Chất lỏng ................................................................................... 52 1
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
CHƯƠNG I - NHỮNG CƠ SỞ CỦA THUYẾT ĐỘNG HỌC CHẤT KHÍ I.
TÓM TẮT LÝ THUYẾT
1. 1. Công thức cơ bản của thuyết động học chất khí 2 p = n E . d 3
p : áp suất của chất khí
E : động năng trung bình của chuyển động tịnh tiến của phân tử. d
n : mật độ phân tử khí 3 Với : E = d k T . 2 Chú ý :
+ Tổng số phân tử trong bình chứa là: N = nV . = .N A : số mol khí. V: thể tích khí NA: số Avôgadrô
+ Khối lượng của 1 phân tử khí là : M D m = = = N N n A
2. 2. Đơn vị của áp suất : atm Torr
Đơn vị đo Pa (N/m2) at (760mmHg) (mmHg) bar Pa 1 – – – 1,02.10 5 9,87.10 6 7,5.10 3 10 - 5 at 9,81.10 4 1 0,968 736 0,981 atm 1,013.10 5 1,033 1 760 1,013 torr 133,322 – – 1,36.10 3 1,316.10 3 1 1,33.10 - 3 bar 10 5 1,02 0,987 750 1
3. 3. Đơn vị của nhiệt độ + Nhiệt giai Kelvin 2
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
T (K ) = t(oC) + 273 + Nhiệt giai Fahrenheit o 9 t F = t C o + 32 5 + Nhiệt giai Reaumur 4 t o R = t oC 5
4. 4. Phương trình trạng thái của khí lý tưởng: khối khí xác định M pV = RT
5. 5. Định luật Boyle – Marriotte : T = const, khối khí xác định pV = const
6. 6. Định luật Gay – Lussac : p = const , khối khí xác định V = const T
7. 7. Định luật Charles : V = const, khối khí xác định p = const T
8. 8. Định luật Dalton: các khí không có tác dụng hoá học, cùng V, cùng T 9. n p = p i i=1
10. 9. Sự phân bố vận tốc phân tử theo Maxwell
a. + Số phân tử có vận tốc nằm trong khoảng vận tốc từ c → c + d c(d c c) dn = n. f(c) . dc
+ Với hàm phân bố Maxwell : 3 2 mc 2 4 m − 2 2 f (c) = .e kT .c 2kT 3
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
b. + Số phần trăm phân tử chuyển động với vận tốc nằm trong khoảng c →c+dc
dn = f (c dc ). n
c. 10. Các loại vận tốc đặc trưng cho chuyển động của phân tử
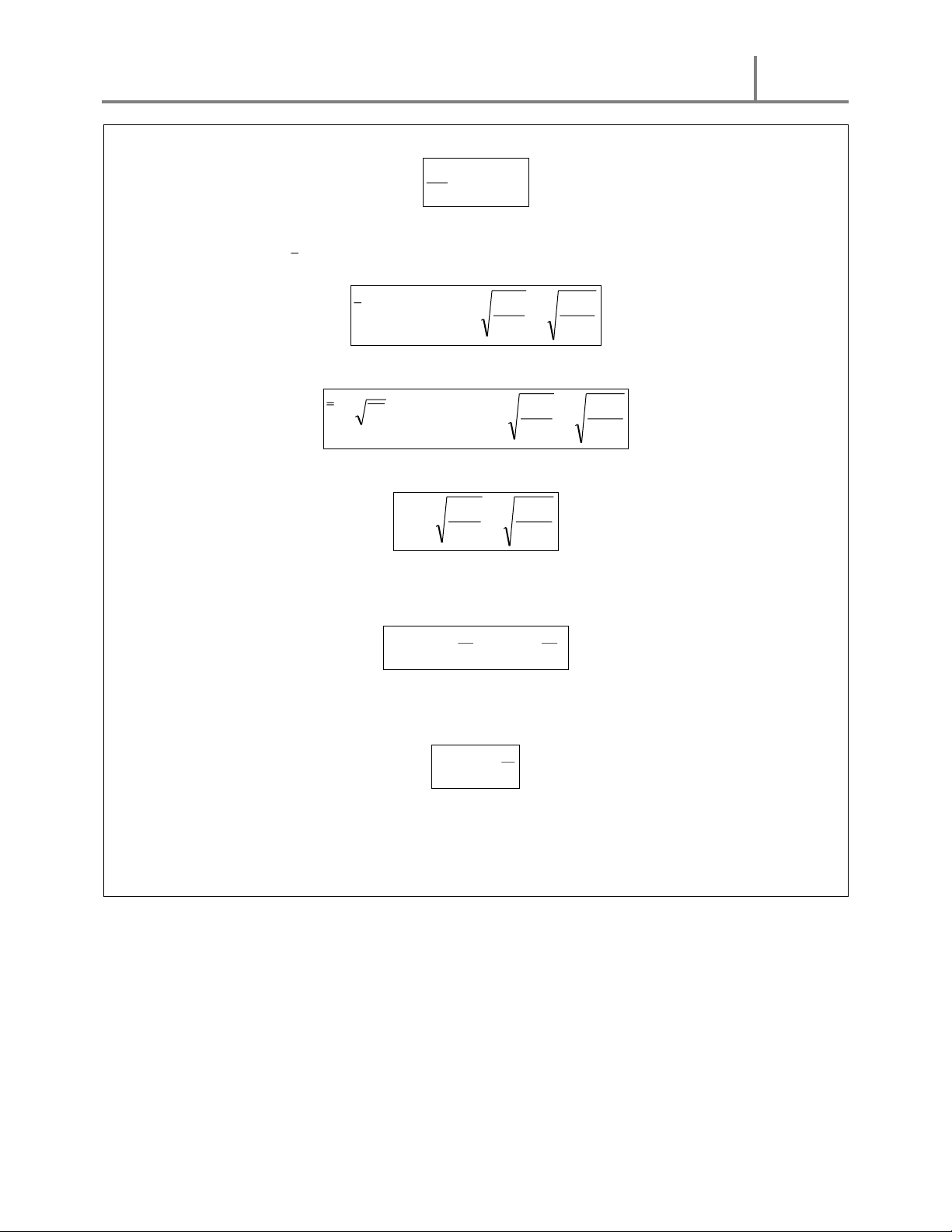
+ Vận tốc trung bình ( c ) kT 8 8RT
c = c. f (c dc ). = = m o
+ Vận tốc căn trung bình bình phương ( Căn quân phương ) : 2 2 kT 3 3RT c =
c = c f (c)dc = = m 0
+ Vận tốc có xác suất cực đại : 2kT 2RT c = = m m
11. Định luật phân bố Boltzmann :
+ Công thức phong vũ biểu : mg g − h − h kT RT p = p e . = p e . 0 0 + Công thức Boltzmann : T − kT n = n e . 0 k : hằng số Boltzmann k = 1,38.10-23( J/K) II. PHƯƠNG PHÁP GIẢI
Các bài toán về các quá trình :
- Quá trình đẳng nhiệt : áp dụng định luật Boyle – Marriotte. Điều kiện áp dụng:
• Khối khí cô lập ( có khối lượng không đổi ).
• Không thay đổi nhiệt độ, chỉ thay đổi thể tích, áp suất.
- Quá trình đẳng tích : áp dụng định luật Charles. Điều kiện áp dụng: 4
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
• Khối khí cô lập ( có khối lượng không đổi ).
• Không thay đổi thể tích, chỉ thay đổi nhiệt độ, áp suất.
- Quá trình đẳng áp : áp dụng định luật Gay – Lussac . Điều kiện áp dụng:
• Khối khí cô lập ( có khối lượng không đổi ).
• Không thay đổi áp suất ( thường là do cân bằng với áp suất khí quyển ) , chỉ
thay đổi nhiệt độ, thể tích. III. BÀI TẬP MẪU
THÍ DỤ 1. Một hỗn hợp không khí gồm 23,6g oxi và 76,4g nitơ. Tính :
a) Khối lượng của 1 mol hỗn hợp.
b) Thể tích hỗn hợp ở áp suất 750mmHg, nhiệt độ 27oC. GIẢI
Gọi V là thể tích của khối khí, p1 và p2 là áp suất riêng phần của khí O2 và khí N2
Theo phương trình trạng thái khí lý tưởng ta có: M p V 1 = RT 1 1 M p V 2 = RT 2 2
Cộng 2 phương trình trên lại ta có: M M ( p + p V ) = ( 1 2 + )RT (1) 1 2 1 2
Gọi p và là áp suất và khối lượng của 1mol hỗn hợp
Theo định luật Dalton ta có :
p = p + p 1 2 M + M Và pV 1 2 = RT (2) 5
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC So sánh (1) và (2) ta có : M + M M M 1 2 1 2 + = 1 2
❖ Khối lượng của 1 mol hỗn hợp. M + M 1 2 = = 29g / mol M M 1 2 + 1 2
❖ Thể tích hỗn hợp ở áp suất 750mmHg, nhiệt độ 27oC. M M
Từ (1) ta có ( p + p V ) = ( 1 2 + )RT 1 2 1 2 M M RT V = ( 1 2 + ) ( p + p ) 1 2 1 2 M M RT V = ( 1 2 + ) = l 86 p 1 2
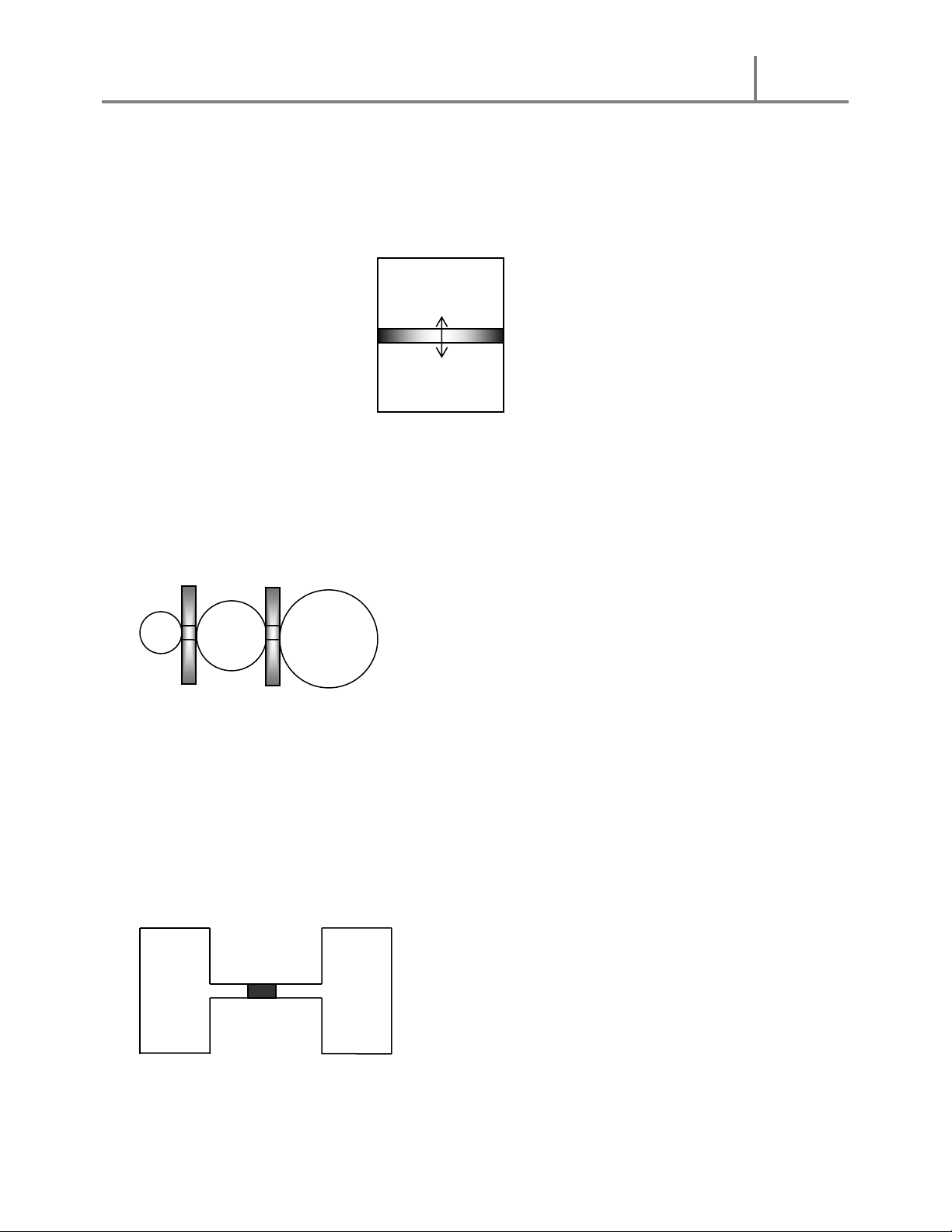
THÍ DỤ 2. Một bình trụ kín thẳng đứng có chiều cao h được chia thành hai phần bởi một 3
pittông cách nhiệt. Pittông cách đáy .
h Phần trên và dưới của bình chứa cùng một khí lý tưởng 4
theo tỷ lệ kilomol là 1:5 và ở cùng một nhiệt độ To.
a) Tính áp suất khí trong mỗi phần của bình.Cho biết pittông có khối lượng m = 10 kg,
bình có tiết diện S = 10 cm2.
b) Để pittông cách đều hai đáy của bình, người ta nung nóng một phần bình, phần còn lại
giữ ở nhiệt độ không đổi. Hỏi phải nung nóng tới nhiệt độ là bao nhiêu ? 1 2 6
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC GIẢI Tóm tắt Ngăn 1: Ngăn 2:
Trước: p ,V ,T
Trước: p ,V ,T 1 1 1 2 2 2
Sau : p,V ,T 1 1 1
Sau : p ,V ,T 2 2 2 Ta có :
V = V + V = V + V 1 2 1 2 p = p + p 2 1
p = p + p 2 1 a) Tìm p1, p2
Phương trình trạng thái cho từng ngăn trước khi nhiệt độ thay đổi
p V = RT (1) 1 1 1 1 p V = RT (2) 2 2 2 2 Lấy (1) : (2) p V RT 1 1 = 1 1 p V RT 2 2 2 2 p V RT 1 1 o = ( p + p V )( − V ) RT . 5 1 1 o p V 1 1 1 = ( p + p V )( − V ) 5 1 1
5 p V = p V − p V + pV − pV 1 1 1 1 1 1 6 p V = pV 1 1 h mg 6 p S. = S h . 1 4 S mg 5 , 1 p = 1 S 7
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC mg p = 1 5 , 1 S . 10 10 p = 1 5 , 1 10 . − 3 p = 10 . 7 , 66 3 (N / 2 m ) 1
Ta có : p = p + p 2 1 mg 3 . 10 10 p = p + = 7 , 66 .10 + 2 1 S . 10 10−4 p = 16670 ( 0 N / 2 m ) 2 V
b) Phải nung nóng phần bình nào để xylanh cách đều 2 ngăn V = V = 1 2 2 Lúc đầu : 1 V = V 1 4 3 V = V 2 4
V1nhiệt độ. Vậy nung nóng khí ngăn 1.
Phương trình trạng thái khí lý tưởng cho ngăn 1 sau khi tăng nhiệt độ ta có :
pV = RT (3) 1 1 1 1
Phương trình trạng thái khí lý tưởng cho ngăn 2 sau khi tăng nhiệt độ của bình 1 ta có :
pV = RT (4) 2 2 2 2 Lấy (3) : (4) ta có : ' p V T ' p V 1 1 1 = → ' 1 T = 5
.T (5) ( vì V = V = ; T = T ) pV 5T 1 ' 0 p 1 2 2 2 0 2 2 2 2 8
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC ' p . ' V Tính ' '
p , p . Ta lấy (4) : (2) ta có : 2 2 = 1 1 2 p .V 2 2 p .V ' 2 2 p = 2 ' V2 3V p . 2 ' 4 p = 2 V 2 ' 3 p = p = ( 250050 N / 2 m ) 2 2 2 mg Ta có p = = 105 (N / 2 m ) S
Ta lại có : p = p + p ' '
p = p − p = 15005 ( 0 N / 2 m ) 2 1 1 2 Thế p' và '
p vào ( 5) ta sẽ tính được ' T = 3T 1 2 1 0 IV. BÀI TẬP
BÀI 1 : Tìm số phân tử n trong 1cm3 và khối lượng riêng ρ của nitơ ở áp suất 2,0nPa và nhiệt độ 150C.
BÀI 2 : Tìm mật độ và động năng trung bình của các phân tử khí trong một bình chứa ở nhiệt độ
270C và áp suất là 8,23.103N/m2.
BÀI 3 : Một căn phòng có thể tích 45m3. Không khí trong phòng có nhiệt độ 27oC và ở áp suất
1atm. Tính số phân tử chứa trong phòng.
BÀI 4 : Động năng tịnh tiến trung bình của các phân tử oxy ở nhiệt độ phòng (300K) là bao
nhiêu eletron von ? của các phân tử nitơ là bao nhiêu ?
BÀI 5: Tính vận tốc căn quân phương và động năng trung bình của chuyển động tịnh tiến của
phân tử oxy ở nhiệt độ 200C.
BÀI 6 : Cho các phân tử khí oxi ở nhiệt độ 270C. Tính:
a) Động năng trung bình của các phân tử khí oxi. b) Vận tốc trung bình. 9
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
c) Vận tốc căn trung bình bình phương.
d) Vận tốc có xác suất cực đại.
BÀI 7 : Một bình dung tích 10 lít chứa 1mol khí Heli ở áp suất 2,5atm. Tính động năng trung
bình và vận tốc trung bình của phân tử khí trong bình.
BÀI 8 : Có 10g khí H2 ở áp suất 8,2 at đựng trong bình kín có nhiệt độ 390K.
a) Tính thể tích của khối khí.
b) Hơ nóng khối khí đến 425K , tính áp suất khí đó.
BÀI 9: Một bình chứa một chất khí nén ở nhiệt độ 300K và áp suất 40at. Tính áp suất của khí khi
đã có một phần ba khối lượng khí thoát ra khỏi bình và nhiệt độ hạ xuống tới 12oC
BÀI 10 : Có 12g khí oxy ở nhiệt độ 10oC, áp suất 3at. Sau khi hơ nóng đẳng áp, khối khí chiếm thể tích 10 lít. Tìm :
a) Thể tích khối khí trước khi giãn nở?
b) Nhiệt độ khối khí sau khi giãn nở ?
c) Khối lượng riêng của khối khí trước khi giãn nở ?
d) Khối lượng riêng của khối khí sau khi giãn nở ?
BÀI 11 : Có 2g oxy ở áp suất 6at sau khi hơ nóng đẳng áp nó chiếm một thể tích 1 lít. Tìm nhiệt
độ sau khi hơ nóng. Coi khí oxy là khí lý tưởng.
BÀI 12 : 12g khí chiếm thể tích 4 lít ở 7oC. Sau khi nung nóng đẳng áp khối lượng riêng của khí
là 1,2g/lít. Tìm nhiệt độ của khí sau khi nung.
BÀI 13 : Khối lượng riêng của không khí trong phòng ( 27oC) lớn hơn khối lượng riêng của
không khí ngoài sân nắng ( 42oC) bao nhiêu lần ? Biết áp suất không khí trong và ngoài phòng là như nhau.
BÀI 14 : Một hỗn hợp khí gồm oxy và nitơ có áp suất p =1atm. Biết khối lượng oxy bằng 20%
khối lượng hỗn hợp khí, tính áp suất riêng phần của mỗi khí thành phần.
BÀI 15 : Bình cứng, kín chứa 14g khí Nitơ và 9g khí hydro ở nhiệt độ 10oC, áp suất 106 N/m2. Tính : 10
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
a) Khối lượng của 1 mol hỗn hợp khí trong bình. b) Dung tích của bình
BÀI 16 : Hai bình cầu, được nối với nhau bằng một ống có khóa, chứa hai chất khí không tác
dụng hóa học với nhau, ở cùng nhiệt độ. Áp suất khí trong hai bình là p1=2.105N/m2 và p2 =
106N/m2. Mở khóa nhẹ nhàng để hai bình thông với nhau sao cho nhiệt độ không đổi. Khi cân
bằng xảy ra, áp suất ở hai bình là p =4.105N/m2. Tính tỉ số thể tích của hai bình cầu.
BÀI 17 : Khối lượng riêng của một hỗn hợp khí heli và Argon ở áp suất 152.103Pa và nhiệt độ 27oC bằng = 00 , 2 kg / 3
m . Có bao nhiêu nguyên tử Heli chứa trong 1cm3 hỗn hợp khí ?
BÀI 18: Một xylanh đặt thẳng đứng, diện tích tiết diện là S = 120cm2, chứa không khí ở nhiệt
độ t1= 27oC. Ban đầu xylanh được đậy bằng một pittông cách đáy h =60cm. Pittông có thể trượt
không ma sát dọc theo mặt trong của xylanh.
Đặt lên trên pittông một quả cân có trọng lượng P = 500N. Pittông dịch chuyển xuống đoạn l
=20cm rồi dừng lại. Tính nhiệt độ của khí trong xylanh sau khi pittông dừng lại. Biết áp suất khí
quyển là po=105N/m2. Bỏ qua khối lượng của pittông. . . . . . . . .
BÀI 19 : Một xylanh kín được chia làm hai phần bằng nhau bởi một pittông cách nhiệt. Mỗi
phần có chiều dài l0=40cm, chứa một lượng khí giống nhau ở 27oC. Nung nóng một phần thêm
15oC và làm lạnh phần kia đi 15oC. Hỏi pittông di chuyển một đoạn bao nhiêu ? 11
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
BÀI 20 : Một xylanh kín hai đầu được đặt thẳng đứng, bên trong có một pittông nặng cách nhiệt
chia xylanh thành hai phần. Mỗi phần chứa một lượng khí giống nhau ở nhiệt độ T = 400K. Áp
suất p2 của phần dưới gấp 2 lần áp suất p1 của phần trên. Hỏi cần phải nung nóng khí ở phần dưới
đến nhiệt độ T2 là bao nhiêu để thể tích khí trong hai xylanh là bằng nhau ? 1 2
BÀI 21 : Có ba bình thể tích V1=V, V2=2V và V3=3V thông với nhau nhưng cách nhiệt đối với
nhau. Ban đầu các bình chứa khí ở cùng một nhiệt độ To và áp suất po. Người ta hạ nhiệt độ của
bình 1 xuống T1 = 0,5To và nâng nhiệt độ của bình 2 lên T2 = 1,5To; bình 3 lên T3 = 2To. Tính áp
suất mới p của khí trong các bình ? 1 2 3
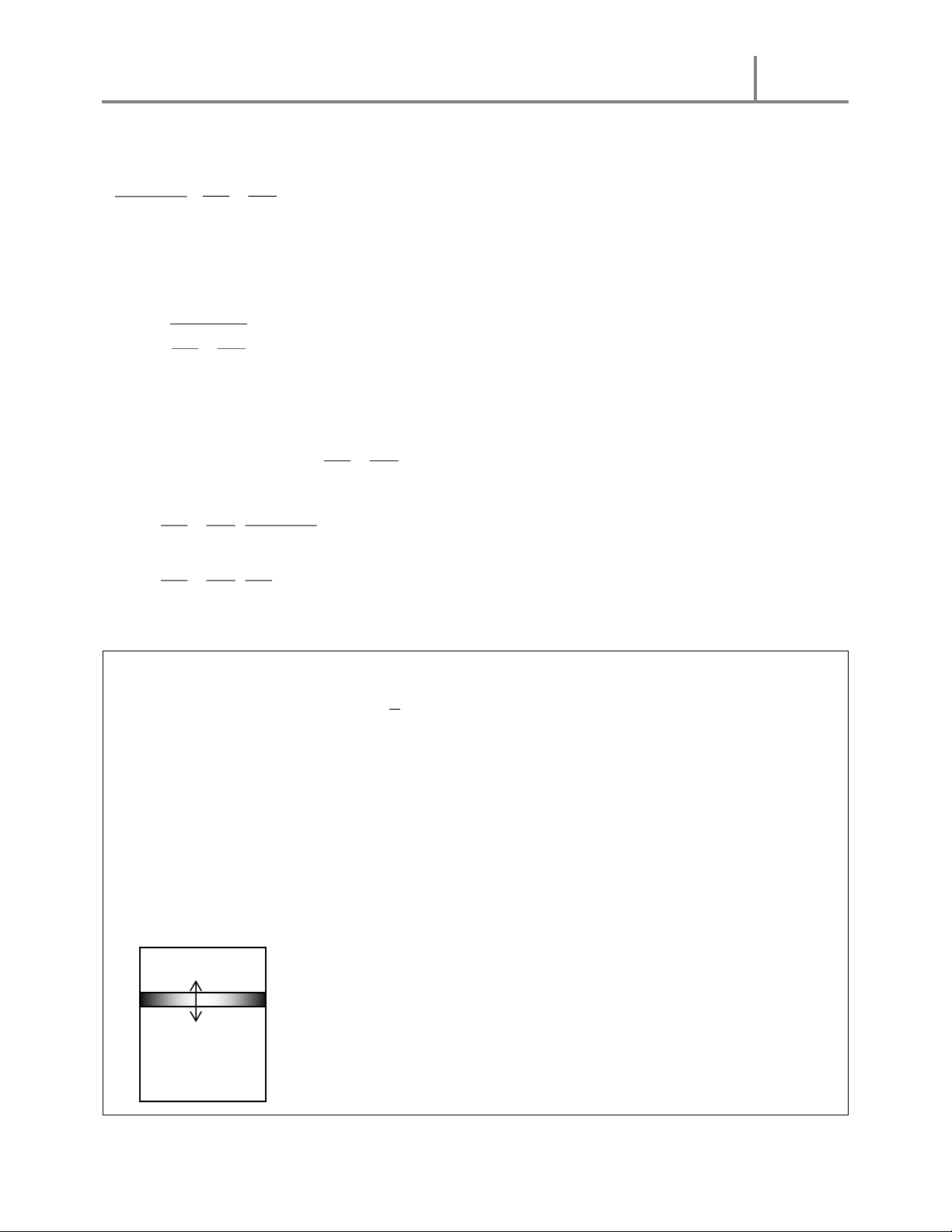
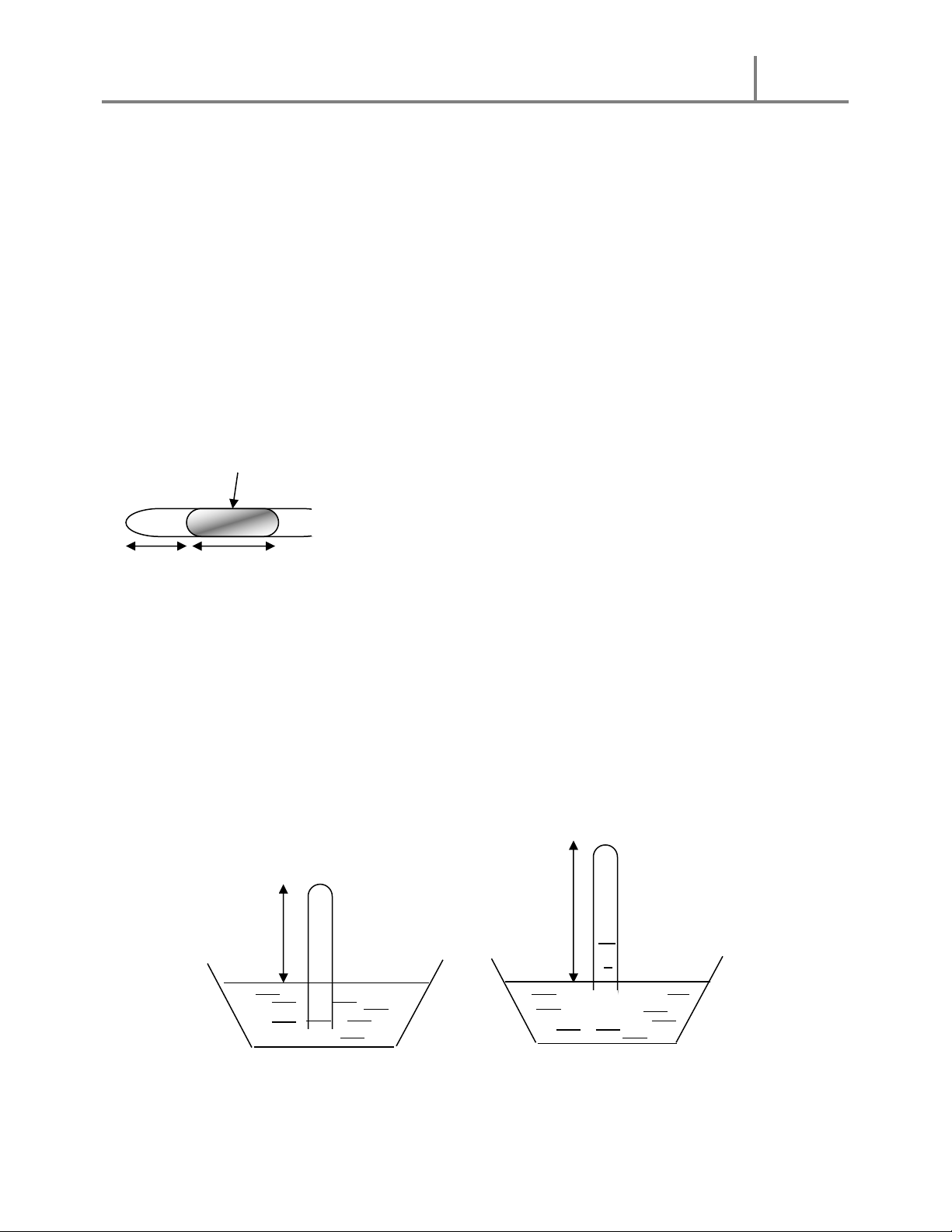
BÀI 22 : Hai bình chứa cùng chất khí được nối với nhau bởi một ống nằm ngang có đường kính
5mm. Trong ống có một giọt thủy ngân có thể dịch chuyển được. Lúc đầu khí trong hai bình
cùng ở nhiệt độ 27oC, giọt thủy ngân nằm yên ở một vị trí nào đó và thể tích của khí trong mỗi
bình ( kể cả phần ống nằm ngang ) đều bằng 0,2l. Tính khoảng cách dịch chuyển của giọt thủy
ngân nếu nhiệt độ khí trong bình tăng thêm 2O còn nhiệt độ khí trong bình kia giảm bớt 2O. Sự
giãn nở của bình không đáng kể. A B T + 2 T - 2 12
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
BÀI 23 : Một cột không khí chứa trong một ống nhỏ, dài, tiết diện đều. Cột không khí được ngăn
cách với khí quyển bởi một cột thủy ngân có chiều dài L = 160mm. Áp suất khí quyển là po=
760mmHg. Chiều dài cột không khí khi ống nằm ngang là lo=125mm. Hãy tính chiều dài cột không khí nếu :
a) Ống thẳng đứng, miệng ống ở trên.
b) Ống thẳng đứng, miệng ống ở dưới. c) Ống đặt nghiêng góc o
= 45 so với phương ngang, miệng ống ở dưới. d) Ống đặt nghiêng góc o
= 45 so với phương ngang, miệng ống ở trên.
( Giả sử ống đủ dài để cột thủy ngân luôn ở trong ống và nhiệt độ không đổi ). Hg lo L
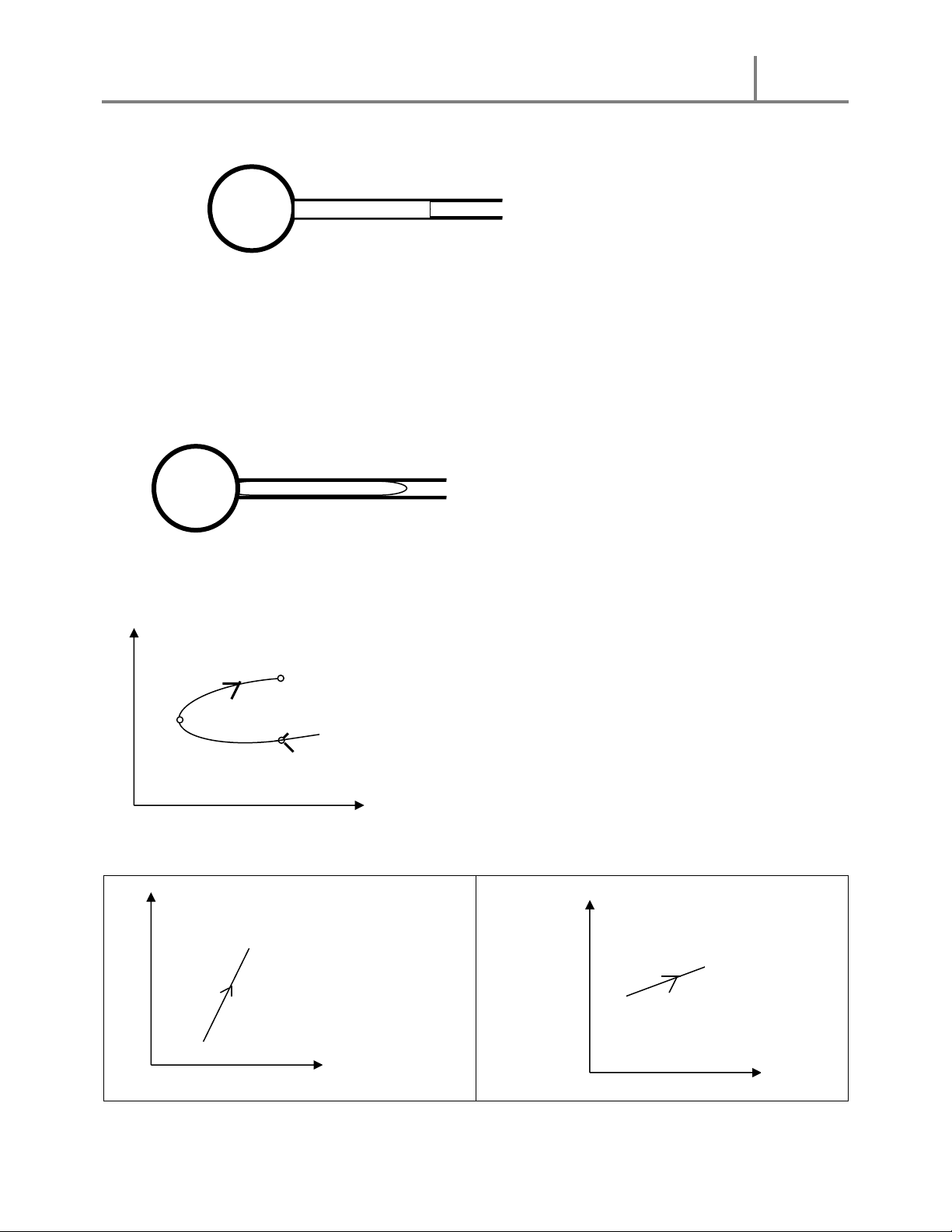
BÀI 24 : Một ống thủy tinh tiết diện đều, một đầu kín một đầu hở. Lúc đầu người ta nhúng đầu
hở vào một chậu nước sao cho mức nước trong và ngoài ống bằng nhau, chiều cao còn lại của
ống bằng 25cm. Sau đó người ta rút ống lên một đoạn 5cm ( như hình vẽ ) . Hỏi mức nước ở
trong ống dâng lên bao nhiêu, biết rằng nhiệt độ xung quanh không đổi và áp suất khí quyển là 760mmHg. 30cm 25cm 13
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
BÀI 25: Một ống thuỷ tinh tiết diện nhỏ có chiều dài l = 1 cm 00
dựng thẳng đứng, đầu hở ở
trên, đầu kín bên dưới. Phía đáy ống chứa cột không khí dài h = cm 50
ở nhiệt độ T = 300K . 1 1
Phía trên cột khí chứa đầy thuỷ ngân. Biết áp suất khí quyển p = c 76 mHg : 0
a) Hỏi nhiệt độ tối đa T2 của không khí ở trong ống là bao nhiêu để thuỷ ngân vẫn còn lại trong ống?
b) Nếu ở nhiệt độ T = 300K được giữ không đổi, ta úp ngược ống ( đầu hở dưới ). Tìm 1
chiều cao của cột thuỷ ngân còn lại trong ống.
BÀI 26: Một ống thuỷ tinh tiết diện nhỏ có chiều dài l = 1 cm 00
kín hai đầu, đặt nằm ngang, ở
giữa có cột thuỷ ngân, dài h = 20cm, hai bên chứa khí lý tưởng có cùng khối lượng ở áp suất p = c
50 mHg . Tìm độ dịch chuyển của cột thuỷ ngân khi: 0
a) Ống đặt thẳng đứng.
b) Ống đặt nghiêng so với phương thẳng đứng một góc 0 60 .
Bỏ qua sự thay đổi của nhiệt độ.
BÀI 27: Một ống thủy tinh chiều dài L = 50cm. Hai đầu kín, ở giữa có một đoạn thủy ngân dài l
=10 cm, hai bên là không khí có cùng một khối lượng. Khi đặt ống nằm ngang thì đoạn thủy
ngân nằm ở đúng giữa ống. Khi dựng ống thẳng đứng thì thủy ngân tụt xuống 6 cm.
a) Tính áp suất khí khi ống nằm ngang?
b) Khi ống nằm ngang, nếu mở một đầu ống thì thủy ngân dịch chuyển bao nhiêu và sang bên nào ?
c) Khi ống thẳng đứng, hai đầu kín. Nếu mở một đầu thì thủy ngân tụt xuống hay lên cao
bao nhiêu trong hai trường hợp : Mở đầu dưới hoặc mở đầu trên ?
Biết áp suất khí quyển là po = 76cmHg và nhiệt độ của khí không đổi.
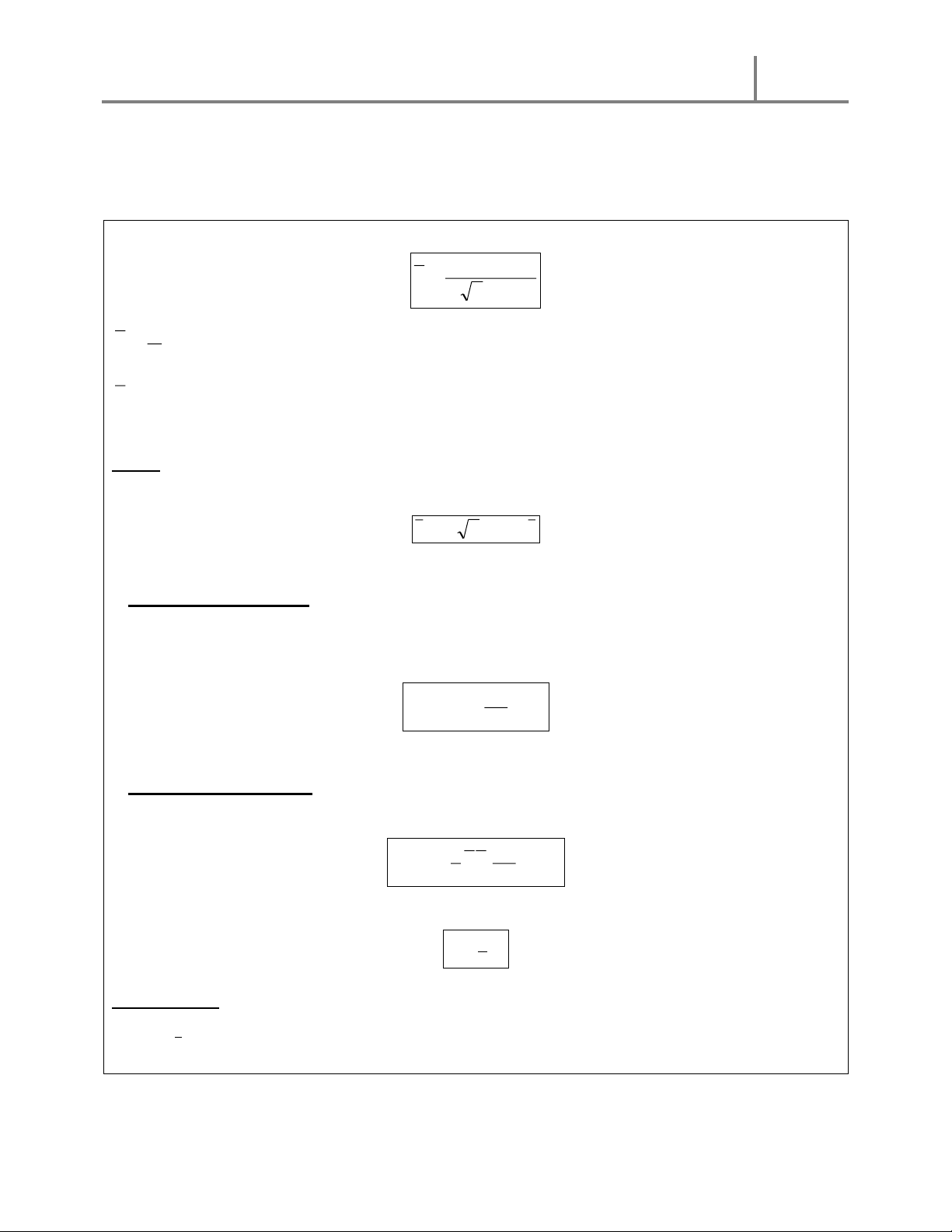
BÀI 28 : Bình thủy tinh có dung tích 15cm3 chứa không khí ở 177oC được ngăn cách bởi cột
thủy ngân trong ống nằm ngang như hình vẽ. Khi hạ nhiệt độ trong bình xuống còn 27oC thì có
một ít thủy ngân lọt vào bình.
a) Phân tích hiện tượng.
b) Tính thể tích thủy ngân lọt vào bình. 14
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
BÀI 29 : Một bình, dung tích V = 10 cm3 , chứa không khí ở nhiệt độ t1= 300oC được nối với
một ống thủy tinh nằm ngang chứa đầy thủy ngân. Tính khối lượng thủy ngân chảy vào bình, khi
làm lạnh không khí trong bình đến nhiệt độ t2=20oC . Dung tích của bình thay đổi không đáng kể
theo nhiệt độ. Biết khối lượng riêng của thủy ngân là 13,6g/cm3.
BÀI 30 : Nhận xét sự biến đổi thể tích của khối khí trong quá trình AB và BC được biểu thị trên đồ thị (p,T). p C B A O T
BÀI 31: Nung nóng một khối khí nhất định, ta vẽ được đồ thị của chúng như sau: V p 2 2 1 1 T T O Hình 1 Hình 2 O 15
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
Dựa vào đồ thị hãy xác định trong thời gian nung nóng khí thì:
a) Hình 1, áp suất tăng hay giảm ? Vì sao?
b) Hình 2, khí bị nén hay dãn? Vì sao?
BÀI 32 : Tính tỉ số phân tử khí có vận tốc không khác quá 0,5% so với :
a) vận tốc có xác suất cực đại.
b) vận tốc trung bình số học.
c) vận tốc căn trung bình bình phương.
BÀI 33 : Ứng với giá trị nào của vận tốc phân tử, các đường phân bố Maxwell đối với nhiệt độ
T1 và T2= 2 T1 sẽ cắt nhau ?
BÀI 34 : Tìm áp suất của không khí :
a) Ở độ cao cách mặt đất 10 km. b) Trong giếng sâu 10km.
Biết áp suất tại mặt đất là 100kPa. Nhiệt độ không khí là 0oC. Cho rằng ,T không phụ thuộc vào độ cao.
BÀI 35 : Tại độ cao h bằng bao nhiêu, khối lượng riêng của ôxy sẽ giảm 1%. Nhiệt độ của ôxy
không thay đổi và bằng 27OC.
BÀI 36 : Ở độ cao h bằng bao nhiêu trên mặt nước biển thì khối lượng riêng của không khí
giảm đi e lần. Biết nhiệt độ của không khí là o
0 C và không phụ thuộc vào độ cao h; không khí
có = 29kg / kmol . Lấy 2 g = 81 , 9 m / s . -Hết chương I- 16
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC
CHƯƠNG II - CÁC HIỆN TƯỢNG TRUYỀN NHIỆT TRONG CHẤT KHÍ
I. TÓM TẮT LÝ THUYẾT
1. 1. Quãng đường tự do trung bình k T . = . 4 2. r . 2 .p 1 ~ p ~ T
Với r là bán kính phân tử Chú ý :
Số va chạm trung bình trong đơn vị thời gian : z = . 4 2 r . 2 n . c .
2. 2. Hiện tượng khếch tán
+ Theo quan điểm vĩ mô : sự truyền khối lượng khí từ chỗ có khối lượng riêng lớn đến chỗ có
khối lượng riêng nhỏ, hiện tượng khếch tán tiếp diễn cho đến khi khối lượng riêng của khí đồng
nhất mọi điểm trong chất khí. d dM = −K. dSdt dx K : hệ số khuếch tán
+ Theo quan điểm vi mô : Sự truyền khối lượng khí gây ra bởi sự chuyển động nhiệt của các
phân tử từ chỗ có mật độ phân tử lớn hơn đến chỗ có mật độ phân tử nhỏ hơn. 1 d dM = − c.. dS . dt . 3 dx Từ (1) và (2) suy ra 1 𝐾 = 𝑐̅𝜆̅ 3
Ý nghĩa của k : 3 K ~ 2 T 17
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC 1 K ~ p
→ Nhiệt độ càng cao hiện tượng khếch tán xảy ra càng nhanh
→ Áp suất nhỏ hiện tượng khếch tán xảy ra nhanh.
3. 3. Hiện tượng dẫn nhiệt
+ Theo quan điểm vĩ mô : Sự dẫn nhiệt trong chất khí là sự truyền nhiệt lượng từ lớp khí nóng
hơn sang lớp khí lạnh hơn khi 2 lớp khí này tiếp xúc với nhau. dT dQ = −D. dS . dt . dx
D : hệ số dẫn nhiệt ( J/msK)
+ Theo quan điểm vi mô : Sự dẫn nhiệt là sự truyền 1 phần động năng của các phân tử ở lớp khí
nóng hơn cho các phân tử ở lớ
p khí lạnh hơn khi các phân tử ở lớp khí nóng hơn do chuyển động nhiệt va chạm vào các phân
tử ở lớp khí lạnh hơn. 1 𝑑𝑇
𝑑𝑄 = − 𝑛𝑘𝑐̅𝜆 ̅ dS. dt 2 𝑑𝑥 Từ (3) và (4) suy ra : 1 D = n k . c . 2
❖ Ý nghĩa của D : 3 D ~ 2 T D p
→Nhiệt độ càng cao chênh lệch nhiệt độ càng cao suy ra hiện tượng dẫn nhiệt càng nhanh.
4. 4. Hiện tượng nội ma sát
+ Theo quan điểm vĩ mô : Là hiện tượng sinh ra những lực ma sát giữa các lớp khí chuyển động
thành những dòng khí với vận tốc khác nhau. Lực nội ma sát nằm trên mặt tiếp xúc giữa 2 lớp
khí và là 1 trong 2 lực sau :
Lực kéo của lớp chất khí chảy nhanh tác dụng lên lớp chất khí chảy chậm hơn f .
Lực hãm của lớp chất khí chảy chậm tác dụng lên lớp chất khí chảy nhanh hơn ' f . 18
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC d f = dS dx
:hệ số nội ma sát ( hệ số nhớt ) (kg/ms) ; Ns/m2
+ Theo quan điểm vi mô : Hiện tượng nội ma sát là do sự trao đổi động lượng giữa các phân tử
khí khi va chạm với nhau. 1 d f = − c dS 3 dx 1 = c 3
❖ Ý nghĩa của hệ số nhớt : 3 ~ 2 T p
+ Đối với chất khí : khi nhiệt độ tăng thì hệ số nhớt tăng và khi nhiệt độ giảm thì hệ số nhớt giảm.
+ Đối với chất lỏng : khi nhiệt độ tăng thì hệ số nhớt giảm và ngược lại.
II. PHƯƠNG PHÁP GIẢI
+ Xác định đúng loại hiện tượng truyền nhiệt ( hiện tượng khuếch tán, hiện tượng dẫn nhiệt, hiện tượng nội ma sát).
+ Áp dụng công thức đối với hiện tượng tương ứng. III. BÀI TẬP MẪU
THÍ DỤ . Bơm 1 mol khí oxy vào bình cứng, dung tích 22,4 lít đến áp suất 1,0atm. Đường kính
phân tử oxy d = 2,9.10-10m, số Avôgadrô NA=6,023.1023mol-1. Xác định mật độ phân tử khí và
quãng đường tự do trung bình của chúng. GIẢI
a) Tính mật độ phân tử khí 19
HỆ THỐNG BÀI TẬP VẬT LÍ PHÂN TỬ & NHIỆT HỌC pV = RT (1) Mà ta lại có :
p = nkT thế vào (1) thì ta được : nkTV = RT R 25 3 n = 10 . 7 , 2 − = m kV
b) Tính quãng đường tự do trung bình của chúng k T . . 1 = = . 4 2. r . 2 . p 2. d . 2 n . . 1 = = mm 1 2. .( 10 . 9 , 2 10 − )2 10 . 7 , 2 . 25 IV. BÀI TẬP
BÀI 1 : Không khí trong bình đã được hút tới áp suất 6
10− mmHg . Bán kính của phân tử không kg khí bằng −8 5 ,
1 .10 cm, khối lượng một kmol = 29
, nhiệt độ của không khí bằng 0 17 C . kmol Tính:
a) Quãng đường tự do trung bình của phân tử.
b) Số va chạm trung bình trong đơn vị thời gian.
BÀI 2 : Biết hằng số Boltzmann k =1,38.10-23J/K, hằng số khí lí tưởng R = 8,31 J/mol.K. Nêu
tên của khí lý tưởng hai nguyên tử sau đây trong bình cứng, nếu :
a) Khí có áp suất 0,997.105Pa, nhiệt độ 27oC, khối lượng riêng 80g/m3
b) Khí có khối lượng 24g, áp suất 2,5.105Pa, động năng trung bình của phân tử là 3,89.10-22 J. Dung tích bình 7,5 lít.
BÀI 3 : Tính quãng đường tự do trung bình của phân tử khí CO2 ở nhiệt độ 100oC và áp suất
13,33Pa. Đường kính phân tử CO2 bằng 3,2.10-7mm.
BÀI 4 : Tính quãng đường tự do trung bình của phân tử không khí ở điều kiện chuẩn. Đường
kính của phân tử không khí quy ước bằng 3.10-10m.
BÀI 5 : Tính số va chạm trung bình trong 1 giây của phân tử nitơ ở nhiệt độ t = 27oC và áp suất
p = 400mmHg. Đường kính của phân tử nitơ bằng 3.10-10m. 20




