






































Preview text:
Lý sinh y học PGS.TS. Trần Quang Huy
Email: huy.tranquang@phenikaa-uni.edu.vn
Chương 3: ĐIỆN SINH HỌC VÀ ĐIỆN ỨNG DỤNG TRONG Y HỌC 3.1 Điện thế sinh vật
3.2 Cơ chế của điện thế sinh vật
3.3 Điện thế của một số của tổ chức sống
3.4 Tác dụng của dòng điện lên cơ thể sống
3.5 Điện ứng dụng trong y học
3.1. Điện thế sinh học của tế bào a) Điện thế nghỉ
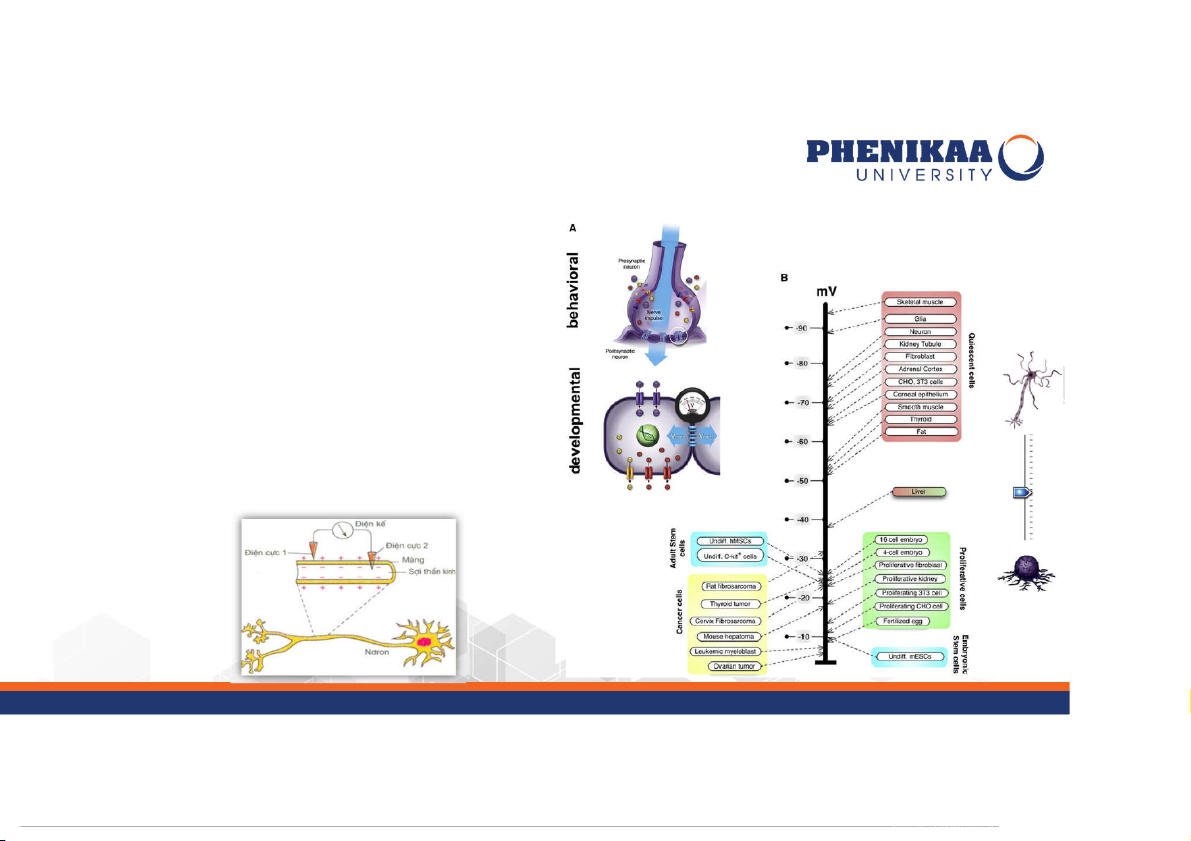
- Chênh lệch về điện thế bên trong và ngoài tế bào: điện thế
nghỉ (hay điện thế tĩnh)
- Ở trạng thái bình thường (tĩnh), điện thế màng luôn ổn định và mang dấu âm
- Các tế bào khác nhau, điện thế nghỉ: -50 mV – (-94 mV)
- Sự hình thành điện thế nghỉ
+ Sự chênh lệch nồng độ của 3 loại ion vô cơ quan trọng Na+, K+, và Cl- ở trong và ngoài màng tế bào
+ Tính thấm có chọn lọc của màng tế bào đối với ion.
+ Bơm ion (bơm K+ – Na+ - ATPase) *Vai trò:
+ Bơm ion tạo nên và duy trì sự chênh lệch nồng độ của các ion giữa hai phía của màng
+ Màng tế bào duy trì sự chênh lêch điện thế giữa hai phía của màng;
+ Sự vận chuyển của các ion qua màng một cách có chọn lọc
- Lý thuyết ion màng về điện thế nghỉ
+ Theo Bernstein: ở trạng thái tĩnh, màng chỉ thấm đối với K+ và không thấm đối với ion Na+ cũng như các ion liên kết với ion K+
+ Vì nồng độ các ion K+ trong tế bào lớn hơn bên ngoài màng tế bào rất nhiều nên ion K+ không ngừng khuếch tán
qua màng. Trong khi đó, lực hút tĩnh điện các anion và cation đã giữ chúng ở lại màng và làm cho màng bị phân cực một cách bền vững.
+Sự phân bố không đồng đều các ion do tính thấm chọn lọc của màng là nguyên nhân tạo ra điện thế nghỉ. Nồng độ ion trong bào Nồng độ ion ngoài màng tương (mM) (mM) Đối tượng Na+ K+ Cl- Na+ K+ Cl- Thần kinh ếch 37 110 26 110 2,6 77 Cơ ếch 37 125 1,2 110 2,6 77 Tim chuột cống 13 140 1,2 150 4,0 120 Cơ vân của chó 12 140 1,2 150 4,0 120
- Điện thế nghỉ U được xác định bởi tỷ số các nồng độ ion K+ (hoặc ion Cl-) có khả năng khuếch tán qua màng ở trong và bên ngoài tế bào [K+ ] [Cl− ] U=0,08lg trong = 0,08lg ngoài [K+ ]ngoài [Cl− ]trong
- Bằng thực nghiệm Boyle và Convey đã chứng minh rằng khi nồng độ ion K+ ở môi trường ngoài có giá trị từ 13-300
mg/l, các ion Cl- và K+ được phân bố ở hai phía của màng đúng theo quy luật cân bằng Donnan [K+ ]trong [Cl− ] = ngoài [K+ ]ngoài [Cl− ]trong
- Lý thuyết trên bị bác bỏ, khi kỹ thuật đánh dấu phóng xạ được áp dụng => phát hiện ion Na+ cũng có thể xâm nhập
qua màng đi vào trong tế bào
- Bằng đánh dấu phóng xạ => giá trị đúng của điện thế nghỉ cần đưa thêm vào công thức hệ số thấm của màng tế bào
đối với các ion K+, Na+, Cl- - Theo Goldman, nếu:
+ Màng tế bào có tính chất đồng nhất và điện trường ở đó không đổi
+ Dung dịch điện ly coi như lý tưởng, nghĩa là không có yếu tố nào ngăn cản các ion đến tiếp xúc với các điện cực
+ Chỉ có các ion hóa trị 1 tham gia vào sự hình thành điện thế nghỉ
+ Môi trường ở hai phía màng tế bào rộng vô tận. Khi đó điện thế nghỉ sẽ được tính theo công thức sau: P
U=RTln K[K+ ]trong + PNa[Na+ ]trong + PCl[Cl− ]ngoài F
PK[K+ ]ngoài + PNa[Na+ ]ngoài + PCl[Cl−]trong
Trong đó, P , P , P là hệ số thấm của màng lần lượt đối với các ion K+, Na+, Cl- K Na Cl - Bơm Na+ – K+ - ATPase
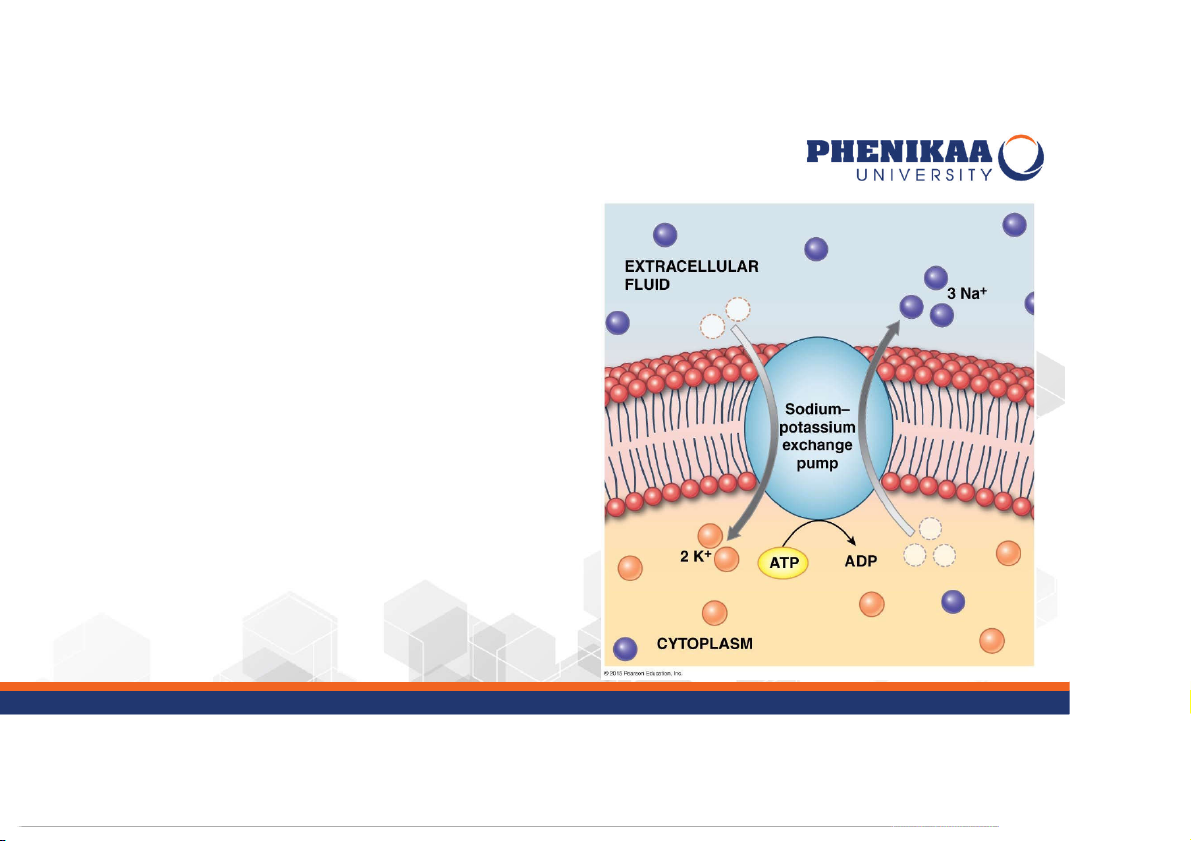
+ Về bản chất là protein xuyên màng, khi hoạt động sử dụng
năng lượng từ phản ứng thủy phân ATP.
+ Mỗi phân tử ATP thủy phân sẽ cung cấp năng lượng để vận
chuyển – “bơm” 3 ion Na+ ra ngoài và 2 ion K+ vào trong tế bào
ngược chiều gradient nồng độ của mỗi ion.
“Sự tồn tại của điện thế nghỉ chính là đặc trưng của tế
bào sống” hay “Sự chênh lệch nồng độ của các ion Na+,
K+, và Cl- được tạo ra và duy trì bởi các bơm ion là biểu
hiện sức sống của tế bào” - Điện thế cân bằng:
+ Điện thế màng: là sự khác biệt về điện thế giữa bên trong và bên ngoài tế bào
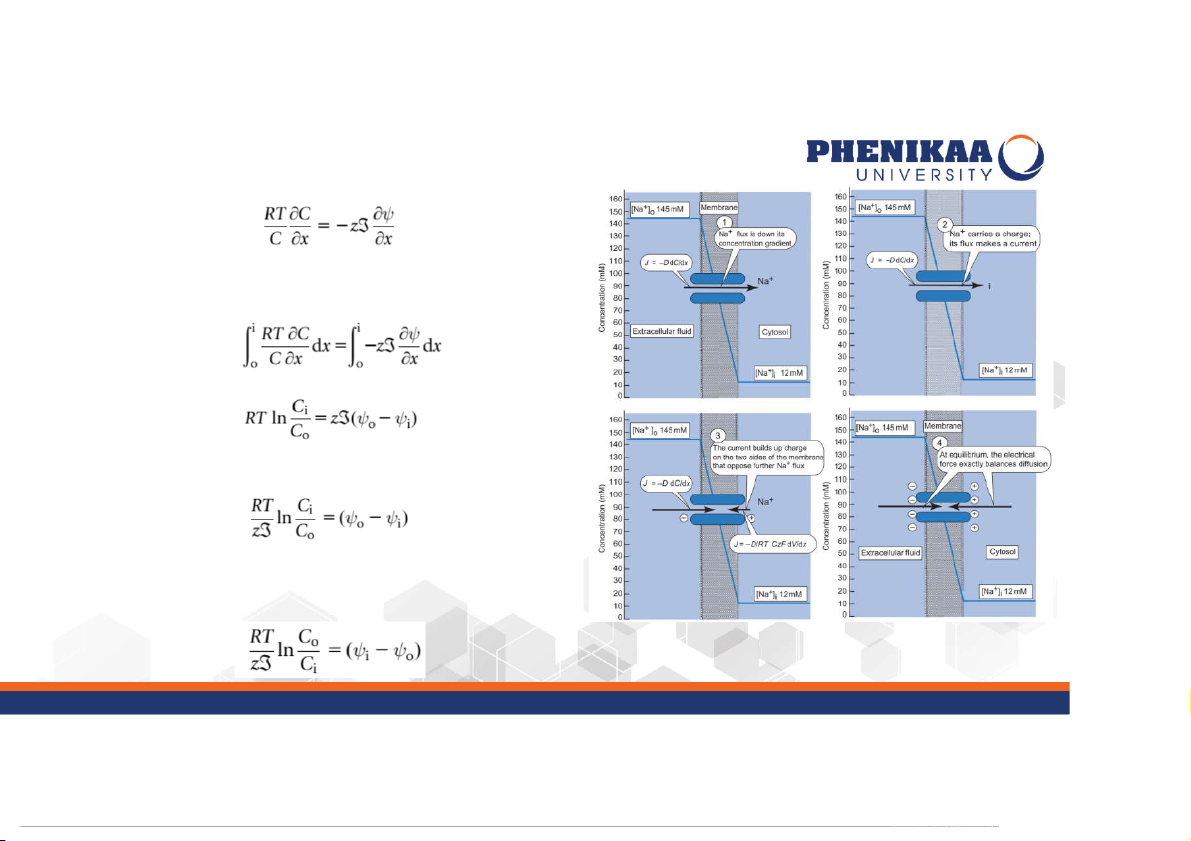
+ Giả sử màng chỉ thấm với các ion Na+, thế cân bằng Na tính
toán theo: định luật Fick dạng và phân tích năng lượng.
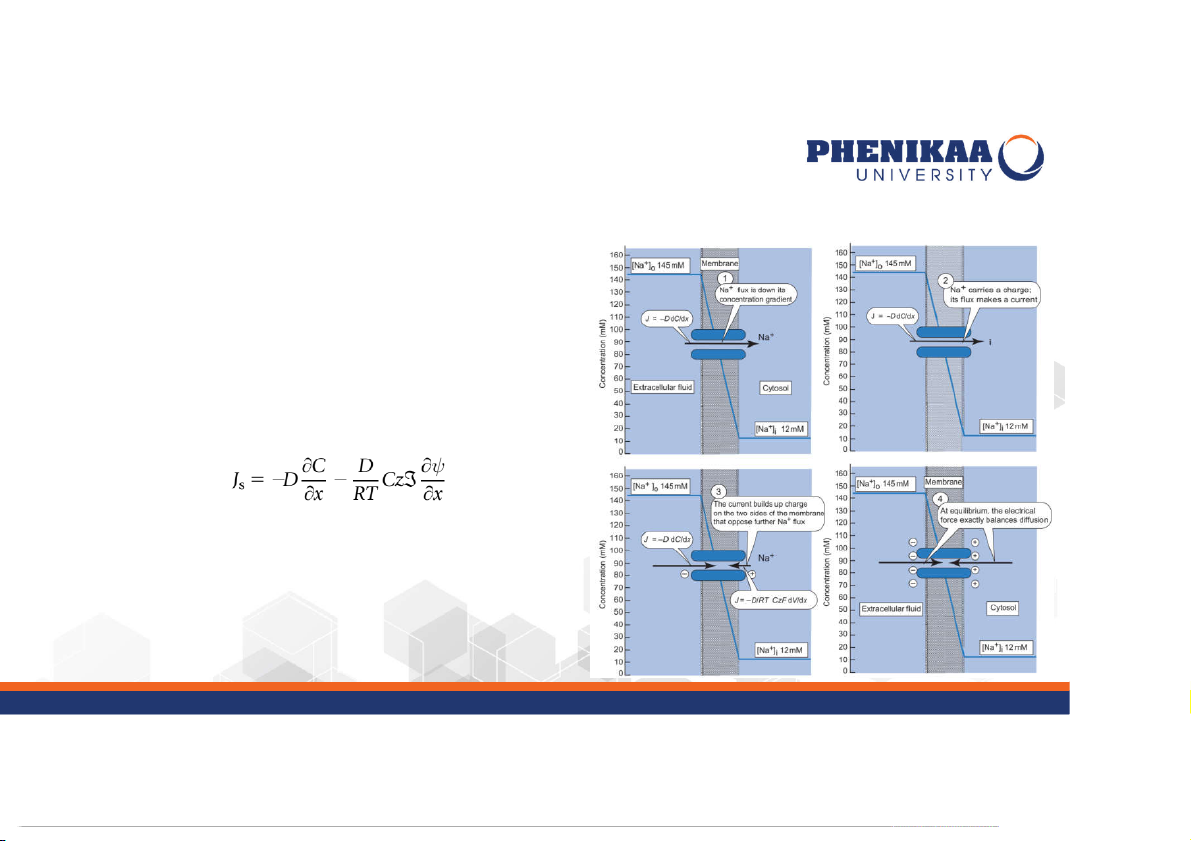
+ Định luận Fick với một lực điện:
J : thông lượng chất tan; D: hệ số khuếch tán; C là nồng độ Na+, R: s
hằng số khí; T: nhiệt độ tuyệt đối; z: điện tích của ion; Ʒ: Faraday (số coulombs/mol)
+ Ở trạng thái cân bằng, J = 0 => lực khuếch tán và lực hiện: s
+ Tích phân cả hai phía từ ngoài vào trong màng: + Thế màng cân bằng
Thường các nhà sinh lý lấy dung dịch phía ngoài làm nền (ψ =0) o => Phương trình Nernst:
Thế màng tại đó lực khuếch tán đúng bằng lực điện
- Thế cân bằng cho K+ mang giá trị âm
+ Giả sử màng không thấm với ion Na+ và Cl-, chỉ thấm với K+
+ Theo gradient nồng độ, K+ sẽ khuếch tán ra ngoài màng tạo ra một dòng điện và tích điện dương ở bên ngoài màng. + Phương trình Nernst:
[K+] = 4 x10-3 M và [K+] = 155 x10-3 M => E = -0,0977V hay -97,7 mV o i K
- Phương trình Nernst cho Cl:
(z=-1 vì ion clo tích điện âm)
b) Điện thế hoạt động trên tế bào thần kinh
- Neuron = đơn vị cấu trúc của hệ thần kinh. Được cấu tạo bởi các than (soma) và các sợi trục




