Preview text:
Bài tập chương 6: Cân bằng lỏng – rắn
Câu 1: nêu một số đặc điểm của điểm eutecti trên giản đồ pha của hệ hai cấu tử A và B
Câu 2: a. Vẽ giản đồ thành phần – nhiệt độ nóng chảy của hỗn hợp đồng – niken dựa vào bảng số liệu sau: Ni (%) 0 20 40 60 80 100 Nhiệt độ bắt đầu 1373 1467 1554 1627 1683 1728 kết tinh (K) Nhiệt độ kết 1373 1406 1467 1543 1629 1728 thúc kết tinh (K)
b. Ghi trên giản đồ các điểm:
- cân bằng giữa đồng nguyên chất lỏng và rắn
- hỗn hợp nóng chảy chứa 45% Ni cân bằng với dung dịch rắn
- Hỗn hợp nóng chảy cân bằng với dung dịch rắn chứa 65% Ni
- Hỗn hợp nóng chảy có 50% Ni ở 1670 K
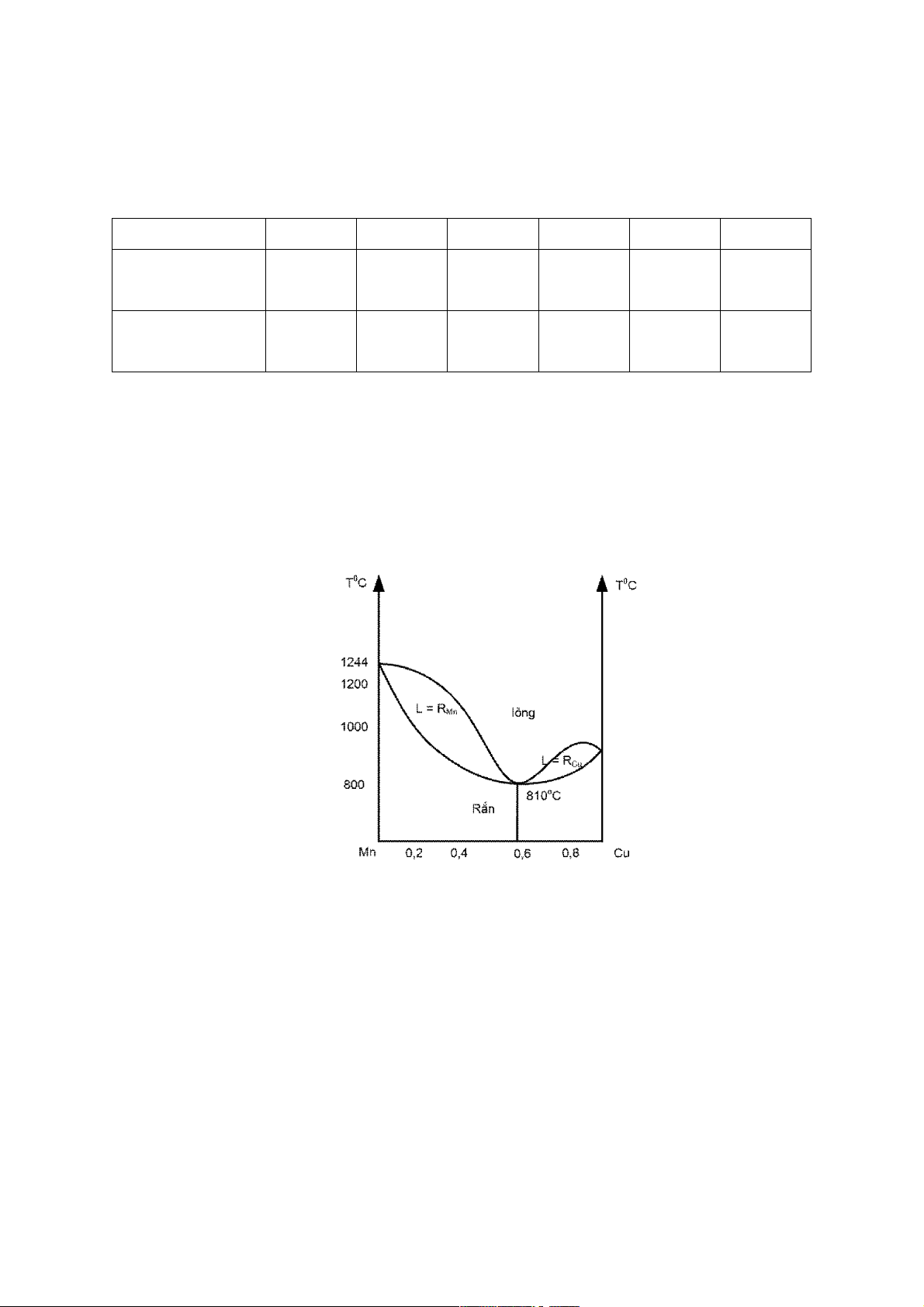
Câu 3: Phân tích các miền, các đường cân bằng và các điểm cân bằng của giản đồ pha sau:
Bài 4: Áp suất hơi của Cl2 rắn là 2,64 mmHg ở - 112oC và 0,26 mmHg ở - 126,5oC. Áp suất hơi
của Cl2 lỏng là 11,9 mmHg ở - 100oC và 58,7 mmHg ở - 80oC.
a. Hãy xác định phương trình phụ thuộc nhiệt độ của áp suất hơi bão hòa.
b. Xác định nhiệt độ và áp suất tại điểm ba.
c. Xác định nhiệt nóng chảy, nhiệt hóa hơi và nhiệt thăng hoa trung bình của Cl2.
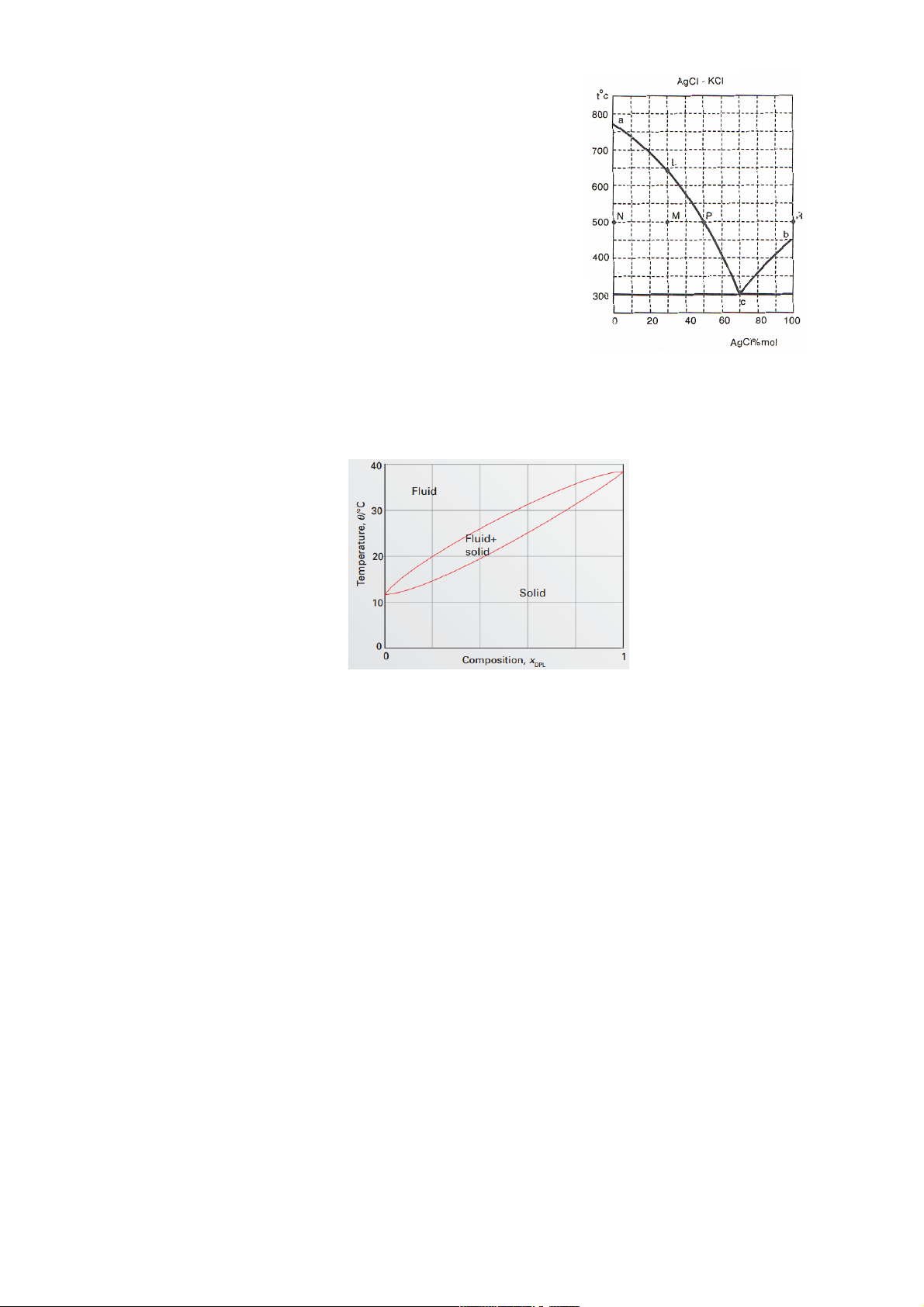
Bài 5: Cho giản đồ pha "Nhiệt độ - Thành phần (% mol)" của
hệ AgCl - KCl như hình vẽ:
a. Từ giản đồ, hãy xác định điểm nóng chảy của AgCl và KCl.
b. Xác định nhiệt độ, số pha và thành phần của hệ M.
c. Nếu có 10 mol hệ M, xác định thành phần hệ N và P.
d. Cân thêm bao nhiêu AgCl ở 500oC vào hệ M để hệ thành đồng thể.
Bài 6: Giải thích quá trình làm lạnh từ 45°C của hỗn hợp lỏng gồm
Dielaidoylphosphatidylcholine (DEL) và Dipalmitoylphosphatidylcholine (DPL) có thành phần xDEL=0,5
Giản đồ nóng chảy của DEL và DPL.




