






Preview text:
LOGO CH3050 - HÓA LÝ I
TS. Nguyễn Thị Tuyết Mai
Bộ môn Hóa lý, Viện Kỹ thuật Hóa học
Trường Đại học Bách Khoa Hà Nội
Email: mai.nguyenthituyet1@hust.edu.vn 1 Chương 5. HÓA LÝ I
CÂN BẰNG LỎNG – LỎNG
1. Hệ 2 chất lỏng không tan lẫn
2. Sự phân bố chất tan vào hai dung môi không
tan lẫn. Định luật phân bố Nernst
3. Hệ 2 chất lỏng tan lẫn có giới hạn 2 CB LỎNG –LỎNG Áp suất hơi
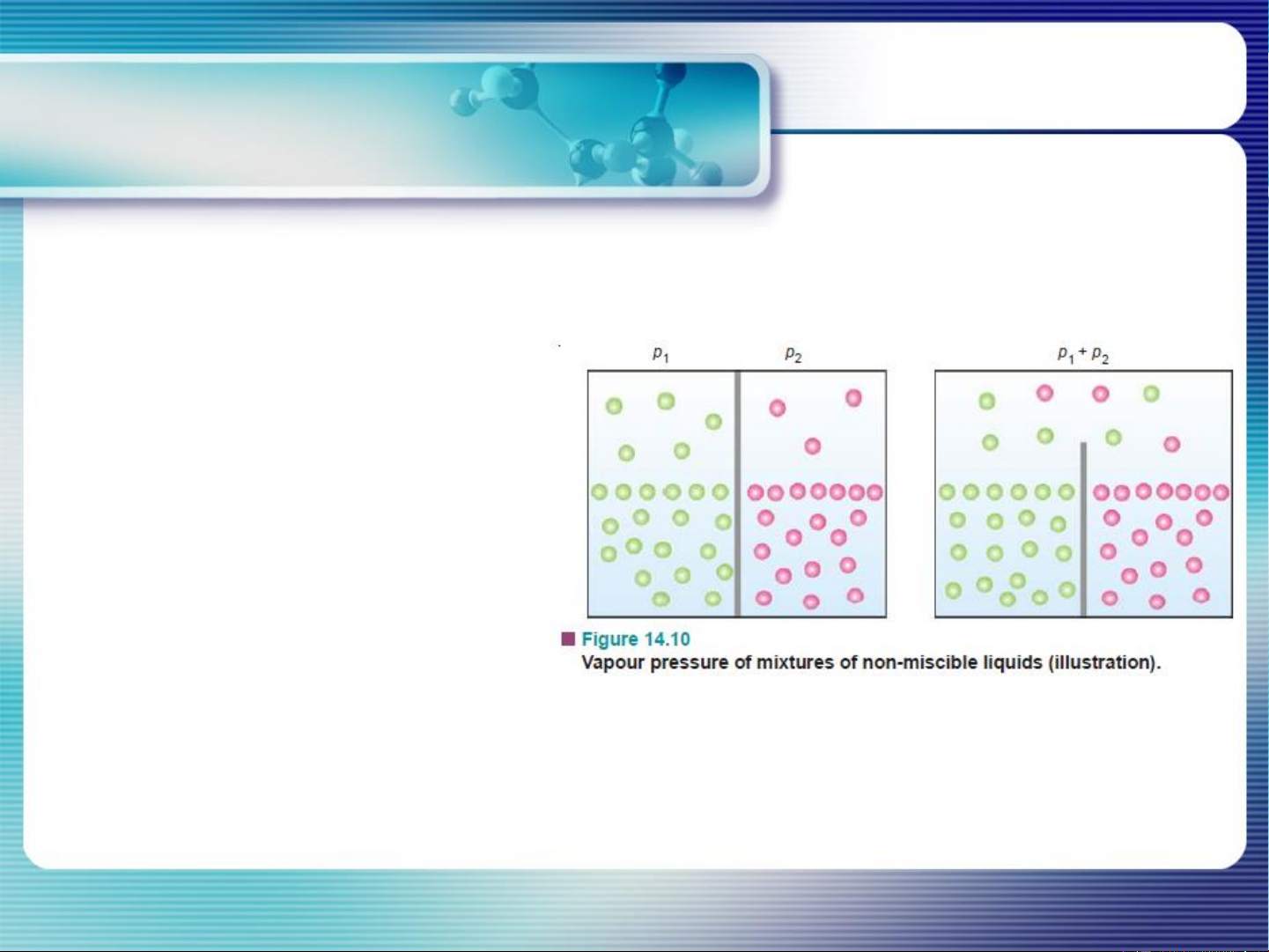
Hệ 2 chất lỏng không tan lẫn
2 chất lỏng ko tan lẫn: x =1 và x =1 P = P* ; P = P* A B A A B B
P = P + P P= P* + P* A B A B
P > P ; P Ts < Ts ; Ts A B hh A B
Ts của hỗn hợp 2 chất lỏng ko tan lẫn thấp hơn
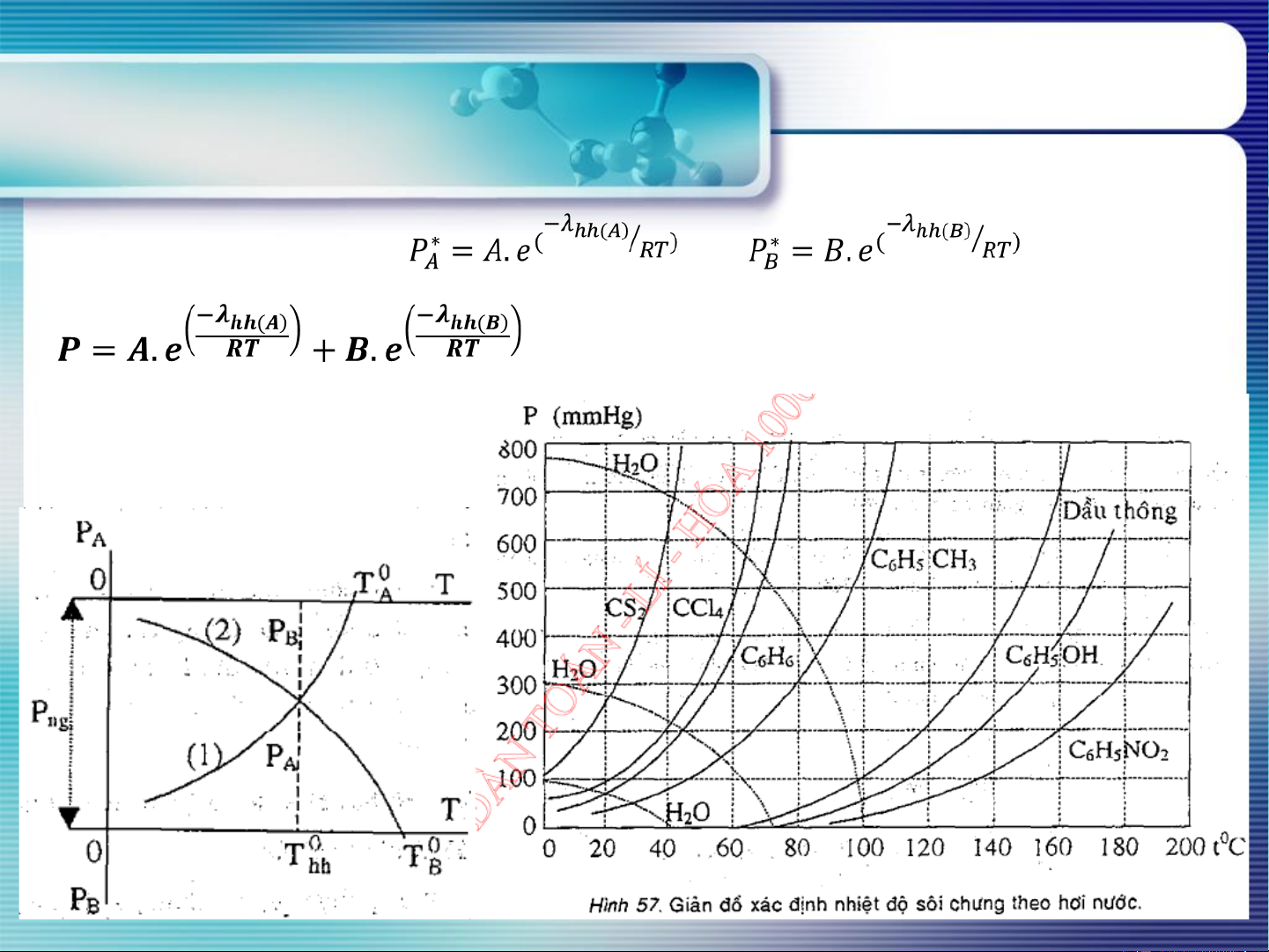
Ts của từng chất lỏng nguyên chất 3 CB LỎNG –LỎNG Nhiệt độ sôi
Hệ 2 chất lỏng không tan lẫn PT Clausius Clapeyron: P = H Ts 4 CB LỎNG –LỎNG
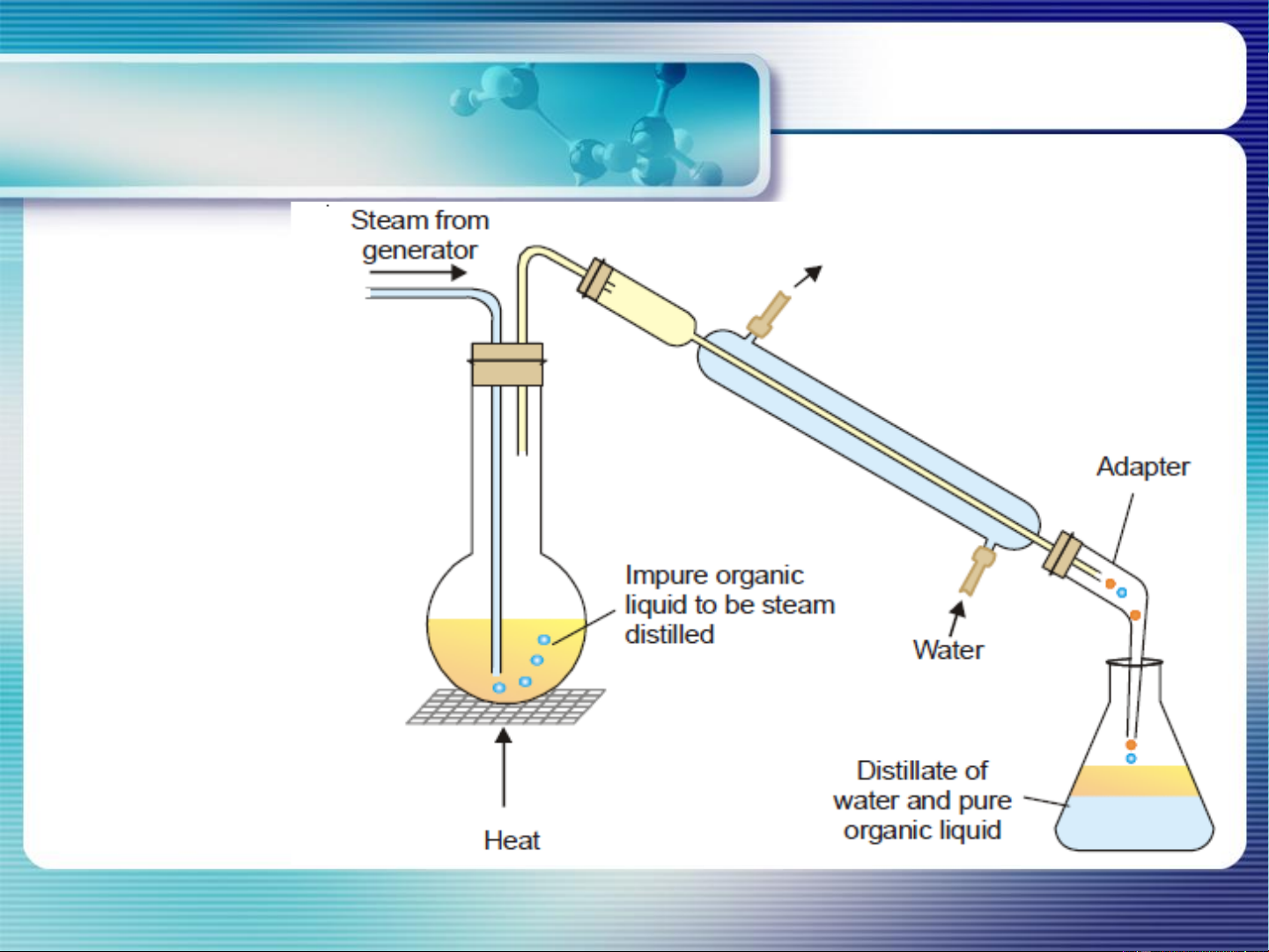
Chưng cất lôi cuốn theo hơi nước
Hệ 2 chất lỏng không tan lẫn Ts < Ts ; Ts hh A B 5 CB LỎNG –LỎNG
Chưng cất lôi cuốn theo hơi nước
Hệ 2 chất lỏng không tan lẫn
Xđ lượng hơi nước tối thiểu để chưng cất chất A: P = P + P = P* + P* H2O A H2O A
Lượng nước tối thiểu (g)
để chưng cất 1 kg chất A:
VD: hệ Benzen-H O sôi ở 66 oC. Biết P* = 540 mmHg. 2 C6H6
Tính lượng hơi nước tối thiểu để chưng cuốn 1 kg C H ở 66 oC 6 6 ĐS: 94 g 6 Chương 5. HÓA LÝ I
CÂN BẰNG LỎNG – LỎNG
1. Hệ 2 chất lỏng không tan lẫn
2. Sự phân bố chất tan vào hai dung môi không
tan lẫn. Định luật phân bố Nernst
3. Hệ 2 chất lỏng tan lẫn có giới hạn 7
Định luật phân bố Nernst CB LỎNG –LỎNG
Hệ 2 chất lỏng không tan lẫn
Xét cân bằng lỏng – lỏng trong hệ 2 chất lỏng ko tan lẫn A và B
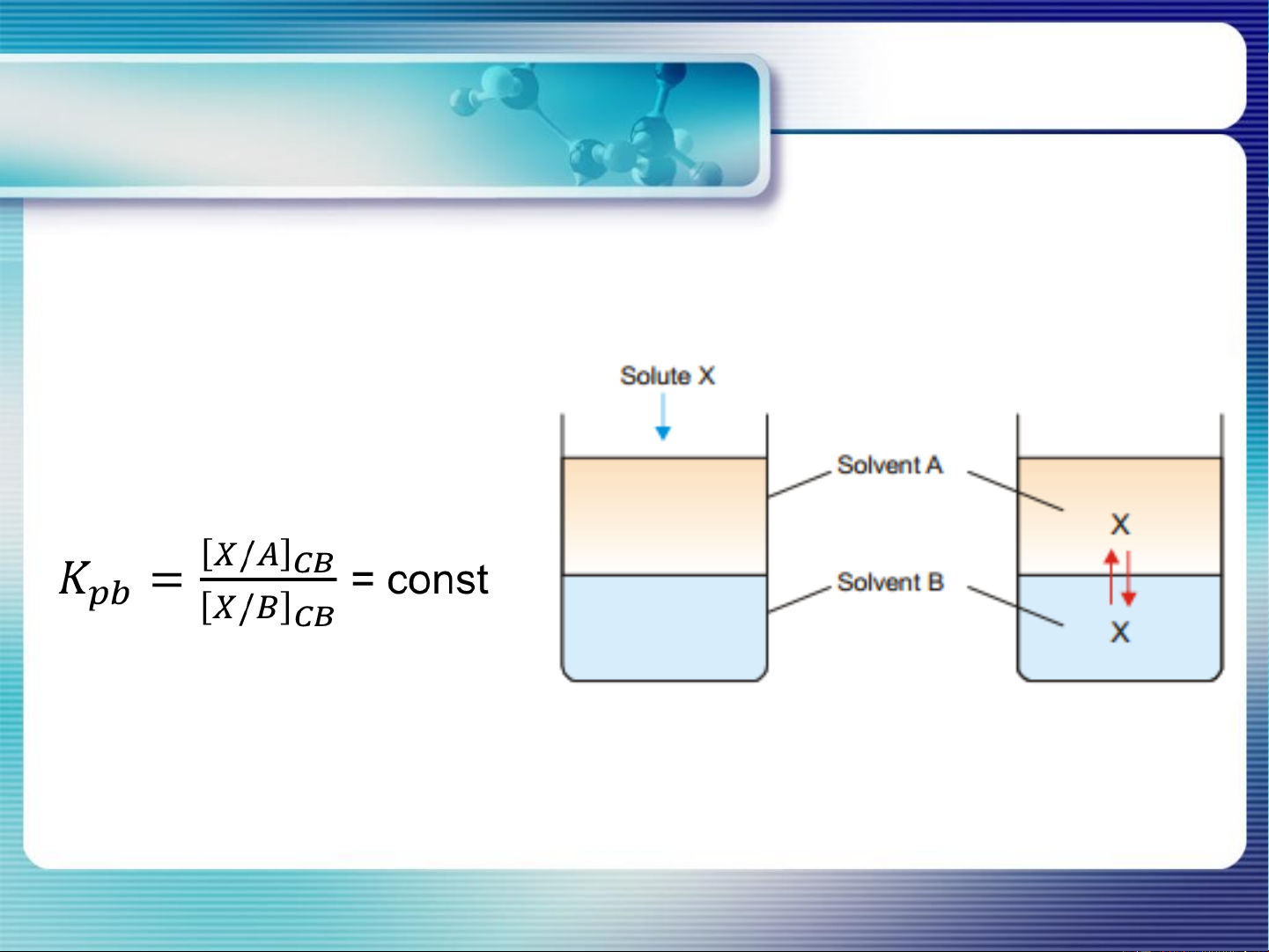
Nếu có 1 cấu tử thứ 3 (chất X) tan vào cả 2 chất lỏng A và B dd X/A dd X/B C = K – f + 2 = 3 T, P = const C = 1
ĐL phân bố Nernst:
Ở điều kiện T, P = const, tỉ số nồng độ của 1 chất tan trong
2 dung dịch không tan lẫn ở TTCB là một hằng số: Kpb 8
Định luật phân bố Nernst CB LỎNG –LỎNG
Hệ 2 chất lỏng không tan lẫn
VD: lấy 10 ml dung dịch I trong CCl có nồng độ C = 4 g/l 2 4 0
trộn với 120 ml H O, lắc kỹ đến khi đạt cân bằng thì nồng độ 2
của I trong H O ở trạng thái cân bằng là 0,04 g/l 2 2 a/ Xác định Kpb
b/ nếu thêm 5 ml dung dịch I /CCl vào bình và tiếp tục lắc 2 4
đến khi cân bằng thì nồng độ I trong H O bằng bao nhiêu? 2 2
ĐS: K = 88; [I /H O] = 0,042 g/l pb 2 2 cb 9
Định luật phân bố Nernst CB LỎNG –LỎNG
Hệ 2 chất lỏng không tan lẫn
Ứng dụng: quá trình chiết tách, trích ly 2 3 10
Định luật phân bố Nernst CB LỎNG –LỎNG
Hệ 2 chất lỏng không tan lẫn
Ứng dụng: quá trình chiết tách, trích ly
VD (câu 5): Hệ số phân bố iot I giữa nước và sulphua carbon CS 2 2 bằng K = C /C
= 0,00167. Tính lượng iot có thể rút ra từ 2.10- H2O CS2
3 m3 nước chứa 2.10-5 kg iot, nếu biết:
a) Dùng 0,05.10-3 m3 CS chiết một lần, 2
b) Dùng lượng CS đó chiết 5 lần. 2
ĐS: 1,875.10-5 kg và 1,998.10-5 kg 11 Chương 5. HÓA LÝ I
CÂN BẰNG LỎNG – LỎNG
1. Hệ 2 chất lỏng không tan lẫn
2. Sự phân bố chất tan vào hai dung môi không
tan lẫn. Định luật phân bố Nernst
3. Hệ 2 chất lỏng tan lẫn có giới hạn 12
Hệ 2 chất lỏng tan lẫn có giới hạn
MIXTURES OF LIQUIDS IN LIQUIDS
Partially miscible liquids
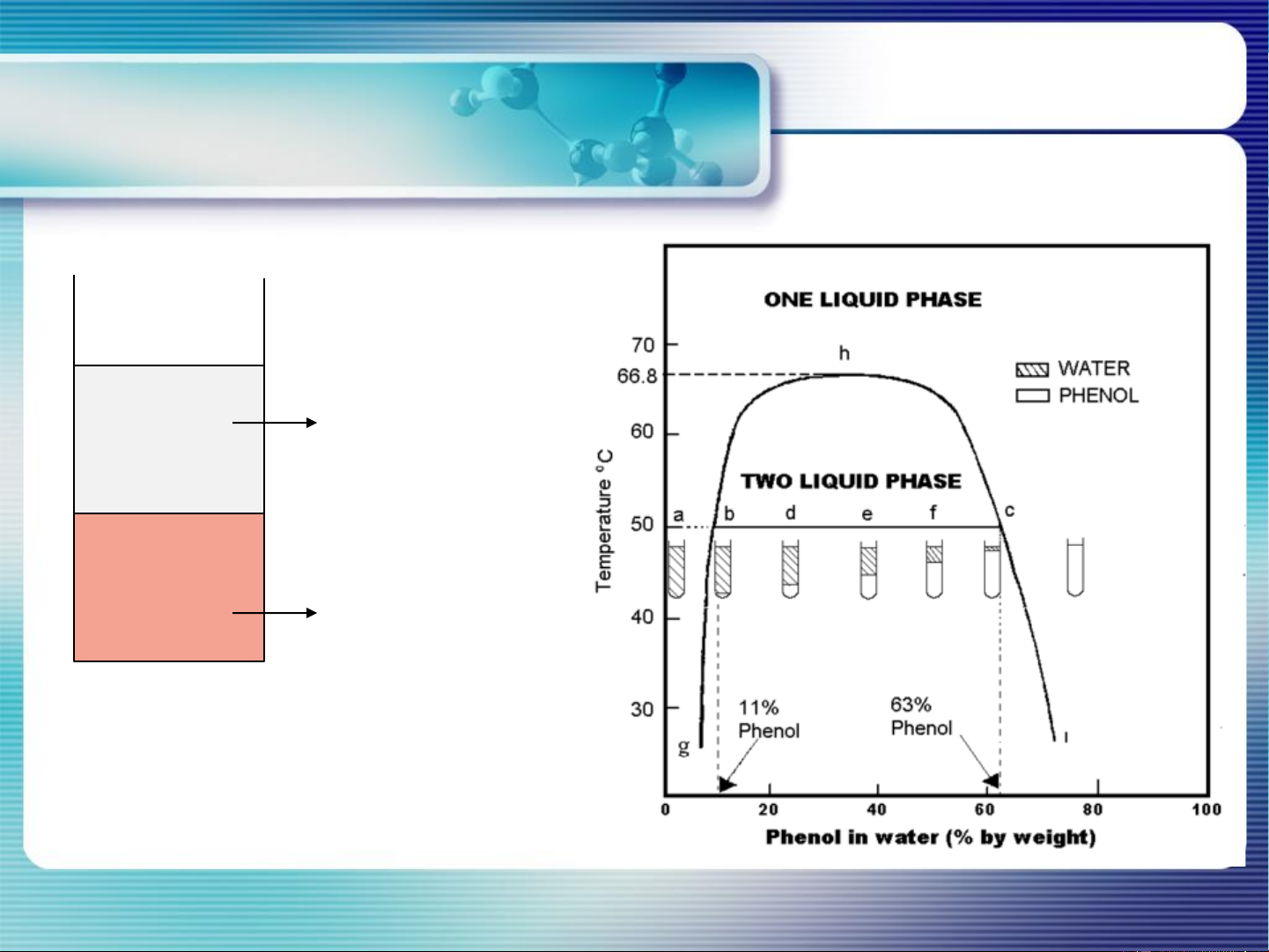
VD: hệ phenol – nước Lớp nước bão hòa phenol Lớp phenol bão hòa nước
Tỷ lệ khối lượng của 2 lớp tuân theo quy tắc đòn bẩy
Xét các quá trình đẳng nhiệt và biến nhiệt:…. 13
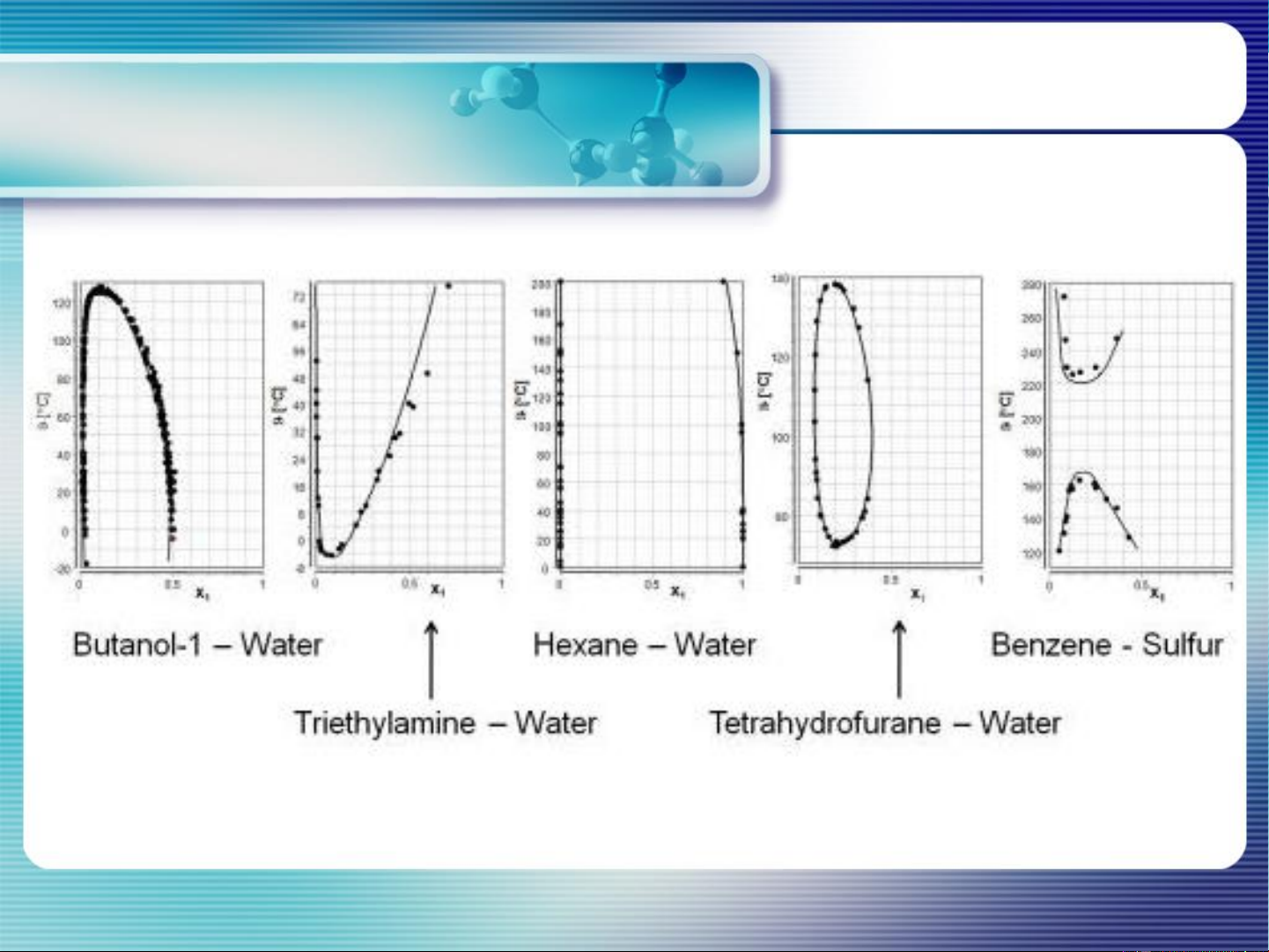
MIXTURES OF LIQUIDS IN LIQUIDS
Hệ 2 chất lỏng tan lẫn có giới hạn
Partially miscible liquids 14




