

Preview text:
LOGO CH3050 - HÓA LÝ I
TS. Nguyễn Thị Tuyết Mai
Bộ môn Hóa lý, Viện Kỹ thuật Hóa học
Trường Đại học Bách Khoa Hà Nội
Email: mai.nguyenthituyet1@hust.edu.vn 1 Chương 6. HÓA LÝ I
CÂN BẰNG LỎNG – RẮN
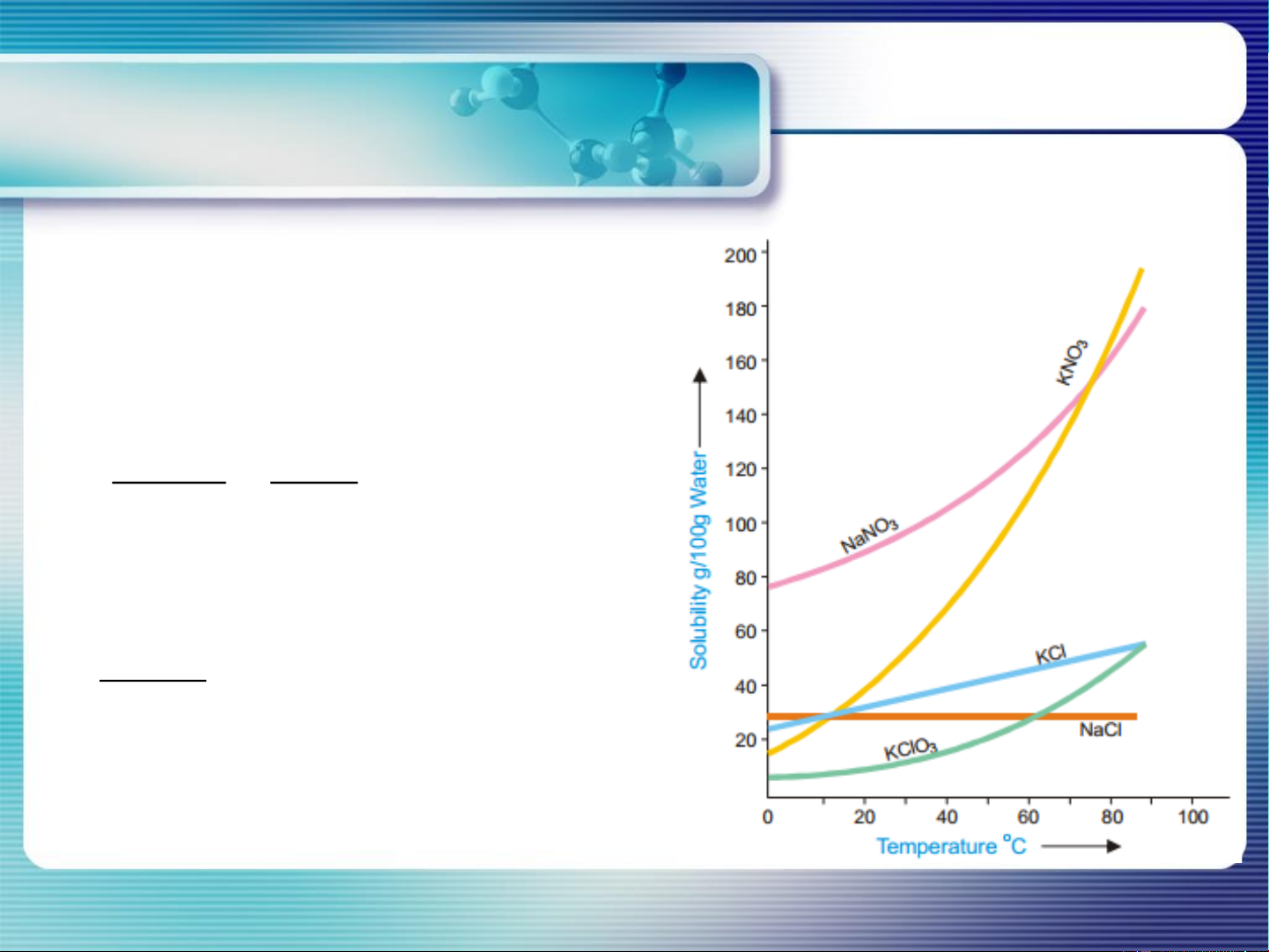
1. Sự hòa tan của chất rắn trong lỏng và các yếu tố ảnh hưởng
2. Sự kết tinh của dung dịch hai cấu tử 2
Sự hòa tan của chất rắn trong lỏng PHYSICAL CHEMISTRY 1 Properties of mixtures 3 PHYSICAL CHEMISTRY 1
Sự hòa tan của chất rắn trong lỏng Properties of mixtures
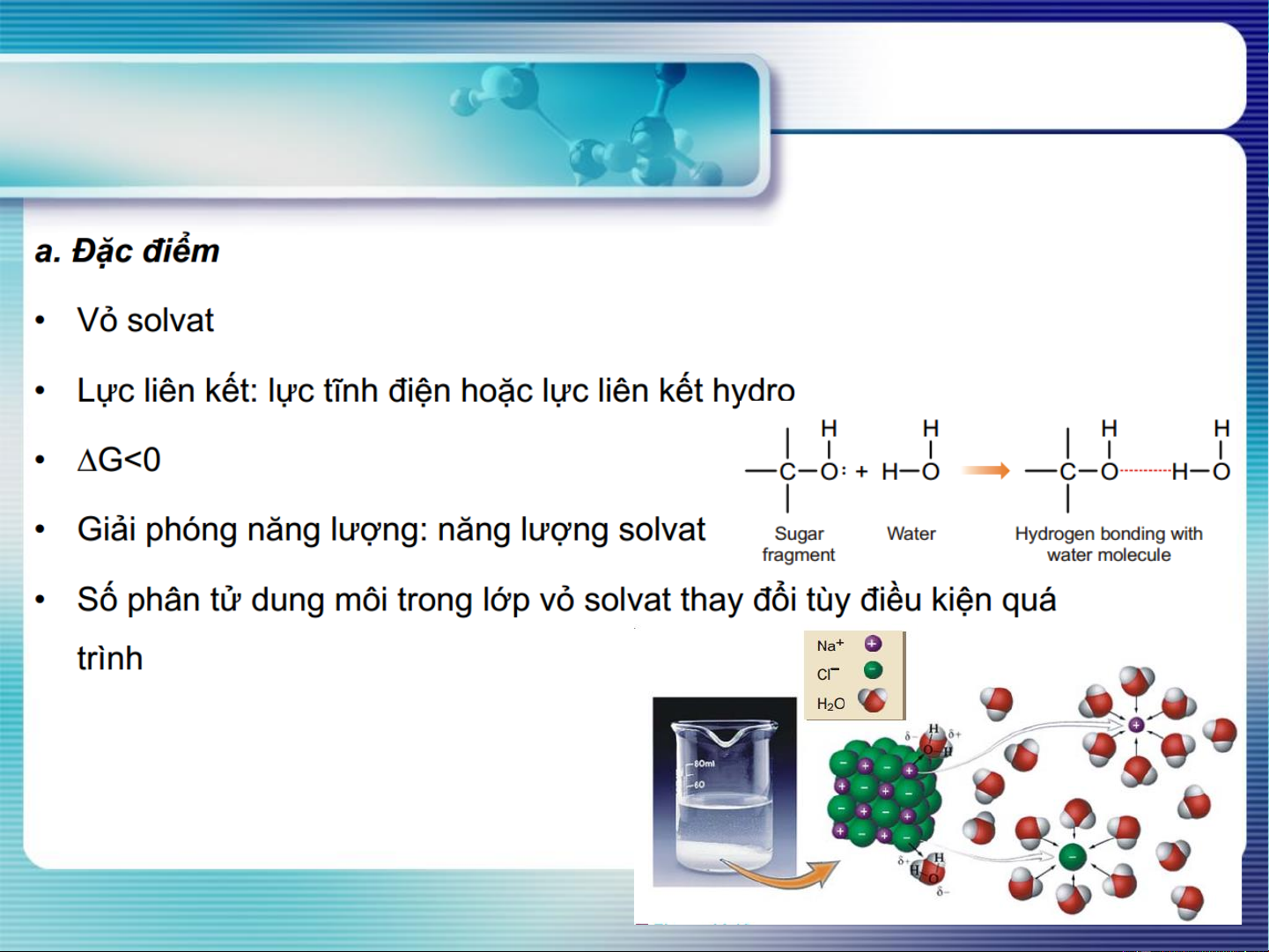
b. Các yếu tố ảnh hưởng:
• Bản chất dung môi và chất tan • Nhiệt độ: d ln x H A ht = PT Sreder 2 dT RT
QT hòa tan thu nhiệt: H > 0 ht d ln x A 0 dT
T tăng → độ hòa tan của R trong L tăng 4 Chương 6. HÓA LÝ I
CÂN BẰNG LỎNG – RẮN
2. Sự kết tinh của dung dịch hai cấu tử:
a. Hệ không tạo dung dịch rắn, không tạo hợp chất hóa học
b. Hệ không tạo dung dịch rắn, kết tinh tạo hợp chất hóa học bền
c. Hệ không tạo dung dịch rắn, kết tinh tạo hợp chất hóa học không bền
d. Hệ tạo thành dung dịch rắn tan lẫn vô hạn 5
Hệ không tạo dung dịch rắn, MIXTURES
không tạo hợp chất hóa học Solid-liquid equilibrium Ex: NaCl-H O; Ag-Pb
Biểu đồ kết tinh/nóng chảy 2 T = f(x)
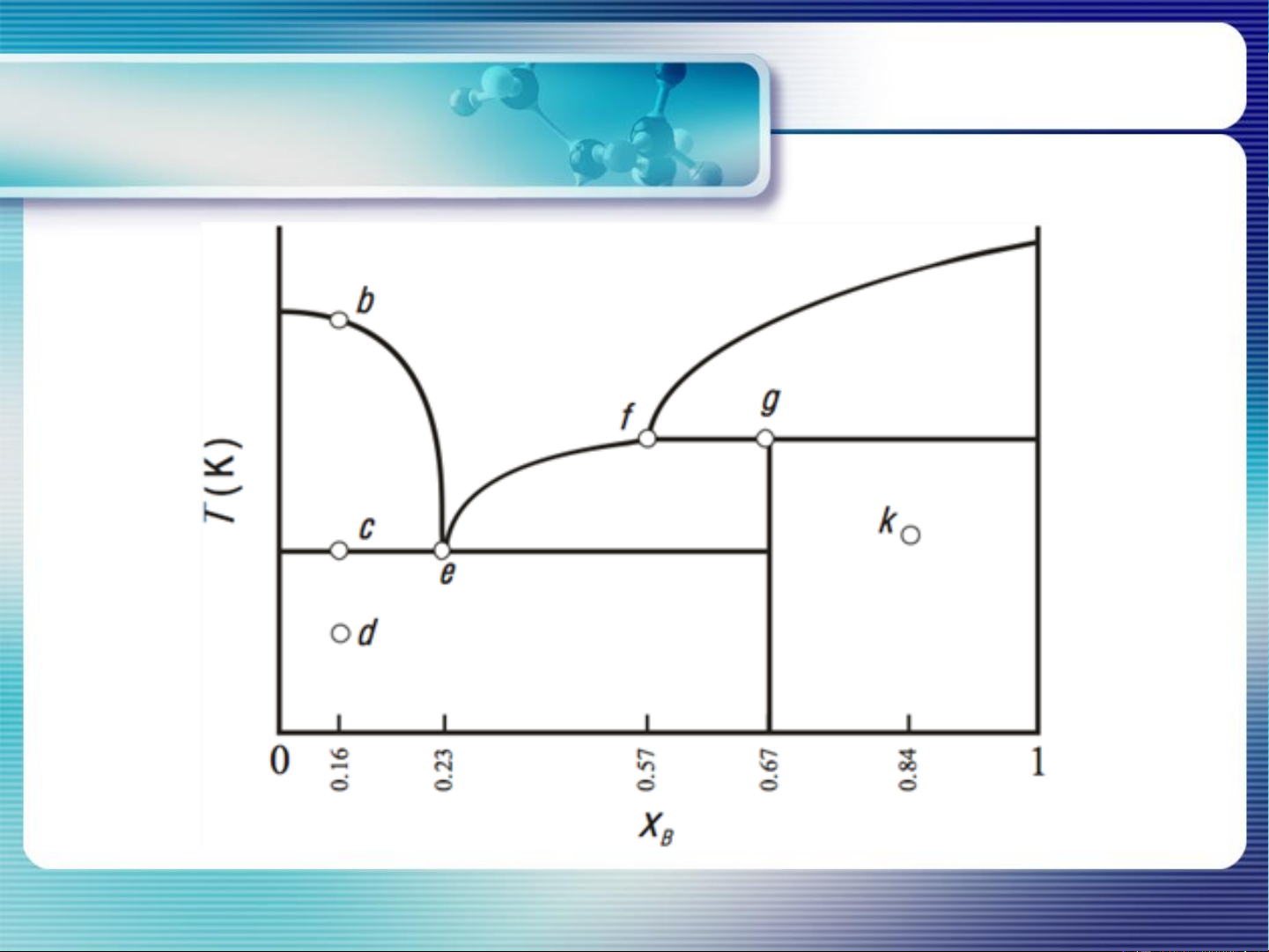
a, b: nhiệt độ kết tinh của A, B ngchất b Đường ae: Lỏng A-B
(nhiệt độ bắt đầu kt của R từ dd có A a
thành phần trong khoảng AE) L + RB Đường be: R + L A
(nhiệt độ bắt đầu kt của R từ dd B
có thành phần trong khoảng EB) R và A RB xB A E B 6
Hệ không tạo dung dịch rắn, MIXTURES
không tạo hợp chất hóa học Solid-liquid equilibrium
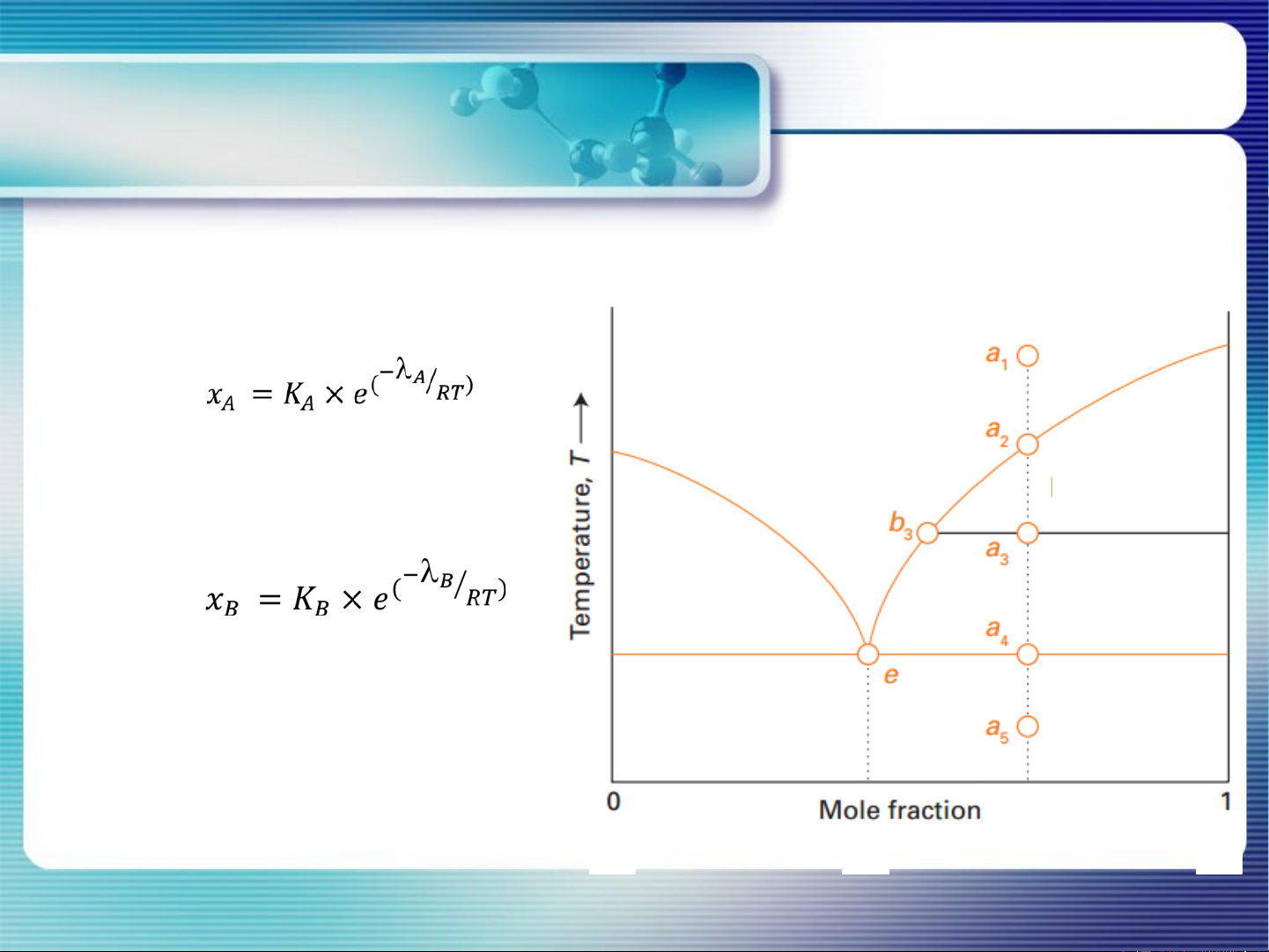
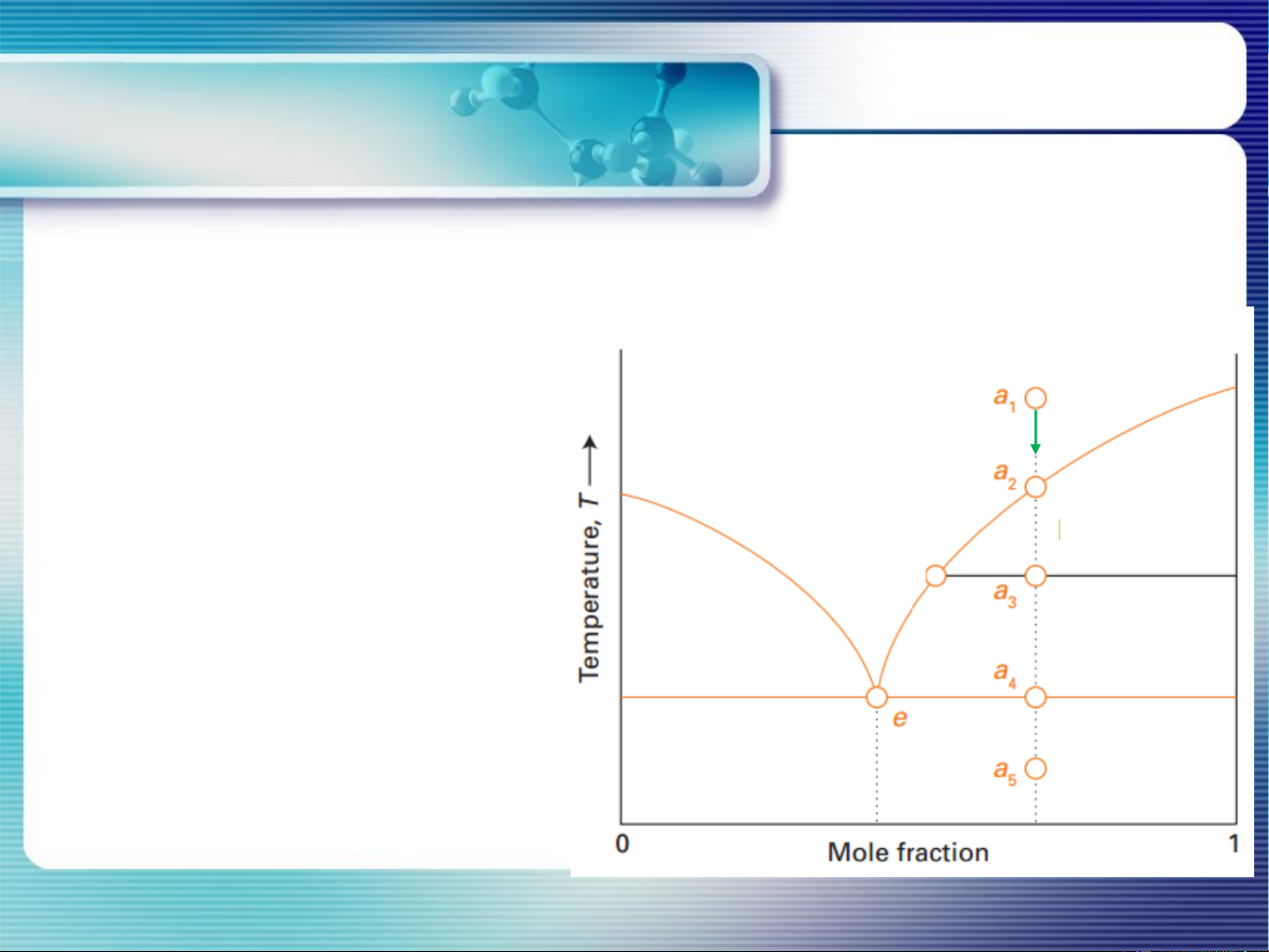
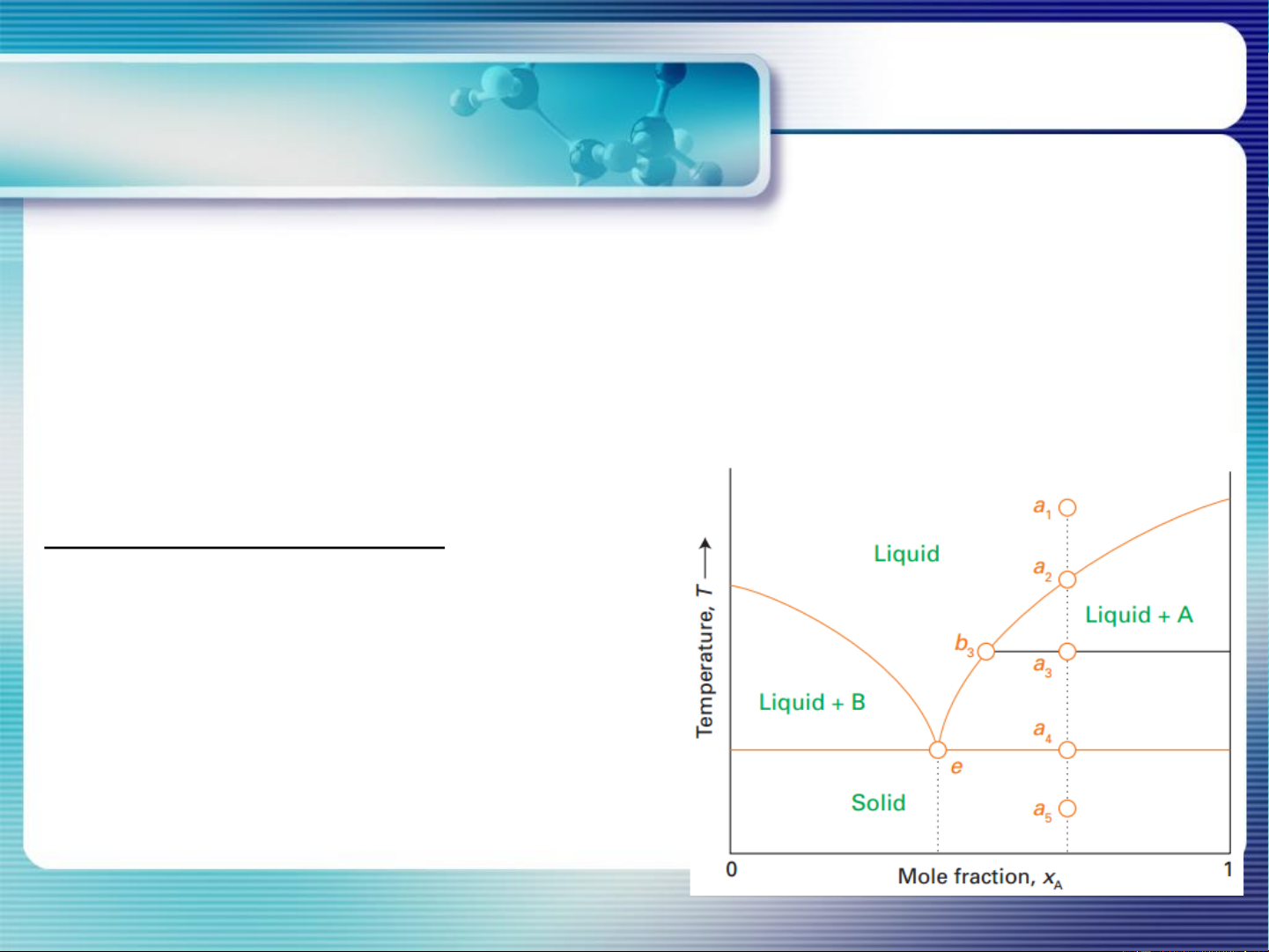
Quá trình kết tinh dd A-B ở điểm a1
Biểu đồ kết tinh/nóng chảy T = f(x)
a2: B(r) bắt đầu kết tinh Tkt b
a3: B(r) lỏng bão hòa B Lượng rắn Lỏng A-B B/lượng lỏng = L a /R a 3 3 3 3 a
Lượng hệ=Lượng rắn B+lượng lỏng L + RB L 3
tính B(r) tinh khiết tách ra khỏi hệ L R 3 3 R3
a4: B(r); dd bão hòa (A,B); A(r) R + L A
Tiếp tục làm lạnh: A và B kết tinh đồng thời: T =T = const R và kt E A a5: A(r) và B(r) xB 7
Hệ không tạo dung dịch rắn, MIXTURES
không tạo hợp chất hóa học Solid-liquid equilibrium
Điểm e là điểm Eutecti
Hỗn hợp có thành phần tương ứng ở điểm eutecti: hỗn hợp Eutecti
• Có nhiệt độ kết tinh thấp nhất
• Kết tinh ở T xác định duy nhất
• A và B kết tinh đồng thời với thành phần không đổi Ứng dụng của hh Eutecti:
T (dd) = T < T (A hoặc B nguyên chất) kt E kt
• thiếc hàn (thiếc 67% và chì 33%): T ~183oC E
• hỗn hợp nước đá-muối (77-23%): T = -21,1 oC E 8
Hệ không tạo dung dịch rắn, MIXTURES
không tạo hợp chất hóa học Solid-liquid equilibrium
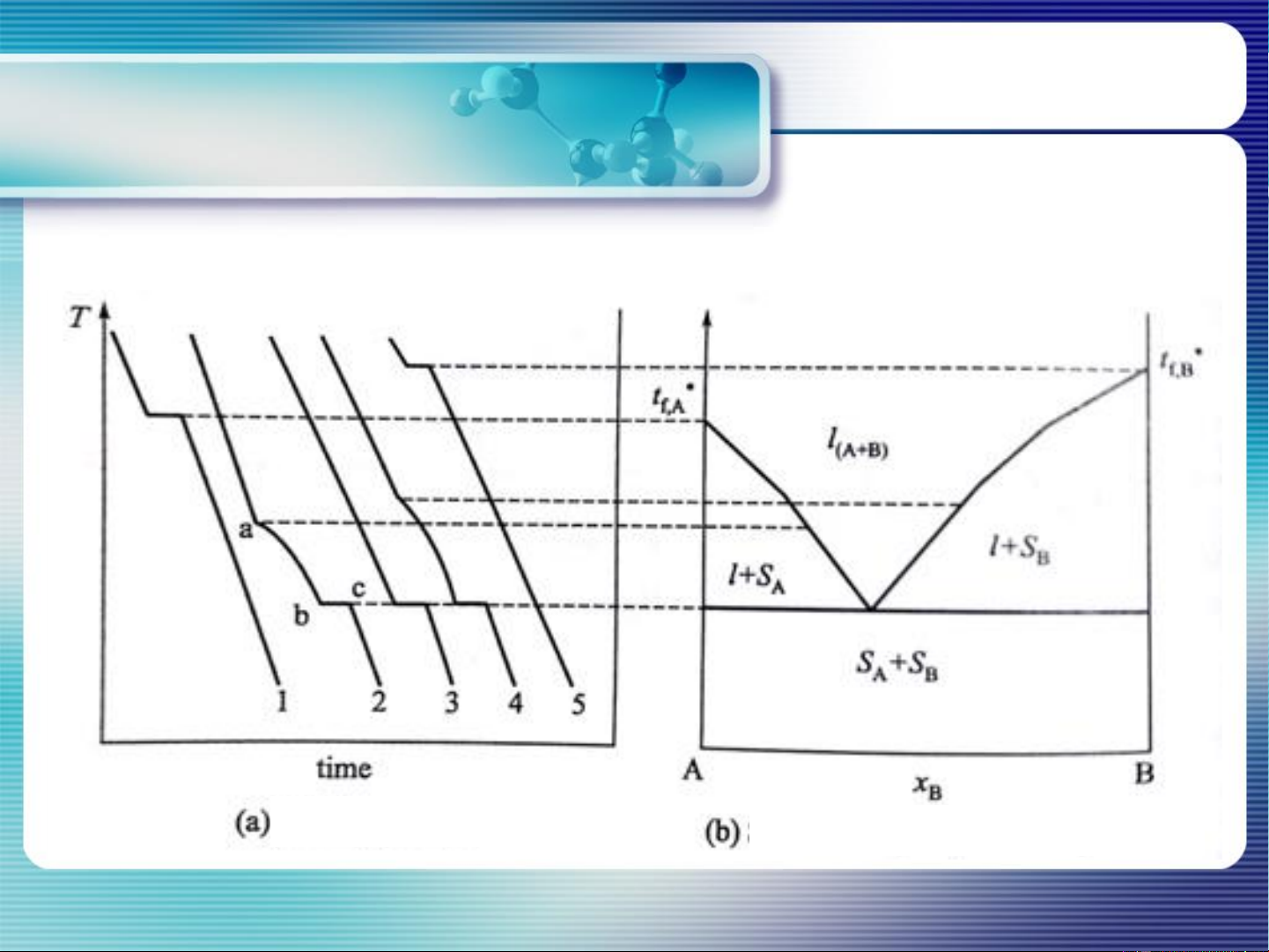
Phép phân tích nhiệt nhằm xây dựng giản đồ T=f(x) Đường nguội lạnh
Giản đồ cân bằng lỏng – rắn 9
Hệ không tạo dung dịch rắn, MIXTURES
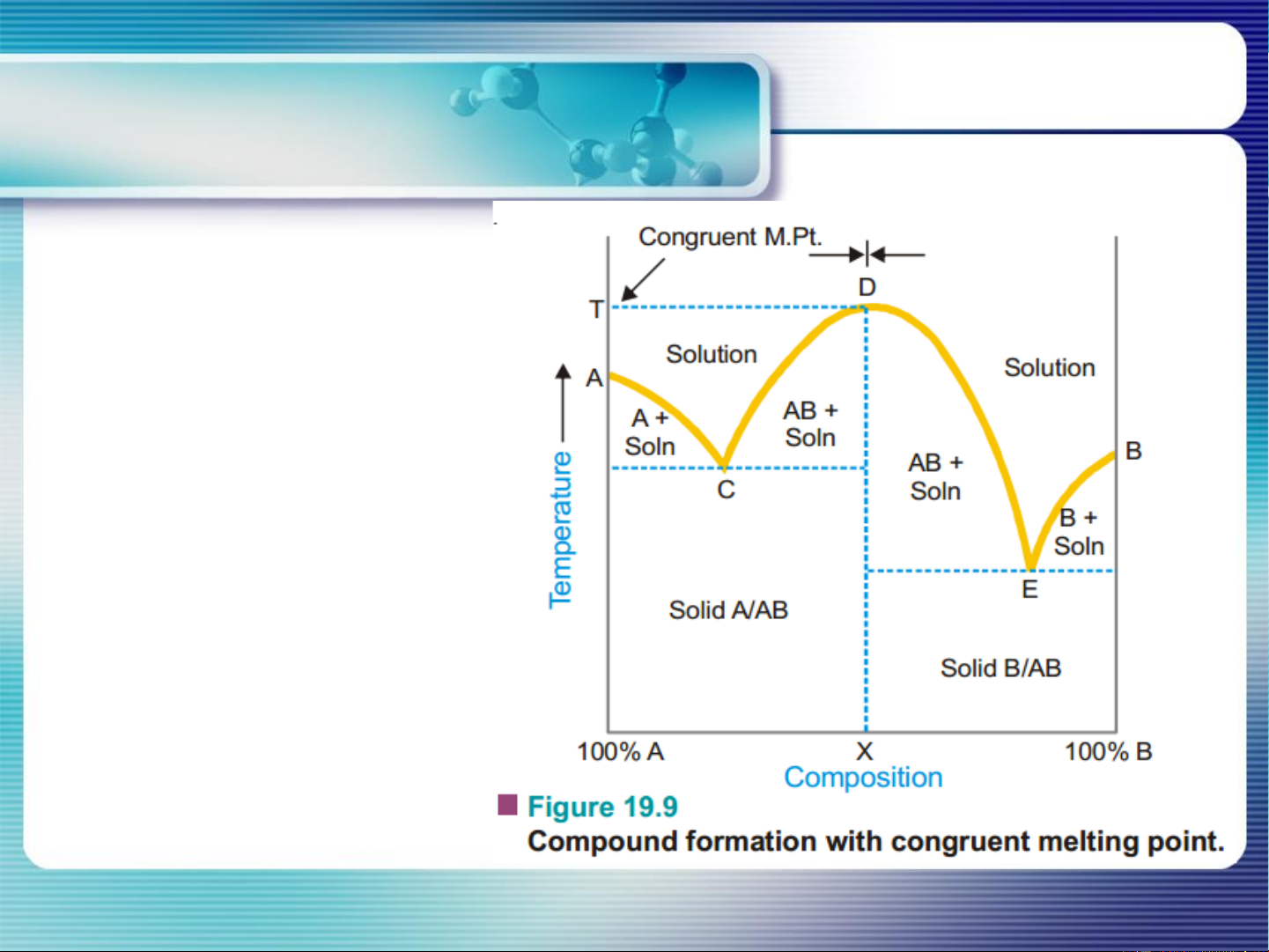
kết tinh tạo hợp chất hóa học bền Solid-liquid equilibrium kt A và B → A-B (bền)
A(r); B(r); A-B(r); dung dịch A-B
Giản đồ gồm 2 giản đồ hệ
eutectic đơn giản ghép lại kt
VD: CuSO và H O → CuSO .5H O 4 2 4 2 4 pha: CuSO (r), H O(r), 4 2 CuSO .5H O(r) và dung 4 2 dịch lỏng CuSO - H O 4 2 10
Hệ không tạo dung dịch rắn, MIXTURES
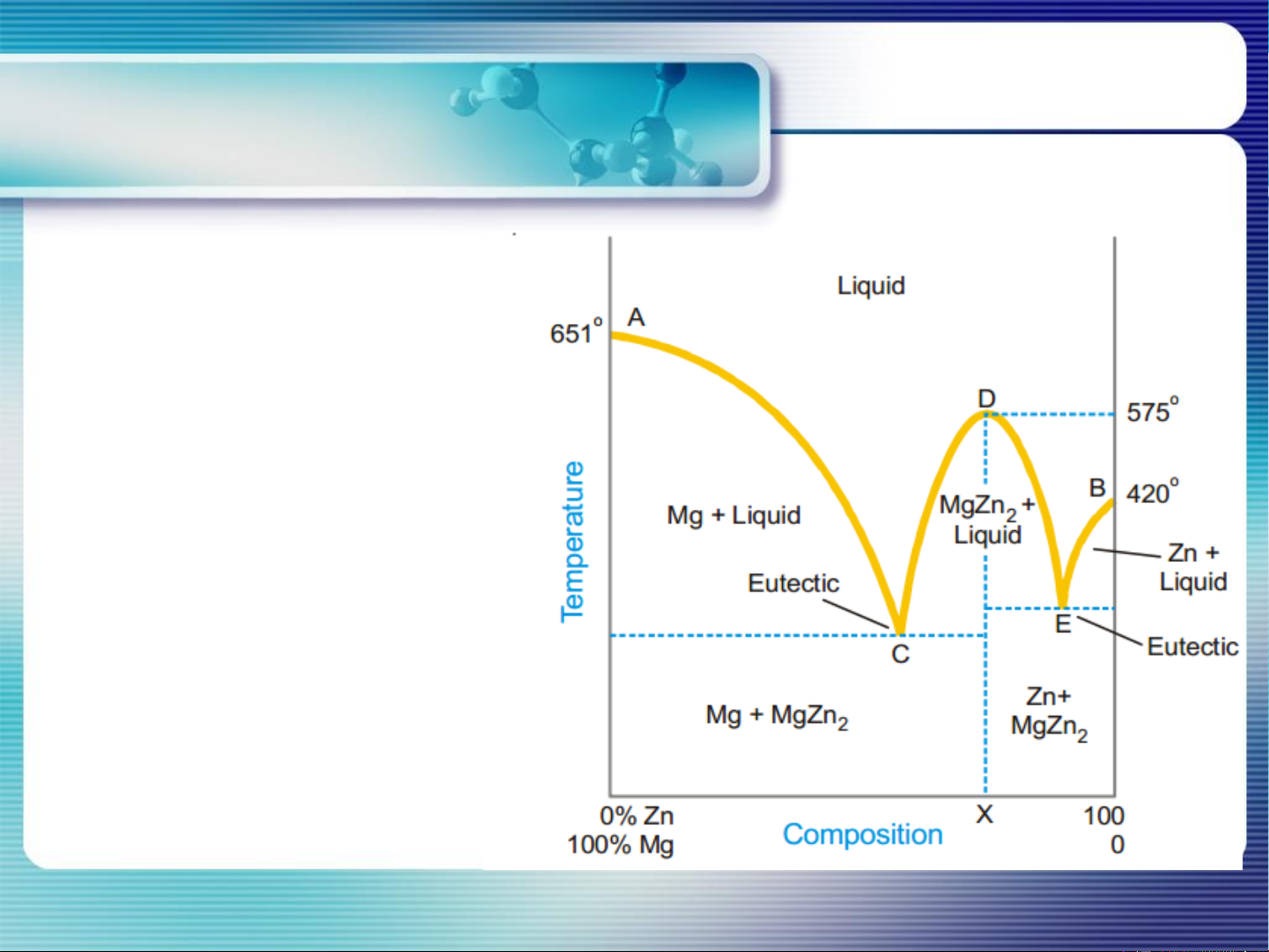
kết tinh tạo hợp chất hóa học bền Solid-liquid equilibrium kt
VD: Mg(r) và Zn(r) → MgZn2. 4 pha: Mg(r), Zn(r), MgZn2(r) và dung dịch lỏng Mg-Zn 11
Hệ không tạo dung dịch rắn, MIXTURES
kết tinh tạo hợp chất hóa học bền Solid-liquid equilibrium
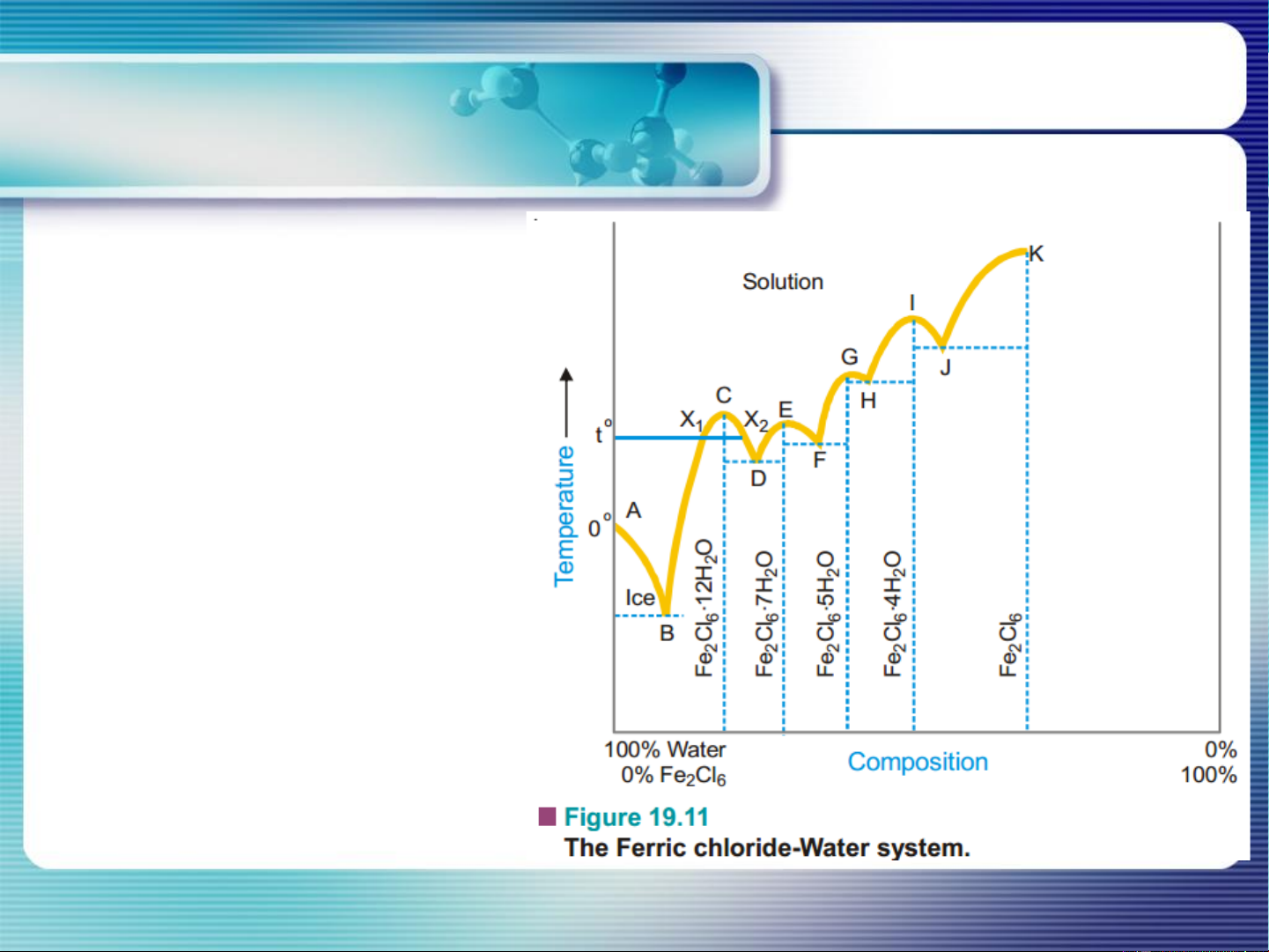
Hệ 2 cấu tử có thể tạo thành
nhiều hợp chất hóa học bền khi kết tinh
Giản đồ gồm nhiều giản đồ
hệ eutectic đơn giản ghép lại. 12
Hệ không tạo dung dịch rắn, MIXTURES
kết tinh tạo hợp chất hóa học ko bền Solid-liquid equilibrium 13
Hệ hai cấu tử tạo thành MIXTURES
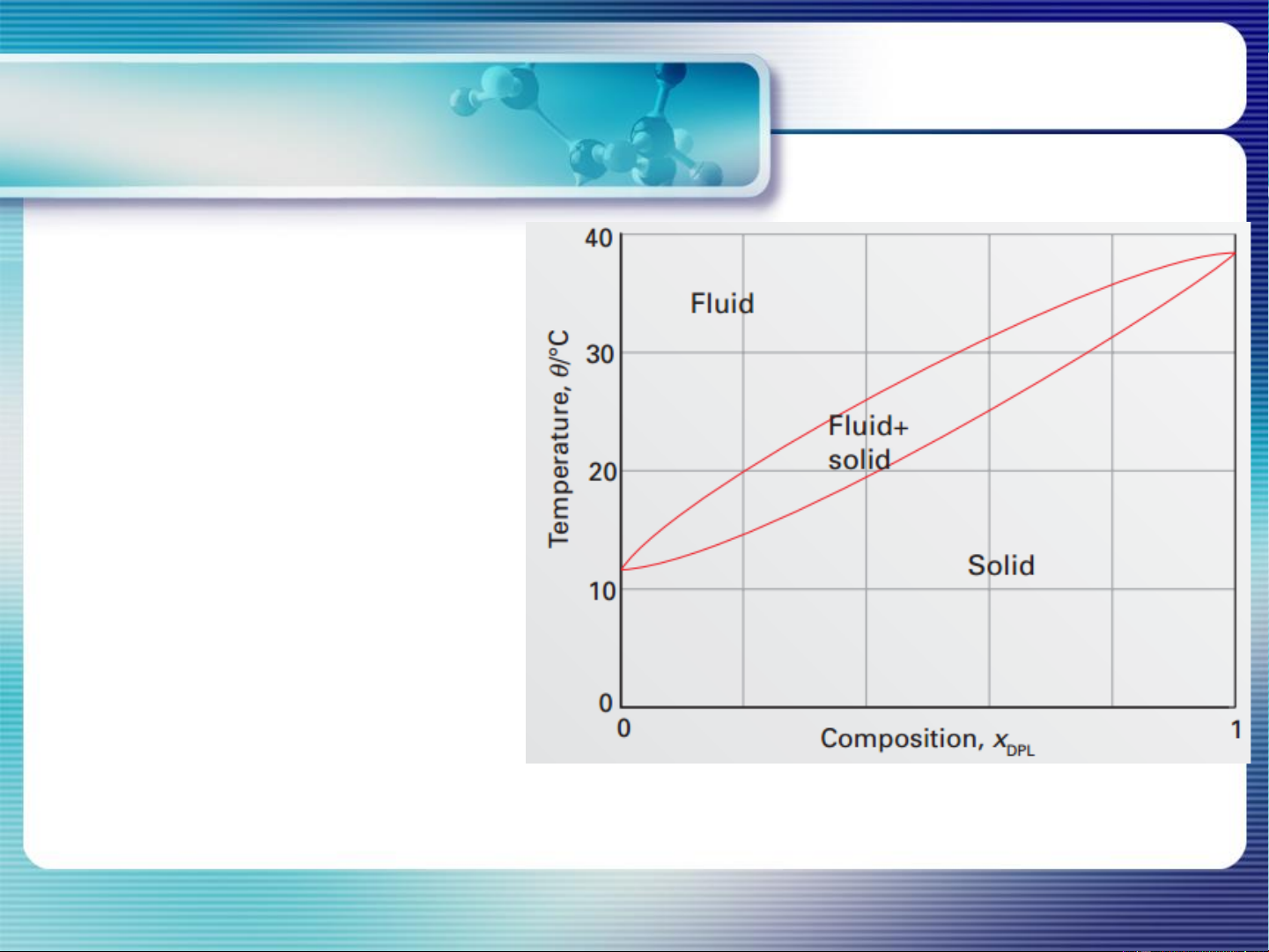
dung dịch rắn tan lẫn vô hạn Solid-liquid equilibrium VD: Ag-Au; DEL-DPL
Giải thích quá trình làm lạnh
từ 40°C của hỗn hợp lỏng có thành phần x =0,4 DEL Kết tinh phân đoạn
Dielaidoylphosphatidylcholine (DEL) and
Dipalmitoylphosphatidylcholine (DPL). 14




