








Preview text:
CHƯƠNG 7. THUYẾT ĐHPT CÁC CHẤT KHÍ & ĐỊNH
LUẬT PHÂN BỐ (3/4LT + 1BT)
7.1. Các đặc trưng cơ bản của chất khí
7.2. Phương trình trạng thái khí lý tưởng
7.3. Thuyết động học phân tử
7.3.1. Các giả thuyết của thuyết động học phân tử
7.3.2. Phương trình quan hệ nhiệt độ và áp suất (không chứng minh)
7.4. Định luật phân bố hạt theo vận tốc của Maxwell.
7.5. Số bậc tự do. Nội năng của khí lý tưởng.
7.6. Công thức khí áp. Định luật phân bố hạt theo thế năng của Boltzmann.
7.1.Cácđặctrưngcơbảncủachấtkhí 1. Hệ nhiệt động ØKhái niệm:
Hệ vật lý bao gồm một số lớn các hạt phân tử, nguyên tử :
- luôn chuyển động nhiệt hỗn loạn
- trao đổi năng lượng khi tương tác
ØPhân loại: •Hệ cô lập: là hệ không tương tác và trao đổi công A,
nhiệt Q với môi trường bên ngoài:
A= 0: hệ cô lập về cơ; Q= 0: hệ cô lập về nhiệt
•Hệ không cô lập: là hệ có tương tác và trao đổi công A,
nhiệt Q với môi trường bên ngoài:
2. Thông số trạng thái
§Mỗi trạng thái của vật được đặc trưng bởi các tính chất của vật
à Tính chất biểu hiện trạng thái. Mỗi tính chất của vật được đặc trưng
bởi một đại lượng vật lý, gọi là thông số trạng thái.
§Hệ thức liện hệ các thông số trạng thái của vật gọi là phương trình trạng thái.
Hệlà khối khí: mỗi trạng thái được biểu diễn bởi 3 thông số trạng thái là áp
suất p, thể tích V, nhiệt độ T. Thực nghiệm chứng tỏ chỉ 2 trong 3 thông số
trên là độc lập với nhau. f ()p,V,T = 0 (1)
7.1.Cácđặctrưngcơbảncủachấtkhí 3. Áp suất
ØĐại lượng vật lý có giá trị bằng lực nén vuông góc lên một đơn vị diện tích. F [] []FN pS= (2) Đơn vị: pSm == 2 1N / m =1Pa [] 2 42
Átmốtphe kỹ thuật: 1at =9,81.10 N / m 1mmHg = 1torr = 736mmHg 1mmHg=133pa 52 Átmốtphe đktc: 1atm = 1,013.10 N / m 52 1Bar =10 N / m = 760mmHg 4. Nhiệt độ
Đại lượng vật lý đặc trưng cho mức độ chuyển động hỗn loạn phân tử của . hệ
CÁC THANG ĐO NHIỆT ĐỘ
Đonhiệtđộbằngnhiệtkế theonguyêntắcdựavàođộ Nước sôi biếnthiêntheonhiệtđộ củamộtđạilượng o Nước đá T(K)=t C ( +273 ) Mặt trăng oo . C 8 , t 2 + 1 F= 3 0K ( ) ( )
7.2.Phươngtrìnhtrạngtháikhílýtưởng
1. Các định luật thực nghiệm
qĐịnh luật Boyle - Mariotte
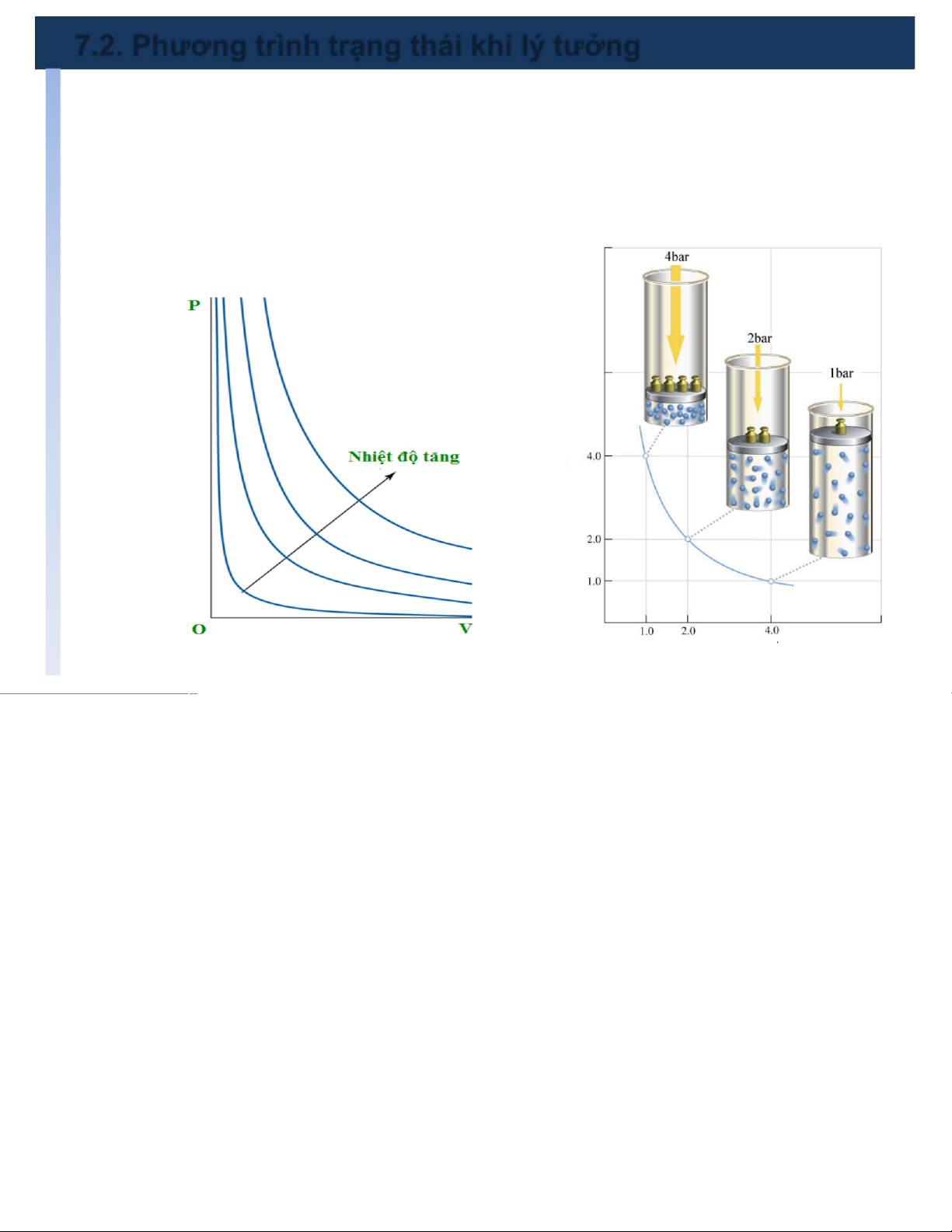
ØTrong quá trình đẳng nhiệt,thể tích của một khối khí tỷ lệ nghịch với
áp suất hay tích số của thể tích và áp suất của khối khí là một hằng số pV = const (3) P (bar) V ( ℓ)
7.2.Phươngtrìnhtrạngtháikhílýtưởng
qĐịnh luật Gay - Lussac
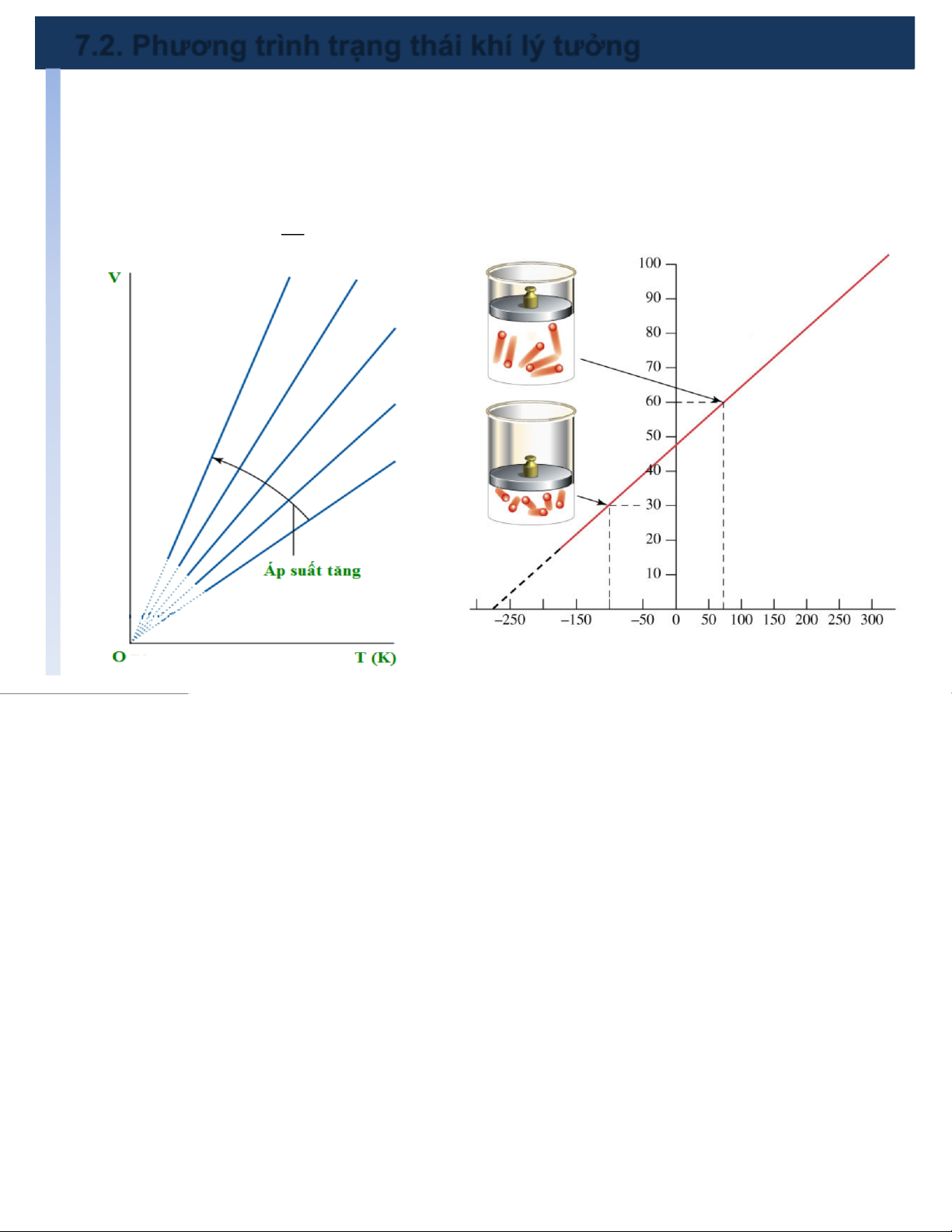
ØTrong quá trình đẳng áp,thể tích của một khối khí tỷ lệ với nhiệt độ tuyệt đối Vconst = (4) V ( mℓ) T T (oC)
7.2.Phươngtrìnhtrạngtháikhílýtưởng
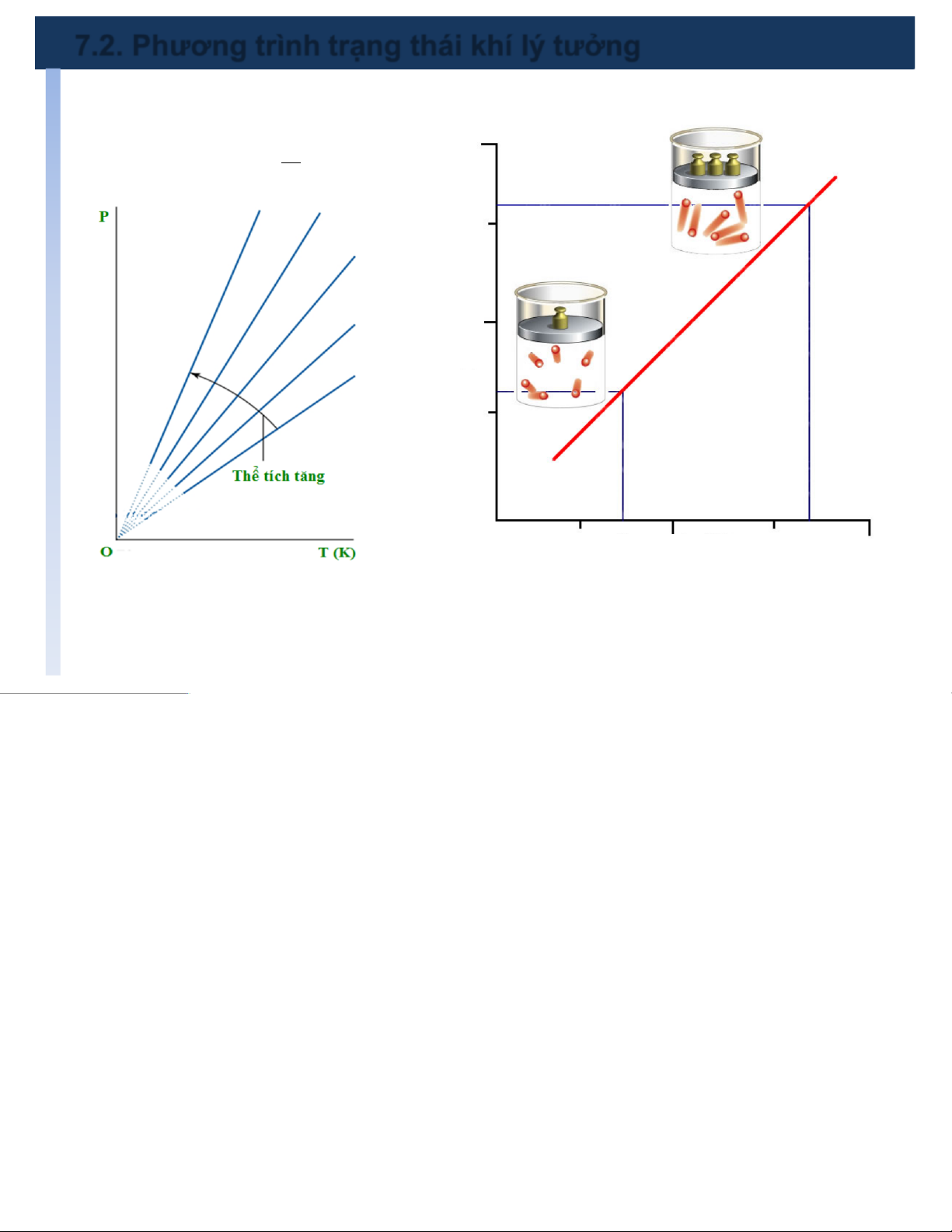
ØTrong quá trình đẳng tích, áp suất của một khối khí tỷ lệ với nhiệt độ tuyệt đối. Pconst = (5) T P (bar) T (oC)
vGiới hạn ứng dụng của các định luật Boyle - Mariotte và Gay - Lussac
Các định luật chỉ đúng trong các điều kiện áp suất khí không quá lớn
hoặc nhiệt độ khí không quá thấp.
7.2.Phươngtrìnhtrạngtháikhílýtưởng
2. Phương trình trạng thái của khí lý tưởng
qKhí lý tưởng: là khí tuân theo đúng hai định luật thực nghiệm B-M và G-L
qPhương trình trạng thái
Xét 1 kmol khí lý tưởng (chứa NA= 6,023.1026phân tử)biến đổi từ
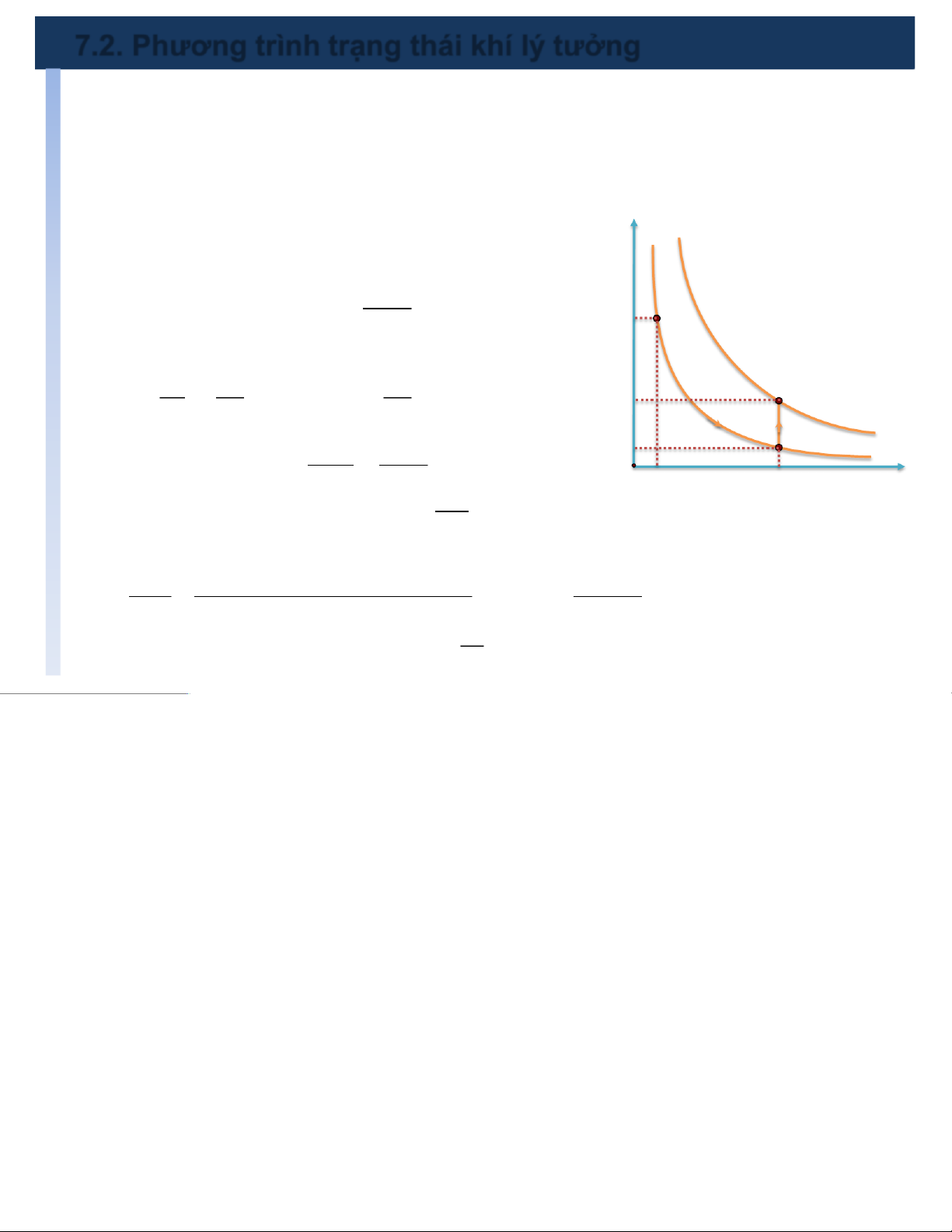
trạng thái M1đến M2:M → 1 M’ →M 1 2 P T2 §Quá trình M1
® M1’: dãn đẳng nhiệt 1 T PV PV =PV ¢ 1 ®1P= ¢ ( (*) 1) P 11 12 1 1 M 1 V2
§Quá trình M1’ ® M2:hơ nóng đẳng tích PP¢¢ T M 12 1 ® (**) P 2 2 = P ( = 2)P 12 TT T 12 2 P ¢ M ¢ 1 1 Từ (1) và (2): PVPV ®= 1122 O V V 1 2 V TT 12 PV con st R PV RT
ØĐối với 1 kmol khí lý tưởng: ==«= (6) T Ởđktc:To=0oC=273 16 , K(0oC);Po=1, .
013 105N/m2(=1atm=1,033at);Vo=22,4m3. 523 PV1,013.10 N /m .22,4m / k mol J J oo R8=== 3 , 83 1 1 . 0
R: hằng số khí lý tưởng T273,16K mol .K kmol.K o
ØĐối với m kg khí lý tưởng: m = P µ VRT (7)
µ: khối lượng phân tử
7.3.Thuyếtđộnghọc phântử
1. Nội dung thuyết động học phân tử
ØCác chất có cấu tạo từ các phần tử rất nhỏ là
phân tử/nguyên tử.
ØCác phân tử khí chuyển động hỗn loạn không ngừng.
ØCường độ chuyển động của phân tử biểu hiện ởnhiệt độ của khối
khí. Cường độ chuyển động càng mạnh thì nhiệt độ của phân tử
khí càng cao. Nhiệt độ tuyệt đối của khối khí tỷ lệ với động năng
trung bình của phân tử khí: T ~ 𝒎" 𝒗𝟐/2
ØKích thước của phân tử khí là rất nhỏ so với khoảng cách giữa
chúng à có thể bỏ qua kích thước phân tử, coi phân tử như một chất điểm.
ØCác phân tử khí không tương tác với nhau trừ lúc va chạm với
nhau và với thành bình.Sự va chạm tuân theo quy luật của va chạm đàn hồi. Đúng với mọi chất
Đúng với khí lý tưởng ! u
7.3.Thuyếtđộnghọc phântử
3. Phương trình quan hệ giữa nhiệt độ và áp suấty v.t Dx
§Áp suất khối khí do các phân tử tác dụng lực khi va chạm thành bình.
§Xét một bình chứa khí lý tưởng đơnnguyên: S D
•không đặt trong trường lực nào ® các phân tử khí ! vx
chuyển động đẳng hướng
•mật độ phân tử khí là no= N/V
§Xét một phân tử khí: x
•vận tốc v theo phương x tới đập thẳng góc vào DSthành bình Z ! !!
•chịu tác dụng của lực fdo thành bình tác dụng trong thời gian va chạm TB Dt: mv -=D mv ft 2m v Chiếu lên Ox: -- D ® = = m - x v mv ft f xx Dt 2m v
•lực f’ mà phân tử khí tác dụng lên thành bình trong Dt, theo ĐL 3: f ¢f== x Dt
§Trong Dt, ½số phân tử khí có vận tốc vnằm trong hình trụ va chạm vào DS(½ ngược lại)là: n 2mv n 0x n2 mv S x D = ()v . t S D D
n0x: mật độ phân tử theo phương x 0 x x = D x 2 t D
§Các phân tử khí chuyển động với vxkhác nhau
à Lực tác dụng cộng lên DStrong Dtbằng: 2 n mv å æ ö 0 x x
Đặt n0: mật độ phân tử theo mọi phương 2 v F ç n D ÷ 0 x mv2 x S = ç å ÷ vx = F2 n v S ® è xn 2 2 0D x =
v : giá trị trung bình của v v ø 0 x x x 2222 2 ü vvv v v 1
§Do các phân tử khí chuyển động hỗn loạn: =++ï xy ® z 2 = ý v 3 2 S . ® v D F m n x = o 22 vv = 2 v 3 xyz =ï þ F1 21
§Áp suất trung bình tác v dụng lên m thàn n v h bình m. 22 æö P = n = =ç÷ àP ~ v Dèø oo S3 32 ! u
7.3.Thuyếtđộnghọc phântử
3. Phương trình quan hệ giữa nhiệt độ và áp suất
qĐộng năng trung bình của một phân tử khí F1 21 22 æö 1 2 n v m Pn (8) oo Wđ mv == =ç÷ Dèø S3 32 = 2 2 m qÁp suất khối khí p= n 0W đ (9) mà = p µVRT 3 æ 2 ö m 2 m 3 R ® ç n W ®! " # ()n V Wđ = RT ® W đ T đ ÷V = RT = è 3 0µ ø 3 0µ 2 N m A N µ A 3 1 3V ,Je R8 -23 - 5 è WBđ k T (10) (11) k = với === = 1, 38.108, 62.10 B23 2 N6, 02.10 K K A 0 Þ pB= n k T (12)
kBlà hằng số Boltzmann
•Ở cùng áp suất và nhiệt độ, mọi chất khí đều có mật độ như nhau
•Định luật Dalton: Áp suất của hỗn hợp khí bằng tổng áp suất riêng
phần của từng khí. ! u
7.4.ĐịnhluậtphânbốhạttheovậntốccủaMaxwell
qVới chất khí: số phân tử rất lớn, các phân tử luôn chuyển động hỗn loạn
Các phân tử có vận tốc khác nhau à động lượng, động năng… khác nhau
à Không thể khảo sát riêng từng phân tử à phải xét chuyển động tập thể
à Các đại lượng vật lý đặc trưng sẽ lấy giá trị trung bình 1
§Vận tốc trung bình:với n v ilà = số phân ni vitử có (13) vận tốc vi å N i ni= N å n i «å = i v v v = P(v i) v . i (14) với P(v để i «
i) = ni/N là xác suất 1 å N i i
phân tử có vận tốc vi: å P(vi )= 1
Ví dụ minh họa: Có N = 1000 phân tử i
với n1 = 100 phân tử có vận tốc v1= 100m/s
P(v1) = 100/1000 = 10% là xác suất với n
để 1 phân tử có vận tốc v
2 = 300 phân tử có vận tốc v2= 200m/s 1. P(v2) = 30%
với n3 = 400 phân tử có vận tốc v3= 300m/s P(v3) = 40%
với n4 = 200 phân tử có vận tốc v4= 400m/s P(v4) = 20% 100 1 . 00 3 + 00 2 . 00 4 + 00 3 . 00 2 + 00 4 . 00 v= 270(m / s) 100 +300 +400 + 200 v 2 =(1)0% 1 . 00 2 ( + 3 % 0 )2002 +
§Vận tốc bình phương trung v bình:P(v 2 ). = v å 2 + ( ) 4 % 0 3002 ( + )2 % 0 4002 i i i = 81000m / s ! u
7.4.ĐịnhluậtphânbốhạttheovậntốccủaMaxwell
qPhân bố Maxwell (1859)
§dN là số phân tử có vận tốc Î (v, v + dv):
§Xác suất (%) để một phân tử có vận tốc Î (v, v + dv):
dN= F(v) dv (15) với F(v) là hàm phân bố Maxwell N ¥ ¥ Î v (Î T) « dN = ( F . N v)dv « òdN = NòF(v)dv ¥ 0 0 (1831-1879)
Số phân tử có vận tốc v với 0 £ v < ¥ bằng N: dN N = ò ¥ ¥ 0 N = ò F . N (v)dv ( F v)dv = ò 1 0 0
Điềukiệnchuẩnhóacủahàmxácsuất 3/ 2 2 a v a - æ ö 2 2 F(v) = 4pç ÷ v e (17) è 2p ø m
aÎ T xác định bằng thực nghiệm a = k T B 3 / 2 mv 2 æ m - ö 2 2 k T B F(v) = 4p v e çç ÷÷ (18) 2pk T è ø B
Định luật phân bố Maxwell
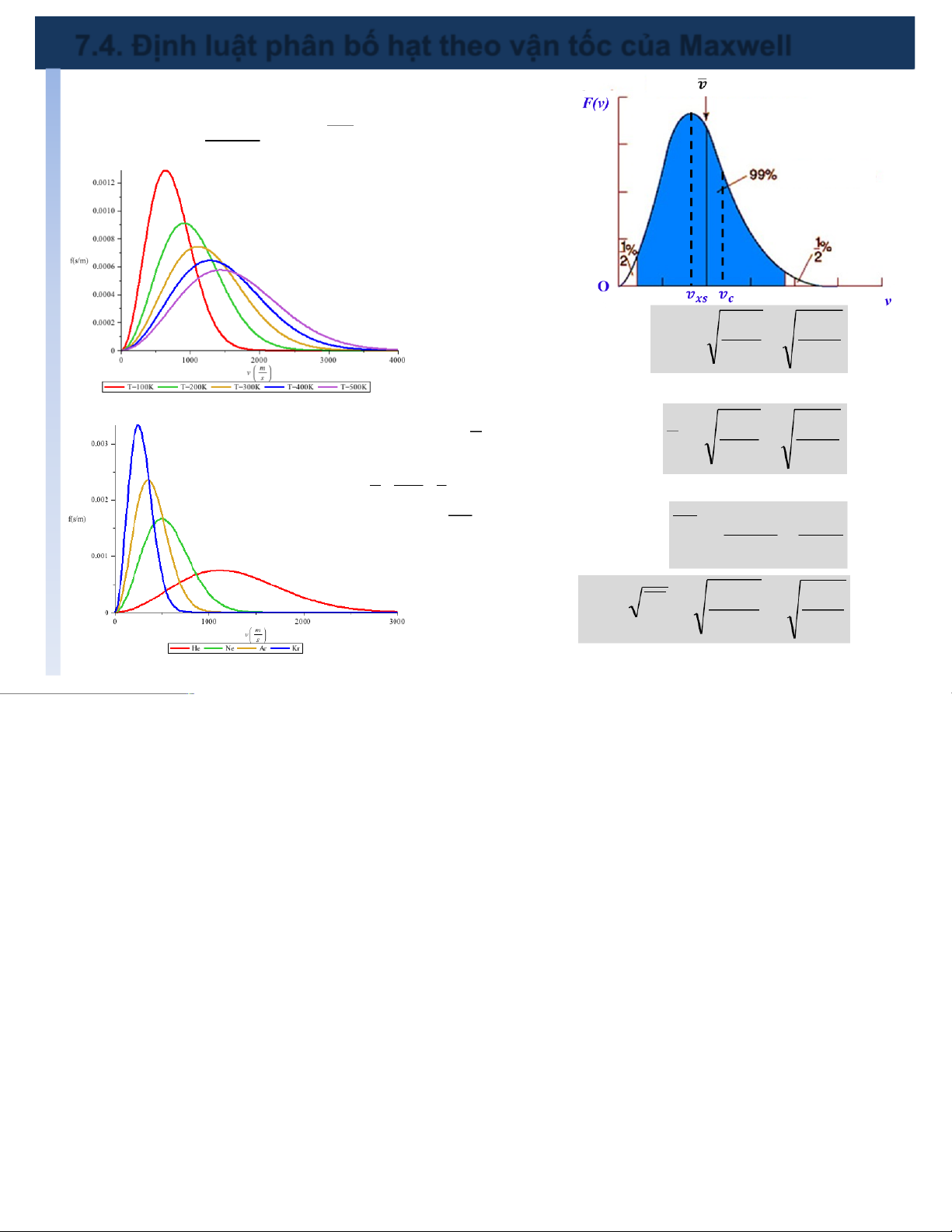
7.4.ĐịnhluậtphânbốhạttheovậntốccủaMaxwell qPhân bố Maxwell 3 / 2 2 mv æ m - ö 2 2k T B 4 F(v) p v e = çç ÷÷
𝒗𝒙𝒔<#𝒗<𝒗𝒄 𝒗 2 k p T è ø
𝒙𝒔 :#vậntốcxác B suất F(v) Î T $
𝒗:#vậntốctrung bình
𝒗𝒄:vậntốccăn quânphương Å 2kT 2RT
dF(v) = 0 à v xs = = (19) m µ
vậntốcmàsốphântửcóđượcnhiềunhất ¥ k 8 T ÅR 8 T v = $ ! ! !# Å ! ! !" ò v ( F v)dv à v = = (20) F(v) m µ Î m 0 ì = k R R = ü í ý m N m . µ
vậntốctrungbìnhcủacácphântử î A þ ¥ k 3B T 3 v v F(v ÅRT 2 2 ) = dv ò 2 à v = = (21) m µ 0 =R 3 T 2 = k 3 T = vB v c (22) m µ
đặctrưngchosựphânbốvậntốcphântử
7.5.Sốbậctựdo.Nộinăngcủakhílýtưởng 1. Số bậc tự do
Sốtọađộđộclậpcầnthiếtđểxácđịnh vịtrícủavậttrongkhônggian.
một nguyên tử (đơn nguyên): i = 3
Số bậc tự do phụ thuộc cấu tạo phân tử
hai nguyên tử (lưỡng nguyên): i = 5
ba nguyên tử trở lên (đa nguyên): i = 6 3
§Động năng trung bình của một phân tử khí đơn nguyên i = 3: WBđ k T = (10) 2 1 1 1 1 1 2 1 2 1 Wđ 2 1 2 2 2 2 đ + m W v + mv mv = mv = à = mv x= mv mv k T x y z y z B 2 2 2 2 2 2 2 3 2
à Mỗi bậc tự do tham gia vào chuyển động tịnh tiến với năng lượng là kBT/2
èĐịnh luật phân bố đều năng lượng theo bậc tự do: động năng/năng lượng
phân bố đều cho mỗi bậc tự do.
§Tổng quát, động năng trung bình phân tử khí có i bậc tự do là: i WBđ k T = (23) 2
7.5.Sốbậctựdo.Nộinăngcủakhílýtưởng
2. Nội năng của khí lý tưởng
§Năng lượng của một hệ/vật:ØĐộng năng ứng với chuyển động có hướng
của hệ (chuyển động cơ). WW WU (24)
ØThế năng của hệ trong trường lực. =++ dt
ØNộinănglàphầnnănglượngứngvớivận
độngnộttạitronghệ.
§Trong nhiệt động học,coi hệ chuyển động không đáng kể và không đặt trong bất
kì trường lực nào:Nội Wnăng đ của = 0 ; Wt hệ
= 0là hàmtrạngthái à W = U
-động năng chuyển động hỗn loạn của các phân tử:tịnh tiến và quay
-thế năng do tương tác của các phân tử. §Nội năng:
-động năng và thế năng dao động của nguyên tử trong phân tử.
-năng lượng vỏ điện tử và hạt nhân nguyên tử
ØHệ nhiệt động:nộinănggồmtổngthếnăngtươngtácvàđộngnăngchuyểnđộng
nhiệtcủacácphântử.
ØKhí lí tưởng:nộinănglàtổngđộngnăngchuyểnđộngnhiệtcủa các phân tử (do
thế năng tương tác giữa các phân tử khí lý tưởng bằng 0). i i §Với 1 mol: UN . WN .k T == hay U T R = (25) Ad AB 2 2 §Với m (kg): mi
Nộinăngcủamộtkhốikhílýtưởngchỉ URT =µ (26) 2
phụthuộcvàonhiệtđộcủanó.
7.6.Côngthứckhíáp.Địnhluậtphânbốhạttheo thếnăngcủaBoltzmann
1. Công thức khí áp
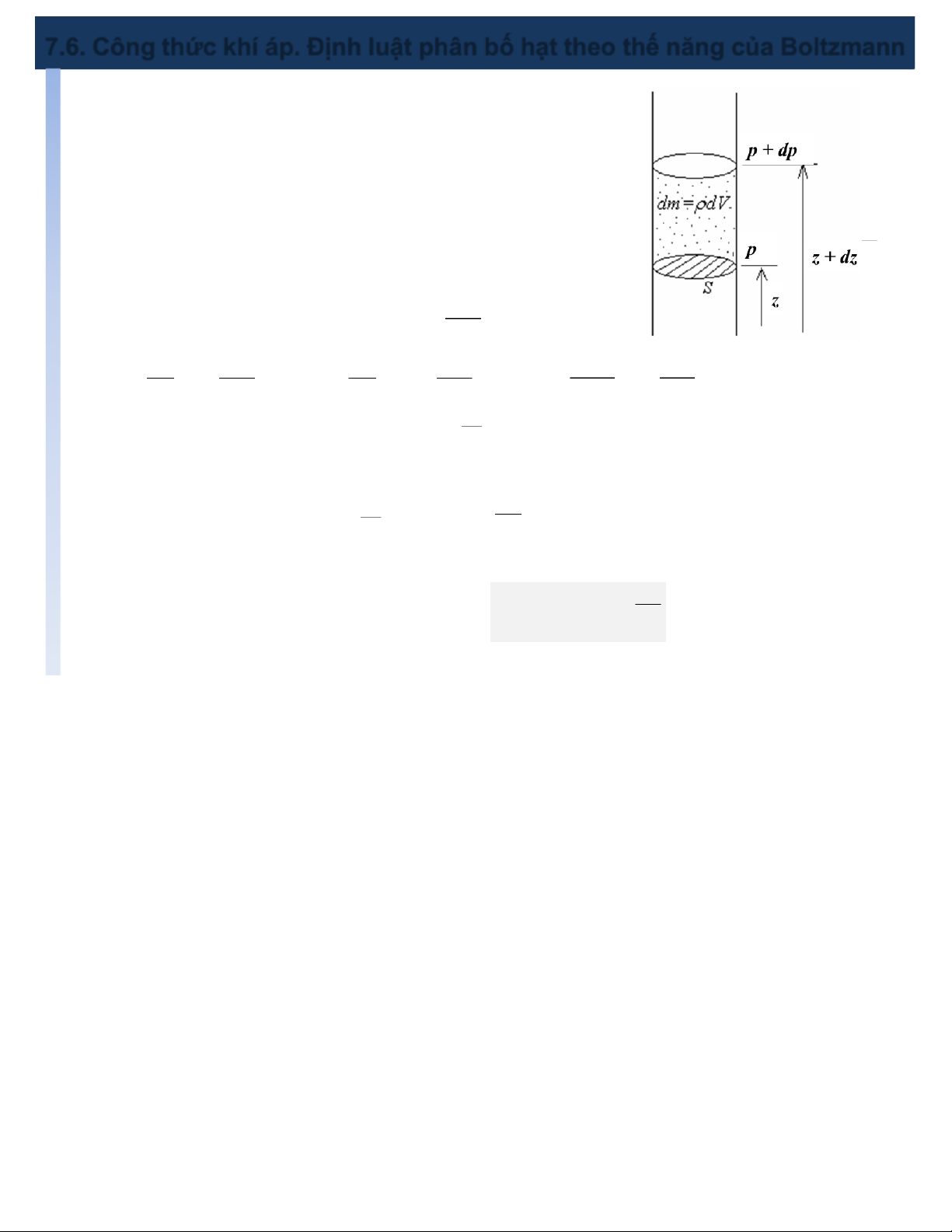
§Xét hai điểm có độ cao z và z + dz trên phương
thẳng đứng có hiệu áp suất dp: dp = – rgdz
-dp là trọng lượng của cột khí chiều cao dz và
đáy bằng một đơn vị diện tích.
- dấu (–) do p và z biến thiên ngược chiều pµ
r là khối lượng riêng chất khí: r = RT dpµ g p( z) z dp g ln p µ (z) g è = - dz è òµ = ò - dz è = - z p RT p RT p(0) RT p(0) 0 µg - z RT p(z) = p(0)e
(27) Côngthứckhíáp
2. Định luật phân bố hạt theo thế năng của Boltzmann mgz µ g z - p = n - k T RT 0kBTè B n (z) = n (0)e = n (0)e
(28) mgz là thế năng của phân tử khí 0 0 0
trong trọng trường đều.
(28) đúng trong trường thế bất kỳ. Wt - k T B n(z) = n ( ) 0 e (29) 0
Định luật phân bố Boltzmann




