

Preview text:
CÂU HỎI ÔN THI HÓA SINH ĐẠI CƯƠNG
Câu 1: trình bày enzyme 1 thành phần:
thành phần cấu tạo: acid amin
chức năng: xúc tác cho các phản ứng sinh hóa diễn ra nhanh hơn, trong các phản ứng này, các phân tử lúc bắt
đầu của quá trình được gọi là cơ chất (substrate), enzyme sẽ biến đổi chúng thành các phân tử khác nhau.
Trung tâm hoạt động của enzyme :
Trong quá trình xúc tác, chỉ một phần rất nhỏ của phân tử enzyme tham gia kết
hợp đặc hiệu với cơ chất, phần đó được gọi là trung tâm hoạt động của enzyme. Trung tâm của enzyme được tạo
nên do một số axit amin đảm trách. Các axit amin khác trong protein không tham gia gắn với cơ chất mà chỉ làm
nhiệm vụ như một chiếc khung cấu trúc không gian của chiếc khung đó.
1. Trung tâm hoạt động của enzyme đơn cấu tử :
Trung tâm hoạt động của các enzyme đơn cấu tử thường bao gồm một tổ hợp các nhóm định chức của axit amin
không tham gia tạo thành trục chính của sợi polypeptit.
Các nhóm chức của axit amin thường gặp trong trung tâm hoạt động của enzyme là: -
Nhóm SH (sunfidryl) của Cysteine -
Nhómε - NH2 (amin) của Lysine -
Nhóm OH (Hydroxyl) của Serine, Threonine và Tyrosine -
Nhóm COOH (Cacboxyl) của axit Glutamic, Aspactic -
Vòng imidazol của Histidine - Vòng indol của Tryptophan - Nhóm guanilic của Acginine
Khi tạo thành trung tâm hoạt động các nhóm này phải ở vị trí gần nhau và được
định hướng trong không gian sao cho chúng có thể tương tác với nhau trong quá trình phản ứng.
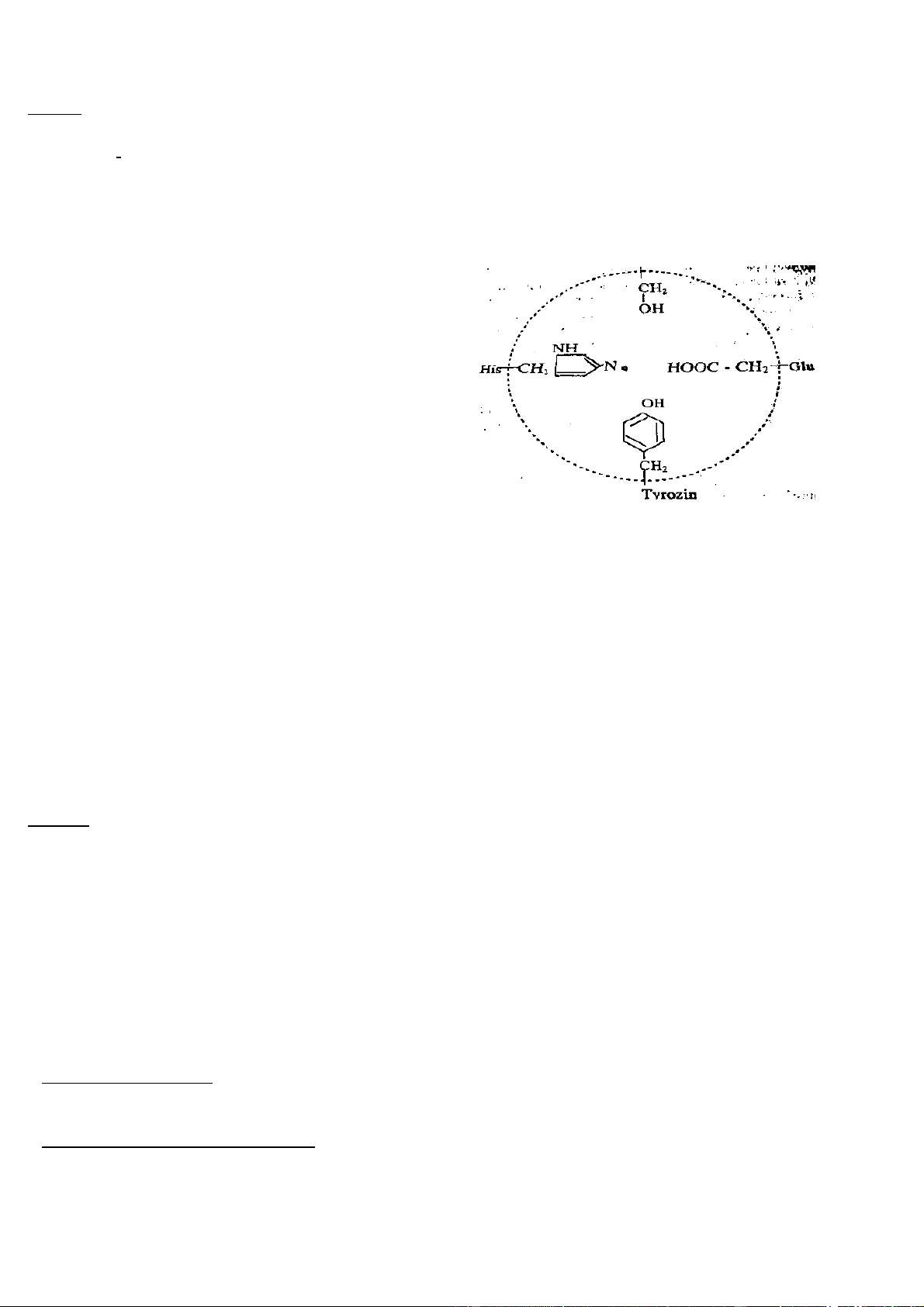
Ví dụ, Trung tâm hoạt động của Colinesteraza bao gồm các nhóm: -OH
của serine, tyrosine, -COOH của
glutamic, imidazolit của histidine.
Hình 1.1 : Trung tâm hoạt động của enzym colinesteraza
Các trung tâm hoạt động có thể hình thành dễ dàng khi các nhóm chức ở gần nhau trên Apoenzyme. Nhưng có
khi chúng ở xa nhau thì phải hoạt hóa bằng cách cắt đi một đoạn peptide nào đó, chúng xích lại gần nhau và tạo
thành trung tâm hoạt động.
Ví dụ, Tripxinogen là trạng thái không hoạt động, nhưng khi dưới tác dụng của enzyme Enterokinaza thì 6 axit
amin bị loại ra, các nhóm chức lúc này xích lại gần và trung tâm hoạt động được dễ dàng. C
âu 32 : Phân loại protein đơn gỉan theo độ hòa tan:
* Protein đơn giản là khi phân giải bằng acid chỉ cho sản phẩm toàn bộ là acid amin
1. Albumins: gồm các loại protein tan trong nước tinh khiết, có hình cầu, gồm nhiều loại enzyme.
2. Globulins: tan trong muối loãng, có hình cầu(thường NaCl)
3. Prolamines: không tan trong nước, tan trong cồn 50%-90%
4. Glutelins: không tan trong hầu hết dung môi, tan trong acid và kiềm loãng.
5. Protamines: không dựa trên độ hòa tan, PTL nhỏ, Arg chiếm 80%, không có Cys
6. Histoneprotein trung tính, có trong thành phần cấu tạo của DNA, chủ yếu là acid amin bazo basic aa’s > 90% Arg, Lys, His.
7. Scleroprotein: không tan trong hầu hết dung môi. Fibrous structure – có trong các mô sụn, mô liên kết.
Collagen – nhiều Gly, Pro và Cys, khi đun sôi tạo gelatin. Keratins – protein của tóc và da , nhiều acid bazo Cys cao.
* Ý nghĩa của phân loại: Phân loại theo độ tan là để tách các loại protein khác nhau trong hợp chất.
Vì mỗi loại protein đều tan trong 1 loại dung môi nhất định hoặc không tan nên có thể dễ dàng phân biệt các loại
protein với nhau, có thể hòa tan protein với dung môi khác nhau để thuận tiện cho quá trình nghiên cứu.
* Ý nghĩa cấu trúc bậc 1 của protein: - Cấu trúc bậc một của protein có vai trò tối quan trọng vì trình tự các acid
amin trên chuỗi polypeptide sẽ thể hiện tương tác giữa các phần trong chuỗi polypeptide, từ đó tạo nên hình dạng
lập thể của protein và do đó quyết định tính chất cũng như vai trò của protein. Sự sai lệch trong trình tự sắp xếp
của các acid amin có thể dẫn đến sự biến đổi cấu trúc và tính chất của protein.
- Cấu trúc bậc 1 xác định tính đặc thù , đa dạng của protein , đồng thời quy định cấu trúc bậc 2 và 3 của protein.
câu 5: Kế tiếp acetyl-CoA đi vào một chuỗi phản ứng của một chu trình gọi là chu trình Krebs (do nhà khoa
học người Anh, Hans Krebs, được giải thưởng Nobel nhờ làm sáng tỏ được chu trình này) hay chu trình
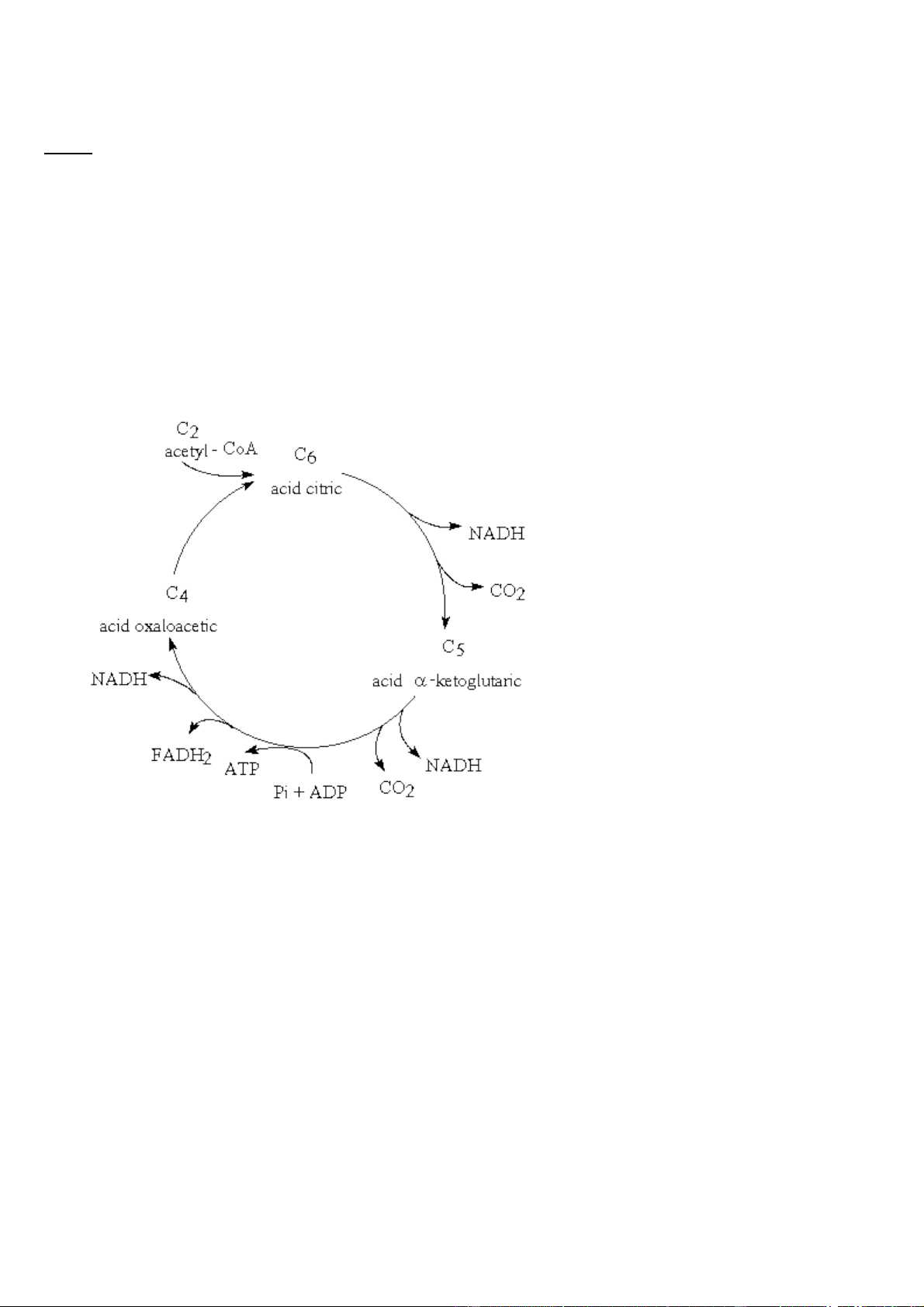
acid citric. Những điểm chính trong chu trình được trình bày trong hình 3. Mỗi phân tử acetyl-CoA được tạo
ra từ phân tử glucoz ban đầu kết hợp với một hợp chất 4C, acid oxaloacetic, đã hiện diện trong tế bào để tạo ra
một hợp chất 6C mới là acid citric. Trong các phản ứng tiếp theo, 2C bị mất đi dưới dạng CO2, như vậy hợp
chất chỉ còn 4C và được biến đổi để trở lại chất 4C ban đầu và chu trình lại tiếp tục. Vì mỗi phân tử glucoz tạo
ra hai phân tử acetyl CoA, nên có hai vòng acid citric xảy ra và tổng cộng là có 4C được giải phóng dưới dạng
CO2; cộng thêm 2C được giải phóng dưới dạng CO2 trong giai đoạn II, như vậy tất cả là 6C của phân tử glucoz ban đầu.
Hình 3. Sơ đồ của chu trình Krebs Trong một vòng của chu trình (Hình 3), một phân tử ATP được tổng hợp
(bởi sự phosphoryl hóa ở mức cơ chất) và 8 điện tử và 8 ion H+ được lấy đi bởi chất nhận điện tử. 6 điện tử và
6 hydro được dùng để khử 3 phân tử NAD+ (tạo ra 3 phân tử NADH và 3 ion H+) và 2 điện tử và 2 hydro được
nhận bởi hợp chất FAD (tạo ra FADH2). Vì sự oxy hóa một phân tử glucoz trải qua hai vòng chu trình Krebs
nên tổng cộng có 2 ATP và 8 phân tử chất khử (6 phân tử NADH và 2 FADH2)
Câu 10: Amino acid là đơn vị cấu trúc cơ bản của protein. Chúng tạo thành các xích polymer ngắn gọi là
peptide hay polypeptides để rồi tạo thành cấu trúc gọi là protein. Quá trình tạo thành từ mRNA làm mẫu gọi là
dịch mã, là một phần của tổng hợp protein.
Có 20 loại amino acids được mã hóa bởi mã di truyền chuẩn và được gọi là proteinogenic hay amino acids
chuẩn. Việc kết hợp các amino acid này tạo ra protein thiết yếu cho việc cấu thành cơ thể người. Có ít nhất hai
loại khác được mã hóa bởi DNA theo một cách khác (không chuẩn):
Công thức cấu tạo chung của axit amin là: RCH(NH2)COOH tính chất chung:
- Chỉ có 20 aa và 2 amid trong số 80 acid amin có mặt trong thiên nhiên tham gia và cấu tạo thành phần protid.
- Gọi là alpha acid amin vì nhóm NH2 đính vào C ở vị trí alpha.
- Nhóm R gắn vào alpha carbon không đối xứng
- 20 nhóm R khác nhau tạo nên các acid amin khác nhau.
- 20 acid amin thường gặp có trong tất cả hệ thống sống, mỗi aa(trừ gly) đều tồn tại dưới hai dạng đồng phân qua gương.
- Acid amin có tính chất lưỡng tính vì trong thành phần vừa có nhóm amin(bazo), vừa có nhóm cacboxyl(acid).
- Acid amin là chất hoạt động quang học vì có C bất đối(trừ glixin): chúng có khả năng quay mặt phẳng ánh sáng
- Hầu hết acid amin của protid thuộc dãy L(ít acid amin thuộc dãy D).
- Dấu(+) và dấu (-) biểu hiện hướng quay của mặt phẳng ánh sáng phân cực( quay phải hay trái).
- Acid amin trong môi trường acid mạnh tích điện dương, trong môi trường kiềm mạnh tích điện âm.
- Điểm đẳng điện là tại điểm pH nhất định aa có điện tích âm bằng điện tích dương
- Trong môi trường nước acid amin phân ly hoàn toàn.
- Acid amin không tồn tại ở dạng tự do mà ở dạng muối nội.
- Acid amin tan được trong nước và trong cồn 75-80%. Phản ứng đặc trưng:
* phản ứng với acid và bazo tạo thành muối:
R- CH- COO- + HCl R- CH – COOH NH + + 3 NH3 Cl- (muối clorua)
R-CH-COO- + NaOH R- CH – COONa + H2O NH + 3 NH2 (muối natri)
* Phản ứng với acid nito( hay phản ứng Van-slyke):
R- CH – COOH + HNO2 R- CH – COOH + N2 + H2O NH2 OH (Oxyacid)
* Phản ứng Sorensen ( phản ứng với Aldehydformtc – formalin): H H H
R-C –COO- + C R- C – COOH + H2O NH + 3 O N= CH2
(acid amin) (Formalin) (Hợp chất Vinyl của acid amin)
* Phản ứng với kim loại nặng: COOH COO NH2
R- CH + Cu2+ R- CH Cu CH - R NH2 H2N OOC
(phức chất Biurê có màu tím)
câu 19: Phân tử nước được cấu tạo từ 2 nguyên tử H và 1 nguyên tử O. Nguyên tử H có 1 electron lớp ngoài
cùng có xu hướng nhận thêm 1 electron nữa để đạt cơ cấu bền của khí hiếm (giống He). Nguyên tử O có 6
electron lớp ngoài cùng sẽ cho mỗi nguyên tử H một electron tạo 2 liên kết cho nhận trong nguyên tử H2O.
Theo phần trên ta thấy nguyên tử O tích 2 lần điện tích âm, mỗi nguyên tử H tích 1 lần điện tích dương.
=> Phân tử H2O có 1 đầu âm và 1 đầu dương. Do đó người ta nói phân tử H2O có tính phân cực.
* Ta đã biết, chất phân cực tan trong dung môi phân cực. Đa số hợp chất vô cơ và hữu cơ là chất phân cực, khi
hòa tan vào nước, các phân tử nước sẽ bao quanh và nhờ lực hút tĩnh điện của nhiều phân tử nước tác động
cùng một lúc làm cho các liên kết của các hợp chất vô cơ và hữu cơ bị cắt đứt, phân ly thành các ion hòa tan.
Chính vì lý do đó, nước là dung môi hòa tan rất tốt cho các hợp chất vô cơ và hữu cơ.



