





Preview text:
70 câu trắc nghiệm (chủ yếu vào ại cương, thuốc virus và các tác dụng phụ) + 10 câu nối ý I. Đại cương
Bài 1. Thuốc và quá trình khám phá thuốc mới
1. Thuốc và quá trình khám phá
− Định nghĩa: Thuốc là chất hoặc hỗn hợp các chất dùng cho người nhằm phòng bệnh, chữa
bệnh, chẩn oán hoặc iều chỉnh chức năng sinh lý cho cơ thể, bao gồm thuốc thành phẩm,
nguyên liệu làm thuốc, vaccine và sinh phẩm y tế
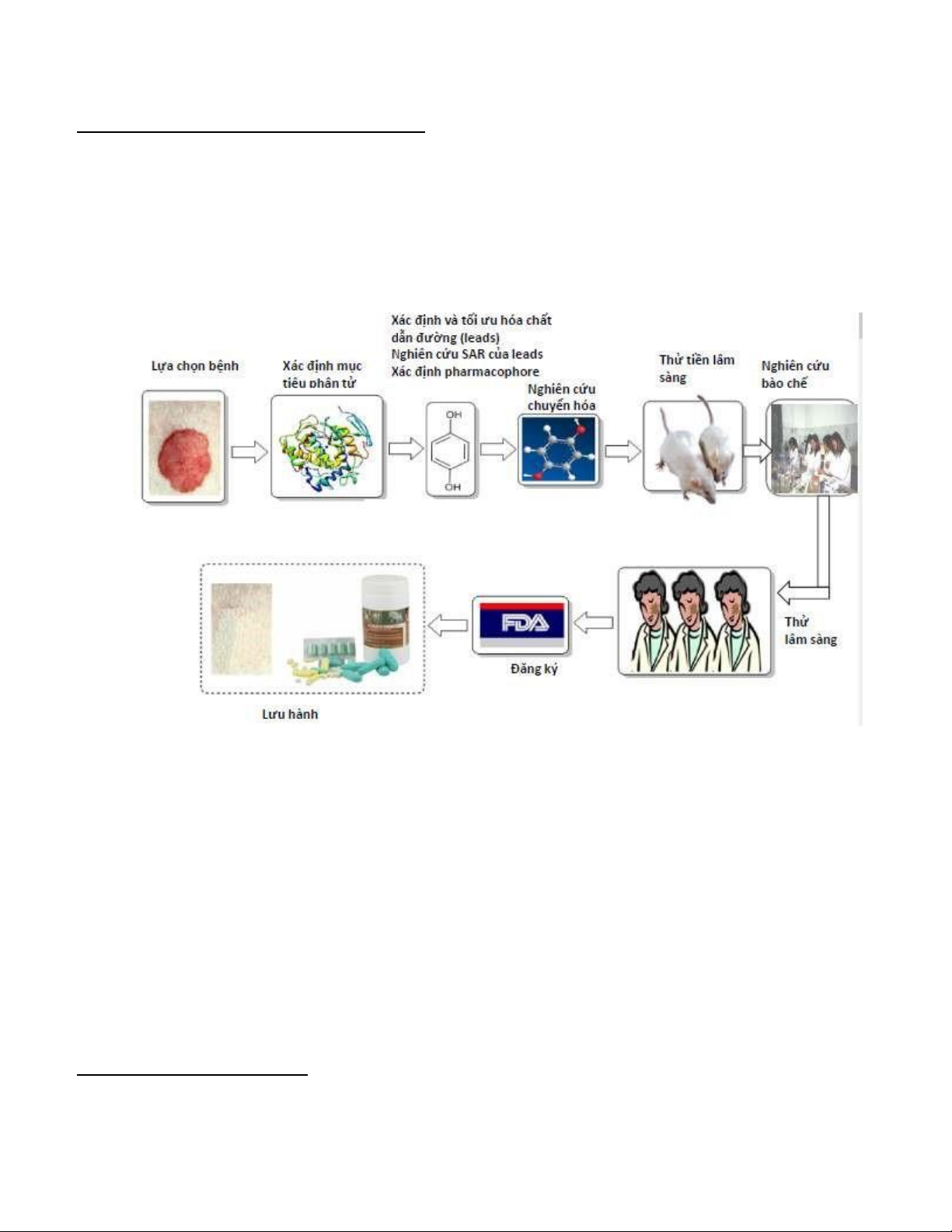
− Quá trình nghiên cứu và phát triển thuốc hiện ại
2. Ứng dụng một số kĩ thuật hiện ại − Tổng hợp tổ hợp
− Sàng lọc hiệu năng cao
− Máy tính hỗ trợ thiết kế
Bài 2. Đích tác dụng của thuốc
1. Enzyme: Chất xúc tác cho nhiều phản ứng hóa học (thuận nghịch) trong TB
− Chất ức chế thuận nghịch: Tạo hệ thống cân bằng ộng với enzyme, thường bị loại bỏ qua các quá trình tự nhiên
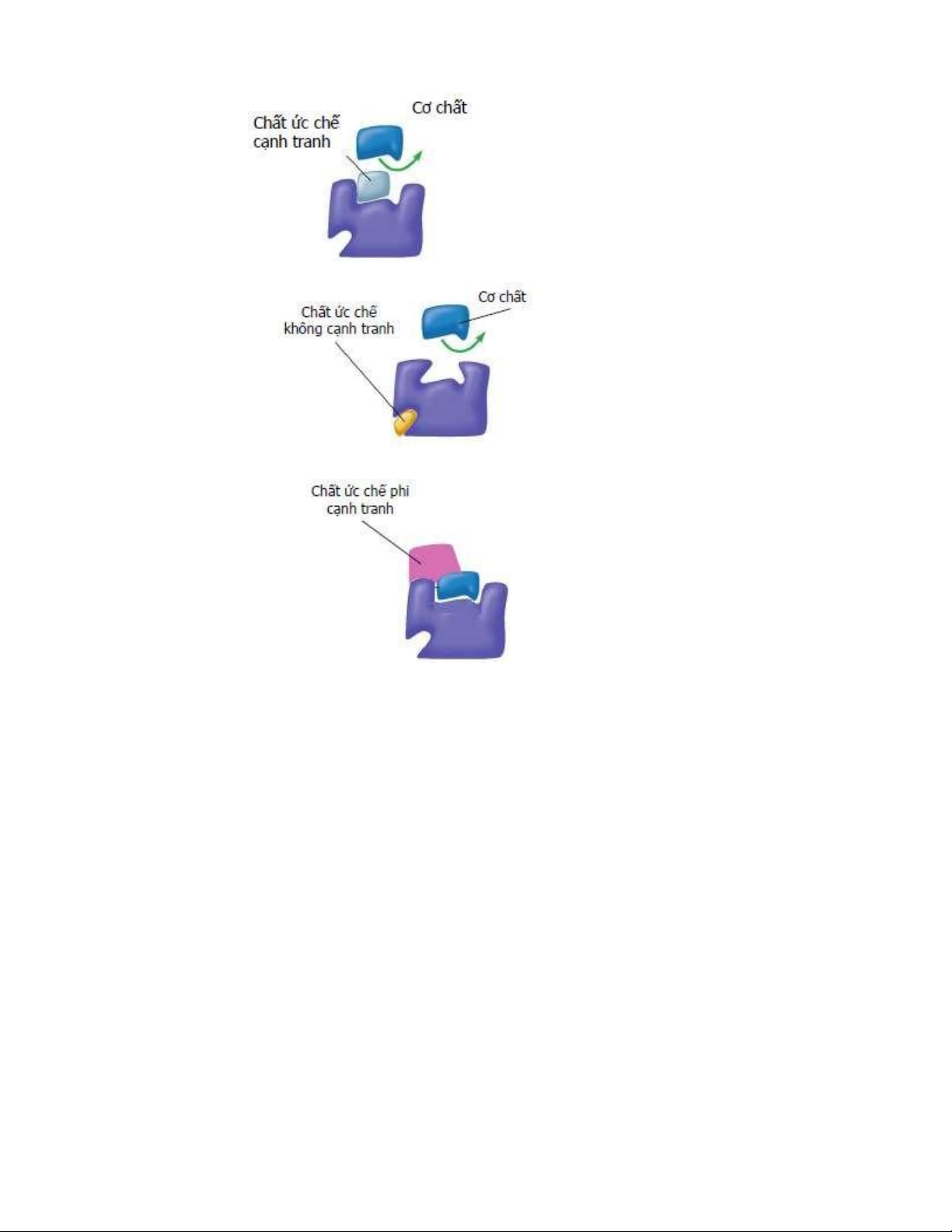
● Chất ức chế cạnh tranh: Cấu trúc tương tự cơ chất
● Chất ức chế không cạnh tranh: Ảnh hưởng ến liên kết của cơ chất với enzyme
● Chất ức chế phi (ϕ) cạnh tranh: Tạo phức hợp với phức hợp enzyme-cơ chất
− Chất ức chế không thuận nghịch: Gắn vào enzyme bằng liên kết mạnh (hóa trị/không hóa
trị), bị phân ly từ từ hoặc mất tác dụng khi cơ thể tổng hợp ủ lượng enzyme ể khôi phục chức năng bị ức chế
● Chất ức chế hướng vị trí hoạt ộng: Gắn kết (thường bằng liên kết cộng hóa trị mạnh
với nhóm chức) tại/gần vị trí hoạt ộng của enzyme
● Chất ức chế tự vẫn: Thường là dẫn chất của cơ chất, bám vào vị trí hoạt ộng và bị
biến ổi bởi enzyme tạo ra phức hợp chất ức chế-enzyme bền vững hoạt ộng
chuyên biệt, ộc tính thấp ọc – SMP − VNU 2
− Chất ức chế trạng thái chuyển tiếp: Chất bền vững có cấu trúc tương tự cơ chất trong trạng
thái chuyển tiếp, bám thuận nghịch/không thuận nghịch vào vị trí hoạt ộng
2. Receptor: Protein tiếp nhận tín hiệu hóa học (ligand) từ bên ngoài, hoạt hóa/ức chế chuỗi phản
ứng sinh hóa liên kết chuyên biệt với nó
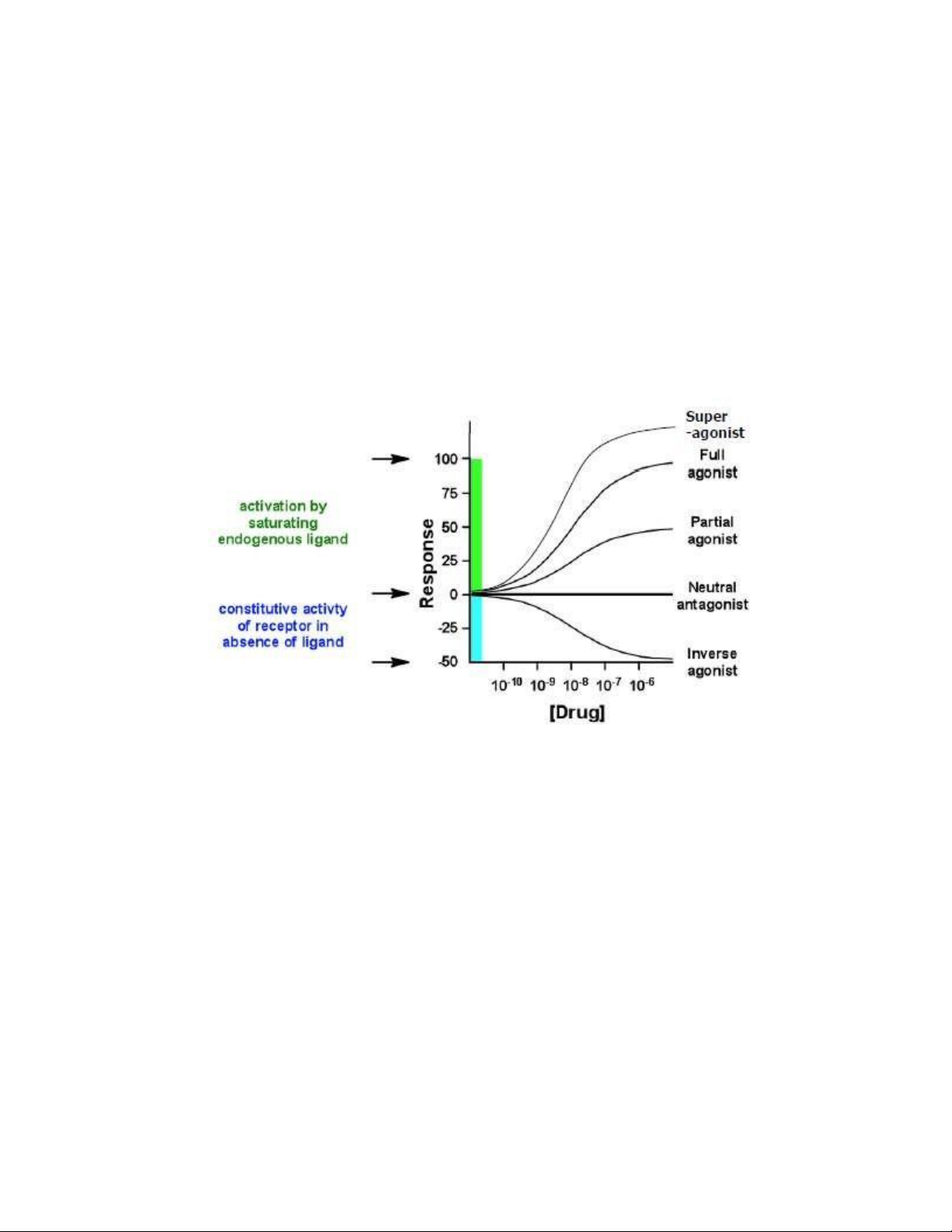
− Chất chủ vận: Hoạt hóa receptor, ặc trưng bới EC50 ● Chất siêu chủ vận
● Chất chủ vận toàn phần
● Chất chủ vận từng phần (tác dụng của hầu hết các thuốc)
− Chất ối vận: Ngăn chặn hoạt ộng của chất chủ vận, ặc trưng bởi IC50
− Chất chủ vận ngược: Gây tác ộng ngược lại với chất chủ vận
3. Acid nucleic: Đại phân tử thiết yếu cho mọi dạng sống, cấu tạo từ ường 5 carbon + nhóm
phosphat + base nitơ purine (A, G) hoặc pyrimidine (T, U, C)
− Chất ức chế quá trình tổng hợp acid nucleic: Ngăn chặn sự tổng hợp DNA
● Chất chống chuyển hóa: Thay thế chất nội sinh tạo sản phẩm không có vai trò,
hoặc ức chế enzyme tham gia vào con ường chuyển hóa
Kháng folate (cofactor trong tổng hợp A, G, T) Kháng purine Kháng pyrimidine
● Chất ức chế enzyme: Ức chế enzyme trực tiếp chịu trách nhiệm tổng hợp acid nucleic
− Chất tác ộng trên phân tử acid nucleic: Ức chế sao chép, nhân ôi, gây chết TB
● Tác nhân chèn mạch: Thường có vòng hoặc dị vòng ngưng tụ phẳng, chèn vào giữa
các base của DNA (liên kết hydro, Van der Waals, tĩnh iện), làm bung từng phần chuỗi xoắn DNA
● Tác nhân alkyl hóa: Hình thành liên kết chéo nội mạch làm vặn chuỗi, hoặc liên
mạch ể khóa chúng lại với nhau
● Tác nhân cắt mạch: Bẻ acid nucleic thành từng mảnh không thể nối lại bằng DNA ligase
4. Màng và thành TB: Lớp vật chất bao quanh giúp bảo vệ, iều hòa, nâng ỡ TB
− Chất ức chế khả năng duy trì sự toàn vẹn của màng TB-màng lipid kép bán thấm gồm nhiều loại lipid và protein
− Chất ức chế quá trình tổng hợp thành TB-nằm bao ngoài màng một số loại TB (ở VK là peptidoglycan)-hoàn chỉnh
− Chất tạo kênh hoặc phá hủy một phần màng/thành TB
Bài 3. Liên quan cấu trúc – tác dụng
1. Mục ích của việc nghiên cứu liên hệ giữa cấu trúc và tác dụng của thuốc
− Khái quát các tác ộng sinh học của việc thay ổi cấu trúc cụ thể
− Phát triển loại thuốc mới tăng cường hoạt tính hoặc có hoạt tính mới và giảm tác dụng phụ so với thuốc hiện hành
2. Tác ộng khi thay ổi hình dạng và kích thước chất lead
− Số lượng nhóm methylene trong chuỗi và vòng
● Khi tăng ở chuỗi có thể tạo dạng hạt micelle làm giảm hoạt tính thuốc
● Khi thay ổi ở vòng có thể thay ổi hoạt tính thuốc − Nồng ộ bão hòa (no) ọc – SMP − VNU 4
● Thêm liên kết ôi làm tăng ộ “cứng” của cấu trúc và có thể tạo ra ồng phân E và Z
● Khử liên kết ôi làm cấu trúc linh hoạt hơn − Hệ vòng
● Thêm vòng có thể tạo ra “túi” thân dầu giúp thuốc dễ dàng bám vào ích
● Các hệ vòng lớn có thể phối hợp với nhau tạo ra chất kháng lại sự tấn công từ enzyme
● Bớt i hệ vòng thường tạo ra chất hoạt ộng tự nhiên hơn
3. Tác ộng khi thêm/thay nhóm thế mới
− Thêm nhóm thế vào vị trí trống Nhóm Độ thân Ảnh hưởng thế dầu -CH3 Tăng Tăng hấp thụ
Giảm giải phóng từ màng TB
Có thể thay ổi con ường và khả năng chuyển hóa
Nhóm alkyl dài hơn có tác ộng tương tự -F và Tăng Tăng hấp thu -Cl
Tích tụ lại trong mô lipid
Thường dùng nhóm -CF3 thay cho -Cl vì chúng có kích thước tương ương -OH Giảm
Tạo trung tâm LK hydro, có thể ảnh hưởng khả năng gắn thuốc vào ích
Có thể tăng tỉ lệ loại bỏ thuốc thông qua con ường chuyển hóa và/hoặc thải trừ mới -NR3 Giảm Tạo muối
Tạo trung tâm LK hydro, có thể ảnh hưởng khả năng gắn thuốc vào ích
Tránh các amine thơm vì chúng thường ộc và/hoặc gây ung thư -COOH Giảm Tạo muối và
Tăng tỉ lệ loại bỏ thuốc -SO3H
Gắn nhóm -COOH vào phân tử nhỏ có thể thay ổi hoạt tính
Gắn nhóm -SO3H thường không thay ổi hoạt tính
− Thay nhóm thế mới vào vị trí cũ: Thường tạo ra chất có cùng hoạt tính với lead
● Nhóm ẳng cấu iện tử (isostere): Phân tử/ion có cùng số nguyên tử và/hoặc số
electron lớp vỏ và/hoặc lớp vỏ electron tương tự nhau
● Nhóm ẳng cấu iện tử sinh học: Hợp chất chứa isostere có hoạt tính sinh học
4. Định lượng liên quan cấu trúc – tác dụng: QSAR
− Phương trình Hansch cho nhóm thế
● log (1/C) = k1*π + k2*σ + k3*ES + k4
● C: nồng ộ chất tối thiểu gây ra áp ứng sinh học
● π: hằng số thân dầu
● σ: hằng số Hammett cho hiệu ứng iện tử
● ES: hằng số Taft cho tác ộng của cấu trúc lập thể
− Biểu ồ Craig: Thể hiện sự kết hợp giá trị của 2 thông số của phương trình Hansch
VD: Để tác dụng cao, nhóm thế cần có giá trị π>0 và σ<0 chọn những nhóm thuộc góc phần tư duới phải
− Cây quyết ịnh Topliss: Định hướng nghiên cứu chất tương ồng có tác dụng tốt nhất
● Với nhóm thế trực tiếp vào vòng thơm
● Với thay ổi trên chuỗi no là nhánh của vòng thơm Bài 4. Chuyển hóa thuốc và thiết kế thuốc 1.
Quá trình chuyển hóa thuốc ọc – SMP − VNU 6
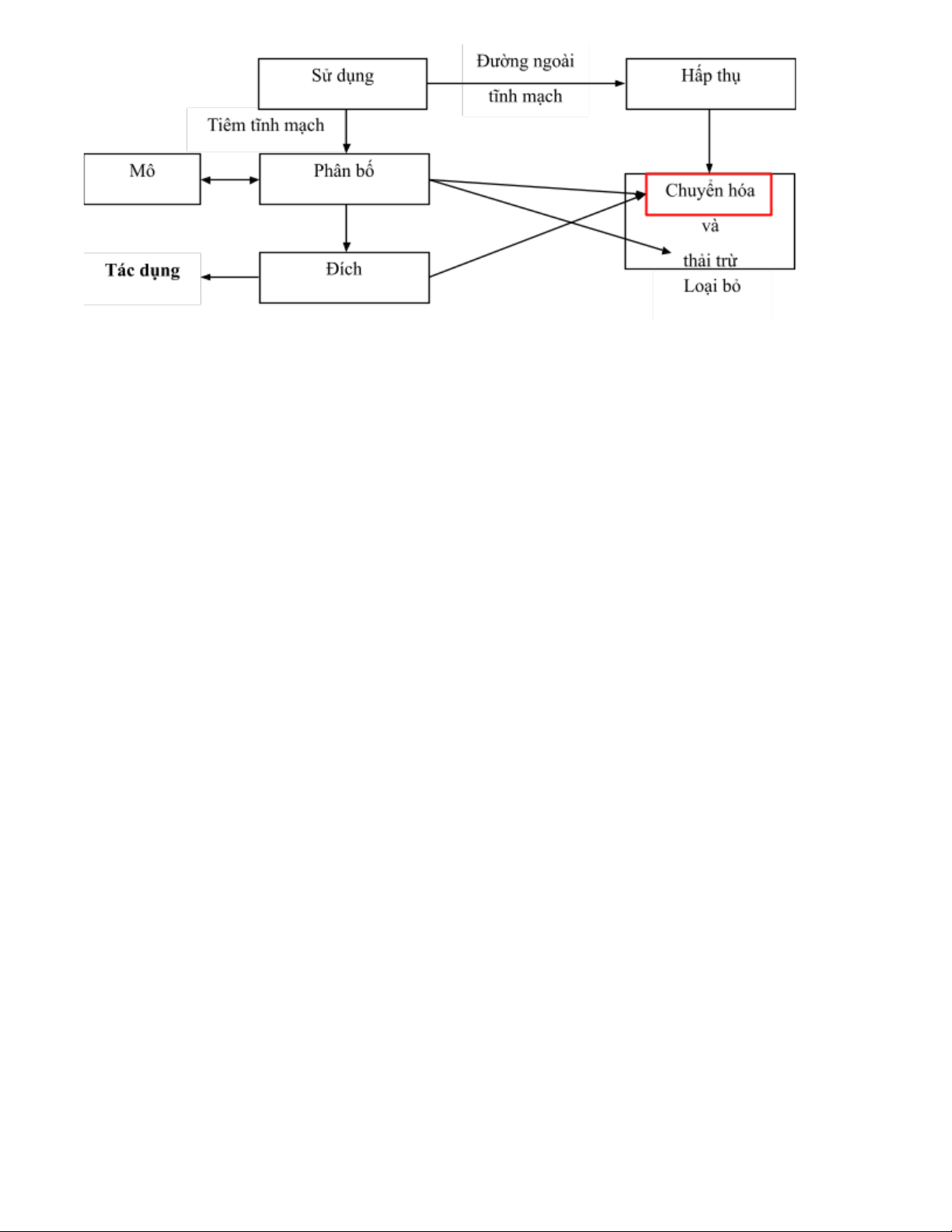
− Số phận của thuốc trong cơ thể
− Các giai oạn của chuyển hóa thuốc
● Chuyển hóa lần ầu (chỉ có ở thuốc dùng ường uống): Ở lòng ruột-dạ dày ● Giai
oạn 1: Biến ổi – Thêm hoặc bộc lộ các nhóm chức (-OH, -SH, -NH2, -COOH,…) ể
hợp chất phân cực hơn bằng các phản ứng: Oxi hóa: Quan trọng nhất
Khử: Quan trọng với các hợp chất chứa cấu trúc chưa bão hòa
Thủy phân: Quan trọng với các hợp chất chứa nhóm ester và amid
Khác: cộng nước, khử carboxyl, alkyl hóa…
● Giai oạn 2: Tiếp hợp – Gắn các chất mang iện (glutathione, sulftate, glycine, acid
glucuronic,…) vào hợp chất, thường thể hiện giai oạn chuyển hóa cuối trước khi thải trừ
● Giai oạn 3: Tiếp tục biến ổi và thải trừ
− Các yếu tố ảnh hưởng
● Loài: Khác biệt lớn do sự thiếu hụt hoặc ủ ầy enzyme
● Yếu tố sinh học (trong 1 loài): Tuổi ời, giới tính, hệ gen, bệnh tật
● Yếu tố ngoại cảnh: Lối sống, dùng thuốc không theo chỉ dẫn
2. Quan hệ giữa chuyển hóa và thiết kế thuốc
− Thay ổi sự chuyển hóa chất lead: Bằng việc thay ổi cấu trúc của thuốc nhằm
● Tăng ộ bền chuyển hóa: Thay vào nhóm ít hoạt ộng hơn
● Giảm ộ bền chuyển hóa: Kết hợp các nhóm bất ổn ịnh vào cấu trúc, có thể tạo ra
Tiền thuốc (prodrug): Hợp chất chỉ có tác dụng khi ã ược chuyển hóa
Thuốc mềm (soft drug): Hợp chất có tác dụng ược chuyển hóa liên tục
thành dạng không ộc, bán thải ngắn − Tiền thuốc (prodrug) ● Phân loại
Chất tiền sinh học: Giải phóng phần có hoạt tính trong cấu trúc sau chuyển hóa
Chất vận chuyển: Chất có hoạt tính ược gắn với chất mang thông qua một
cầu nối (nhóm chức dễ bị chuyển hóa) ● Mục ích
Tăng khả năng hấp thụ và vận chuyển qua màng
Tăng sức chịu ựng từ bệnh nhân Giải phóng chậm
Tác dụng hướng ích ( ặc biệt là khả năng qua hàng rào máu não và tìm kiếm khối u)
Tác dụng phụ tối thiểu
II. Thuốc kháng sinh Bài 1. Đại cương
1. Định nghĩa: Kháng sinh là các chất có nguồn gốc VSV, tổng hợp, bán tổng hợp có tác dụng tiêu
diệt hoặc ức chế sự sinh trưởng của VSV và iều trị nhiễm trùng ở liều nhỏ 2. Phân loại
− Theo nguồn gốc: tự nhiên, bán tổng hợp, tổng hợp. Chỉ số trị liệu (TI): tỉ số giữa MTC và
MEC; chỉ số càng lớn thuốc càng ít ộc
− Theo tác dụng: diệt khuẩn ( ặc trưng bởi MBC) và kìm khuẩn ( ặc trưng bởi MIC)
− Theo phổ tác dụng: phổ rộng ( ộc với vật chủ cao) và phổ hẹp ( ộc với vật chủ thấp)
− Theo cơ chế: ức chế tổng hợp thành TB, ức chế chức năng màng TB, ức chế tổng hợp
protein, chống chuyển hóa, ức chế tổng hợp acid nucleic
− Theo loại VSV ích: thuốc kháng khuẩn (TB nhân sơ), thuốc kháng nấm (TB nhân chuẩn),
thuốc kháng virus (TB chủ) ( ộc tính tăng dần)
− Theo cấu trúc hóa học: các họ kháng sinh 3. Đề kháng
− VSV không bị tiêu diệt hoặc ức chế, do tự nhiên hoặc mắc phải − Cơ chế:
● Sản xuất enzyme phá hủy phân tử thuốc
● Thay ổi khả năng thấm của màng TB với thuốc
● Thay ổi cấu trúc iểm gắn thuốc
● Thay ổi ường biến dưỡng làm mất tác dụng của thuốc ● Thay ổi phân tử ích 4. Sử dụng
− Phải úng, ủ liều, không bỏ liều − Dùng dự phòng
− Phối hợp 2 kháng sinh diệt/kìm khuẩn khác cơ chế, không phối hợp 2 loại với nhau Bài 2. Họ beta-lactam 1. Tính chất chung
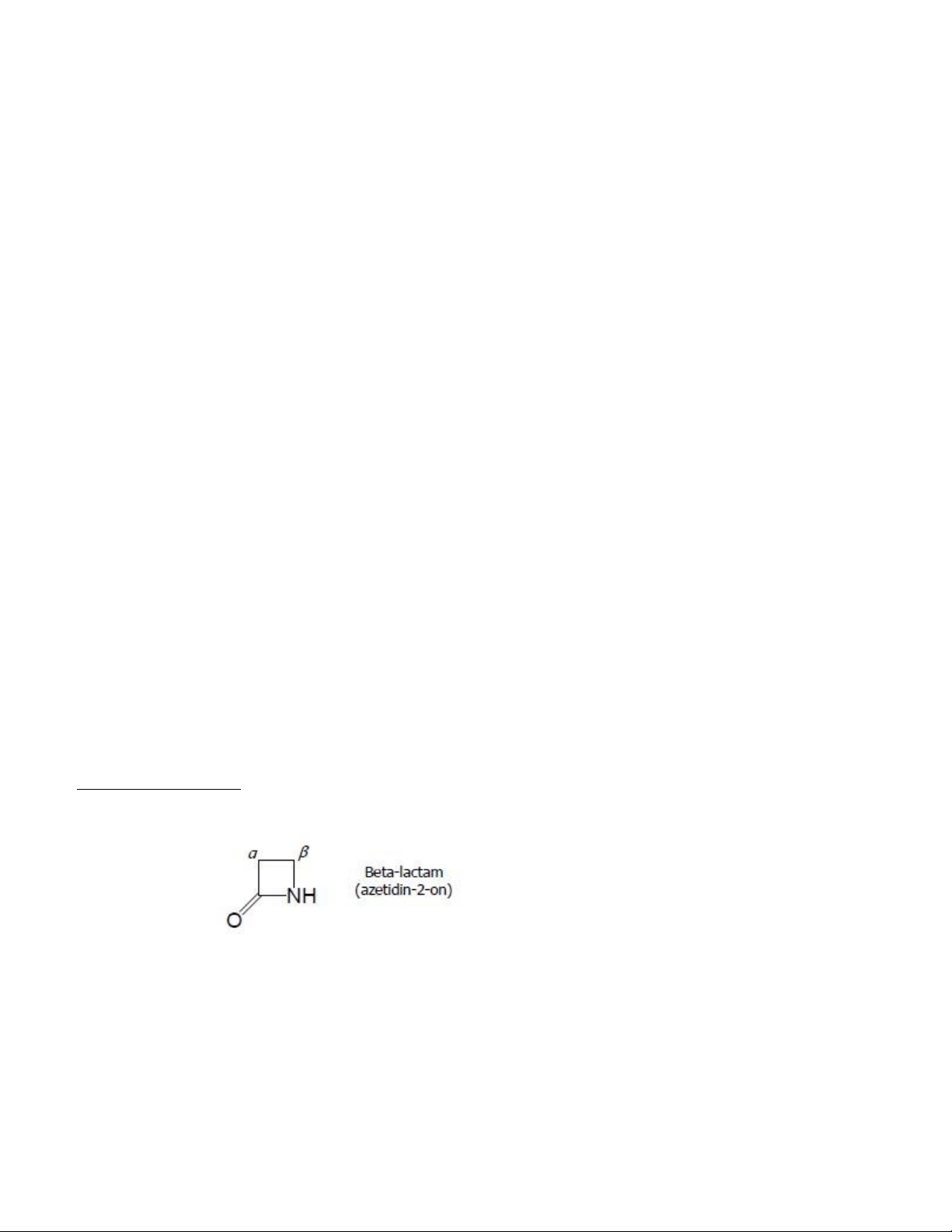
− Cấu trúc: Nguyên tử N gắn vào β-carbon so với nhóm carbonyl
− SAR: Hoạt tính phụ thuộc vào
● Vòng beta-lactam nguyên vẹn
● Nhóm chức có tính acid trên nguyên tử N1 hoặc C2
● Mạch nhánh trên vòng beta-lactam ● Dị vòng ngưng tụ ● C bất ối
− Cơ chế tác dụng: Kháng sinh diệt khuẩn, ngăn chặn sự phát triển và nhân ôi của TB VK
● Ức chế giai oạn transpeptidation cuối cùng trong quá trình tổng hợp peptidoglycan của thành TB VK
● Được xúc tác bởi enzyme PBP bám không thuận nghịch với β-lactam
● Làm tích tụ tiền chất peptidoglycan, hoạt hóa thủy phân peptidoglycan − Đề kháng
● Tự nhiên: beta-lactam phải vượt qua thành TB, khó i qua màng giàu lipid (Gram (-
)), bị chặn lại ở lỗ vận chuyển do nội ộc tố
● Enzyme: VK tổng hợp beta-lactamase. Để khắc phục, β-lactam ược dùng chung
với chất ức chế β-lactamase (hoạt tính kháng sinh yếu, tác dụng ối vận không
thuận nghịch với β-lactamase) ● Biến ổi PBP 2. Phân loại
− Nhóm penicillin (vòng β-lactam ngưng tụ với vòng 5 cạnh có S): Tính acid, ly trích từ
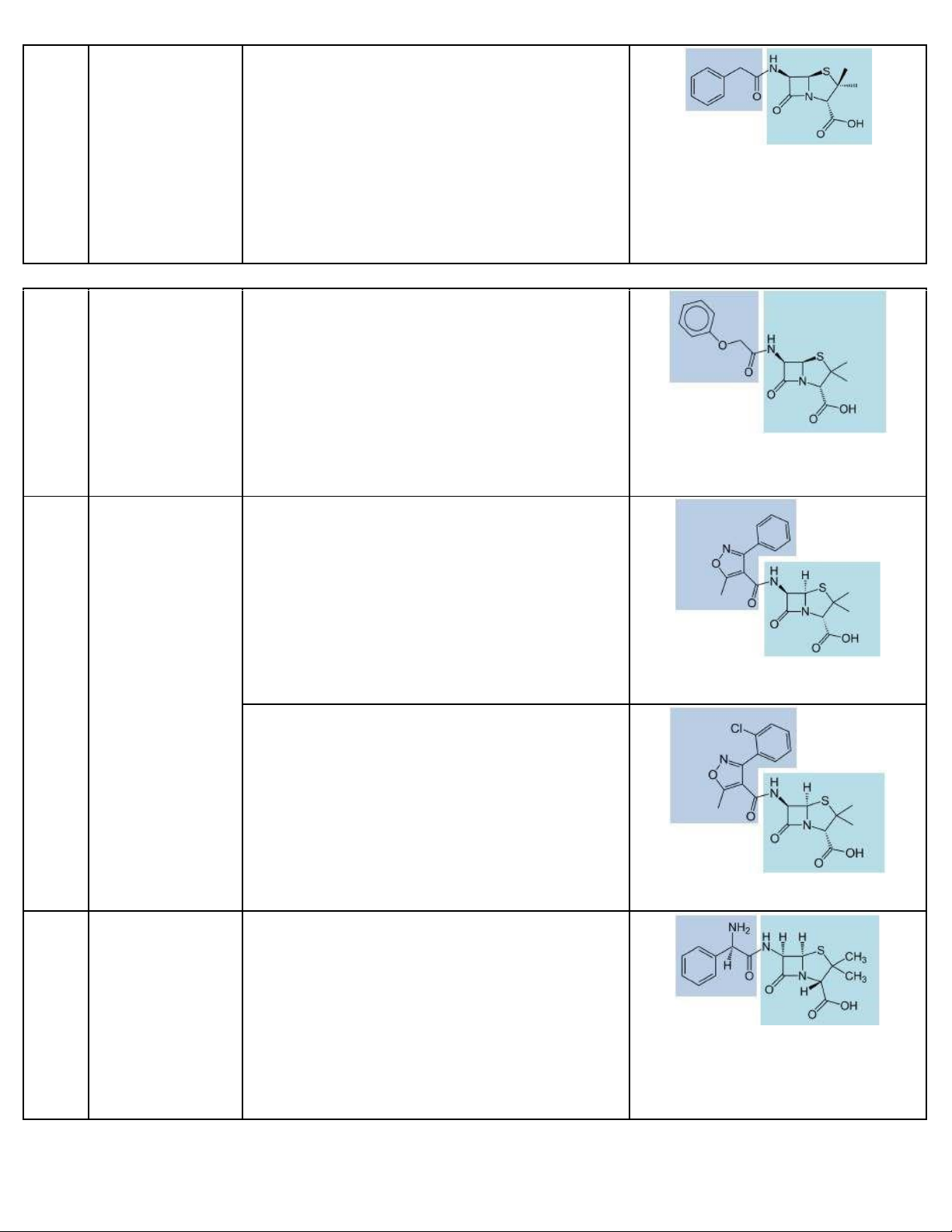
penicillum và bán tổng hợp từ 6-APA Nhóm Phổ kháng khuẩn Chất iển hình Cấu trúc Penicillin G (Benzylpenicillin)
Không bền trong acid dạ dày
Dùng ường tiêm dạng muối kali Phổ hẹp, chủ yếu
Chủ yếu Gram (+), một số Gram (-) I trên Gram (+) Penicillin V (Phenoxylmethylpenicillin)
Bền trong acid dạ dày hơn G
Dùng ường uống dạng muối kali
Gram (+) tương tự G, Gram (-) kém hơn II Phổ hẹp gần Oxacillin giống nhóm I, kháng S. aureus tiết penicillinase Bền trong acid
Dùng ường uống hoặc tiêm dạng muối natri
Chủ yếu iều trị S. aureus Cloxacillin Bền trong acid
Dùng ường uống hoặc tiêm dạng muối natri
Chủ yếu iều trị S. aureus Ampicillin
Mở rộng phổ trên Bền trong acid III Gram (-)
Dùng ường uống hoặc tiêm dạng muối Na+
Chủ yếu Gram (+) và vài chủng Gram (-)
Có thể phối hợp Sulbactam ể mở rộng phổ Amoxicillin Bền trong acid
Dùng ường uống (hấp thu tốt hơn Amp) hoặc tiêm dạng muối natri Phổ rộng
Phối hợp acid Clavulanic ể mở rộng phổ Piperacillin Bền trong acid
Dùng ường tiêm dạng muối natri
Chủ yếu Gram (-), ặc biệt P. aeroginosa Phối
hợp tazobactam hoặc aminoglycoside ể tránh ề kháng IV Mở rộng phổ trên Ticarcillin Gram (-) so với nhóm III, có hoạt tính trên P. Bền trong acid aeruginosae
Dùng ường tiêm dạng muối dinatri
Chủ yếu trên Gram (-), ặc biệt P. aeruginosa Phối
hợp clavulanic acid hoặc aminoglycoside ể tránh ề kháng V Ít hoạt tính trên Gram (+), hoạt tính trung bình trên Gram (-) VI Phổ hẹp, chủ yếu trên Gram (-)
− Nhóm cephalosporin (vòng β-lactam ngưng tụ với vòng 6 cạnh có S): Tính acid, bán tổng hợp từ
7-ACA hoặc penicillin tương ứng Thế hệ Thuốc iển hình Hoạt tính I Cefadroxil
Gram (+): VK tiết penicillinase, tụ cầu và liên cầu nhạy cảm Cefalexin methicillin Cefalotin
Gram (-): P. mirabilis, E. coli, K. pneumoniae (PEcK) Cefazolin II Cefaclor
Gram (+): yếu hơn thế hệ I Cefuroxime
Gram (-): H. influenzae, E. aerogenes, Neisseria (HEN) + PEcK Cefamandol
*: tác dụng trên VK kị khí Cefoxitin* III Cefixime
Gram (+): một số yếu hơn Cefotaxime Gram (-): tăng tác dụng Ceftriaxone *: kháng Pseudomonas Cefoperazone* Ceftazidime* IV Cefepime
Gram (+): mở rộng phổ, tương ương thế hệ I Cefquinome
Gram (-): kháng beta-lactamase hơn thế hệ III, có thể qua hàng rào máu dịch não-tủy V
Ceftobiprole: kháng Pseudomonas Ceftaroline
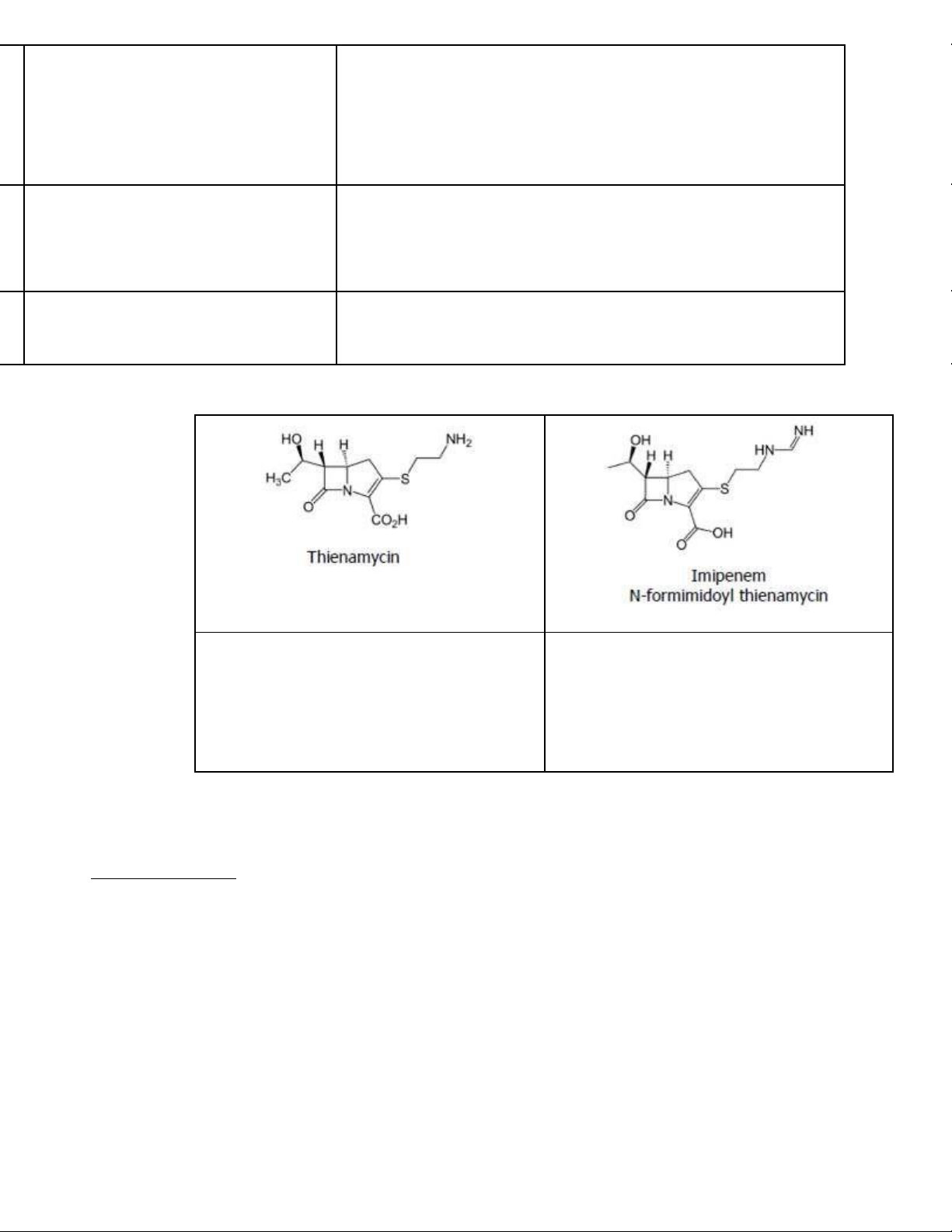
− Nhóm carbapenem (vòng β-lactam ngưng tụ với vòng 5 cạnh không có S): Phổ rộng,
hiệu lực cao trên cả 2 nhóm VK Gram, kháng hầu hết β-lactamase
Không bền hóa học, thu ược bằng cách lên
Bền hơn Thienamycin, phổ cực rộng trên
men Streptomyces, từ ó phát triển các
VK hiếu khí, kỵ khí, Gram (+) và (-), ặc carbapenem khác
biệt kháng Pseudomonas aeruginosa và Enterococcus species
− Nhóm monobactam (vòng β-lactam không ngưng tụ): Chỉ tác dụng trên VK Gram (-); chỉ
có aztreonam ược thương mại hóa Bài 3. Họ aminosid 1. Tính chất chung
− Cấu trúc: Heterosid = Genin + Ose
● Genin: aminocyclitol (cycloalkan có ít nhất 3 nhóm OH gắn vòng + nhóm amino)
● Ose: ường có ít nhất 1 ose amin (glucosamin, ribose, streptose…)
● Tính base rất phân cực (khó thấm màng, bài tiết nhanh), kháng penicillinase
● Nguồn gốc thiên nhiên (streptomyces và micromonospora) và bán tổng hợp − SAR
● Chức amin: Tương tác với receptor ở 30S ribosom
● Nhóm OH: Điều chỉnh sự hấp thu
− Cơ chế tác dụng: Kháng sinh diệt khuẩn, ức chế sinh tổng hợp protein của VK
● Vận chuyển qua màng phụ thuộc oxy
● Gắn vào 30S ribosom gây ọc nhầm tín hiệu, sản xuất protein lạ
● Phổ rộng, chủ yếu là Gram (-) hiếu khí và trực khuẩn Gram (+)
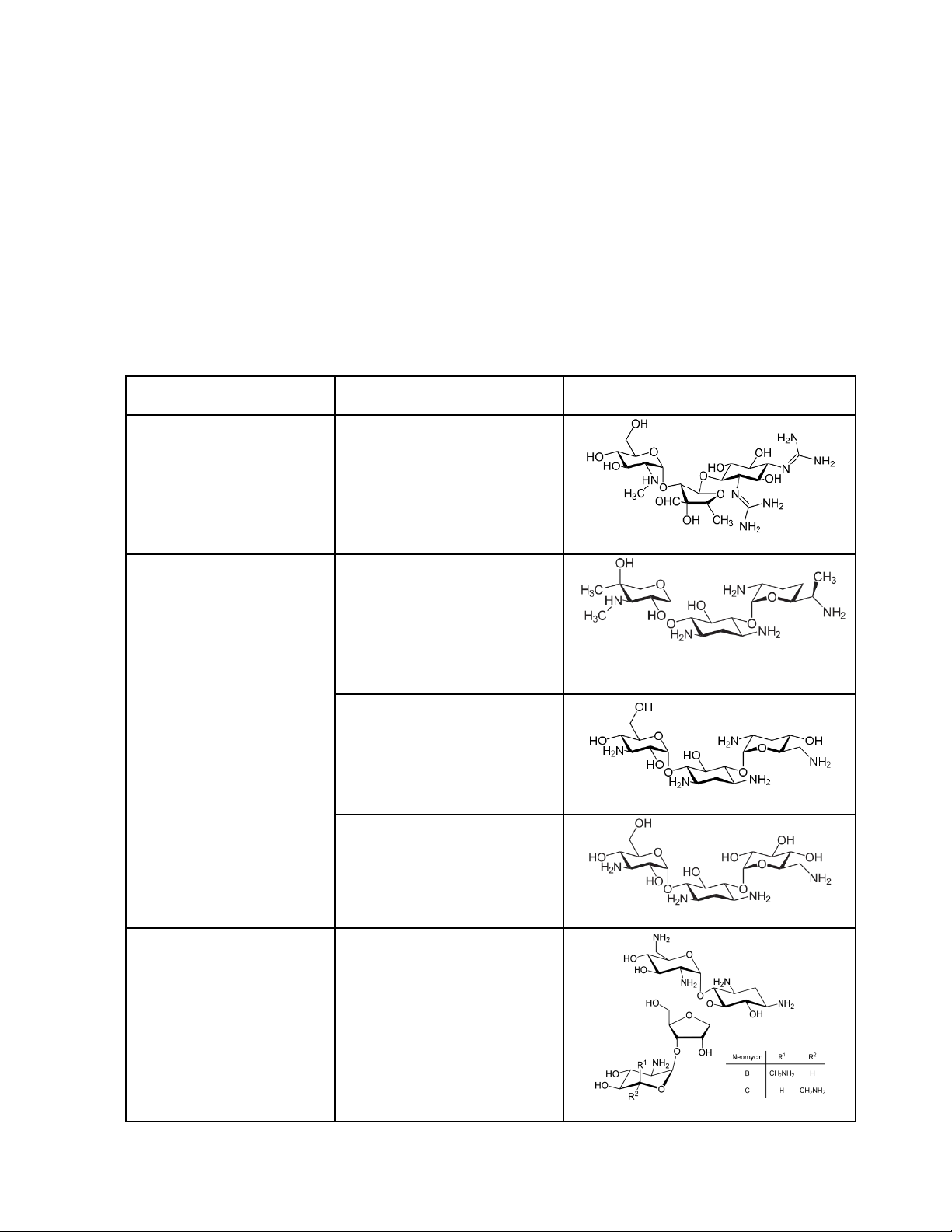
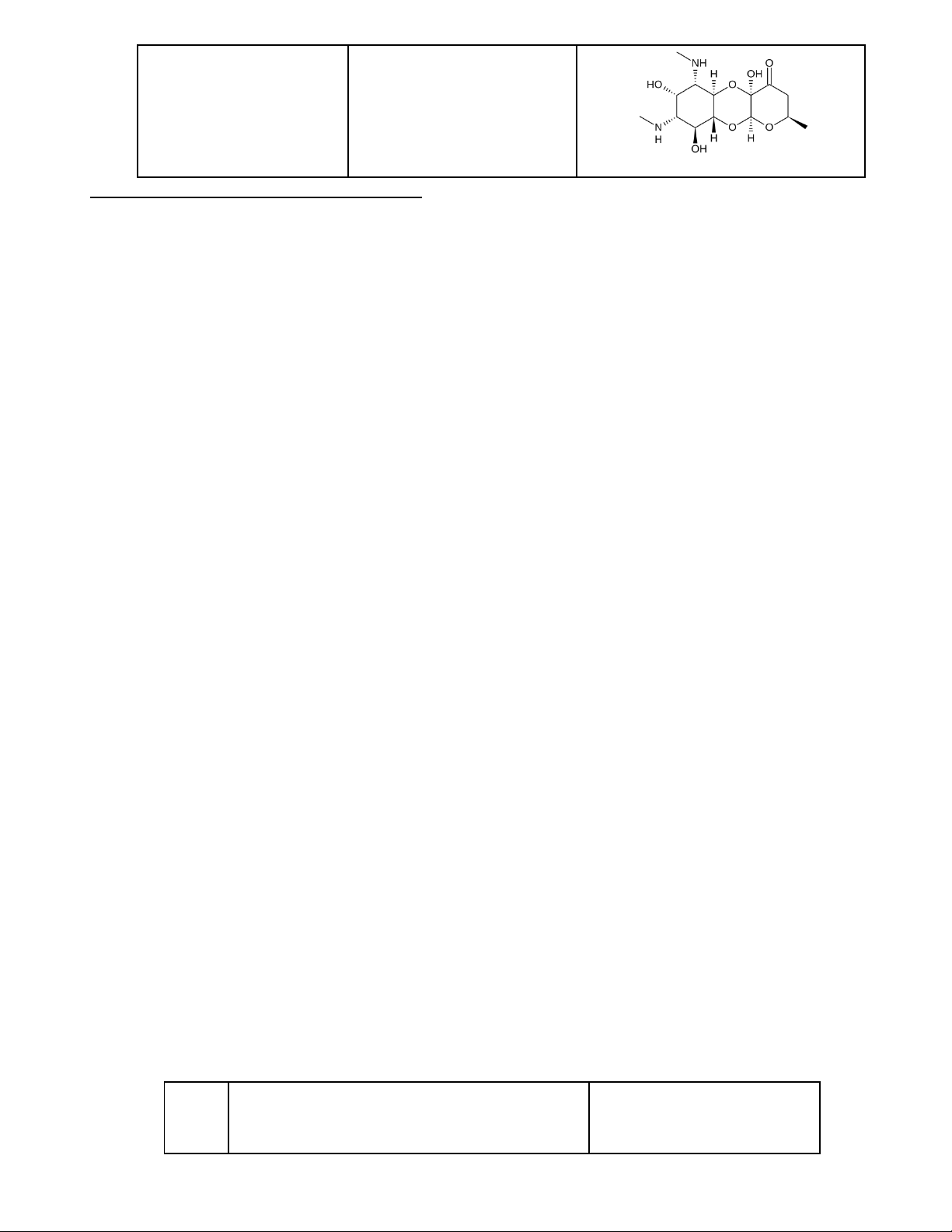
● Tác dụng tốt trên S. aureus, Nesseria miningtidis, N. gonorrhoeae; không tác ộng H. influenzae 2. Phân loại Genin Thuốc iển hình Cấu trúc Streptidin Streptomycin Dạng muối distreptomycin trisulfat Desoxy-2-streptamin thế Gentamycin 4, 6
Là hỗn hợp, dạng muối sulfat Tobramycin Gần giống Gentamycin Kanamycin Dạng muối monosulfat Desoxy-2-streptamin thế Neomycin 4, 5
Là hỗn hợp, dạng muối sulfat Streptamin Spectinomycin Dạng muối hydroclorid
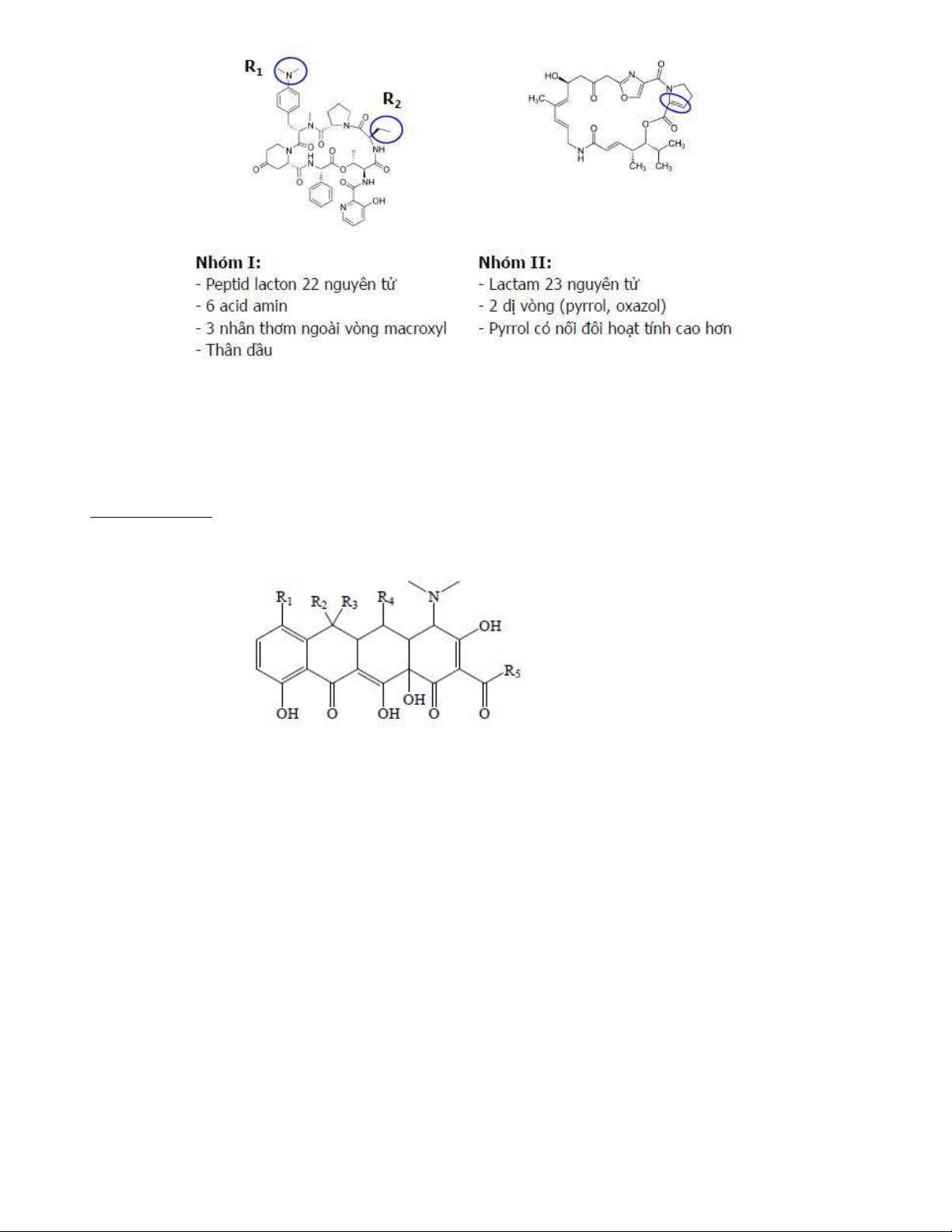
Bài 4. Họ macrolid và kháng sinh tương ồng 1. Tính chất chung
− Cấu trúc: Heterosid = Aglycon + Ose
● Aglycon: lacton 14-16 nguyên tử, gắn OH
● Ose: 2-3 phân tử ường, ít nhất 1 ose amin ● Tính base thân dầu
● Nguồn gốc thiên nhiên (streptomyces) và bán tổng hợp − SAR
● Tính thân dầu: Tăng hoạt lực
● Gắn kết ribosom: Nhóm thế 10, ester, các gốc ường, nhóm amino của ường ●
Mở vòng lacton: Bất hoạt
− Cơ chế tác dụng: Kháng sinh kìm khuẩn ở liều trị liệu, diệt khuẩn ở liều cao, ức chế tổng hợp protein ở VK
● Thấm qua màng Gram (+) cao hơn Gram (-)
● Gắn vào receptor 50S ribosom (trừ ộng vật có vú), ngăn cản giải mã di truyền
● Phổ khá hẹp, chủ yếu trên cầu khuẩn, trực khuẩn Gram (+), một số cầu khuẩn,
trực khuẩn Gram (-), VK yếm khí − Đề kháng
● Tự nhiên: Trực khuẩn Gram (-) ngăn thuốc thấm qua porin
● Thu nhận (qua plasmid): Cầu khuẩn Gram (+) giảm tính thấm qua thành hoặc
thay ổi thụ thể; VK ường ruột tiết enzyme thủy phân thuốc
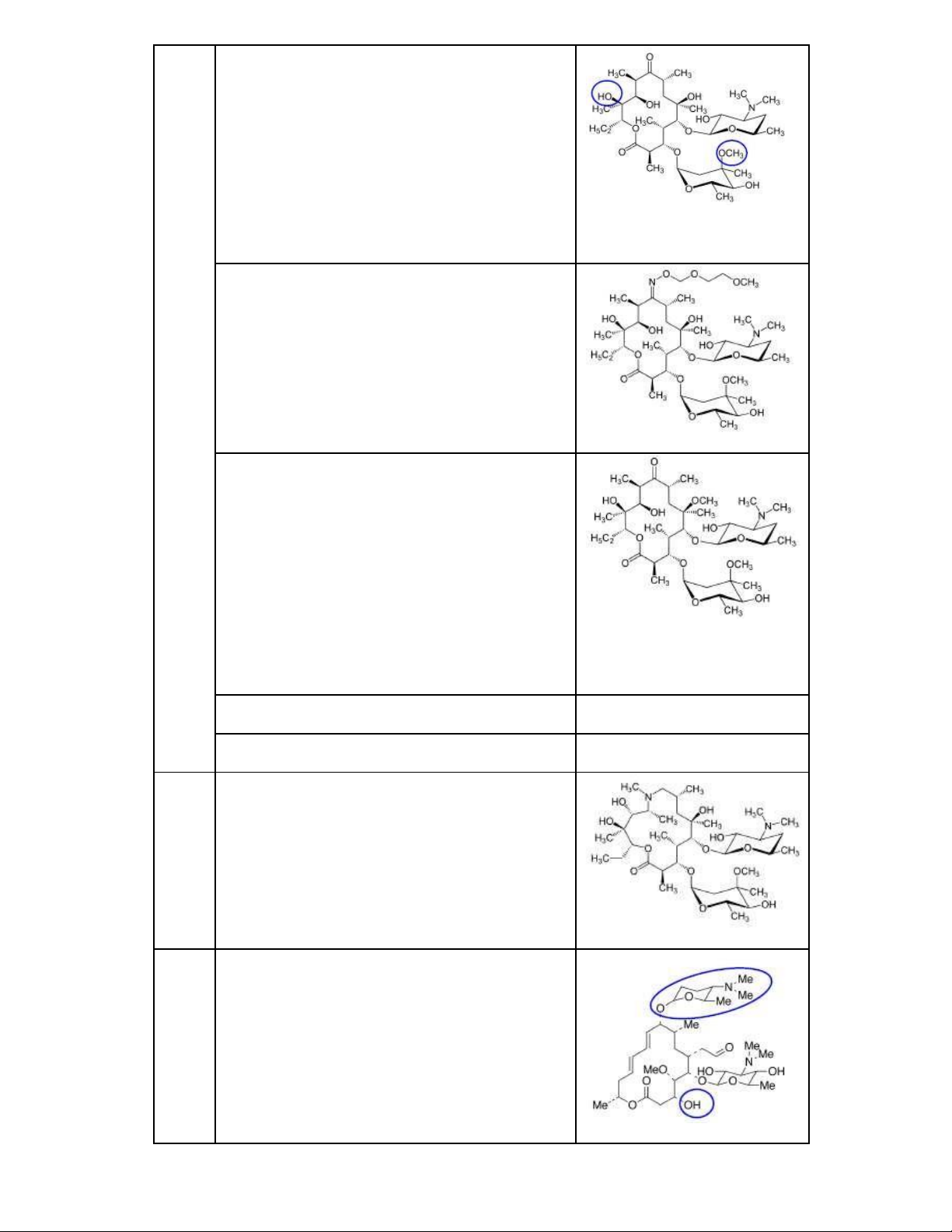
● Chéo: Giữa các kháng sinh cùng nhóm, nhất là macrolid cổ iển 2. Phân loại Vòng Thuốc iển hình Cấu trúc lacton 14 Erythromycin Là hỗn hợp
Dạng base, muối, ester, muối ester
Độc tính thấp, có thể dùng cho phụ nữ mang thai (trừ dạng estolat) Roxithromycin
Bền hơn erythromycin trong acid, mạnh hơn
trên một số mầm Gram (-) Clarithromycin
Bền hơn erythromycin trong acid, mạnh hơn
trên tụ cầu, liên cầu và chủng ề kháng
Chất chuyển hóa qua gan có hoạt tính mạnh gấp ôi
Chỉ ịnh loét dạ dày do H. pylori Dirithromycin Flurithromycin 15 Azithromycin
Bền hơn erythromycin trong acid, phổ mở rộng sang Gram (-) 16 Spiramycin Là hỗn hợp
Độc tính thấp, chỉ ịnh nhiễm toxoplasma ở phụ nữ mang thai 3. Họ streptogramin − Cấu trúc
− Phổ kháng khuẩn tương tự macrolid, ít ề kháng, ồng vận với aminosid, rifampicin Bài 5. Họ cyclin 1. Tính chất chung
− Cấu trúc: Octahydronaphtacen
● Tính base; tính acid nhẹ
● Nguồn gốc thiên nhiên (streptomyces) và bán tổng hợp − SAR ● Thân dầu
● Nhóm alkyl cồng kềnh, dễ tạo phức với cation a hóa trị giảm hấp thu qua màng ruột
− Cơ chế tác dụng: Kháng sinh kìm khuẩn (trừ minocyclin), ức chế tổng hợp protein
● Dạng muối HCl hấp thu nhanh qua tiêu hóa
● Bám vào 30S ribosom, ngăn tRNA kết hợp mRNA ribosom không thể phóng thích acid amin
● Phổ rộng: Gram (+), (-), mầm nội bào, Candida, amip ruột
● Chỉ ịnh cho viêm, H. influenza, Brucella, protozoa, mụn
− Đề kháng: Tác dụng mạnh trên Gram (+) nhưng nhanh bị ề kháng ít dùng
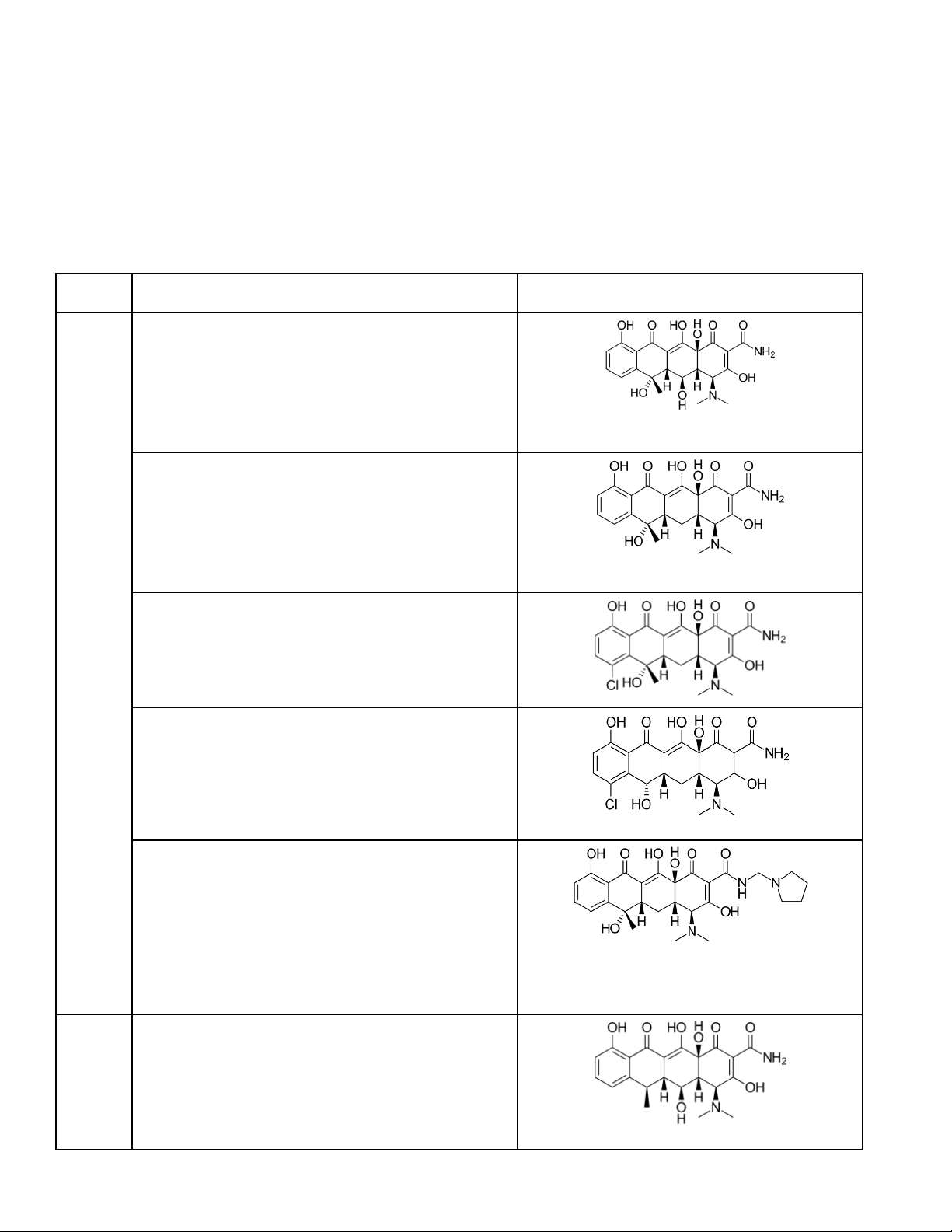
2. Phân loại (hoạt tính mạnh dần) Thế hệ Thuốc iển hình Cấu trúc I Oxytetracyclin
Hoạt tính giảm trong acid, phân hủy nhanh trong kiềm Tetracyclin
Thêm công dụng trị H. pylori dạ dày, nhiễm toxoplasma Clotetracyclin
Dạng muối HCl, tương tự tetracyclin Demeclocyclin Dạng muối HCl, bền hơn Rolitetracyclin
Tiền chất của tetracyclin, dạng base hoặc muối nitrat Trị Mycobacterium marium II Doxycyclin
Bền hơn, hấp thu nhanh, hoạt tính hơn tetracyclin 2 lần
Chuyên trị tiêu chảy cho người du lịch, VK yếm
khí (Leptospirosis), T. palladium, N. gonorrhea Minocyclin
Bền hơn, hấp thu tốt, dạng muối HCl, hoạt tính hơn 2-4 lần
Đặc biệt trị Streptococcus viridans, M. marium Bài 6. Họ lincosamid 1. Tính chất chung
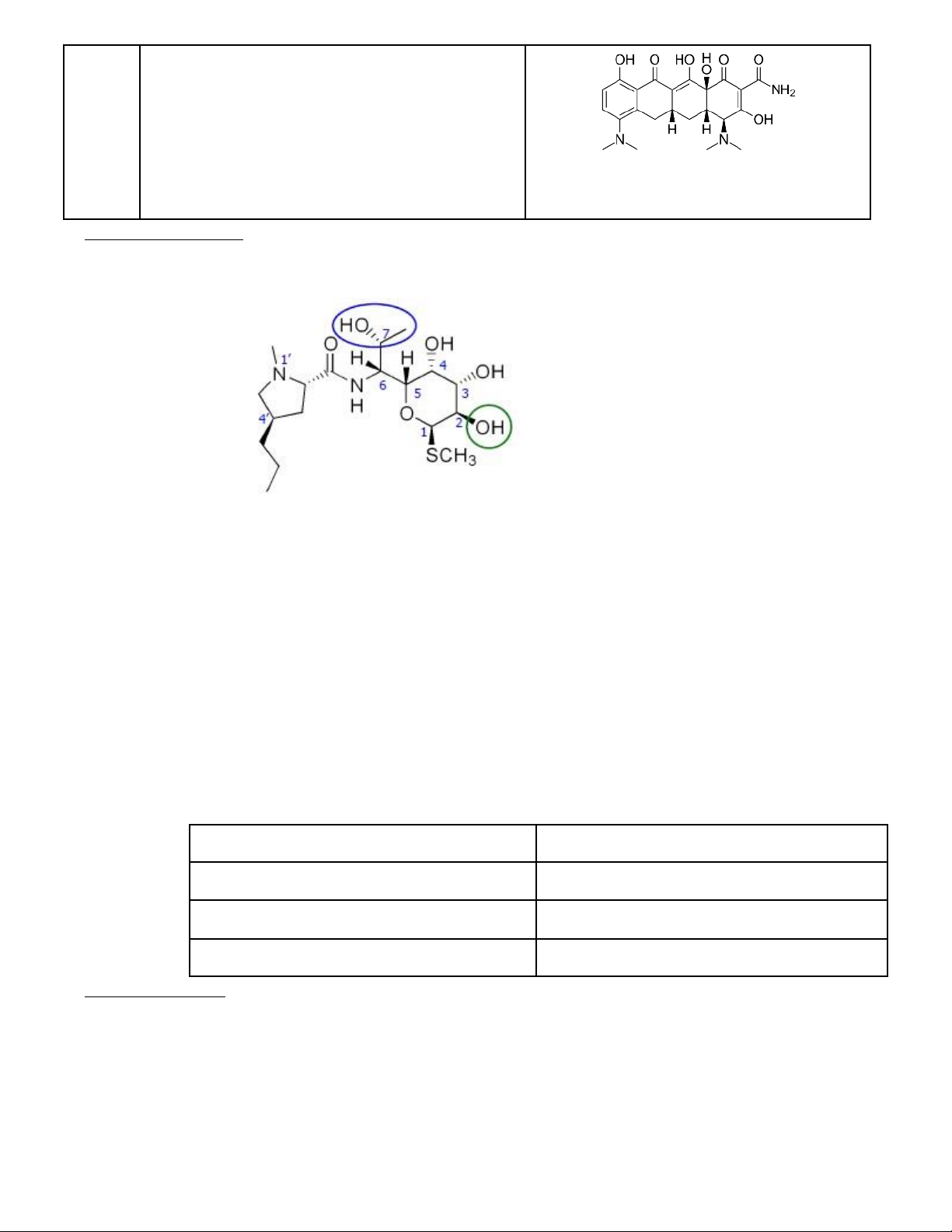
− Cấu trúc: Amid = Acid hygric + Ose amin chứa S
− Cơ chế tác dụng: Kháng sinh kìm khuẩn, ức chế giai oạn ầu tổng hợp protein
● Phân phối tốt vào các mô, không vào dịch não tủy
● Tác ộng lên 50S ribosom (giống macrolid) làm peptidyl-tRNA phân ly sớm khỏi ribosom
● Hoạt tính trên trực khuẩn Gram (-), cầu khuẩn Gram (+), một số VK yếm khí, KST sốt rét 2. Phân loại Lincomycin (7R) –CHOHCH3 Clindamycin (7S) –CHClCH3 Clindamycin phosphat -O-PO3H2 Clindamycin palmitat -OCO(CH2)14CH3 Bài 7. Họ phenicol 1. Tính chất chung − SAR
● Cần sự toàn vẹn cấu trúc học – SMP − VNU 19