
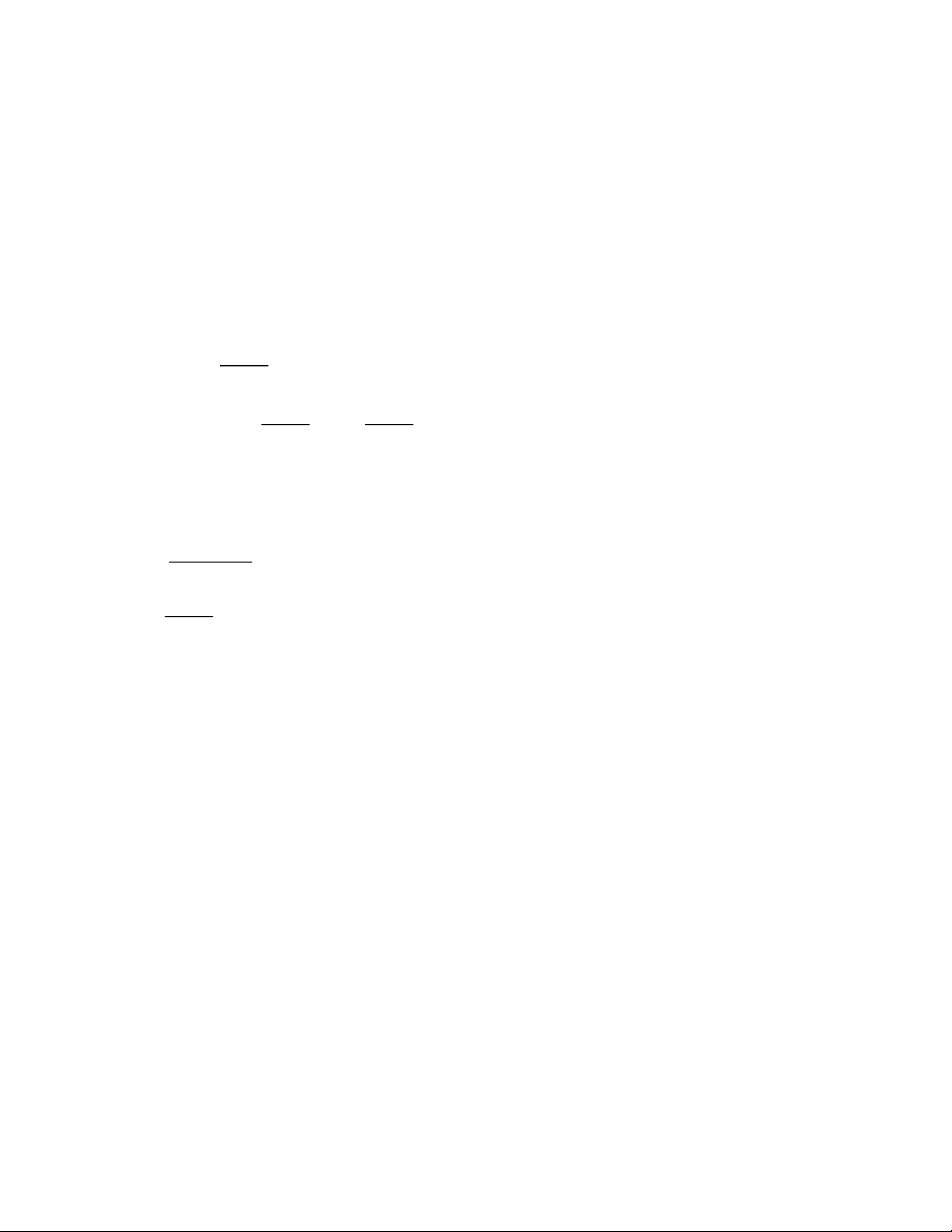
Preview text:
7. Động học các phản ứng phức tạp
7.1 Phản ứng thuận nghịch
Xét trường hợp phản ứng thuận nghịch – bậc nhất: kt A B kn t = 0 : a b
t = t : a − x b + x 1
t = t : a − x b + x
Trong đó: - kt, kn lần lượt là hằng số tốc độ phản ứng thuận và phản ứng nghịch.
- a, b là nồng độ ban đầu của A và B
- x và x lần lượt là lượng chất A đã phản ứng tại thời điểm t1 và thời điểm cân bằng.
Tốc độ phản ứng thuận, phản ứng nghịch – bậc nhất là:
v = k .(a − x) t t
v = k .(b + x) n n dx
Tốc độ tổng cộng của phản ứng là:
= v − v = k (a − x) + k (b + x) t n t n dt x
Giải phương trình tích phân có: (k + k ).t = ln t n x − x b + x k
Tại thời điểm cân bằng: t K = = cb a − x k n 7.2 Phản ứng song song
Định nghĩa: phản ứng song song là phản ứng chỉ có một chất đầu tham gia vào các phản
ứng tao ra các sản phẩm theo các hướng khác nhau.
Xét trường hợp đơn giản nhất là hai phản ứng song song bậc nhất một chiều:
Tốc độ phản ứng thứ nhất và thứ hai là : dx dx 1 v =
= k (a − x) (1) ; 2 v =
= k (a − x) (2) 1 1 dt 2 2 dt
Vận tốc tiêu thụ A theo hai phản ứng song song là: dx
d (x + x ) dx dx 1 2 1 2 v = = = +
= (k + k ).(a − x) 1 2 dt dt dt dt a [ ] A Tích phân ta có:
(k + k ).t = ln = ln o 1 2 a − x [ ] A t −( + 1 k k2 ). C = [ ] A = [ ] A . t e A t o k .[ ] A 1 o −( + 1 k k2 ). C = x = (1 t − e ) B 1 k + k
Dùng các phép biến đổi ta có: 1 2 k .[ ] A 2 o −( + 1 k k2 ). C = x = (1 t − e ) C 2 k + k 1 2 C
+ C + C = a = [ ] A A B C o x k
Lấy p.t (1) chia (2) và tích phân ta có: 1 1 = x k 2 2
Tổng quát: Nồng độ chất sản phẩm trong phản ứng song song tỉ lệ thuận với hằng số tốc
độ phản ứng tương ứng: x : x :...: x = k : k :...: k 1 2 n 1 2 n 7.3 Phản ứng nối tiếp
Định nghĩa: các phản ứng gọi là nối tiếp nếu một sản phẩm được tạo ra ở phản ứng này
lại bị tiêu thụ trong phản ứng khác.
Xét trường hợp đơn giản nhất: hai phản ứng nối tiếp bậc nhất: 1 k k2 A ⎯⎯ → B ⎯⎯→C t = 0 : a 0 0
t = t : a − x x − y y 1
Sử dụng định nghĩa tốc độ phản ứng, ĐL tác dụng khối lượng, tích phân ta thu được biểu thức
tính nồng độ các chất như sau: −k .t −k .t 1 1 C = a − x = . a e = [ ] A .e A o k 1 − − 1 k .t k2 .
C = x − y = .[ ] A .( t e − e ) B o k − k 1 2 k − k 2 − 1 k .t 1 k2 . C = y = [ ] A . 1− .e + . t e C o k − k k − k 2 1 2 1 C
+ C + C = a A B C
Ngoài ra, cần phản xác định thời điểm tmax khi nồng độ B đạt cực đại: ln k − ln k 1 2 t = max k − k 1 2 k 1 − − 1 k .tmax k2 .tmax C = .[ ] A .(e − e ) B o k − k 1 2




