














Preview text:
lOMoAR cPSD| 45734214
BỘ GIÁO DỤC VÀ ĐÀO TẠO
TRƯỜNG ĐẠI HỌC LẠC HỒNG GIÁO TRÌNH
THỰC HÀNH HOÁ DƯỢC HỒ DŨNG MẠNH
PHÙNG THỊ THU THUỶ KIM NGỌC SƠN HOÀNG VIẾT NHÂM HUỲNH VĂN THỐNG Tháng 9/2020 lOMoAR cPSD| 45734214 LỜI MỞ ĐẦU
Trong vài thập kỷ gần đây, cùng với sự phát triển mạnh mẽ của các ngành khoa học kỹ
thuật nói chung, ngành Hoá Dược cũng có đóng ghóp nhiều thuốc mới, phục vụ công
tác ph ng và chữa bệnh cho người dân. Nhằm đáp ứng nhu cầu đào tạo trong chương
trình đại học cho sinh viên nghành Dược, giáo trình này được biên soạn nhằm giúp sinh
viên làm quen với các kỹ thuật tổng hợp và kiểm nghiệm nguyên liệu Hoá Dược trong ph ng thí nghiệm.
Giáo trình Thực hành Hoá Dược bao gồm phần lý thuyết cơ bản giới thiệu các dụng cụ
cơ bản, cách sử dụng các thiết bị trong tổng hợp và kiểm nghiệm nguyên liệu Hoá Dược.
Phần thực tập bao gồm các bài thực hành cụ thể như tổng hợp và kiểm nghiệm nguyên
liệu acid benzoic, sulfacetamid, methyl salicylat, paracetamol.
Giáo trình được sử dụng cho các sinh viên ngành Dược năm 3 hệ Chính quy và
năm 2 hệ Liên thông trung cấp.
Trong quá trình biên soạn không thể tránh khỏi những thiếu sót, ban biên soạn mong
nhận được những góp ý quý báu của quý Thầy cô đồng nghiệp, các bạn sinh viên để giáo
trình hoàn thiện hơn trong những lần tái bản sau.
Biên Hoà, ngày 20 tháng 9 năm 2020 2 lOMoAR cPSD| 45734214 MỤC LỤC
LỜI MỞ ĐẦU .................................................................................................................. 2
MỤC LỤC ........................................................................................................................ 3
CHƯƠNG 1. TỔNG HỢP VÀ KIỂM NGHIỆM PARACETAMOL ............................... 3
CHƯƠNG 2. TỔNG HỢP ACID BENZOIC ................................................................... 8
CHƯƠNG 3. KIỂM NGHIỆM ACID BENZOIC .......................................................... 11
CHƯƠNG 4. KIỂM NGHIỆM SULFANILAMID ........................................................ 15
CHƯƠNG 5. TỔNG HỢP SULFACETAMID ............................................................... 21
CHƯƠNG 6. TỔNG HỢP METHYL SALICYLAT ...................................................... 24
CHƯƠNG 7. KIỂM NGHIỆM METHYL SALICYLAT .............................................. 27
TÀI LIỆU THAM KHẢO .............................................................................................. 31
CHƯƠNG 1. TỔNG HỢP VÀ KIỂM NGHIỆM PARACETAMOL Mục tiêu:
- Tổng hợp paracetamol và tính toán được hiệu suất phản ứng tổng hợp 3 lOMoAR cPSD| 45734214
- Kiểm nghiệm dược chất paracetamol và trình bày kết quả vào phiếu kiểm nghiệm
- Thể hiện được khả năng làm viêc nhóm nhỏ để hoàn thành bài thí nghiệm
A. CƠ SỞ LÝ THUYẾT
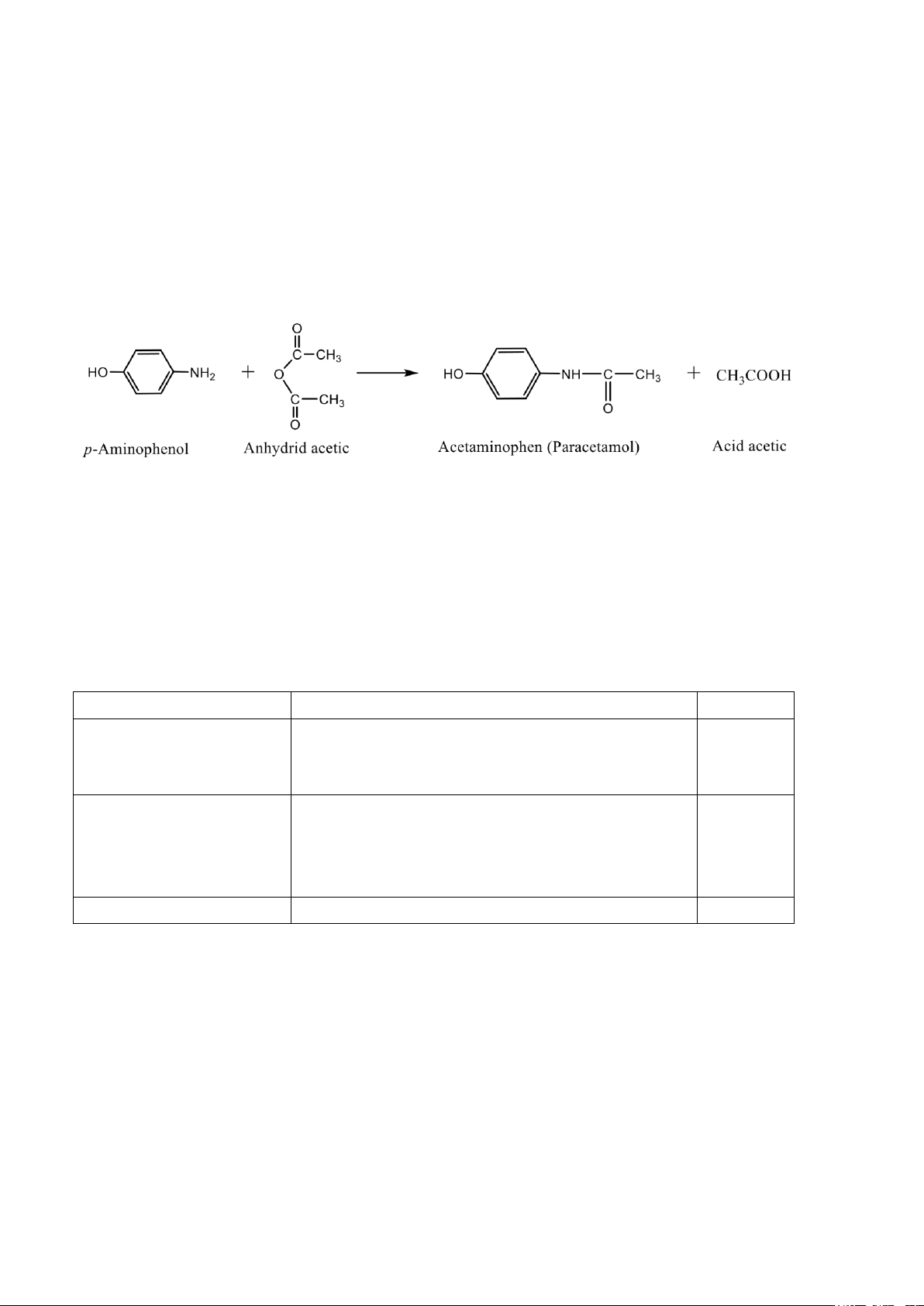
Paracetamol là một amid, được tổng hợp thông qua phản ứng giữa p-aminophenol và anhydrid acetic.
Nguyên liệu paracetamol (N-(4-hydroxyphenyl)acetamid) phải chứa không ít hơn 98%
và không nhiều hơn 101% C8H9NO2, tính theo chế phẩm đã làm khan.
Tính chất: Tinh thể không màu hoặc bột kết tinh trắng, không mùi hoặc gần như không
mùi. Khó tan trong nước, dễ tan trong ethanol 96%, tan ít trong methylen clorid. Điểm
chảy ở khoảng 168 - 172 oC.
Công dụng: giảm đau, hạ sốt. Chỉ tiêu
Tiêu chuẩn trong bài thực hành Kết luận Định tính
Điểm chảy: 168 oC đến 172 oC
Có phản ứng đặc trưng của gốc 4-aminophenol
Có phản ứng đặc trưng của nhóm acetyl
Các giới hạn tạp chất Clorid Không được quá 0,015% Sulfat Không được quá 0,04% Kim loại nặng Không được quá 0,001% Hàm lượng
98,0-101,0% C8H9NO2, tính trên chất khan B. THỰC HÀNH
TỔNG HỢP PARACETAMOL
- Cho 1,50 g p-aminophenol vào erlen nút mài 100 ml. Thêm 20 ml nước và 5 giọt acid
H3PO4 đậm đặc và 2 ml anhydrid acetic, lắc đều hỗn hợp.
- Giữ erlen ở nhiệt độ 80 oC trong v ng 20 phút (sử dụng bếp cách thủy). Thỉnh thoảng lắc đều. 4 lOMoAR cPSD| 45734214
- Làm lạnh hỗn hợp sau phản ứng trong chậu nước đá để kết tinh sản phẩm. (có thể dùng
đũa cạ vào thành bình để khơi mầm kết tinh) - Lọc thu tinh thể bẳng phễu lọc Buchner.
- H a tan paracetamol thô trong khoảng 10 ml nước cất ở 80 oC. Làm lạnh để kết tinh.
- Lọc qua phễu buchner để thu tinh thể . Rửa lại tinh thể bằng 10 ml nước lạnh.
- Sấy khô, đem cân và tính hiệu suất.
KIỂM NGHIỆM PARACETAMOL 1. Định tính
A. Điểm chảy: 168 oC đến 172 oC
B. Đun cách thủy 0,1 g chế phẩm trong 3 ml acid hydrocloric 10% ở nhiệt độ 80 - 90
oC trong 5 phút, làm lạnh trong đá, không có tủa tạo thành. Thêm 0,05 ml dung dịch
kali dicromat 0,49%, xuất hiện màu tím và không chuyển sang màu đỏ.
C. Lấy một ống nghiệm (kích thước 18 mm × 180 mm), cho vào khoảng 0,1 g chế phẩm
hay một lượng theo chỉ dẫn trong chuyên luận và 0,5 ml acid phosphoric (TT). Đậy
ống nghiệm bằng một nút có mang bên trong một ống nghiệm nhỏ hơn (kích thước
10 mm × 100 mm), ống nghiệm này chứa nước để làm sinh hàn. Cho một giọt dung
dịch lanthan nitrat 5% (TT) bám vào thành đáy ngoài của ống nghiệm nhỏ (sao cho
giọt thuốc thử này không bị rơi xuống ống nghiệm chứa chế phẩm trong suốt quá
trình thí nghiệm, nếu rơi phải làm lại thí nghiệm từ đầu). Đun hỗn hợp từ từ tới sôi
trên ngọn lửa trong 5 phút sau đó lấy ống nghiệm nhỏ ra, gạt chất lỏng thu được ở
đáy ngoài ống nghiệm vào một tấm sứ trắng đã chứa sẵn 0,05 ml dung dịch lanthan
nitrat 5% (TT) và 0,05 ml dung dịch iod 0,02 N (TT), thêm vào cạnh đó 0,05 ml dung
dịch amoniac 2 M (TT). Sau 1 phút đến 2 phút, ở v ng tiếp xúc giữa hai dung dịch
xuất hiện màu xanh lam dần dần thẫm lên và bền trong một thời gian ngắn.
2. Thử tinh khiết
Pha dung dịch A: Cho vào becher 2,0 g chế phẩm và khoảng 40 ml nước cất, siêu âm
trong 5 phút. Lọc vào bình định mức và dùng nước cất để tráng becher và giấy lọc đến
khi vừa đủ 50 ml (dung dịch A) để làm các kiểm định dưới đây.
2.1. Giới hạn clorid: không được quá 0,015%
Ống thử: Cho 8,3 ml dung dịch A, thêm nước cất vừa đủ 16 ml.
Ống chuẩn: Cho 10 ml dung dịch chuẩn clorid 5 ppm (10 ml chứa 0,05 mg ion clorid),
thêm nước cất vừa đủ 16 ml. 5 lOMoAR cPSD| 45734214
Cho vào mỗi ống 0,5 ml dung dịch HNO3 30%, 0,5 ml dung dịch AgNO3 2%, lắc đều.
Sau 5 phút, so sánh độ đục của hai ống: ống thử không được đục hơn ống chuẩn.
(Cách quan sát độ đục: đặt ống thử và ống chuẩn thẳng đứng trên nền đen, nhìn từ trên
xuống theo trục ống.)
2.2. Giới hạn sulfat: không được quá 0,04%
Ống thử: Cho 9,4 ml dung dịch A, thêm nước cất vừa đủ 16 ml.
Ống chuẩn: Cho 15 ml dung dịch chuẩn sulfat 10 ppm (10 ml chứa 0,1 mg ion sulfat),
thêm nước cất vừa đủ 16 ml.
Cho vào mỗi ống 0,5 ml dung dịch HCl 3 M, 1 ml dung dịch BaCl2 5%, lắc đều. Sau 5
phút, so sánh độ đục của hai ống: ống thử không được đục hơn ống chuẩn.
2.3. Giới hạn kim loại nặng: không được quá 0,001%
Pha 50 ml dung dịch chế phẩm 5% trong ethanol 96% (dùng bình định mức).
Ống thử: lấy 12 ml dung dịch trên, thêm 2 ml dung dịch đệm acetat pH 3,5.
Ống đối chiếu: gồm 5 ml ethanol 96% trộn đều với 5 ml dung dịch chuẩn chì 1 phần
triệu và 2 ml dung dịch chế phẩm, thêm 2 ml dung dịch đệm acetat pH 3,5.
Cách pha dung dịch thioacetamid: Thêm 1 ml hỗn hợp gồm 15 ml dung dịch natri
hydroxyd 1 N (TT), 5 ml nước cất và 20 ml glycerin 85% (TT) vào 0,2 ml dung dịch
thioacetamid 4% (TT), đun nóng trong cách thuỷ 20 giây, làm lạnh và dùng ngay.
Thêm 1,2 ml dung dịch thioacetamid (TT) vào hai ống thử và đối chiếu, lắc đều rồi để yên 2 phút.
So sánh màu tạo thành trong ống thử với màu ống đối chiếu. Ống thử không được đậm
màu hơn ống đối chiếu (quan sát trên nền trắng, nhìn từ trên xuống). 3. Định lượng
Phương pháp quang phổ hấp thụ tử ngoại và khả kiến. (theo USP35-Acetaminophen)
Cân chính xác 0,12 g paracetamol, h a tan với 10 ml methanol trong bình định mức 100
ml, thêm nước vừa đủ đến vạch. Lấy chính xác 10 ml dung dịch cho vào bình định mức
100 ml, pha loãng với nước đến định mức, lắc đều. Tiếp tục lấy chính xác 10 ml dung
dịch này cho vào bình định mức 100 ml khác, thêm nước đến vạch, lắc đều. Chuẩn bị
dung dịch paracetamol chuẩn có nồng độ 12 µg/ml. Đo độ hấp thụ của dung dịch thu
được ở bước sóng 244 nm, cuvet dày 1 cm. Hàm lượng % paracetamol được tính theo công thức: 6 lOMoAR cPSD| 45734214 𝑃%=! " ! !! ! !𝑥100% ! ! !!
A: độ hấp thu của mẫu
A0: độ hấp thu của dung dịch chuẩn
C0: nồng độ dung dịch chuẩn (12 µg/ml) m:
khối lượng cân (đơn vị mg)
C. CÂU HỎI CHUẨN BỊ CHO BÀI THỰC TẬP
1. Viết phương trình phản ứng tổng hợp Paracetamol
2. Trình bày quy trình tổng hợp Paracetamol
3. Vai tr của HCl trong phản ứng định tính gốc 4-aminophenol?
A. Chất xúc tác cho phản ứng thủy phân paracetamol B.
Môi trường acid cho phản ứng oxy hóa khử
C. Chất khử trong phản ứng tạo màu. D. A, B đúng
4. Chỉ tiêu nào không thuộc nhóm chỉ tiêu định tính paracetamol? A. Điểm chảy
B. Phản ứng định tính gốc p-aminophenol.
C. Giới hạn 4-aminophenol trong chế phẩm
D. Phản ứng định tính nhóm acetyl.
5. Phổ hấp thụ tử ngoại và khả kiến của paracetamol cho đỉnh hấp thu cực đại tại bước sóng nào? A. 254 nm B. 365 nm C. 244 nm D. 241 nm
6. Viết sơ đồ phản ứng xảy ra trong phần định tính B (định tính p-aminophenol)?
7. Viết sơ đồ phản ứng xảy ra trong phần định tính C (định tính acetyl)?
8. Cân 120,4 mg chế phẩm paracetamol, h a tan với 10 ml methanol trong bình định mức
100 ml, thêm nước vừa đủ đến vạch. Lấy chính xác 10 ml dung dịch cho vào bình
định mức 100 ml, pha loãng với nước đến định mức, lắc đều. Tiếp tục lấy chính xác
10 ml dung dịch này cho vào bình định mức 100 ml khác, thêm nước đến vạch, lắc 7 lOMoAR cPSD| 45734214
đều. Chuẩn bị dung dịch paracetamol chuẩn có nồng độ 12 µg/ml. Đo độ hấp thụ của
dung dịch thu được ở bước sóng 244 nm, cuvet dày 1 cm.
Kết quả đo độ hấp thu của mẫu (A) là 0,776, độ hấp thu của dung dịch chuẩn (Ao) là 0,780.
a) Thiết lập công thức tính hàm lượng của paracetamol?
b) Tính hàm lượng % của paracetamol trong chế phẩm?
9. Tính hiệu suất của phản ứng tổng hợp paracetamol theo quy trình trong bài học. Cho
biết khối lượng paracetamol thu được trước khi sấy là 1,20 g (hàm ẩm 30%) , Mpaminophenol
= 109,1 , Mparacetamol = 151,2.
CHƯƠNG 2. TỔNG HỢP ACID BENZOIC Mục tiêu:
− Tổng hợp và tinh chế acid benzoic
− Tính toán được hiệu suất của phản ứng tổng hợp
− Thể hiện được khả năng làm việc nhóm nhỏ để hoàn thành bài thí nghiệm 8 lOMoAR cPSD| 45734214
A. CƠ SỞ LÝ THUYẾT
Acid benzoic (acid benzen carboxylic) được điều chế từ sự oxy hoá benzyl alcol bằng
kali permanganat trong môi trường trung tính.
3C6H5CH2OH + 4KMnO4 → 3C6H5COOK + 4MnO2 + KOH + 4H2O
C6H5COOK + HCl → C6H5COOH + KCl
Trong công nghiệp, acid benzoic được điều chế từ sự oxy hoá trực tiếp toluen bằng
KMnO4, K2CrO4, HNO3 dưới áp suất cao. B. THỰC HÀNH
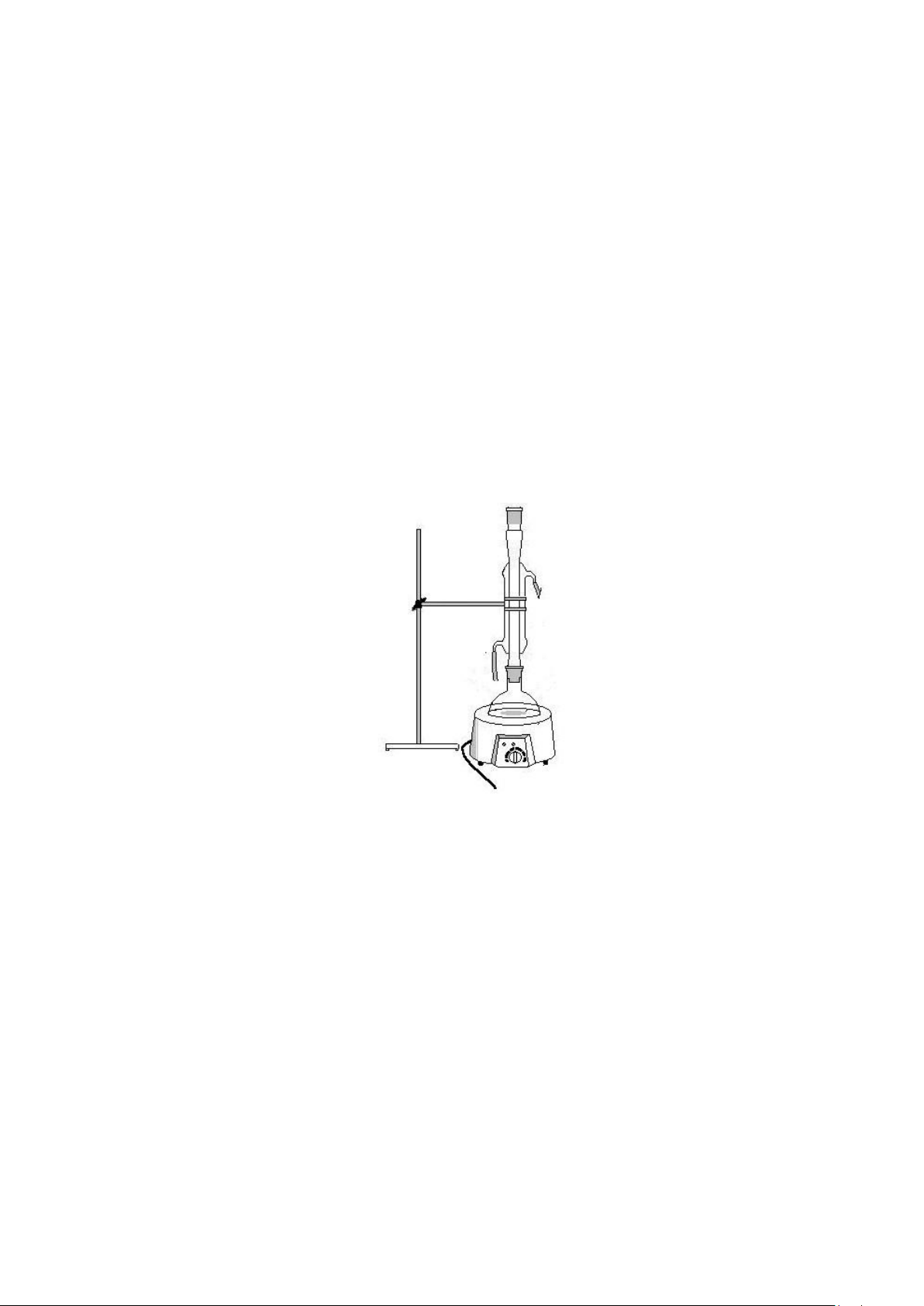
Hình 1: Đun hồi lưu
Quy trình thực hiện
− Cho 3,3 g KMnO4 và 60 ml nước cất vào bình cầu 250 ml. Khuấy cho tan. Thêm
1,5 ml benzyl alcol ( D = 1,04 g/ml).
− Gắn sinh hàn nước vào bình cầu để đun hồi lưu. Đun hỗn hợp phản ứng đến sôi nhẹ trong 60 phút.
− Để nguội bình cầu dưới v i nước.
− Lọc dưới áp suất giảm, lấy dịch lọc, tráng phễu với 10 ml nước cất. 9 lOMoAR cPSD| 45734214
− Cẩn thận thêm từ từ HCl đậm đặc (trong tủ hút khí độc) vào dịch lọc đến pH =1
(dùng giấy chỉ thị pH).
− Cho dung dịch Na2SO3 20% vào từ từ, dùng đũa khuấy đều đến khi hỗn hợp mất
màu chỉ c n lại tủa trắng của acid benzoic.
− Ngâm becher trong thau nước đá trong 15 phút.
− Lọc dưới áp suất giảm. Rửa tủa với 10 ml nước cất lạnh.
Tinh chế acid benzoic bằng phương pháp kết tinh lại −
Hoà tan acid benzoic thô trong 50 ml nước sôi.
− Đun nhẹ và khuấy mạnh đến khi hỗn hợp trong suốt.
− Lọc nhanh hỗn hợp c n nóng trên giấy lọc xếp (phễu và giấy lọc được tráng trước bằng nước sôi).
− Để nguội. Ngâm becher trong thau nước đá trong 15 phút để kết tinh hoàn toàn.
− Lọc dưới áp suất giảm cho đến khô.
− Sấy sản phẩm trong tủ sấy ở 60 0C trong 4 giờ.
− Cân và tính hiệu suất.
C. CÂU HỎI CHUẨN BỊ CHO BÀI THỰC TẬP
1. Viết phương trình phản ứng và tóm tắt quy trình tổng hợp acid benzoic?
2. Kể tên các chất có trong bình phản ứng sau khi đun hồi lưu 60 phút?
3. Cho biết vai tr của HCl đậm đặc?
4. Cho biết vai tr của dung dịch Na2SO3 20% ?
5. Kể tên các bước chính của phương pháp kết tinh lại?
6. Tổng hợp acid benzoic bằng phản ứng hóa học ?
a. Oxy hóa khử b. Thủy phân c. Nitro hóa d. Sulfo hóa
7. Vai tr của sinh hàn cầu trong quá trình đun hồi lưu?
a. Giúp phản ứng xảy ra hoàn toàn b. Giúp phản ứng sôi nhanh hơn
c. Tránh thất thoát dịch phản ứng d. Cả 3 đáp án
8. Sau khi đun hồi lưu 60 phút, benzyl alcol chuyển hóa thành chất? 10 lOMoAR cPSD| 45734214 a. Kali benzoat b. Natri benzoat c. Acid benzoic d. Benzaldehyd
9. Sau khi đun hồi lưu 60 phút, KMnO4 chuyển hóa thành chất? a. MnO2 b. MnO c. Mn d. K2MnO4
10. Tinh chế acid benzoic bằng phương pháp kết tinh lại dựa vào sự thay đổi độ tan của acid benzoic theo? a. Dung môi b. pH c. Nhiệt độ
d. Không có đáp án đúng
11. Một quy trình tổng hợp đã được thực hiện với 5,5 g KMnO4, 2,5 ml benzyl alcol
(có 10% tạp chất) và các hóa chất cần thiết khác; thu được 2,3 g acid benzoic (có độ tinh khiết 95%).
Tính hiệu suất của quy trình này. (Biết phân tử lượng MKMnO4 = 158,03 ;
Mbenzyl alcol = 108,14 ; Macid benzoic = 122,12; Dbenzyl alcol = 1,04 g/ml)
CHƯƠNG 3. KIỂM NGHIỆM ACID BENZOIC Mục tiêu:
− Kiểm nghiệm acid benzoic qua các phản ứng định tính, thử tinh khiết và định lượng.
− Trình bày kết quả thí nghiệm vào phiếu kiểm nghiệm 11 lOMoAR cPSD| 45734214
− Thể hiện được khả năng làm việc nhóm nhỏ để hoàn thành bài thí nghiệm
A. CƠ SỞ LÝ THUYẾT C7H6O2 PTL: 122,12 Tính chất
− Tinh thể hình kim hay mảnh, không màu hoặc bột kết tinh trắng, không mùi hoặc
thoảng mùi cánh kiến trắng.
− Khó tan trong nước, tan trong nước sôi, dễ tan trong ethanol 96%, ether và dầu
béo. Acid benzoic bắt đầu thăng hoa ở 100 0C.
Bảo quản: Chế phẩm được bảo quản trong chai lọ nút kín.
Loại thuốc: Kháng nấm, chất bảo quản chống vi sinh vật.
Tiêu chuẩn kiểm nghiệm Chỉ tiêu Tiêu chuẩn Kết luận Định tính
Phản ứng benzoat Điểm Màu vàng nâu chảy 121-124 0C
Giới hạn tạp chất Độ trong và màu sắc Trong và không màu Các hợp chất chứa clor Đạt theo quy định
Các chất khử kali permanganat Đạt theo quy định Kim loại nặng Không quá 10 ppm Tro sulfat Không quá 0,1% Định lượng 99,0-100,5%
B. THỰC HÀNH 1. Định tính
1.1. Phản ứng benzoat
Hoà tan 0,1 g chế phẩm trong 1 ml dung dịch NaOH 0,1 N (TT) và thêm nước vừa đủ
10 ml. Thêm vài giọt FeCl3 10%, dung dịch có tủa vàng nâu. 1.2. Điểm chảy
Đo bằng phương pháp mao quản trên máy đo điểm chảy. 12 lOMoAR cPSD| 45734214 2. Thử tinh khiết
2.1. Các chất khử kali permanganat
Cho 100 ml nước sôi vào becher 250 ml đã có sẵn cá khuấy từ, thêm 5 ml acid sulfuric 10%.
Bật bếp khuấy từ, chỉnh nhiệt độ 350- 400 oC, tốc độ khuấy từ 200-400.
Thêm từng giọt dung dịch kali permanganat 0,1 N vào 100 ml nước đang sôi đến khi
màu hồng tím xuất hiện và bền vững trong 30 giây.
Hoà tan 1,0 g chế phẩm trong dung dịch đang nóng trên và chuẩn độ bằng dung dịch kali
permanganat 0,1 N đến khi có màu hồng bền vững trong 15 giây.
Chế phẩm đạt chỉ tiêu giới hạn chất khử khi thể tích KMnO4 0,1 N chuẩn độ không quá 0,5 ml và ngược lại.
2.2. Kim loại nặng: Không được quá 0,001%
Pha 50 ml dung dịch chế phẩm 5% trong ethanol 96%: h a tan 2,50 g chế phẩm với vừa
đủ ethanol trong bình định mức 50 ml.
Ống thử: lấy 12 ml dung dịch chế phẩm, thêm 2 ml dung dịch đệm acetat pH 3,5. Lắc đều.
Ống đối chiếu: gồm 5 ml ethanol 96% với 5 ml dung dịch chuẩn chì 1 ppm và 2 ml dung
dịch chế phẩm, thêm 2 ml dung dịch đệm acetat pH 3,5. Lắc đều.
Cách pha dung dịch thioacetamid: Thêm 5 ml hỗn hợp (NaOH – Glycerol - Nước) (bộ
môn đã pha sẵn) và 1 ml dung dịch thioacetamid 4% (TT) vào ống nghiệm sạch, đun
cách thuỷ 20 giây, làm lạnh trong thau nước đá 30 giây và dùng ngay.
Thêm 1,2 ml dung dịch thioacetamid (TT) vào ống thử và 1,2 ml dung dịch thioacetamid
(TT) vào ống đối chiếu, lắc đều rồi để yên 2 phút.
So sánh màu tạo thành trong ống thử với ống đối chiếu. Quan sát trên nền trắng, nhìn từ trên xuống.
Chế phẩm đạt chỉ tiêu giới hạn kim loại nặng khi ống thử không đậm màu hơn ống đối chiếu và ngược lại. 3. Định lượng
Cách trung tính hoá alcol dùng cho định lượng: Lấy khoảng 20 ml ethanol 96%, thêm
vào đó 3-4 giọt phenolphtalein. Nếu dung dịch không màu, nhỏ từ từ từng giọt dung dịch 13 lOMoAR cPSD| 45734214
NaOH 0,1 N cho đến khi vừa xuất hiện màu hồng bền trong 30 giây. Dùng ethanol này
làm dung môi để định lượng.
Định lượng: Cân chính xác 0,20 g chế phẩm, hoà tan trong 20 ml ethanol 96% (TT) đã
trung tính hoá, thêm 20 ml nước và vài giọt phenolphtalein (CT). Chuẩn độ bằng dung
dịch natri hydroxyd 0,1 N.
1 ml natri hydroxid 0,1 N tương ứng với 0,01221 g C7H6O2. Hàm lượng 𝑃%= ! ! !,!"##" 𝑥 100 !!â!
C. CÂU HỎI CHUẨN BỊ CHO BÀI THỰC TẬP
1. Viết phương trình định tính acid benzoic: phản ứng benzoat? 2.
Nêu nguyên tắc xác định giới hạn tạp khử kali permanganat?
3. Nêu nguyên tắc xác định giới hạn kim loại nặng ?
4. Trong phản ứng định tính, cho quá thừa NaOH có ảnh hưởng gì không? a. Không ảnh hưởng
b. NaOH dư phản ứng tạo tủa Fe(OH)3
c. Fe(OH)3 che mất tủa vàng nâu d. Cả b, c
5. Định lượng các chất khử kali permanganat bằng phương pháp chuẩn độ? a. Oxy hóa khử b. Acid base c. Tạo tủa d. Tạo phức
6. Trong kiểm kim loại nặng, dung dịch thioacetamid có vai tr ?
a. H a tan acid benzoic b. Thủy phân tạo ion sulfua tạo màu với ion kim loại nặng
c. Đóng vai tr là hệ đệm d. Cả a, b, c
7. Trong định lượng acid benzoic, ethanol có vai tr ?
a. H a tan acid benzoic b. Chỉ thị định lượng c. Trung h a NaOH d. Cả a, b, c
8. Trong định lượng acid benzoic, tại sao phải trung tính hóa ethanol trước khi định lượng?
a. Ethanol có tính acid mạnh
b. Trong sản xuất, ethanol bị lẫn acid
c. Không loại hết acid, khi chuẩn d. Cả b, c
độ với NaOH sẽ gây sai số 14 lOMoAR cPSD| 45734214
9. Cho quy trình định lượng sau
Cân chính xác khoảng 0,2 g acid benzoic, h a tan trong 20 ml ethanol 96 % (TT) đã
trung tính hóa, thêm 20 ml nước và vài giọt phenolphtalein (CT). chuẩn độ bằng dung dịch NaOH 0,1 N.
Cho biết Macid benzoic = 122,1
a. Viết phương trình định lượng acid benzoic.
b. Cho biết hàm lượng acid benzoic là 90%. Xác định thể tích NaOH 0,1 N dùng để chuẩn độ.
CHƯƠNG 4. KIỂM NGHIỆM SULFANILAMID Mục tiêu :
− Kiểm nghiệm sulfanilamid qua các phản ứng định tính, thử tinh khiết và định lượng.
− Trình bày kết quả thí nghiệm vào phiếu kiểm nghiệm
− Thể hiện được khả năng làm việc nhóm nhỏ để hoàn thành bài thí nghiệm 15 lOMoAR cPSD| 45734214
A. CƠ SỞ LÝ THUYẾT
C6H8O2N2S PTL: 172,21 Tính chất:
− Bột kết tinh trắng, không mùi.
− Ít tan trong nước; tan trong cồn, dễ tan trong aceton; không tan trong benzen,
cloroform. Sulfanilamid tạo muối tan trong nước với các acid và kiềm. − Điểm chảy: 163-167 oC.
Tiêu chuẩn kiểm nghiệm: Chỉ tiêu Tiêu chuẩn Kết quả Định tính
Phản ứng nhóm amin thơm Xuất hiện tủa màu đỏ cam đến đỏ thắm Sắc ký lớp mỏng
Giá trị Rf của mẫu thử và chuẩn tương đương nhau Thử tinh khiết Giới hạn clorid Không được quá 0,02% Giới hạn sulfat Không được quá 0,05% Định lượng 99,0-101,0% B. THỰC HÀNH 1. Định tính
1.1. Phản ứng của nhóm amin thơm bậc nhất
H a tan 0,05 g chế phẩm (bằng hạt đậu) vào 1 ml HCl 10% trong ống nghiệm. Làm lạnh
trong nước đá trong 5 phút. Thêm từ từ 2 ml dung dịch NaNO2 1% vào ống nghiệm bằng
pipet pasteur, vừa thêm vừa lắc đều. Thêm tiếp 3 ml dung dịch β-naphtol trong kiềm (bộ
môn pha sẵn). Màu đỏ tươi đến đỏ thắm xuất hiện (Lưu ý: trong toàn bộ quá trình
ống nghiệm đều được làm lạnh trong nước đá).
1.2. Định danh sulfamid bằng phương pháp sắc ký lớp mỏng 16 lOMoAR cPSD| 45734214
Chuẩn bị bản mỏng
Dụng cụ: Bản mỏng silica gel F254 có kích thước 2×10 cm.
Pha mẫu thử: H a tan 0,05 g chế phẩm (bằng hạt đậu) vào 5 ml ethanol 96o.
Pha mẫu chuẩn: H a tan 0,05 g chất chuẩn vào 5 ml ethanol 96o (Bộ môn pha sẵn).
Chấm mẫu: Dùng mao quản chấm các mẫu thử và mẫu đối chiếu (mỗi mẫu 10 µl,
khoảng 2 lần chấm) lên bản mỏng, cách mép dưới khoảng 1 cm, hai vết chấm liền kề
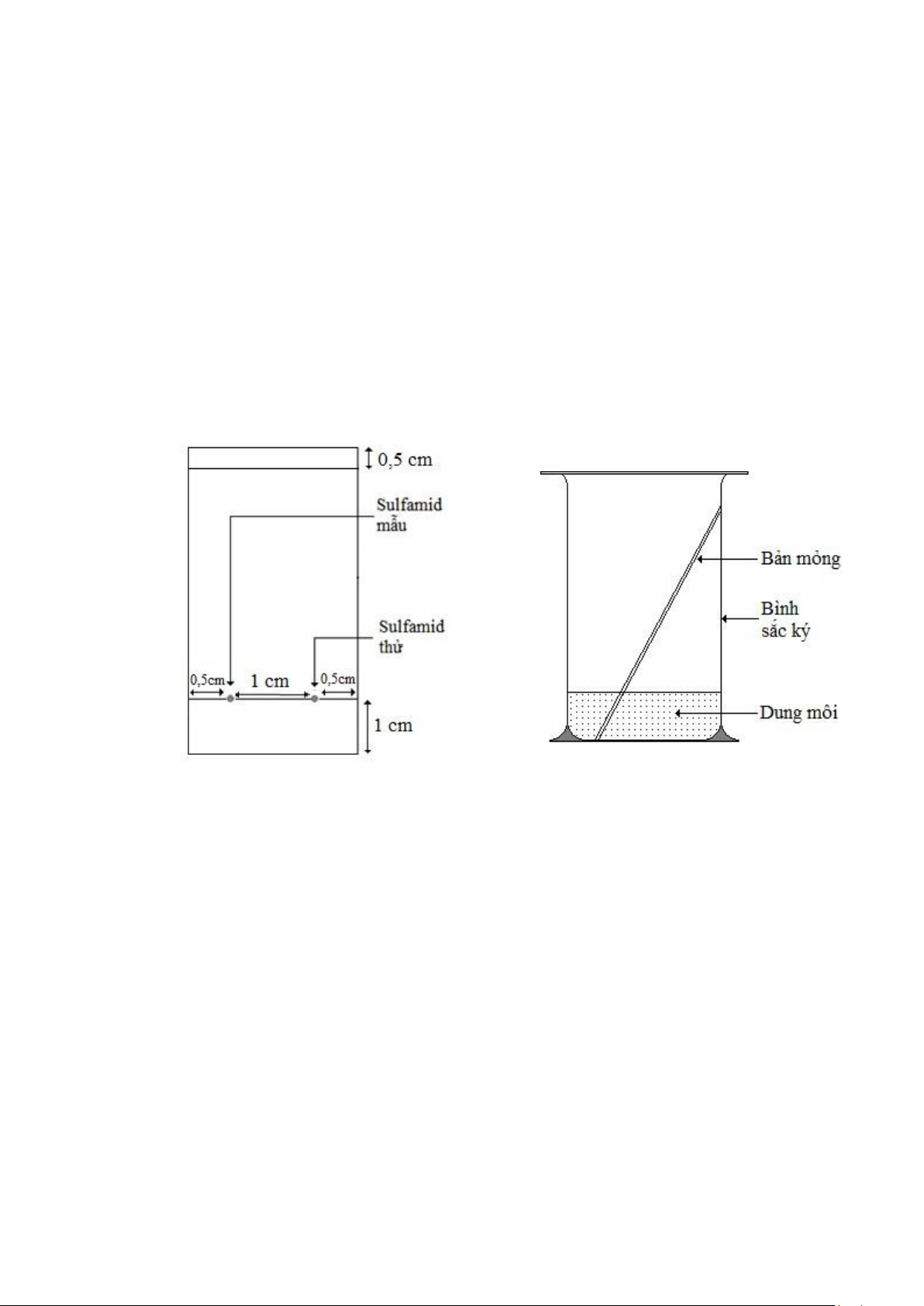
cách nhau 1 cm, đường kính mỗi chấm không lớn hơn 2 mm (Hình 1). Sau khi chấm
xong, sấy khô bản mỏng bằng máy sấy tóc.
Hình 2. Tri ể n khai s ắ c k ý
Hình 1. Chu ẩ n b ị b ả n m ỏ ng
Triển khai sắc ký
Cho vào bình sắc ký 28 ml hỗn hợp dung môi ethyl acetat-methanol-amoniac đậm đặc
(17:6:5), trộn đều, đậy nắp bình lại, để yên 15 phút để hơi dung môi bão hoà bình (Lưu
ý: Để bão h a dung môi tốt hơn có thể đặt một tờ giấy lọc kích thước phù hợp vào trong bình).
Đặt bản mỏng vào bình triển khai sao cho vết chấm cao hơn mực dung môi. Đậy nắp bình lại (Hình 2).
Triển khai đến khi mức dung môi cách bìa trên 0,5 cm. Lấy bản mỏng ra khỏi bình, sấy
khô dung môi bằng máy sấy tóc (thực hiện trong tủ hút).
Phát hiện vết sắc ký
Soi bản mỏng dưới đèn UV ở bước sóng 254 nm. So sánh Rf của sulfamid cần định tính
với sulfamid đối chiếu (hình 3). Kết luận tên sulfamid cần xác định. 17 lOMoAR cPSD| 45734214 d dm 𝑑 đ ố ! ! ! ! ế ! d đ c ℛ d t !(đố! !!!ế!) = 𝑑 ! " 𝑑 !! ử d th ử ℛ!(!!ử) = 𝑑 ! "
Hình 3. S ắ c k ý l ớ p m ỏ ng 2. Thử tinh khiết
Cân chính xác 0,50 g chế phẩm cho vào bình định mức 50 ml. Thêm khoảng 30 ml nước
cất, siêu âm ở 40 oC cho đến tan hoàn toàn, để nguội đến nhiệt độ ph ng, rồi thêm nước
cất đến vạch, thu được dung dịch A (1%). Dung dịch A được sử dụng để làm các kiểm nghiệm dưới đây.
2.1. Giới hạn clorid: Không được chứa nhiều hơn 0,02%.
Nguyên tắc: Tuỳ theo nồng độ, ion clorid tạo với dung dịch AgNO3 2% kết tủa trắng hay
đục, không tan trong HNO3 loãng. Tiến hành
− Ống thử: Cho 12,5 ml dung dịch A, thêm nước cất vừa đủ 16 ml.
− Ống chuẩn: Cho 5 ml dung dịch chuẩn clorid 5 ppm (10 ml chứa 0,05 mg clorid),
thêm nước cất vừa đủ 16 ml.
Cho vào mỗi ống 0,5 ml HNO3 30%, 0,5 ml dung dịch AgNO3 2%, lắc đều. Sau 5 phút,
so sánh độ đục của hai ống (nhìn từ trên xuống, dọc theo trục ống nghiệm, trên nền đen).
Ống thử không được đục hơn ống chuẩn.
2.2. Giới hạn sulfat: Không được chứa nhiều hơn 0,05%.
Nguyên tắc: Tuỳ theo nồng độ, ion sulfat tạo với dung dịch BaCl2 5% một tủa trắng hay
đục, không tan trong HCl loãng. 18 lOMoAR cPSD| 45734214 Tiến hành
− Ống thử: Cho 15 ml dung dịch A, thêm 1 ml nước cất.
− Ống chuẩn: Cho 7,5 ml dung dịch chuẩn sulfat 10 ppm (10 ml chứa 0,1 mg sulfat), thêm 8,5 ml nước cất.
Cho vào mỗi ống 0,5 ml HCl 3 M, 1 ml dung dịch BaCl2 5%, lắc đều. Sau 10 phút, so
sánh độ đục của hai ống (nhìn từ trên xuống, dọc theo trục ống nghiệm, trên nền đen).
Ống thử không được đục hơn ống chuẩn. 3. Định lượng
Cân chính xác 0,25 g chế phẩm cho vào erlen cổ trơn 100 ml, thêm 10 ml dung dịch HCl
10% lắc tan hoàn toàn. Thêm 1,0 g KBr, 30 ml nước cất và 4 giọt chỉ thị tropeolin 00, 2
giọt xanh methylen. Làm lạnh hỗn hợp trong thau nước đá trong 5 phút.
Chuẩn độ bằng dung dịch NaNO2 0,1 N: nhỏ dung dịch NaNO2 0,1 N trên buret xuống
bình nón luôn được lắc đều cho đến khi màu xanh tím chuyển sang màu xanh ngọc bền
(Lưu ý hỗn hợp định lượng luôn được làm lạnh trong suốt quá trình định lượng). Ghi
thể tích dung dịch NaNO2 0,1 N đã dùng (V)
Song song tiến hành với mẫu trắng (cùng điều kiện như trên nhưng không chứa chế
phẩm), ghi thể tích dung dịch NaNO2 0,1 N đã dùng (Vtrắng) Tính kết quả
1 ml NaNO2 0,1 N tương ứng với 0,01722 g C6H8O2N2S.
Hàm lượng sulfanilamid được tính theo công thức: (V−V trắng)×1,722 𝑃%= 𝑚
m: khối lượng cân sulfanilamid (g).
Sulfanilamid phải chứa ít nhất 99,0% C6H8O2N2S.
C. CÂU HỎI CHUẨN BỊ CHO BÀI THỰC TẬP
1. Cho biết các phương pháp khác có thể dùng để định lượng sulfanilamid. 19 lOMoAR cPSD| 45734214
2. Nêu các phương pháp khác để phát hiện điểm kết thúc định lượng.
3. Trong thí nghiệm kiểm giới hạn clorid, tủa tạo thành là chất gì và có tính chất hóa học là:
A. AgCl, tan trong HNO3 không tan trong NH4OH
B. AgCl2, không tan trong HNO3 tan trong NH4OH
C. AgCl, không tan trong HNO3 tan trong NH4OH
D. AgCl2, tan trong HNO3 không tan trong NH4OH
4. Tại sao trong chỉ tiêu định lượng cần phải làm lạnh hỗn hợp trong quá trình định lượng?
A. Đảm bảo acid nitrơ (HNO2) tạo thành bền
B. Đảm bảo acid nitrơ (HNO2) và muối diazonium tạo thành bền
C. Đảm bảo muối diazonium tạo thành bền D. Tất cả đều sai
5. Thực hiện quy trình định lượng như sau:
Cân 0,25 g chế phẩm cho vào erlen 100 ml, thêm 10 ml dung dịch HCl 10% lắc tan hoàn
toàn, Thêm 30 ml nước cất và 4 giọt chỉ thị tropeolin 00, 2 giọt xanh methylen. Làm
lạnh hỗn hợp trong thau nước đá trong 5 phút. Tiến hành chuẩn độ bằng dung dịch
NaNO2 0,1 N, song song tiến hành một mẫu trắng.
a) Viết phương trình oxy hóa – khử sulfanilamid xảy ra trong quá trình định lượng
b) Sau đinh lượng thu được kết quả như sau. Thể tích NaNO2 dùng định lượng mẫu
thử (V) là 14,7 ml. Thể tích NaNO2 dùng định lượng mẫu trắng (Vtrắng) là
0,05 ml. Tính phần trăm (C%) sulfanilamid trong chế phẩm? Biết 1 ml NaNO2
0,1 N tương ứng với 0,01722 g C6H8O2N2S.
6. Cho quy trình định lượng như sau:
Cân 0,25 g chế phẩm cho vào erlen 100 ml, thêm 10 ml dung dịch HCl 10% lắc tan
hoàn toàn, Thêm 30 ml nước cất và 4 giọt chỉ thị tropeolin 00, 2 giọt xanh methylen.
Làm lạnh hỗn hợp trong thau nước đá trong 5 phút. Tiến hành chuẩn độ bằng dung dịch
NaNO2 0,15 N, song song tiến hành một mẫu trắng. 20



