











Preview text:
lOMoAR cPSD| 47207194
B Ộ GIÁO D Ụ C VÀ ĐÀO T Ạ O
TRƯ Ờ NG Đ Ạ I H Ọ C L Ạ C H Ồ NG BÁO CÁO TH
Ự C HÀNH HÓA H Ữ U CƠ
Giáo viên hư ớ ng d ẫ n:
ThS. NGUY Ễ N XUÂN CHƯƠNG
ThS. DƯƠNG TH Ị NG Ọ C DUNG Tháng 10 năm 2024 lOMoAR cPSD| 47207194 BÁO CÁO
THỰC HÀNH HÓA HỮU CƠ
LỚP: 23DS112 – NHÓM 4
1. Châu Thị Tuyết Nhung MSSV: 123000222
2. Nguyễn Thị Mỹ Nhân MSSS: 123000200
3. Nguyễn Trung Hiếu MSSV: 123000648 4. Phạm Thị Hân Hân MSSV: 123001534 lOMoAR cPSD| 47207194 LỜI CẢM ƠN
Trước tiên, nhóm chúng em xin bày tỏ lòng biết ơn sâu sắc đến Thầy ThS. Nguyễn Xuân Chương
và Cô ThS. Dương Thị Ngọc Dung, người đã tận tâm hướng dẫn và truyền đạt kiến thức quý báu
trong suốt quá trình thực hành môn Hóa Hữu Cơ. Sự hỗ trợ và chỉ dẫn tận tình của Thầy và Cô
chính là nguồn động lực để chúng em nỗ lực hết mình và cùng nhau hoàn thành bài báo cáo này.
Chúng em hiểu rằng, do kiến thức còn hạn chế, sẽ không tránh khỏi những thiếu sót trong quá
trình thực hành cũng như khi trình bày báo cáo. Nhóm em rất mong nhận được sự góp ý chân
thành từ Thầy và cô, để mỗi chúng em có thể cải thiện, trau dồi thêm kinh nghiệm, và tiến bộ hơn
nữa trong hành trình học tập và sự nghiệp sắp tới.
Nhóm chúng em xin chân thành cảm ơn Thầy và Cô!! MỤC LỤC
BÀI 7: TỔNG HỢP ACETANILID .....................................................................................1 lOMoAR cPSD| 47207194 I.
MỤC TIÊU THÍ NGHIỆM ......................................................................................1 II.
CƠ SỞ LÝ THUYẾT ...............................................................................................1
1. Khái niệm về Acetanilid...........................................................................................1
2. Khái niệm về acyl hóa, acetyl hóa ...........................................................................1 3. Tác
nhân acetyl hóa .................................................................................................2 III.
DỤNG CỤ VÀ HÓA CHẤT ...................................................................................3 IV.
TIẾN HÀNH THÍ NGHIỆM ...................................................................................3 V.
TRẢ LỜI CÂU HỎI ................................................................................................5
1. Viết phương trình phản ứng xảy ra ..........................................................................5
2. Khi trong anilin có lẫn chất bẩn, tất cả chất bẩn trong anilin sẽ hiện diện trong sản
phẩm. Nêu cách khắc phục?.....................................................................................6
3. Cho biết vai trò của than hoạt tính? .........................................................................6
4. Cho biết vai trò của dung dịch natri acetat? .............................................................6
5. Trình bày cách tính hiệu suất phản ứng? .................................................................7
6. Có thể thay anhydride acetic bằng các chất gì? Mức độ phản ứng của chất đó so với
anhydride acetic? .....................................................................................................7
7. Cho biết thành phần của hỗn hợp sau phản ứng? ....................................................7
8. Tại sao phải khuấy và làm lạnh sau khi thực hiện xong phản ứng? ........................8
BÀI 8: TỔNG HỢP AXIT SULFANILIC ..........................................................................9 I.
MỤC TIÊU THÍ NGHIỆM ......................................................................................9 II.
CƠ SỞ LÝ THUYẾT ...............................................................................................9
1. Khái niệm về axit sulfanilic .....................................................................................9
2. Khái niệm về Sunfo hóa .........................................................................................10 III.
DỤNG CỤ VÀ HÓA CHẤT ................................................................................. 11 IV.
TIẾN HÀNH THÍ NGHIỆM .................................................................................12 V.
TRẢ LỜI CÂU HỎI ..............................................................................................14
1. Phương trình phản ứng...........................................................................................14
2. Khi thêm H2SO4 đặc vào bình cầu 2 cổ phải thực hiện trong thau nước đá tại vì:.14
3. Phải đun hỗn hợp ở 180-190oC trong 2 tiếng 30 phút tại vì: .................................14
4. Đun hỗn hợp phản ứng dưới nhiệt độ 180-190oC thì sản phẩm là: .......................14
5. Vai trò của ống sinh hàn: ........................................................................................14
6. Phải kết tinh acid sulfanilic bằng nước đá vì: ........................................................15
7. Vai trò của than hoạt tính: ......................................................................................15 8.
Phương pháp tinh chế trong tổng hợp acid sulfanilic là: .......................................15 lOMoAR cPSD| 47207194
BÀI 7: TỔNG HỢP ACETANILID
I. MỤC TIÊU THÍ NGHIỆM:
- Nắm vừng lý thuyết về phản ứng acetyl hóa amin thơm.
- Điều chế acetanilid dựa trên phản ứng acetyl hóa anilin sử dụng tác nhân acetyl hóa là anhydrid acetic.
- Trình bày được kết quả thí nghiệm. Nhận xét, giải thích đúng các hiện tượng và viết báo cáo thực hành.
II. CƠ SỞ LÝ THUYẾT:
1. Khái niệm về Acetanilid:
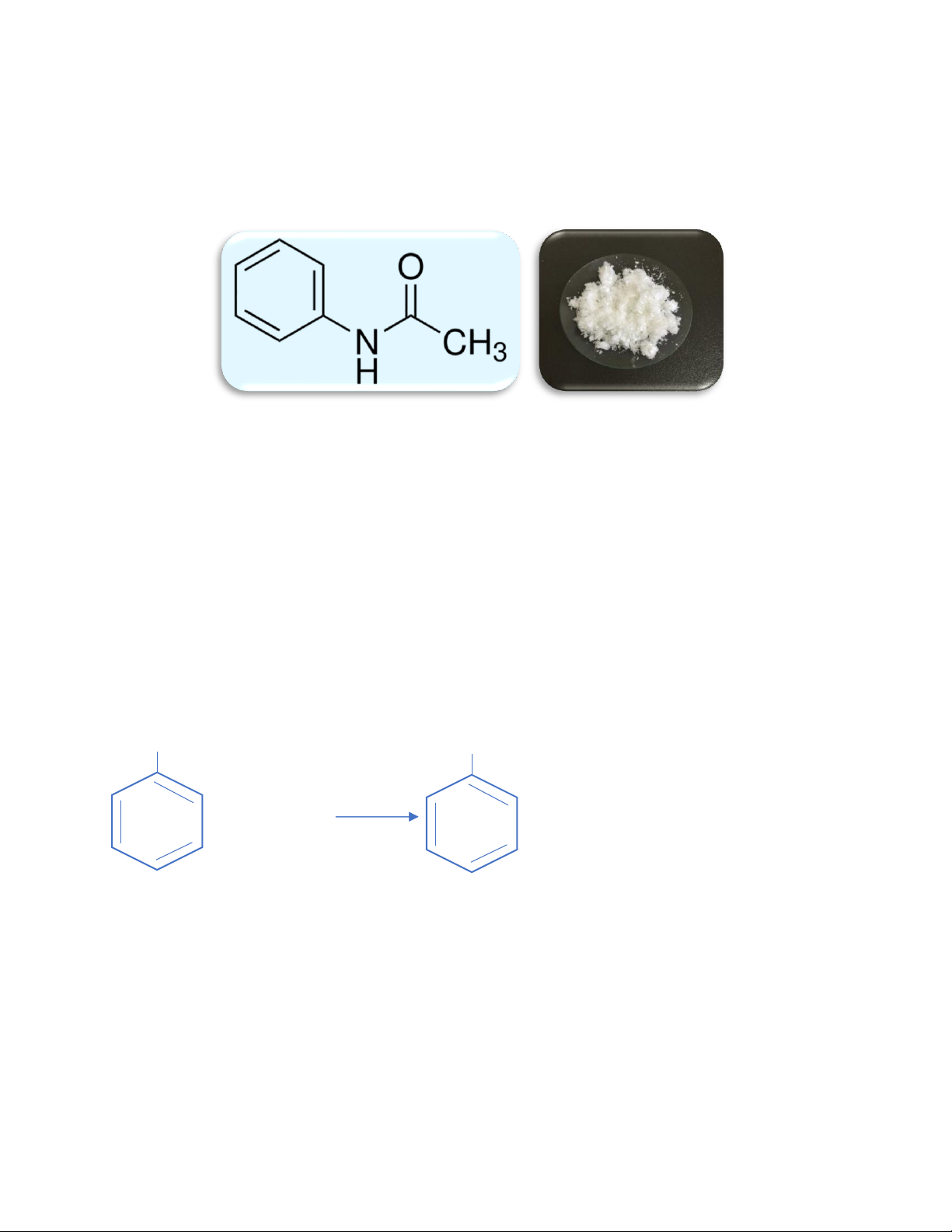
* Acetanilid là một chất hóa học hữu cơ có công thức phân tử C8H9NO, là tinh thể vảy trắng
bóng, không màu, không mùi, vị đắng. Ít tan trong nước lạnh, tan trong nước nóng, methanol,
ethanol, ete, cloroform, aceton, bezen. Acetanilid là dẫn suất anilin đầu tiên có đặt tính giảm
đau cũng như hạ sốt trước khi tìm ra paracetamol. Acetanilid là sản phẩm đầu tiên được giới
thiệu vào năm 1886, nhưng việc sử dụng nó bị hạn chế ở liều cao do tác dụng phụ độc hại của
methemoglobinemia (Chứng xanh tím) và vàng da. * Ứng dụng:
- Là nguyên liệu thô và chất trung gian của sulfonamid.
- Là tiền chất trong quá trình tổng hợp penicillin và các dược phẩm khác.
- Tổng hợp thuốc nhuộm và tổng hợp long não.
- Làm thuốc giảm đau, hạ sốt.
- Được sử dụng như một chất ức chế sự thủy phân hydrogen peroxide.
2. Khái niệm acyl hóa, acetyl hóa:
* Phản ứng acyl hóa amin thơm là quá trình thay thế nguyên tử hydro của nhóm -OH-NH2
bằng nhóm acyl RCO. Nếu R=CH3- thì ta có phản ứng acetyl. * Ứng dụng: -
Là một phản ứng hóa học quan trọng trong quá trình sản xuất và chế biến trong công
nghiệp nhử: sản xuất polyme, dược phẩm và chất tẩy rửa. 1 lOMoAR cPSD| 47207194 -
Là một quá trình hóa học quan trọng trong việc tổng hợp các chất hữu cơ, tạo ra các hợp
chất có giá trị trong lĩnh vực hóa học và dược phẩm.
3. Tác nhân acetyl hóa:
Các tác nhân acetyl hóa: CH3COCl , (CH3CO)2O, CH3COOH - Ứng dụng:
+ Bảo vệ nhóm chức amin.
+ Điều chế chuyển hóa chất thế một lần.
+ Giảm hoạt nhóm -NH2 và tăng tỷ lệ sản phẩm thế para- trong các phản ứng thế ái điện tử vào nhân thơm.
- Phương trình phản ứng:
• Tác nhân acetyl hóa là acetyl clorid
2Ar-NH2 + CH3COCl → ArNHCOCH3 + ArN(+)H3Cl(-)
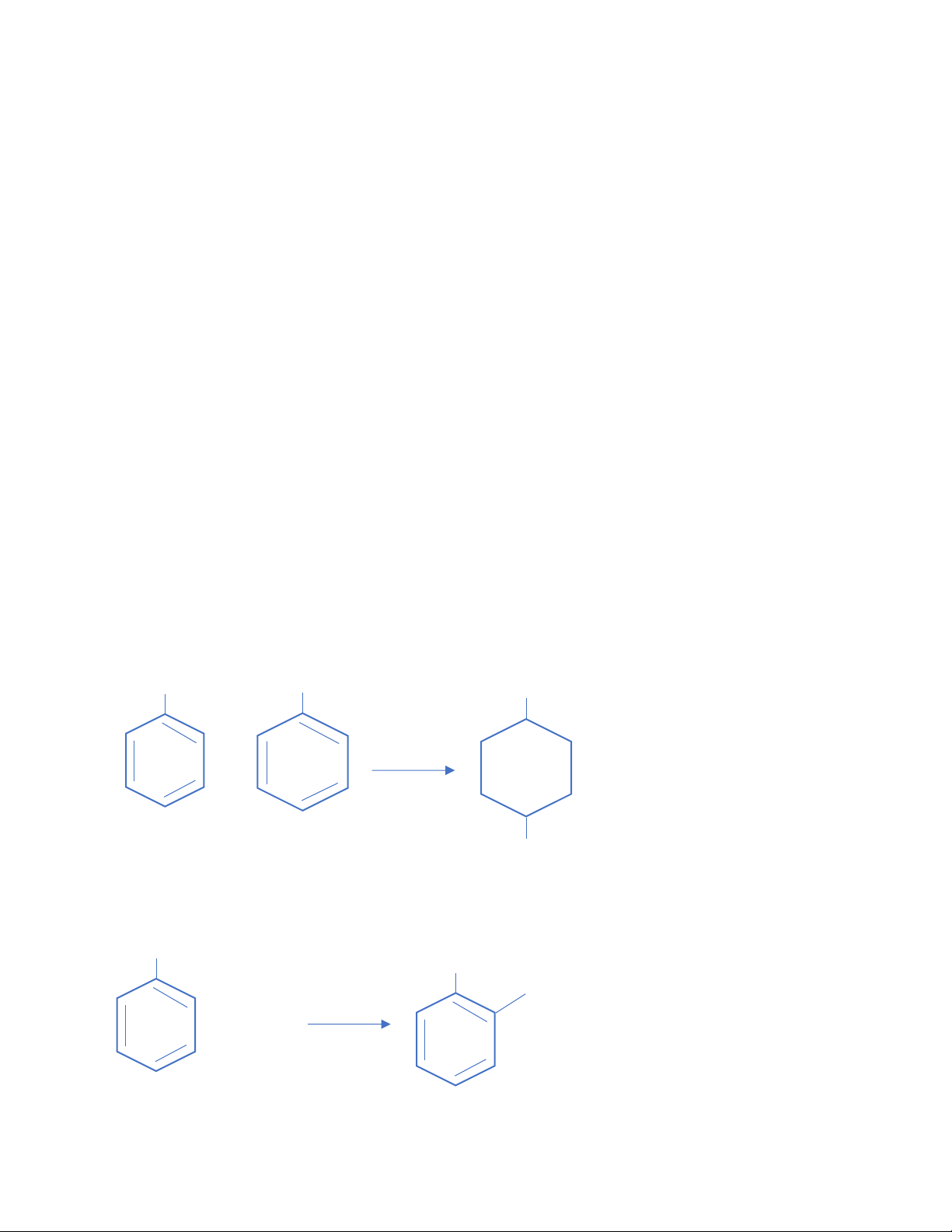
• Tác nhân acetyl hóa là anhydrid acetic NH 2 NH COCH 3 + (CH 3 CO) 2 O + CH 3 COOH
• Tác nhân acetyl hóa là acid acetic 2 lOMoAR cPSD| 47207194 NH 2 NHCOCH 3 + CH 3 CO OH + H 2 O
* Cơ chế phản ứng:
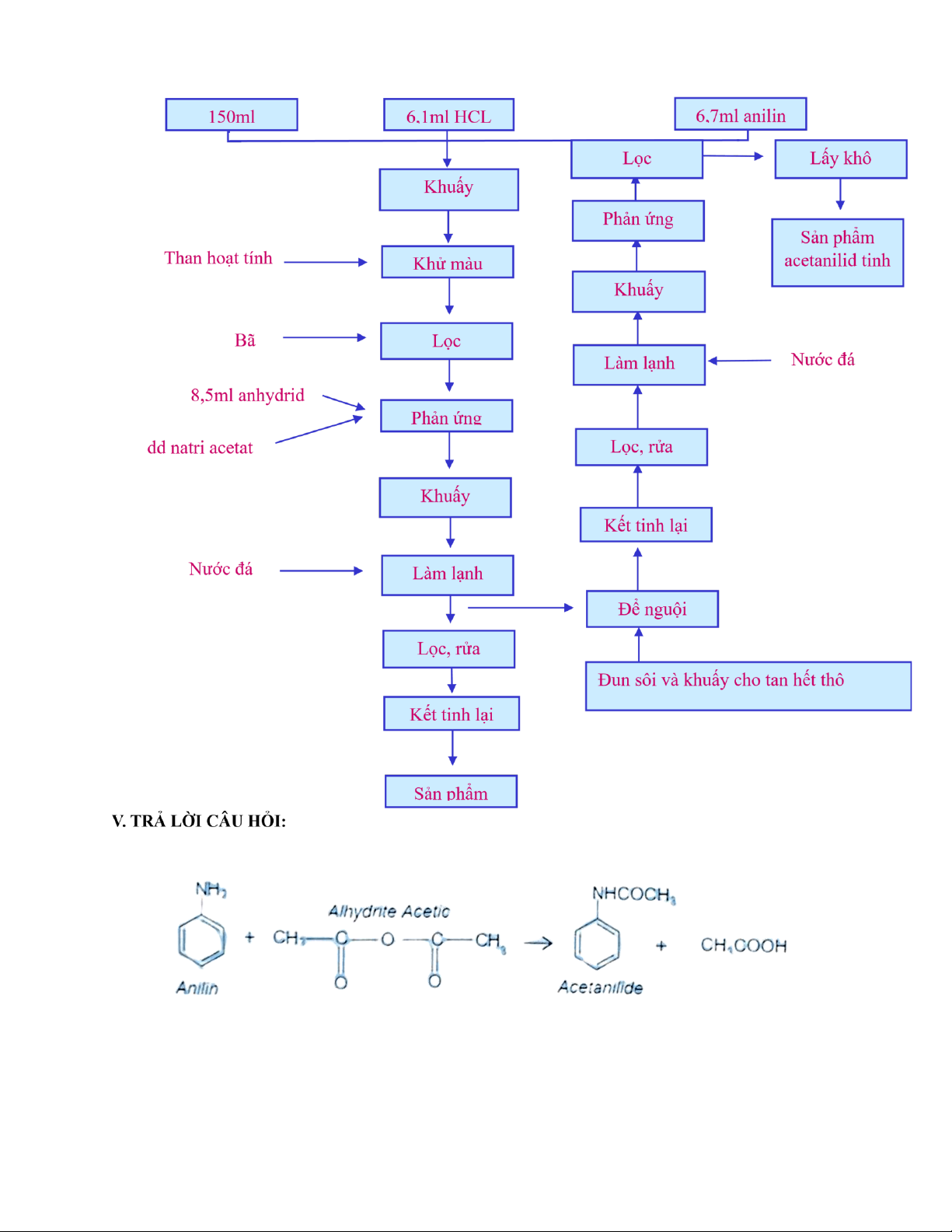
- Cơ chế phản ứng acyl hóa amine đòi hỏi phải có proton trên nguyên tử nitrogen của amine để
có thể xảy ra. Không giống với phản ứng alkyl hóa, các amine sinh ra không có khả năng tiếp tục
tham gia phản ứng acyl hóa, do đôi diện tử nitrogen đã tham gia liên kết với nhóm carbonyl C=O.
III. DỤNG CỤ VÀ HÓA CHẤT: Hóa chất Số lượng Dụng cụ Số lượng Anilin 6,7 ml Pipet 10 ml 2 HCI đặc 6,1 ml Cốc có mỏ 250 ml 1 Anhydrid acetic 8,5 ml Cốc có mỏ 100 ml 1 Than hoạt tính 2 g
Thiết bị lọc chân không 1 Natri acetat 11 g Phễu thủy tinh 1 Nước cất Ống đong 250 ml 1 Nước đá 100 g Pipet pasteur 1
IV. TIỀN HÀNH THÍ NGHIỆM:
- Dùng ống đong 250ml lấy 150ml nước cho vào cốc có mỏ 250ml.
- Dùng pipet lấy 6,1ml HCl đậm đặc cho vào cốc có mỏ có chứa nước (cẩn thận cho thật chậm HCl vào nước). 3 lOMoAR cPSD| 47207194
- Tiếp tục dùng một pipet khác lấy 6,7 ml anilin cho vào cốc có mỏ có chứa nước và acid. -
Khuấy đều cho đến khi anilin tan hoàn toàn nếu dung dịch có màu thêm khoảng 1g than hoạt
tính vào và tiến hành đun và khuấy ở 60°C - 70°C trong 5 phút.
- Hỗn hợp sau đó được đem lọc trên thiết bị lọc áp suất chân không.
- Cho 8,5ml anhydrid acetic vào nước lọc, khuấy mạnh và đổ nhanh dung dịch natri acetat (pha
11g natri acetat vào 35ml nước).
- Khuấy mạnh và làm lạnh bằng nước lạnh, sau đó lọc bằng thiết bị lọc chân không sẽ thu được acetanilid thô.
- Acetanilid thô sau đó được tinh chế theo các bước sau:
Đun sôi khoảng 120 ml nước trong cốc có mỏ 250 ml.
Khi nước sôi, cho acetanilid thô vào và khuấy đều.
Tiếp tục đun cho đến khi acetanilid tan hết.
Lọc nóng dung dịch bằng giấy lọc xếp nếp.
Dung dịch thu được để nguội và tiếp tục khuấy.
Sau khi dung dịch đã nguội, tiến hành làm lạnh bằng nước đá. Sau đó đem lọc trên thiết bị lọc
chân không. Sấy khô thu được acetanilid tinh. 4 lOMoAR cPSD| 47207194
Hình ảnh: Các bước điều chế tổng hợp Acetanilid
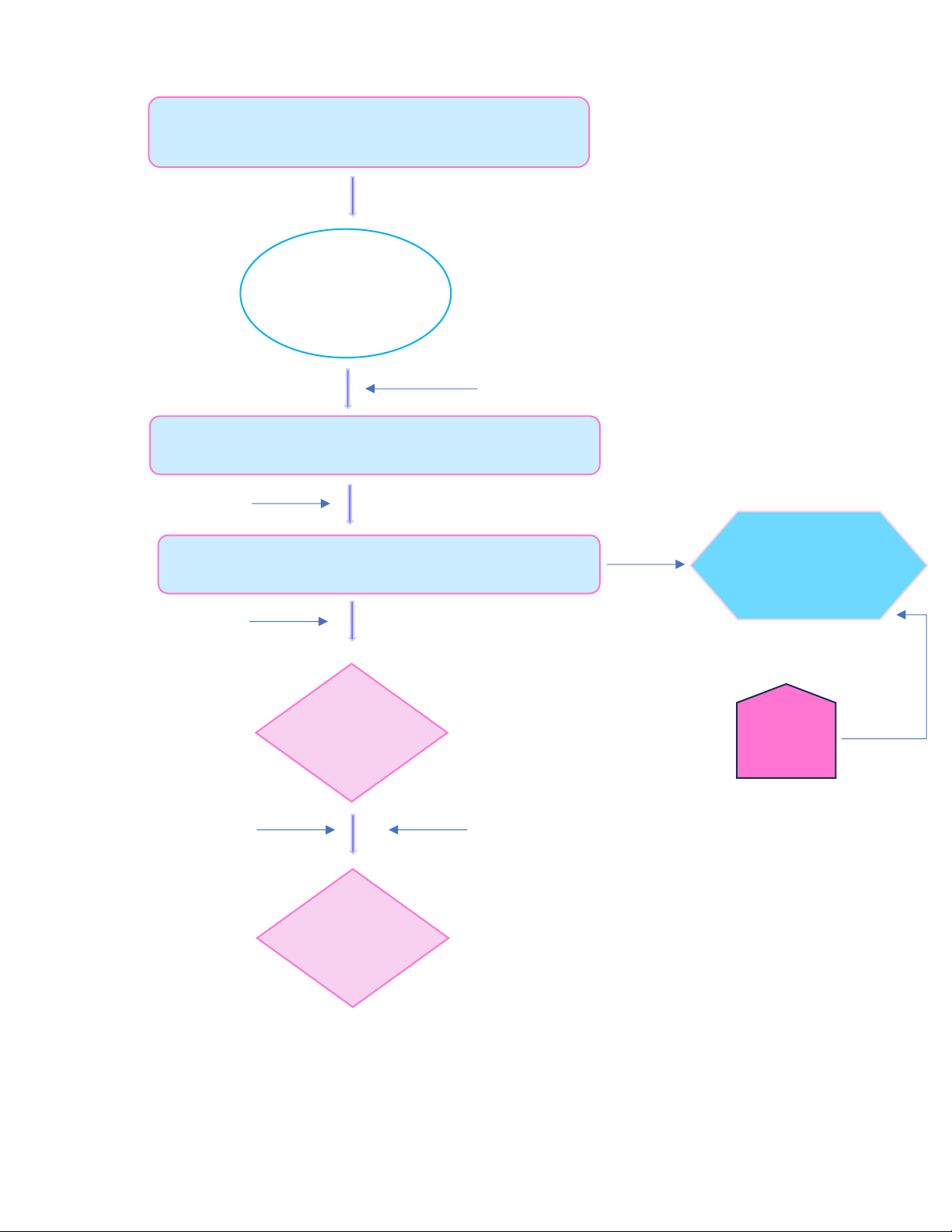
Sơ đồ quy trình tiến hành thí nghiệm: 5 lOMoAR cPSD| 47207194
1. Viết phương trình phản ứng xảy ra: 2 3 3 3 3 6 lOMoAR cPSD| 47207194
2. Khi trong anilin có lẫn chất bẩn, tất cả chất bẩn trong anilin sẽ hiện diện trong sản phẩm.
Nêu cách khắc phục?
Ta có thể sử dụng nhiều phương pháp để loại bỏ các chất bẩn
• Lọc: Sử dụng quá trình lọc để tách anilin tinh khiết khỏi chất bẩn dùng giấy lọc xếp nếp để lọc.
Hoặc lọc trên thiết bị có áp suất chân không.
• Chưng cất: Anilin có nhiệt độ sôi khá thấp ( khoảng 184°C), các chất bần có nhiệt độ cao hơn.
Bằng cách này ta làm bay hơi anilin và sau đó ngưng tụ lại để thu được anilin tinh khiết.
3. Cho biết vai trò của than hoạt tính?
Than hoạt tính có tác dụng làm sạch hỗn hợp khỏi các tạp chất và loại màu của hỗn hợp vì
cacbon có trong than hoạt tính có những lỗ xốp rất nhỏ giống như vi quản có khả năng hấp thụ.
4. Cho biết vai trò của dung dịch natri acetat?
Natri acetat giúp tạo điều kiện phản ứng tạo môi trường kiềm giúp cho phản ứng tổng hợp
acetanilid diễn ra thuận lợi hơn. Cung cấp các ion acetat ( CH3COO-) giúp cho phản ứng xảy ra dễ dàng hơn.
Natri acetat tạo kết tinh Acetanilid dưa anilin trong muối tạo thành base. Phương trình phản ứng:
- Natri acetat tạo kết tinh Acetanilid → Đưa anilin trong muối tạo thành base.
Phương trình phản ứng: N H 2 N H 3 Cl CH + NaCl + CH 3 COOH 3 COONa + 7 lOMoAR cPSD| 47207194 N H 2 + (CH3CO)2O Acetanilid
Anilin ở dạng muối sẽ tích điện dương (do N+) nên tác nhân acetyl cũng tích điện dương khó tác
động vào. Do đó, Natri acetate trả lại về aniline để acetyl có thể tác động vào.
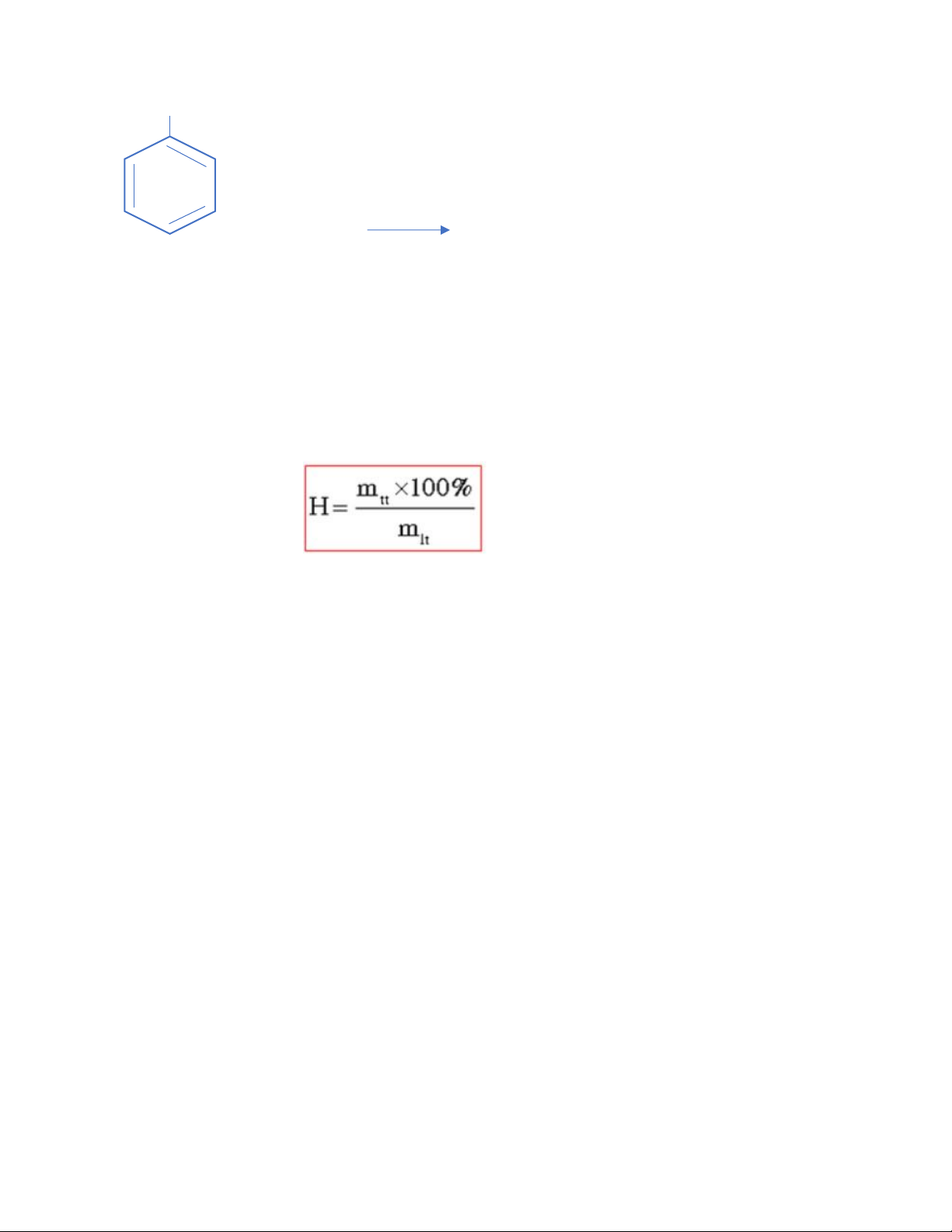
5. Trình bày cách tính hiệu suất phản ứng?
- Để tính hiệu xuất phản ứng ta cần hai tham số là khối lượng sản phẩm thu được ở thực tế, và
khôi lượng sản phẩm dự kiến thu được ở lý thuyết.
Công thức tính hiệu xuất:
• mu: Khối lượng thực tế (g).
•mlt: Khối lượng lý thuyết (g).
•H: Hiệu xuất phản ứng (%).
6. Có thể thay anhydrid acetic bằng tác chất gì? Mức độ phản ứng của chất đó so với anhydrid acetic?
Có thể thay anhydrid acetic bằng: axit acetic, acetyl clorid.
Chất kích thích càng lớn thì càng dễ hấp thụ màu.
Mức độ phản ứng của các chất: acetyl clorid > anhydrid acetic > acid acetic. -
Ta chọn ưu tiên phản ứng anhydrid acetic để thực hiện phản ứng: Vì anhydrid acetic tạo
ra acid acetid, đây là acid yếu không gây độc nhiều và phản ứng xảy ra một chiều. -
Ở phản ứng acid acetic là phản ứng thuận nghịch, phản ứng yếu nhất nên sẽ thu được ít
sản phẩm dẫn đến tốn nhiều thời gian, chi phí và giảm hiệu suất. -
Ở phản ứng acetyl clorid là phản ứng 1 chiều, xảy ra mạnh nhưng sau phản ứng tạo ra
HCl (rất độc) có thể làm viêm kết mạc nên ta không chọn phản ứng này.
7. Cho biết thành phần của hỗn hợp sau phản ứng?
Trong sản phẩm thô có chứa:
- Acetanilid, acid acetid, anhydrid acetic, NaCl, anilin dư, HCl/Natriceta dư (tuỳ theo tỷ lệ).
- Acetanilid thô sau đó đem tinh chế ta thu được acetanilin tinh khiết. 8 lOMoAR cPSD| 47207194
8. Tại sao phải khuấy và làm lạnh sau khi thực hiện xong phản ứng?
- Phải khuấy và làm lạnh sau khi thực hiện xong phản ứng để tạo mầm kết tinh (thu được acetalid
tinh thể nhỏ, nếu không khuấy để nguội từ từ sẽ thu được tinh thể lớn). 9 lOMoAR cPSD| 47207194
BÀI 8: TỔNG HỢP AXIT SUNFANILIC
I. MỤC TIÊU THÍ NGHIỆM:
- Tìm hiểu quá trình tổng hợp acid p-aminobenzensulfonic acid dựa trên phản ứng sulfo hóa xảy
ra giữa anilin và acid sulfuric.
- Điều chế axit p-aminobenzensulfonic acid dựa trên phản ứng sulfo hóa xảy ra giữa anilin và acid sulfuric.
- Sử dụng hiệu quả hóa chất và các thiết bị cơ bản để tiến hành điều chế acid sulfanilic theo đúng quy trình.
- Tổng hợp được acid sulfanilic đạt hiệu suất yêu cầu và viết báo cáo thực hành.
II. CƠ SỞ LÝ THUYẾT:
1. Khái niệm về acid sulfanilic:
Acid sulfanilic C.H4(SO3H)NH2: là chất rắn màu trắng, không mùi và tan trong nước, etanol, axit và base yếu.
Ứng dụng trong hóa dược:
Phân tích hóa học để xác định nồng độ của một số kim loại như đồng, niken và coban.
Các phức hợp kim loại sulfanilic rất ổn định, dễ nhận dạng và đo lường.
Dùng làm chất trung gian tổng hợp các chất hữu cơ khác, như các loại axit amin, chất
hoạt động bề mặt và chất chống ăn mòn.
Các phân tử sulfonyl được đưa vào phân tử hữu cơ làm tăng độ hòa tan của các hợp chất
trong nước thuận tiện cho việc bào chế thuốc.
Dùng làm chất hoạt động bề mặt, chất làm giảm sức căng bề mặt, tăng khả năng hòa tan, tạo bọt,nhũ hóa.
Acid sulfanilic dược sử dụng làm chất trung gian trong tổng hợp một số loại thuốc như:
thuốc kháng viêm, tiền chất tổng hợp kháng sinh họ sulfamid, thuốc điều trị tiểu đường type 2 họ sulfamid.
Ứng dụng trong đời sống: 10 lOMoAR cPSD| 47207194
Được sử dụng trong quá trình sản xuất nhựa, chất đẻo, cao su và sản phẩm dệt may. Được
sử dụng như một chất trung gian trong sản xuất thuốc nhuộm thực phẩm màu vàng, các ứng dụng
dược phẩm cụ thể, chất làm sáng quang học cho giấy trắng và làm phụ gia cho bê tông.
2. Khái niệm về Sunfo hóa:
Phản ứng sulfo hóa là phản ứng thế nguyên tử hydro của hợp chất hữu cơ bằng nhóm sulfo (SO3H).
Đây là phản ứng thuận nghịch, để nâng cao hiệu suất người ta thường dùng tác nhân sulfo hóa.
→ Sản phẩm phụ sinh ra là nước, mà H2SO4 háo nước nên nó sẽ giúp phản ứng xảy ra 1 chiều.
Tác nhân sulfo hóa là acid sulfuric đậm đặc, hỗn hợp acid sulfuric với SO3 ở các nồng độ khác nhau.
Ngoài ra tác nhân sulfo hóa là H2SO4 đậm đặc còn dùng Oleum (H2SO4.nSO3), các hydrocacbon
đa vòng được sunfo hóa dễ dàng, naphtalen được sunfo hóa khó hơn, còn benzen thì rất khó.
Phản ứng sunfo hóa với acid có tính thuận nghịch.
Axit sunfanilic được tổng hợp giữa anilin (C6H5NH2) và axit sulfuric đặc (H2SO4)
- Phương trình phản ứng:
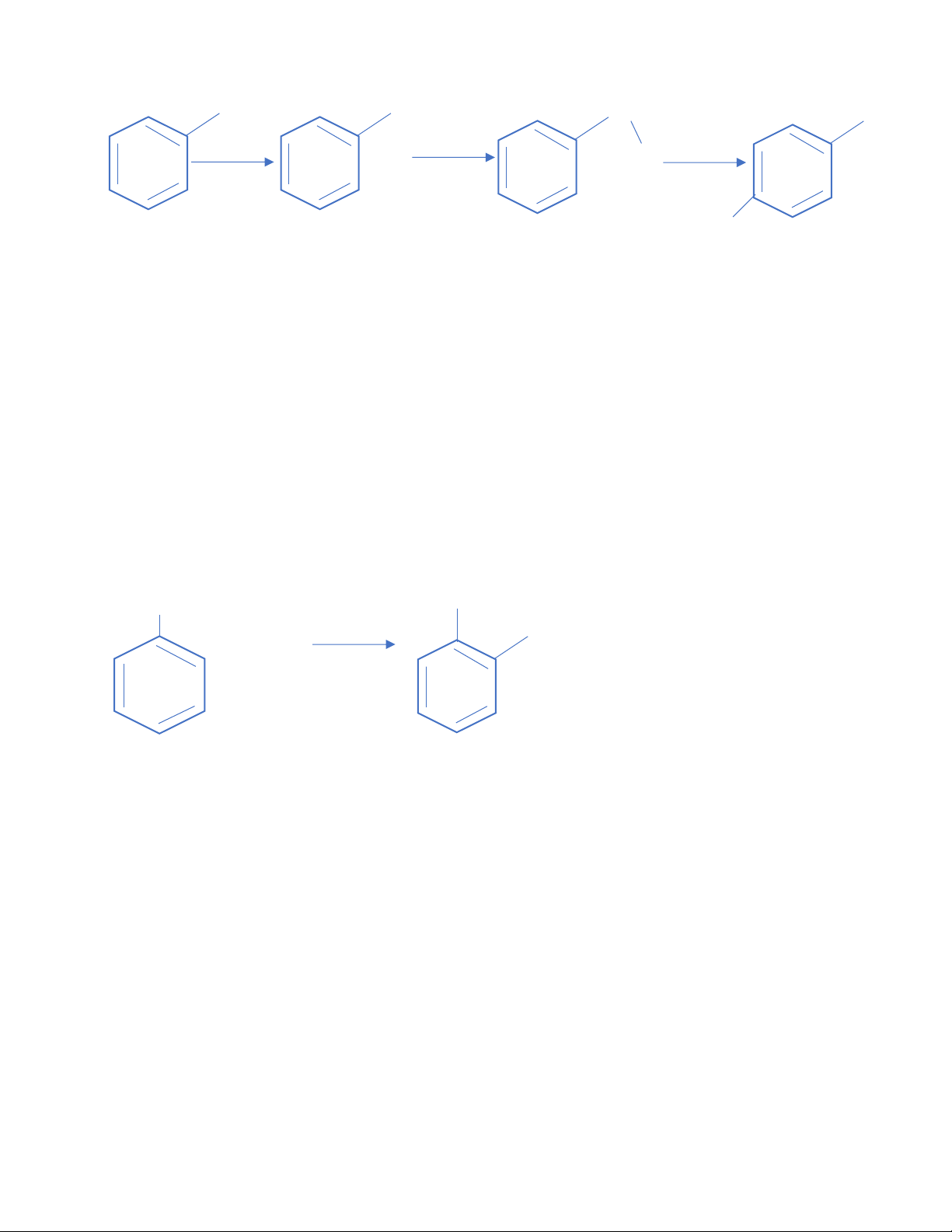
- Phán ứng chính: NH 2 NH 3 HSO 4 NH 2 180 - 190 o C + H 2 O + Anilin Sulfat SO3H
Acid Sulfanilic -
Phản ứng phụ: NH 2 NH 2 SO3H + H2SO4 11 lOMoAR cPSD| 47207194 Acid Orthonilic
III. DỤNG CỤ VÀ HÓA CHẤT: HÓA CHẤT SỐ LƯỢNG DỤNG CỤ SỐ LƯỢNG Anilin 9ml
Bình cầu 2 cổ nhám 250 ml 1 H2SO4 đặc 18ml
Sinh hàn cầu 0,5m cổ nhám 1 NaOH 2N 5ml Bếp đun bình cầu 1 Than hoạt tính 2g Nhiệt kế 300 °C 1 Nước đá 1000g Cốc có mỏ 250 ml 1 Giấy lọc tròn 5 tờ Cốc có mỏ 100 ml 1 Pipet 10 ml 1 Phễu thủy tinh Ø11 1
Thiết bị lọc áp suất thấp 1 Bếp điện 1 Thau nhựa 1
IV. TIỀN HÀNH THÍ NGHIỆM:
- Đặt bình cầu vào chậu nước lạnh, sau đó ta cho lần lượt 9ml Anilin và 18ml H2SO4 vào. 12 lOMoAR cPSD| 47207194
- Đun hỗn hợp ở nhiệt độ 180-190°C trong khoảng 2 giờ 30 phút.
- Thử phản ứng kết thúc bằng cách lấy 1-2 giọt hỗn hợp hòa tan trong 3-4 ml dung dịch.
NaOH 2N. Nếu dung dịch tiếp tục đun, nếu dung dịch trong thì ngừng đun và để hỗn hợp nguội xuống 70-90°C.
* Tiến hành thu sản phẩm: 13 lOMoAR cPSD| 47207194
Đ ổ h ỗ n h ợ p vào c ố c có s ẵ n 100 ml
Khu ấ y đ ề u cho sulfanilic acid k ế t tinh
L ọ c b ằ ng ph ễ u áp su ấ t th ấ p
R ử a s ả n ph ẩ m thô 3 l ầ n b ằ ng nư ớ c l ạ nh
S ấ y th ậ t khô Có màu
Đ ể ngu ộ i r ồ i cho 1g
S ả n ph ẩ m thô cho vào 100ml nư ớ c sôi than ho ạ t tính
L ọ c nóng, nư ớ c qua l ọ c
đư ợ c làm l ạ nh b ằ ng đá Sulfanilic k ế t tinh Đun sôi 2 - 3 phút
L ọ c b ằ ng ph ễ u
R ử a tinh th ể và hút khô
áp su ấ t th ấ p
Cân và tính hi ệ u su ấ t
V. TRẢ LỜI CÂU HỎI:
1. Phương trình phán ứng: 14 lOMoAR cPSD| 47207194 NH 2 NH + 3 NH NH 2 ∆ SO 3 H ∆ H 2 SO 4 [ HSO 4 ] HO 3 S
2. Khi thêm H2SO4 đặc vào bình cầu 2 cố phải thực hiện trong thau nước đá tại vì:
Khi cho acid vào nước sẽ tạo ra nhiệt lượng lớn nếu không tiến hành trong thau nước đá, nhiệt
lượng phát sinh sẽ làm cho bình cầu và acid trở nên quá nóng, gây nguy hiểm và có thể gây cháy
hoặc nổ. Đặt bình cầu trong thau nước đá giúp hấp thu nhiệt lượng phát sinh nhanh chóng, giữ
cho nhiệt độ được kiểm soát và đảm bảo an toàn trong quá trình thực hiện.
3. Phải đun hỗn hợp ở 180-190°C trong 2h30 phút tại vì:
Việc này sẽ giúp phản ứng được xảy ra hoàn toàn không có chất dư thừa, sản phẩm đạt hiệu suất
cao và tinh khiết. Ngoài ra, nếu nhiệt độ không đảm bảo thì sẽ sinh ra sản phẩm phụ Aminobenzene Sulfonic.
4. Đun hỗn hợp phản ứng dưới nhiệt độ 180-190°C thì sản phẩm là: Sản phẩm phụ NH 2 NH 2 SO 3 H + H 2 SO 4 Acid Orthonilic
5. Vai trò của ống sinh hàn:
Ông sinh hàn có tác dụng làm lạnh để các chất (ở trạng thái lỏng trong điều kiện thường).
đang hóa hơi, đi ngang qua ống sẽ ngưng tụ và quay trở lại bình cầu thay vì thoát ra ngoài. Trong
thí nghiệm trên khi tiến hành phản ứng anilin sẽ bị bay hơi khi đun sôi.
Chính vì vậy cần phải sử dụng sinh hàn để hồi lưu anilin, phản ứng dễ dàng xảy ra.
6. Phải kết tinh acid sulfanilic bằng nước đá vì:
Acid sulfanilic ít tan trong nước lạnh, dễ tan trong nước nóng, nên điều này tránh phản ứng tách
HSO3 tạo lại các chất ban đầu do phản ứng sulfo hóa bằng acid sulfurid có tính thuận nghịch.
7. Vai trò của than hoạt tính: 15 lOMoAR cPSD| 47207194
Làm sạch acid sulfanilic khỏi những tạp chất, và khử màu giúp sản phẩm thu được tinh khiết hơn
nhờ tính hấp thụ mạnh của than hoạt.
8. Phương pháp tinh chế trong tổng hợp acid sulfanilic là :
Phương pháp kết tinh, ban đầu acid sulfanilic được tạo ra dạng dung dịch, sau đó được lọc, rửa,
và sấy khô cho kết tinh lại tạo ra được sản phẩm acid sulfanilic. 16




