



Preview text:
lOMoAR cPSD| 45148588
ĐỀ THI KẾT THÚC HỌC PHẦN - MÔN: HÓA HỌC
HỌC KỲ 1 - Thời gian: 70 phút; Lớp: YTCC1
Họ, tên sinh viên:................ Lớp: ……… Số báo danh:...
(Thi sinh không được sử dụng tài liệu- nộp lại đề sau khi thi xong) PHẦN 1 Mã đề thi YTCC-B
Câu 1: Cho biết [MnO -4 ] = [Mr2+] = 1mol/l và MnO4 +8H+ + 5e ⇆ Mn2+ + 4H2O 𝛆0 = 1,51V. Thế oxi hoá-khử của cặp MnO -
4 +8H+ / Mn2+ + 4H2O ở pH= 5 ở 25°C là: A. 1,152V B. 1,348V C. 1,049V D. 1,038V E. 1,51V
Câu 2: Cầu nào sau đây SAI: CO (k) + H2(k) = CO(k) + H_O(1) A. Tăng áp suất không làm cân bằng chuyến dịch
A. Tăng áp suất không làm cân bằng chuyển dịch
B. Tăng nhiệt độ cân bằng chuyển dịch theo chiều thuận
C. Tăng nồng độ khí hydro cân bằng chuyển dịch theo chiều thuận
D. Giảm nồng độ cacbon monoxit cân bằng chuyển dịch theo chiều thuận
E. Chiều phản ứng tạo khí cacbonic là chiều tỏa nhiệt
Câu 3: Yếu tố nào ảnh hưởng đến trạng thái cân bằng của phản ứng sau:
2A(k) + B(k) ⇆ 3C(k) + D(k) 𝛥H = 0 A. Nhiệt độ B. Nồng độ C. Áp suất D. B và C E. A, B và C
Câu 4: Vì sao ở các cửa sông đổ ra biển, các hạt keo đất bị đông tụ tạo thành các châu thổ, bãi bồi 7? A.
Do nước sông và nước biển là hai hệ keo trái dấu nhau nên trung hòa lẫn nhau B.
Do sự thay đổi nhiệt độ giữa nước sông và nước biển C.
Do tác dụng của muối trong nước biết D.
Do nước biển không tạo được lớp vỏ solvat E.
Tất cả đều đúng Câu 5: Theo Bronsted:
A. Axit là chất có khả năng cho proton
B. Axit là chất có pH<7
C. Axit là chất khi hòa tan vào dung môi bất kì phân li thành ion H+ và anion
D. Axit là chất khi hòa tan vào nước phân li thành ion H+ và anion E. Tất cả đều đúng
Câu 6: Lý do làm cho tốc độ phản ứng tăng lên khi tăng nhiệt độ là:
A. Tần số va chạm giữa các phân tử tăng
B. Làm giảm năng lượng hoạt hóa
C. Làm cho 𝛥G của phản ứng âm hơn
D. Số phân tử phân tử hoạt động tăng E. A và D đúng
Câu 7: Phát biểu nào sau đây SAI:
A. Quá trình khử là quá trình nhận electron.
B. Hệ keo có kích thước hạt phân tần từ 1-100nm
C. Chất oxi hóa là chất nhận electron
D. Nguyên tố Galvani là thiết bị biến đổi điện năng thành hóa
E. Entropi có tính cộng tính
Câu 8: Cho: CaCO3(r) = CaO(r) + CO2(k) có 𝛥H = 42,4 kcal/mol và 𝛥S = 38,4 cal/mol.K.
Áp suất khí CO2 ở 25°C là: A. 4,7atm B. 2.10-23atm C. 3,7.10-6atm D. 2,3.108atm E. e-1266,9atm
Câu 9: Phát biểu nào sau đây SAI:
A. Chất xúc tác làm thay đổi tốc độ phản ứng
B. Chất xúc tác không làm cân bằng chuyển dịch
C. Chất xúc tác không thay đổi về lượng và chất sau phản ứng
D. Chất xúc tác làm trạng thái cân bằng được thiết lập nhanh hơn
E. Chất xúc tác có thể làm đổi dấu giá trị biển thiên thế đẳng áp-đẳng nhiệt (𝛥G) lOMoAR cPSD| 45148588
Câu 10: Cân bằng Donald chứng minh điều gì?
A. Tiểu phân keo không đi qua màng sinh vật nhưng cũng góp phần quyết định lượng chất điện ly đi qua màng sinh vật.
B. Khi nồng độ chất điện ly nhỏ hơn nồng độ chất keo rất nhiều thì chất điện ly hầu như không đi qua màng sinh vật.
C. Khi nồng độ chất điện ly bằng nồng độ chất keo thì có 1/3 chất điện ly đi qua màng sinh vật.
D. Khi nồng độ chất keo nhỏ hơn nồng độ chất điện ly rất nhiều thì chất điện ly hầu như phân bố đều hai bên màng sinh vật.
Câu 11: Cho phản ứng: 2A + B ⟶ C + D
Nồng độ ban đầu CA = 0,2mol/l và Cb = 0,1mol/l. Sau 30 phút phản ứng, nồng độ còn lại của B là 0,06mol/l
Tốc độ phản ứng ở thời điểm này giảm so với thời điểm ban đầu là: A. 6,3 lần B. 4,6 lần C. 2,8 lần D.10,4 lần E. 15, 3 lần
Câu 12: Cho biết: 𝛆0(Ti2+/Ti) = -1,63V và 𝛆0(Co2+/Co) = -0,28V. Cho phản ứng:
Ti2+ + Co ⇆ Ti + Co2+ A. -62267,4J B. 368630J C. -260550J D. 260550J E. 62267,4J
Câu 13: Cho phản ứng: 2Mg(r) + O2(k) ⟶ 2MgO(r) Mg(r) O2(k) MgO(r) 𝛥H0S(kcal/mol) 0 0 -143,8 S0(cal/mol) 7,8 49 6,4
(Giả thiết 𝛥Hs và S của các chất thay đổi theo nhiệt độ không đáng kể).
Biến thiên thế đẳng áp – đẳng nhiệt ở 500°C của phản ứng là: A. 117,9 kcal
B. -103,8 kcal C. -247,7 kcal D. 39,8 kcal E. -261,7 kcal
Câu 14: Tốc độ phản ứng tăng 8 lần khi tăng nhiệt độ từ 30°C đến 60°C. Vậy, tăng nhiệt độ từ 0°C đến 60°C thì tốc
độ phản ứng tăng lên: A. 16 lần B. 64 lần C. 32 lần D. Không tăng E. 8 lần
Câu 15: Ở 37°C, điều kiện đẳng áp, đốt cháy 1gam mỡ gà (M=304g) thoát ra 10kcal. Tính thiêu nhiệt của nó ở
37°C, biết phản ứng đốt cháy là: C20H32O2 (r) + 27O2 (k) = 20 CO2 (k) + 16H2O (l) A. +3040 kcal B. +10 kcal C. -370 kcal D. -10 kcal E. -3040 kcal
Câu 16: Cho phản ứng: C(than chì) + 2H2 + O2 ⟶ CH3OH C(than chì) H2 CH3OH 𝛥H0 C (kcal/mol) -94,05 -68,32 -173,65
Hiệu ứng nhiệt của phản ứng là: A. 57,04 kcal/mol B. 11,28 kcal/mol C. -57,04 kcal/mol D. -336,02 kcal/mol
Câu 17: Phát biểu nào sau đây SAI:
A. Sinh nhiệt tiêu chuẩn của một hợp chất là hiệu ứng nhiệt của phản ứng tạo thành một mol hợp chất đó từ đó
các đơn chất bền ở điều kiện chuẩn
B. Sinh nhiệt của các đơn chất bền ở diều kiện chuẩn bằng 0
C. Thiêu nhiệt tiêu chuẩn của một chất là hiệu ứng nhiệt của phản ứng đốt cháy một mol chất đó bằng oxy vừa
đủ để tạo thành oxyd bền ở điều kiện chuẩn
D. Hệ cô lập là hệ không trao đổi cả chất và năng lượng với môi trường xung quanh
E. Entanpi đặc trưng cho mức độ hỗn độn của hệ Câu 18: Phát biểu nào ĐÚNG:
A. Khả năng xúc tác của enzim xảy ra trên trên toàn bộ phân tử
B. Lực cần tác dụng lên 1 đơn vị diện tích màng bán thấm để ngăn cản hiện tượng thẩm thấu xảy ra gọi là áp suất thẩm thấu
C. Chất điện ly ít tan sẽ kết tủa khi tích số nồng độ ion của nó (với số mũ là số ion trong phân tử chất đó) nhỏ hơn tích số tan
D. Khi tiêm dung dịch ưu trương vào máu thì hồng cầu phình ra và vỡ
E. Dung dịch đệm có pH không thay đổi khi thêm vào đó một acid mạnh, base mạnh hoặc pha loãng Câu 19:
Hệ keo có thể được điều chế bằng phương pháp 1/…… hay phương pháp 2/……..
Câu 20: Cho biết thế oxi hóa-khử của các quá trình: lOMoAR cPSD| 45148588
I2 + 2e ⇆ 2 ¯I̅ 𝛆0 = 0,54V ; Cd2+ + 2e ⇆ Cd 𝛆0 = -0,40V Cl 2-
2 + 2e ⇆ 2Cl¯ 𝛆0 = 1,36V ;
Cr2O7 + 14H + 6e ⁺ ⇆ 2Cr3+ + 7H20 𝛆0 = 1,33V
Các chất khử được sắp xếp thành dãy mạnh dần như sau: A.
I2 < Cd2+ < Cr2O7 < Cl2 B. Cr 2-
2O7 < Cl2 < I2 < Cd2+ C. Cd < ¯ < CrI̅ 3+ < Cl¯ D.
Cl¯ < Cr3+ < ¯ < CdI̅ E.
Cd < Cd2+ < Cl¯ < Cl2 Câu 21: Phát biểu nào đúng: A.
Phản ứng tự diễn biến có hiệu ứng nhiệt âm B.
Hạn chế trong quan điểm acid-base theo Arrhenius là chỉ xét dung môi nước C.
Cứ tăng nhiệt độ lên 10°C, tốc độ phản ứng tăng lên 2 lần D.
Nội năng không phải là hàm trạng thái E.
Hệ chuyển từ trạng thái rắn sang trạng thái lỏng có entropi giảm Câu 22: Phát biểu nào sau đây SAI:
A. Dưới tác dụng của nhiệt độ và chất điện lỵ, các tiểu phân keo bị đông tụ.
B. Điện tích của keo thân dịch phụ thuộc vào môi trường.
C. Hiện tượng Tyndan có thể dùng để nhận biết hệ keo.
D. Dưới tác dụng của điện trường, lớp ion đối sẽ đi về một cực và hạt keo sẽ đi về cực còn lại của điện trường.
E. Áp suất thẩm thấu của hệ keo nhỏ hơn của dung dịch thật có cùng nồng độ khối lượng chất tan.
Câu 23: Tính hằng số cân bằng của phản ứng: 2A(k) + B(k) ⇆ 3C(k). Biết lúc cân bằng nồng độ các chất là:
[A] = 0,2M ; [B] = 0,5M ; [C] = 0,3M ; A. 0,33 B. 0 C. 1,35 D. 3 E. 0,74
Câu 24: Áp suất hơi nước bão hòa ở 25°C là 23,76mmHg. Áp suất hơi bão hòa của dung dịch chứa 45g chất tan A
(MA = 150g) không điện Iy, không bay hơi trong 117g nước ở 25°C là: A. 7,13mmHg B. 1,05mmHg C. 1,10mmHg D. 22,71 mmHg E. 22,10mmHg
Câu 25: Cho 3 dung dịch nước của NaCl, glucose, K2SO4 cùng nồng độ mol/l. Áp suất thẩm thấu của bà dung dịch xếp theo
thứ tự tăng dần như sau:
A. Glucose < NaCl < K2SO4
B. NaCl < glucose < K2SO4
C. K2SO4 < glucose < NaCl D. Glucose < NaCl = K2SO4
E. K2SO4 < NaCl < glucose
Câu 26: Cho biết: 𝛆0 (Fe3+/Fe2+) = +0,77V và 𝛆0 (Cu2+/Cu) = +0,34V. Phản ứng tự diễn biến như sau:
A. 2Fe3+ + Cu2+ ⟶ 2Fe2+ + Cu
B. 2Fe3+ + Cu2+ ⟶ 2Fe2+ + Cu2+
C. 2Fe2+ + Cu2+ ⟶ 2Fe3+ + Cu
D. 2Fe3+ + Cu2+ ⟶ 2Fe3+ + Cu2+ E. Tất cả đều sai
Câu 27: 500ml dung dịch chứa 9g chất tan A không điện lỵ, không bay hơi có áp suất thẩm thấu là 4,674atm ở 12°C. Khối
lượng phân tử chất tan A: A. 90g B. 18g C. 2883g D. 86g E. 2181g
Câu 28: Tích số tan của PbSO4 là 1,8.10-8. Khi trộn 50ml dung dịch Pb (NO3)2 0,001M với 200ml dung dịch Na2SO4 5.10-3N
thì có kết tủa PbSO4 không và tích số nồng độ ion để so sánh? A. 8.10-7 có kết tủa
B. 1,3.10-6 không có kết tủa C. 5.10-7 có kết tủa D. 5.10-6 có kết tủa E. 4.10-7 có kết tủa
Câu 29: Ở 1 atm và 1000°C, có phản ứng: C(r) + CO2(k) ⟶ 2CO(k) 𝛥H = -41,24 kcal/mol.
Vậy, 𝛥U của phản ứng là: lOMoAR cPSD| 45148588 A. 41,24 kcal/mol B. 38,71 kcal/mol C. 39,25 kcal/mol
D.-1,95 kcal/mol E - 2.49kcal/mol Câu 30:
Cho dung dịch sau: 1- KCI; 2- Na2CO3; 3- CuSO4; 4- CH3COOK; 5- Al2(SO4)3 35; 6- NH4NO3; 7- KNO3; 8- K2S. Dung dịch có pH = 7 là: A. 1, 7 B. 1, 7, 8 C. 2, 4, 8 D. 1, 6, 7, 8 E. 1, 4, 7, 8
Câu 31: Hòa tan 10,88g ZnCl2 vào 1000g nước thu được dung dịch đông đặc ở -0,385°C. Tính nhiệt độ sôi của dung dịch
đó? Biết: M(ZnCl2) = 136g; nước có Kđ=1,86 độ/mol và KS = 0,52 A. 100,04°C B. 101,10°C C. 102,59°C D. 100,02°C E.100,11°C
Câu 32: Ở 25°C, hòa tan được tối ta 0,25mg BaSO4 trong nước tạo thành 100ml dung dịch. Xác định tích số tan của BaSO4? Biết M(BaSO4) = 233g. A. 1,15.10-4 B. 1,1510-10 C. 6,2510-6 D. 1,3210-8 E. 1,0710-5
Câu 33: Cho 2 NO2(k) ⇆ N2O4(k) ở 100°C có Kp = 0,08. Hằng số cân bằng KC ở nhiệt độ đó là: A. ≈ 0,08 B. ≈ 59 C. ≈ 248 D. ≈ 2,6.10-3 E. ≈ 2,45
Câu 34: Vì sao tiểu phân keo không đi qua màng sinh vật?
A. Tiểu phân keo mang điện tích
B. Tiểu phân keo có kích thước lớn
C. Tiểu phân keo bị hấp phụ trên màng sinh vật
D. Tiểu phân keo bị đông tụ khi gặp màng sinh vật E. Tất cả đều đúng
Câu 35: Phát biểu nào ĐÚNG:
A. Trong dung dịch chất điện ly yếu: càng pha loãng, độ điện ly càng tăng.
B. Nhiệt độ sôi của dung môi nguyên chất thấp hơn dung dịch chứa chất tan không điện lỵ, không bay hơi
C. Nhiệt độ đông đặc của một dung dịch chứa chất tan không điện lỵ, không bay hơi là nhiệt độ tại đó áp suất
thẩm thấu của pha lỏng và pha rắn bằng nhau.
D. Giá trị hằng số cân bằng không phụ thuộc vào nhiệt độ. E. Tất cả đều sai
Câu 36: Fe2(SO4)3 + 6NaOH ⟶ 2Fe(OH)3 + 3Na2SO4 (M(Fe2(SO4)3) = 208g). Đương lượng gam của Fe2(SO4)3 A. 34,7g B. 208g C. 104g D.69,3g E. 20,8g Câu 37:
Câu 38: Cho K2Cr2O7 + 3H2S + 4H2SO4 ⟶ Cr2(SO4)3 + 3S + K2SO4 + 7H2O. Đương lượng gam của H2S (M(H2S) =34g) là: A. 34g B. 17g C. 11,3g D. 5,7g E. 3,4g
Câu 39: 500g dung dịch nước đường C6H12O6 có chứa 9g chất tan đông đặc ở -0,186°C. Dung dịch nước glyxerin cần có
nồng độ bao nhiêu để đông đặc ở cùng nhiệt độ như dung dịch đường trên. M(C6H12O6) = 180g A. 0,098mol/l B. 1.10-4 molan C. 1,8% D. 0,1 molan E. 0,098 molan PHẦN II
Câu 41: Acid glutamic phản ứng được với những chất nào sau đây:
A. Anhydrid acid, aceton, acid halogenid, ninhydrin, metan.
B. Ninhydrin, alcol etylic, toluen, acid acetic, metyl halogenid. lOMoAR cPSD| 45148588
C. Dung dịch CuSO4, aldehyd acetic, acyl halogenid, etylen, ninhydrin.
D. Ninhydrin, metyl halogenid, aceton, acid acetic, propen.
E. Dung dịch CuSO4, alcol etylic, acyl halogenid, ninhydrin.
Câu 42: Cho phản ứng sau: cis-3,4-dimetylhex-3-en + H (PtO₂2) ⟶ sản phẩm. Hãy cho biết sản phẩm là gì? A. Đồng phân meso B. Đồng phân hình học
C. Đồng phân meso và hỗn hợp racemic D. Hỗn hợp racemic
E. Hai đồng phần quang học.
Câu 43: Hợp chất 2,3,4-tricloropentandial có bao nhiêu đồng phân quang học? A. 4 B. 3 C. 1 D. 2 E. 5
Câu 44: Aldohexose có bao nhiêu nguyên tử carbon bất đối (C*), số lượng đồng phân quang học, số đôi đối quang?
A. Có 4 C*, 8 đồng phân quang học, 4 đôi đối quang.
B. Có 4 C*, 16 đồng phân quang học, 4 đôi đối quang.
C. Có 3 C*, 6 đồng phân quang học, 2 đôi đối quang.
D. Có 4 C*, 16 đồng phân quang học, 8 đôi đối quang.
E. Có 3 C*, 8 đồng phân quang học, 4 đôi đổi quang.
Câu 45: Cetoheptose có bao nhiêu nguyên từ carbon bất đối (C*), số lượng đồng phân quang học, số đôi đối quang?
A. Có 3 C*, 6 đồng phân quang học, 2 đôi đối quang.
B. Có 3 C*, 8 đồng phân quang học, 4 đôi đối quang. C. Có 4 C*, 8 đồng phân
quang học, 4 đồi đối quang.
D. Có 2 C*, 4 đồng phân quang học, 2 đôi đối quang.
E. Có 4 C*, 16 đồng phân quang học, 4 đối đối quang.
Câu 46: Khí cacbonic chiếm tỉ lệ 0,03% thể tích không khí. Cần bao nhiêu lít không khí (ở đktc) để cung cấp CO2 cho phản
ứng quang hợp tạo ra 50 gam tỉnh bột: A. 112554,3 lít B. 125541,3 lít C. 136628,7 lít D. 116554,3 lít E. 138271,6 lít
Câu 47: Phát biểu nào sau đây KHÔNG ĐÚNG:
A. Tất cả các monosaccarid đều có tính khử.
B. Các disaccarid bị oxy hóa bởi thuốc thử Tollens và thuốc thứ Fehling.
C. Deoxyribose (C5H10O4) thuộc loại monosaccarid.
D. Lactose là một disaccarid được cấu tạo từ một phân tử D-galactose và một phân tử D-glucose.
E. Maltose là một disaccarid có tính khử.
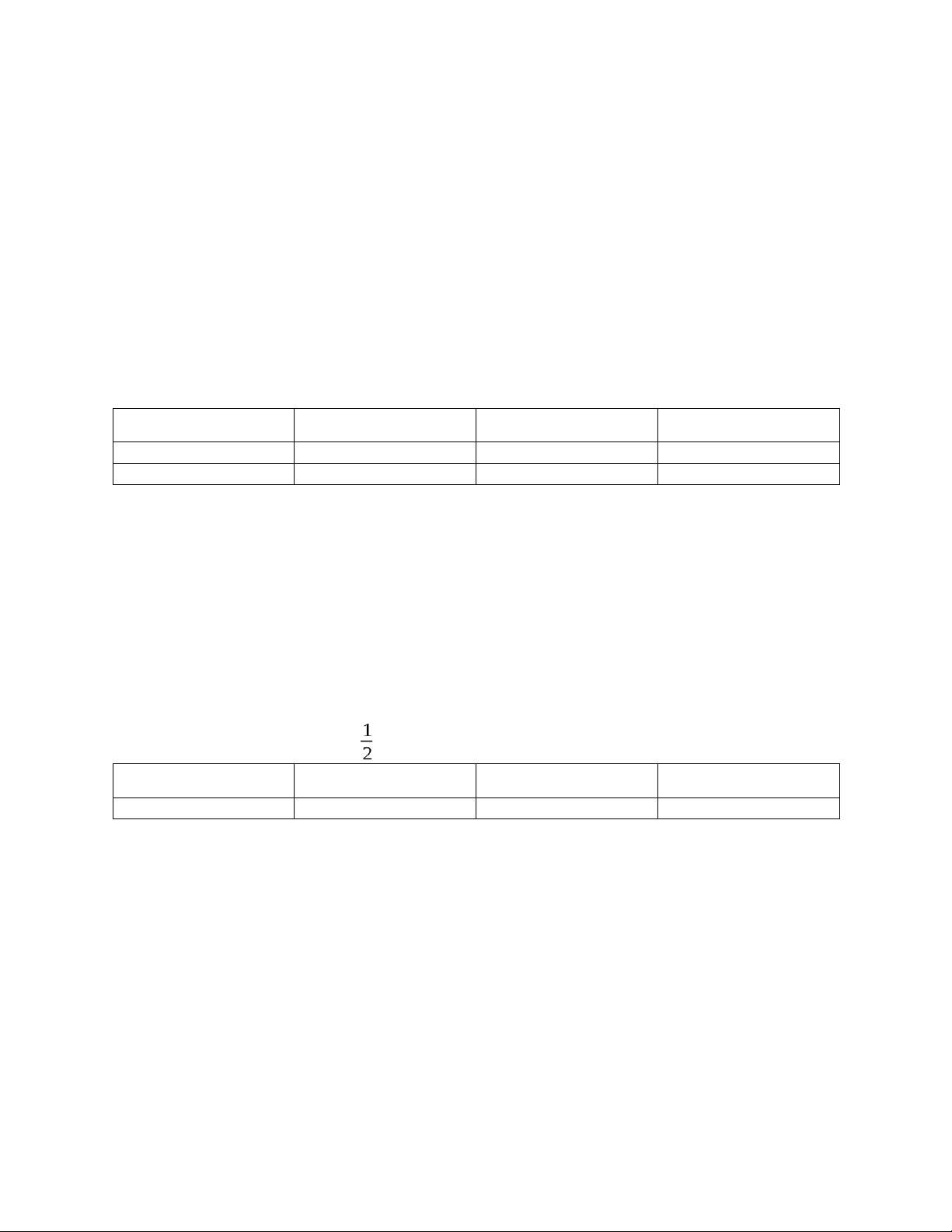
Câu 48: Tổng số đồng phân quang học khi hợp chất có số nguyên tử carbon bất đối khác nhau là: A. 2n-1 + 2(n-1)/2 B. 2n-1 - 2(n-1)/2 C. 2n-1 D. 2(n-2)/2 E. 2n
Câu 49: Chọn đáp án ĐÚNG:
A. Đồng phân quang học là những chất có cùng công thức cấu tạo phẳng nhưng có cấu trúc không gian khác
nhau, do đó có khả năng làm quay mặt phẳng ánh sáng phân cực khác nhau.
B. Đồng phân quang học là những chất có công thức cấu tạo và cấu trúc không gian giống nhau, do đó có khả
năng làm quay mặt phẳng ánh sáng phân cực khác nhau.
C. Đồng phân quang học là những chất có công thức cấu tạo phẳng và cấu trúc không gian khác nhau, do đó có
khả năng làm quay mặt phẳng ánh sáng phân cực khác nhau. D.
Đồng phân quang học là những đồng phân quang hoạt.
E. Đồng phân quang học là những chất có cấu trúc không gian giống nhau nhưng có công thức cấu tạo khác
nhau, do đó có khả năng làm quay mặt phẳng ánh sáng phân cực khác nhau. lOMoAR cPSD| 45148588
Câu 50: Cho các chất sau: CH3‒CHCl CH‒3 , CH3‒CHBr CHBr CHBr CH‒ ‒ ‒ 3 , CH3‒CH2‒ CHBr CH‒ 2‒CH3 ,
HOOC CH‒2‒CH(NH2) CH(NH‒2) COOH , C‒6H5‒CH(NH2) CH(OH) CH(NH‒ ‒ 2) COOH , CH‒ 3-CO CH‒ 2‒ COOCH3 , HO CH‒ 2‒(CHOH)3‒CO CH‒ 2OH
Hãy cho biết trong số các chất trên, có bao nhiêu chất có đồng phân quang học A. 4 B. 2 C. 3 D. 5 E. 6
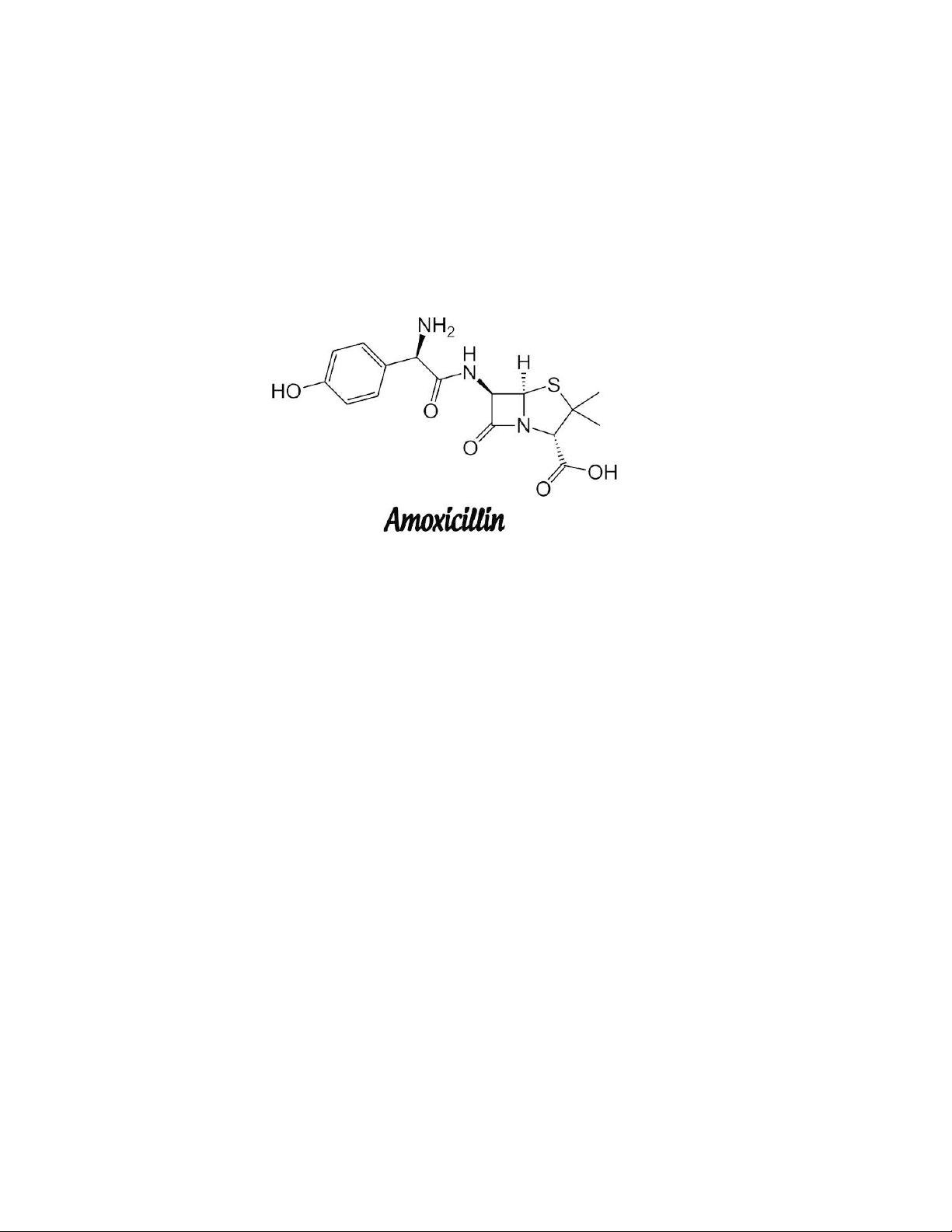
Câu 51: Amoxicillin (C16H19N3O5S) là loại kháng sinh dùng trong y học. Hãy cho biết trong công thức cấu tạo của
Amoxicillin cho bên dưới đây, có bao nhiêu nguyên tử carbon bất đổi, số lượng đồng phản quang học và số đôi đối quang?
A. Có 3 nguyên tử carbon bất đối, 6 đồng phân quang học và 3 đôi đối quang.
B. Có 4 nguyên tử carbon bất đối, 16 đồng phân quang học và 8 đôi đối quang.
C. Có 2 nguyên tử carbon bất đối, 4 đồng phân quang học và 2 đôi đối quang.
D. Có 3 nguyên tử carbon bất đối, 8 đồng phân quang học và 4 đôi đối quang.
E. Có 4 nguyên tử carbon bất đối, 8 đồng phân quang học và 4 đôi đối quang.
Câu 52: Phát biểu nào sau đây SAI:
A. Celobiose là một disaccarid khử.
B. Để phân biệt đường khử và đường không khử tiến hành phản ứng tạo oxim.
C. Cellulose được hình thành từ các β – D-glucopyranose, còn tỉnh bột từ các α — D- glucopyranose.
D. Tất cả các monosaccarid đều có đồng phân quang học.
E. Trong môi trường kiềm, các aldose và cetose có hỗ biến endiol.
Câu 53: Vitamin C (Acid ascorbic) thuộc dây D- hay L-? số lượng đồng phân quang học, số đôi đối quang, đồng
phân meso (nếu có)?
A. L-, 3 đồng phân quang học, 1 đôi đối quang, 1 đồng phân meso.
B. L-, 4 đồng phân quang học, 2 đối đối quang, không có đồng phân meso.
C. L-, 5 đồng phân quang học, 2 đôi đối quang, 1 đồng phân meso.
D. D-, 4 đồng phân quang học, 2 đôi đối quang, không có đồng phân meso.
E. D-, 3 đồng phản quang học, 1 đôi đối quang, 1 đồng phân meso.
Câu 54: Để phân loại các chất quang hoạt, người ta dùng danh pháp D- và L-. Chọn đáp án ĐÚNG: A.
Đối với glucid, nếu nhóm -OH ở C* xa nhóm chức chính nhất ở bên phải so với đường thẳng đứng thì
thuộc dãy -L và ngược lại ở bên trái thì thuộc dãy D- B.
Đối với amino acid, nếu nhóm – NH2 ở C* xa nhóm chức chính nhất ở bên phải so với đường thẳng đứng
thì thuộc dãy D, và ngược lại ở bên trái thì thuộc dãy L. C.
Đối với glucid, nếu nhóm -OH ở C* gần nhóm chức chính nhất ở bên phải so với đường thẳng đứng thì
thuộc dãyD- và ngược lại ở bên trái thì thuộc dãy L-. lOMoAR cPSD| 45148588 D.
Đối với amino acid, nếu nhóm -NH2 ở gần nhóm chức chính nhất ở bên phải so với đường thẳng đứng thì
thuộc dãy L- và ngược lại ở bên trái thì thuộc dãy D-. E.
Đối với glucid, xét nhóm -OH ở C* xa nhóm chức chính nhất ở bên phải so với đường thẳng đứng thì thuộc
dãy D- và ngược lại ở bên trái thì thuộc dãy L-.
Câu 55: Có ba hợp chất: A,B và C
Số nguyên tử carbon bất đối (C*) lần lượt trong từng hợp chất trên là: A. 2, 4, 4 B. 1, 4, 3 C. 3, 3, 4 D. 3, 3, 4 E. 4, 8, 6
Câu 56: Acid lactic có trong sữa chua ở dạng nào và có tổng số bao nhiêu đồng phân hình học?