
Preview text:
lOMoAR cPSD| 45148588 1
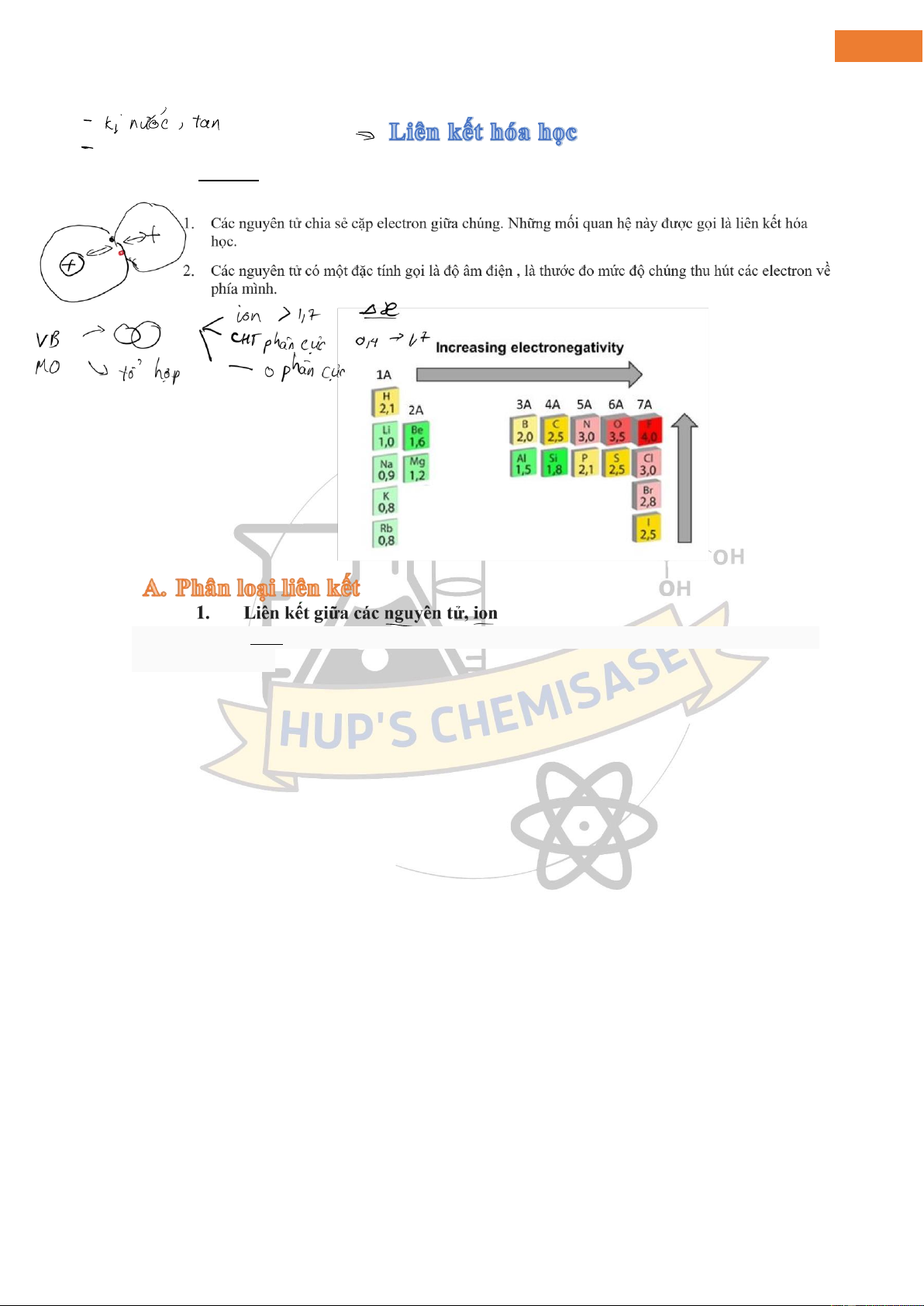
Định luật Coulomb – lực hút và lực ẩy giữa các iện tích – ảnh hưởng ến tính chất của nguyên tử và gây ra hiện
tượng liên kết hóa học. -
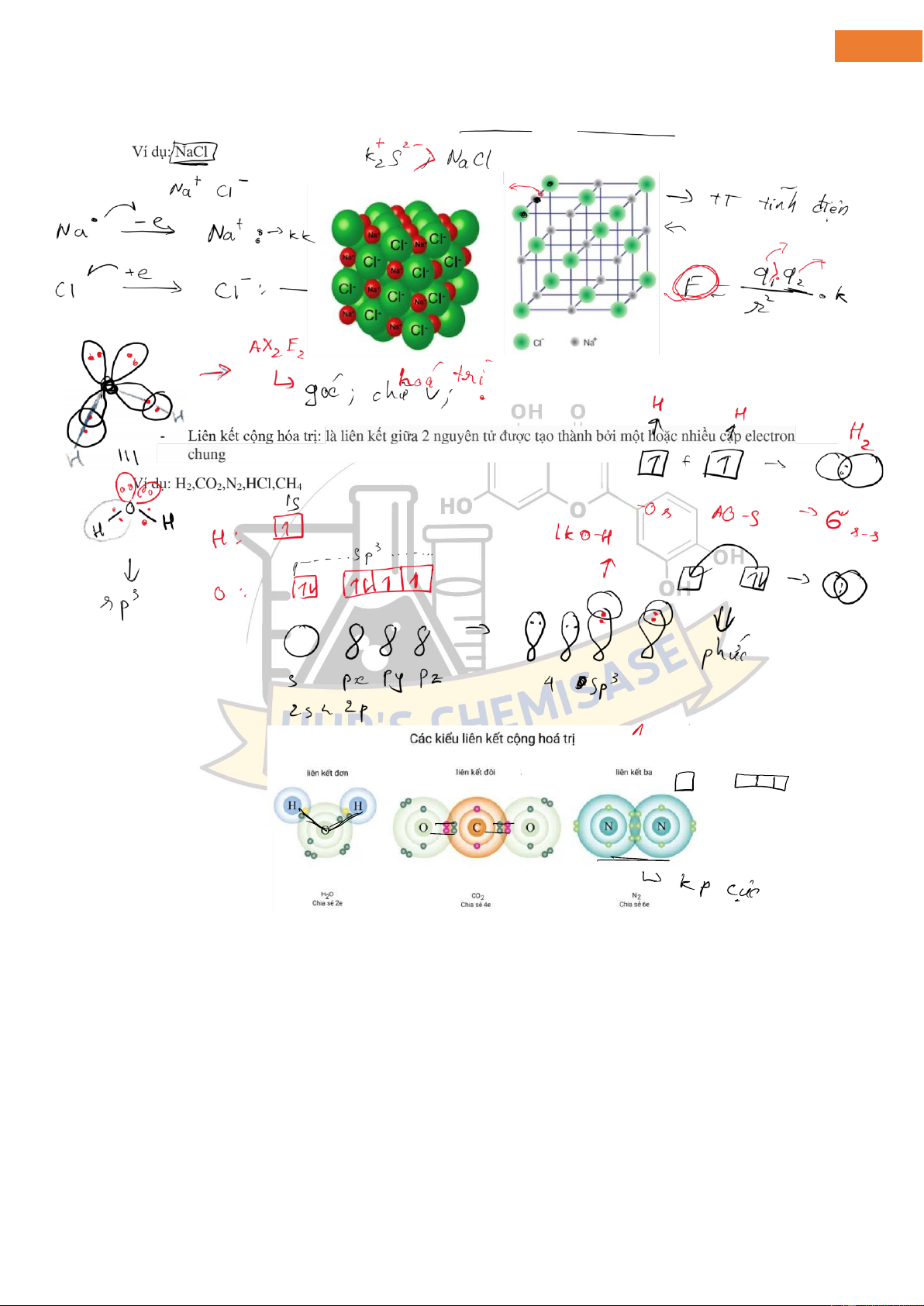
Liên kết i-on (hay liên kết iện tích) là một liên kết hóa học có bản chất là lực hút tĩnh iện giữa 2 ion mang iện tích trái dấu
những tương tác này càng mạnh thì iểm nóng chảy và iểm sôi càng cao . lOMoAR cPSD| 45148588 2 lOMoAR cPSD| 45148588 3
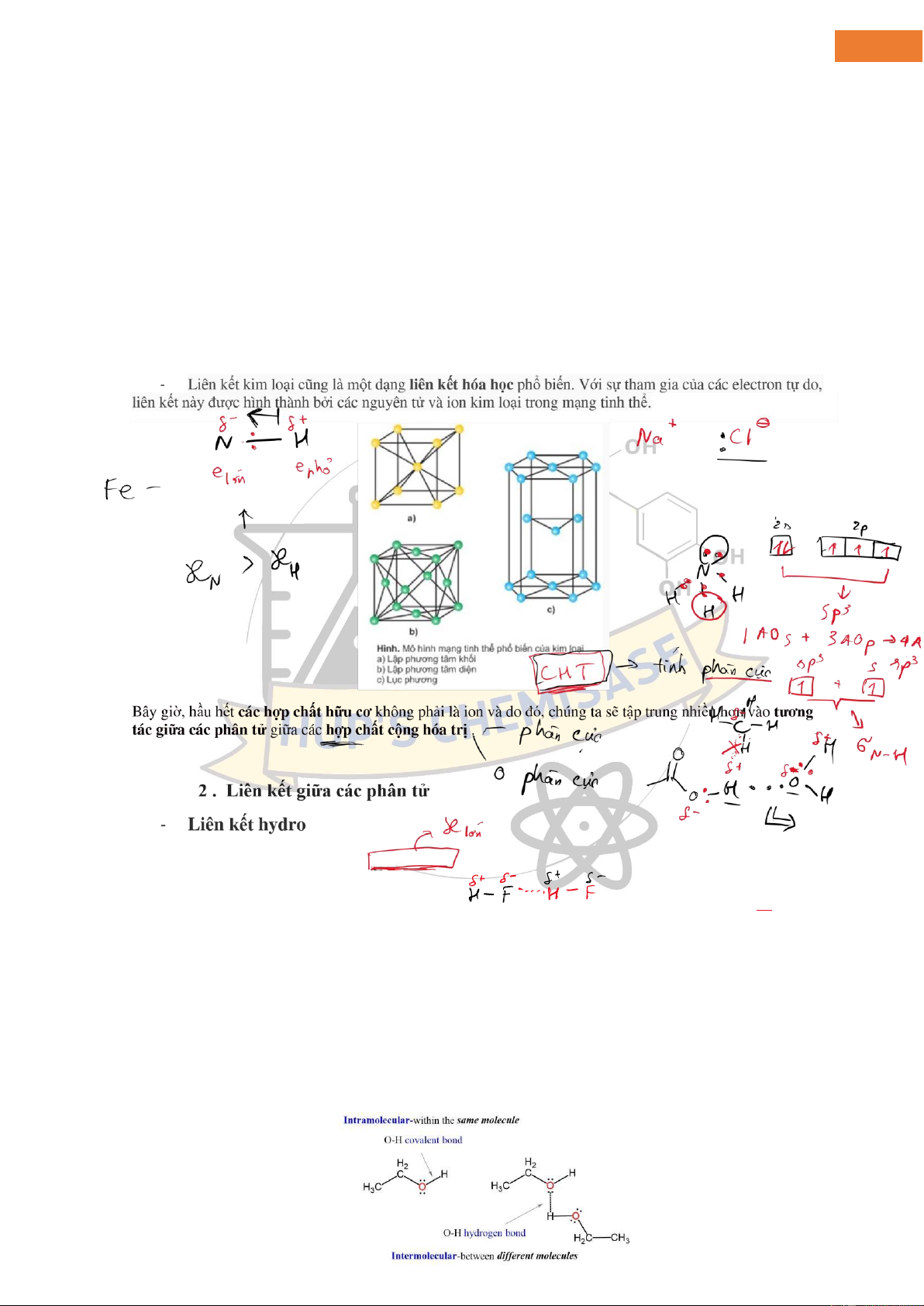
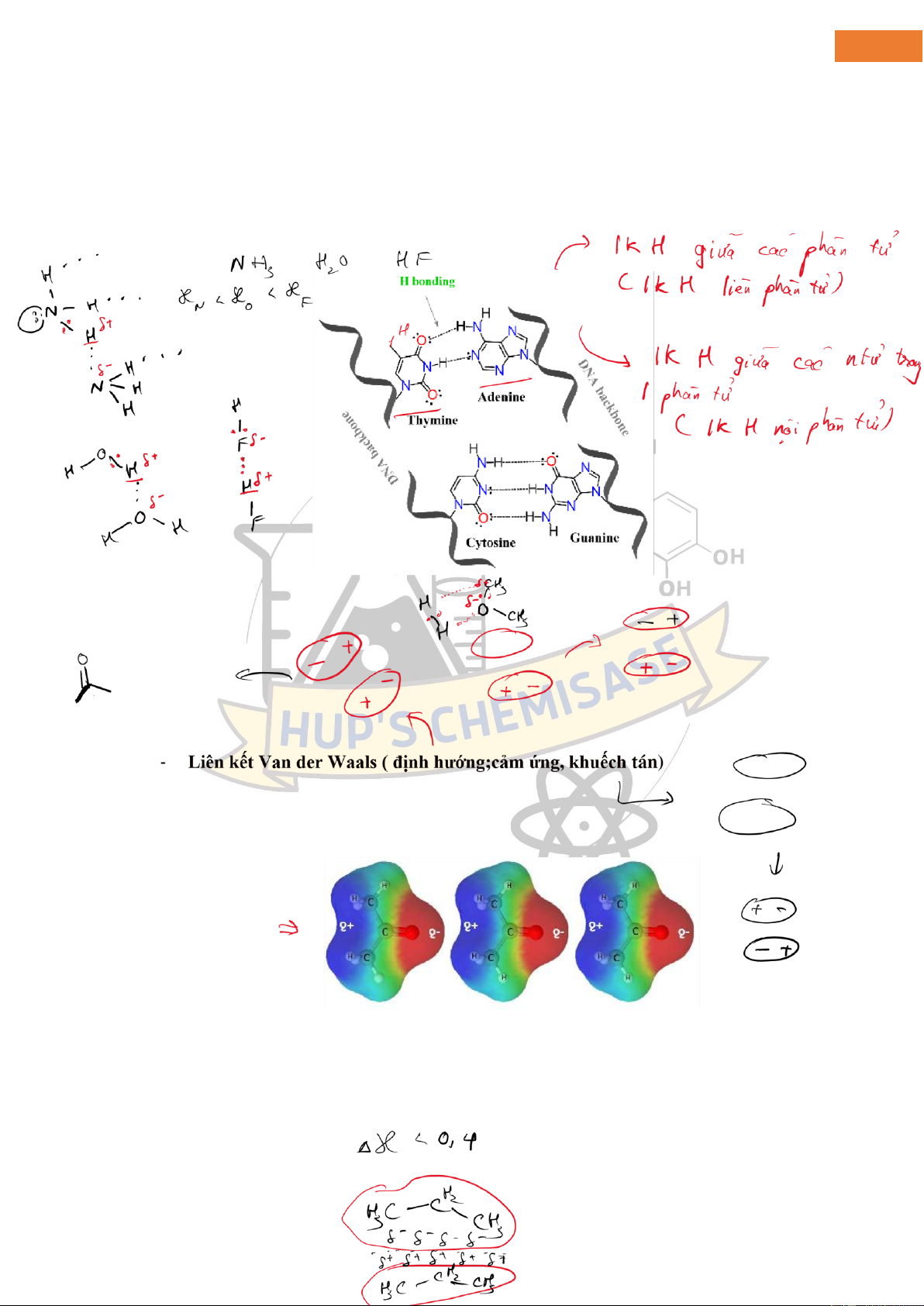
Liên kết hydro là một loại tương tác tĩnh iện liên
phân tử khác xảy ra giữa một
nguyên tử hydro liên kết với một nguyên tử có ộ
âm iện như O, N hoặc F, bị hút
bởi một cặp electron ơn ộc trên một nguyên tử trong phân tử khác. Để nhấn mạnh iều này một lần nữa; Liên
kết hydro không phải là liên kết cộng hóa trị trong phân tử mà là một loại tương tác lưỡng cực-lưỡng cực
cụ thể. Cơ sở của nó là lực hút giữa iện tích dương một phần của hydro và cặp electron của phân tử kia. Liên kết
hydro ược thể hiện bằng các ường chấm chấm nối một cặp ơn ộc với hydro.
Ví dụ, chúng ta hãy so sánh liên kết cộng hóa trị giữa oxy và hydro trong cùng một phân tử ethanol với liên kết
hydro của hydro với nguyên tử oxy trong một phân tử ethanol khác: lOMoAR cPSD| 45148588 4
Điều xảy ra là nguyên tử hydro kết nối với nguyên tử oxy có ộ âm iện lớn hơn mang iện tích dương một phần
(δ+) do oxy kéo mật ộ electron thông qua cảm ứng. δ+ này sau ó tương tác với một cặp nguyên tử oxy có ộ âm
iện lớn hơn của một phân tử etanol khác .
Liên kết hydro rất phổ biến trong tự nhiên bắt ầu từ nước và i ến các hệ thống sinh học phức tạp như DNA và
protein. Chính liên kết hydro chịu trách nhiệm về tính chất bổ sung của các nucleobase DNA và do ó tạo nên
nguyên tắc mã hóa di truyền. lOMoAR cPSD| 45148588 5
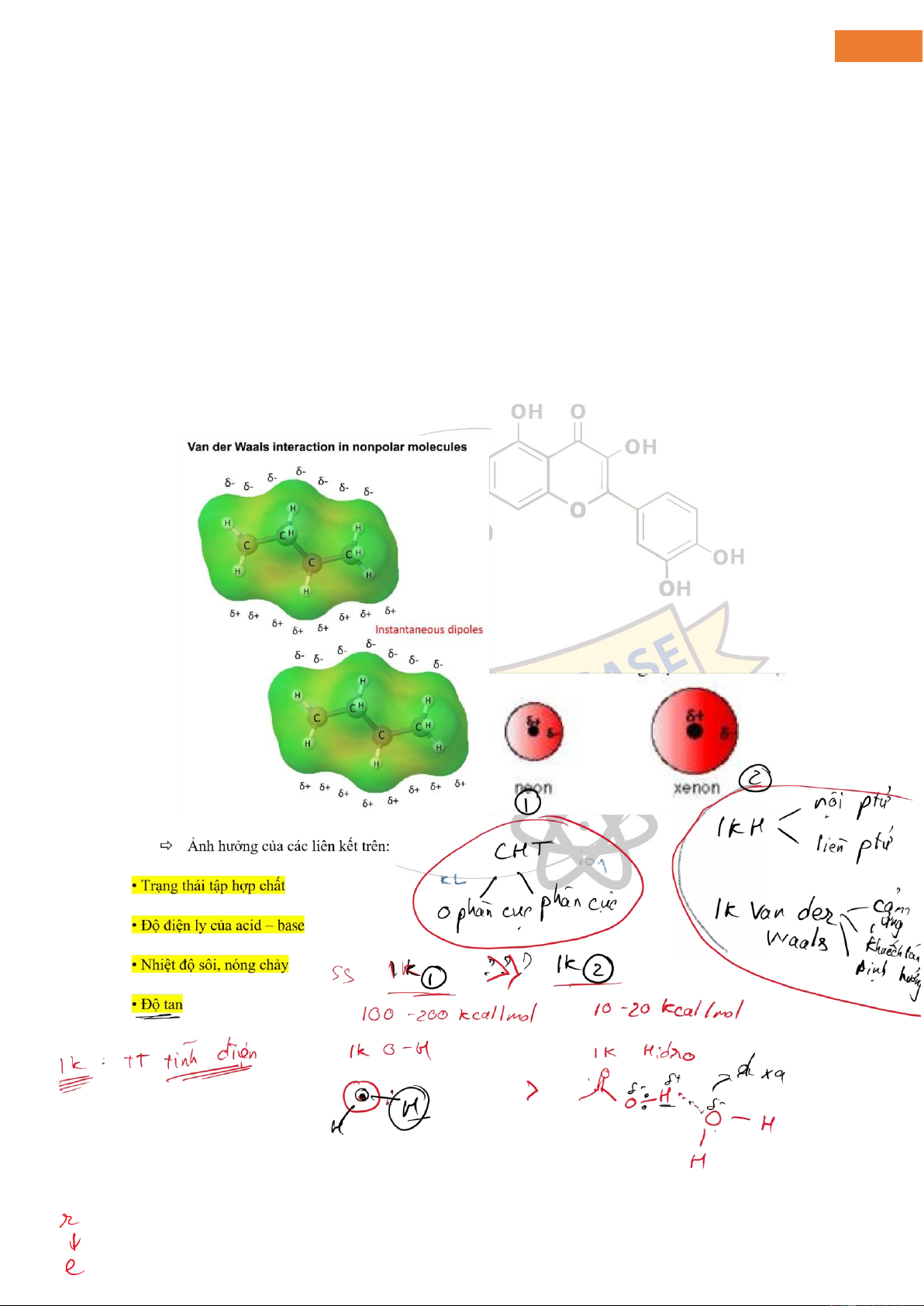
Đây là những tương tác nội phân tử yếu nhất và xảy ra dưới dạng tương tác tĩnh iện của các khoảnh khắc
lưỡng cực tạm thời ược hình thành trong phân tử ngay tại thời iểm chúng ở khoảng cách ủ gần. Điều xảy ra
trong thời iểm này là mật ộ electron của phân tử bị biến dạng do lực hút và lực ẩy giữa hạt nhân và electron của hai phân tử.
Đây là các tương tác tạo ra một mômen lưỡng cực tức thời rất nhỏ do sự mất cân bằng iện tích. Các iện tích trái
dấu tạm thời trong các phân tử khác nhau sắp xếp thẳng hàng sau ó ảnh hưởng ến các tính chất vật lý. Lực phân
tán London chỉ ặc trưng cho các phân tử nhỏ. Chúng áp dụng như nhau cho các hợp chất hữu cơ và vô cơ lớn hơn: lOMoAR cPSD| 45148588 6 lOMoAR cPSD| 45148588 7
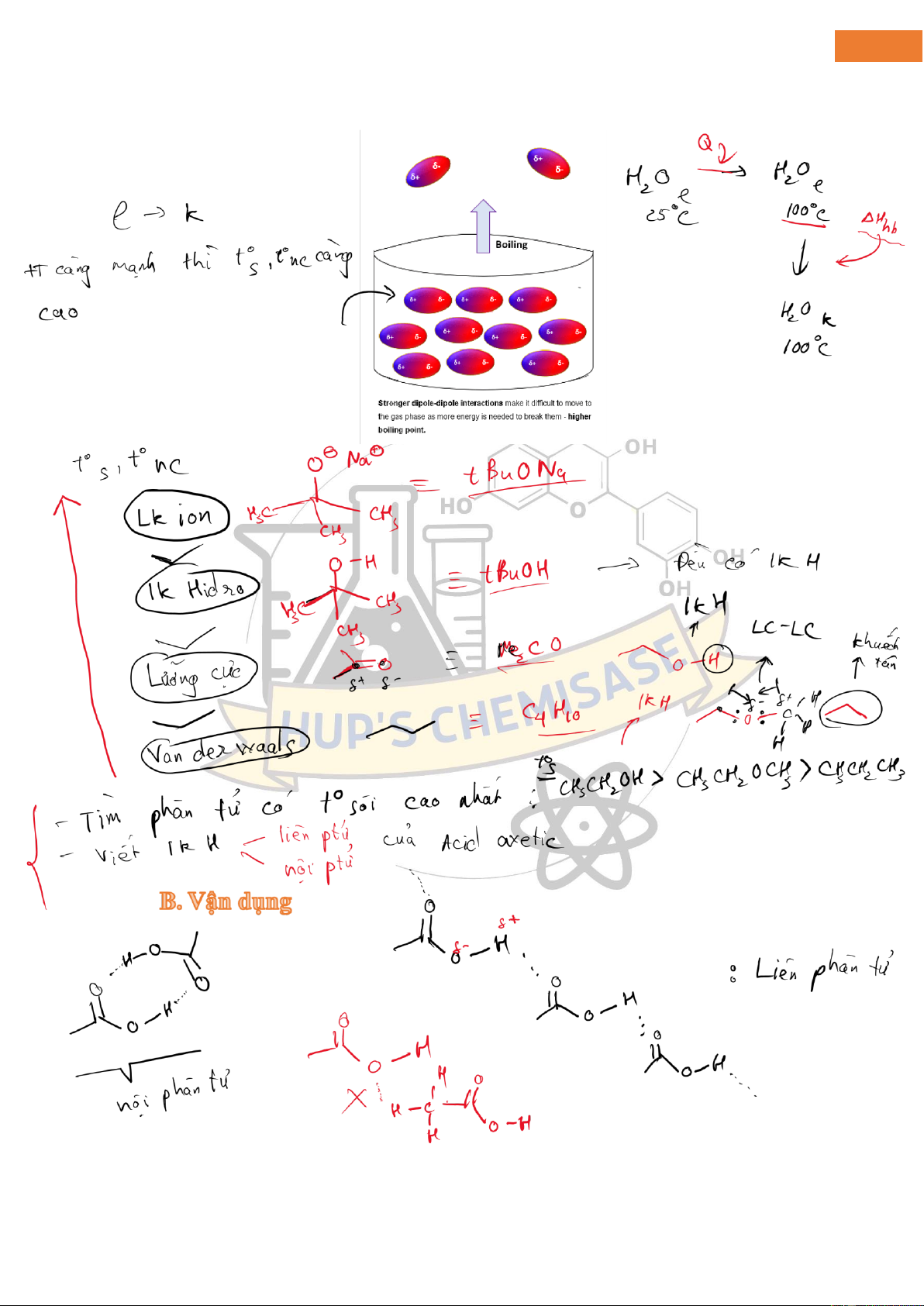
Định nghĩa về iểm sôi nói rằng ó là nhiệt ộ khi áp suất hơi của hợp chất bằng áp suất khí quyển . Nói cách
khác, chúng ta có thể nói chính nhiệt ộ mà tại ó có quá nhiều hợp chất bay hơi sẽ tạo ra áp suất bằng áp suất bên
ngoài. Ở một góc ộ ơn giản hơn, hãy nói rằng ó là nhiệt ộ khi chất lỏng biến thành chất khí mặc dù quá trình
này có thể xảy ra ở quy mô lớn về sự kết hợp nhiệt ộ và áp suất.
Bây giờ, ể chuyển sang pha khí, các phân tử phải vượt qua các tương tác giữa các phân tử và thoát ra khỏi bề mặt
chất lỏng, và những tương tác này càng mạnh thì các phân tử càng khó vượt qua những tương tác ó. lOMoAR cPSD| 45148588 8 lOMoAR cPSD| 45148588 9 lOMoAR cPSD| 45148588 10