






Preview text:
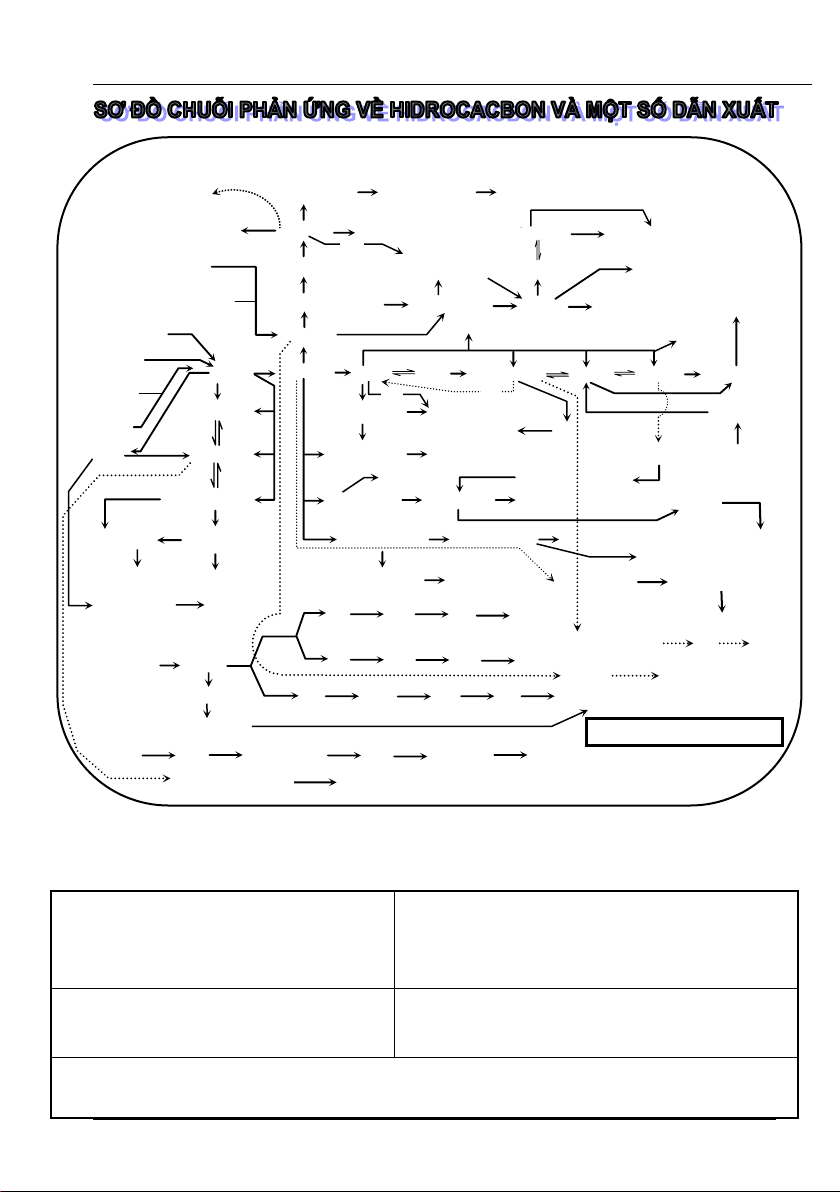
Sơ đồ tư duy HÓA HỌC HỮU CƠ 11 & 12-ban KHTN & CƠ BẢN Mèi quan hÖ gi÷a hidroca cbon vµ dÉn xuÊt (100) (42) (43) Phenyl axetat Xiclohexanol Xiclohexanon
12- brom xiclohexanon (91) (41) (39) (90) 2,4,6-tribrom phenol (40) Phenol
2,4,6-tri nitro phenol A xXe ton (?) Xianohidrin +Br2/H2O,H+ (38b) (38) (88) (89) Phenyl fomat (7) Hexan (46)
Natri phenolat 1-brom-1-phenyl etan (R) Poli(butadien-stiren) (38) (44c) (44d) (87) Xiclo hexan (8)
Phenyl bromua (44) Etyl benze n (45) (47) Stiren Poli stiren Etyl axetat (37) (44b) (1) ● Oxit etilen Nat ri axetat Benzen Poli etilen (96 ) (35) (2) (34) (36) ● (34) P ropan (31) (32) (21) (33) (22) (23) (25) (26) (28) (30) Metan Axetilen Etilen Etan (5) Et (24) yl bromua Etanol Etanal Axit axetic (9) (27) (29) (64) ● Bu tan (3) (48) (94) (95) (18) (49) Metyl clo rua (63) 1,2-diclo etan Etilen gly (25a) col (4) Glucozơ ● Al 4C3 (25b) (10) (65) (50) CH (11) 3CH2-C (62) (6) (19) (51) (52) OOH CH3CH2-C N CO Methan ol Vinyl clorua
Poli vinyl clorua (pVC) CH ● 3CH(OH)CN Tinh bột (12) Tơ olon (67) (66) (13) (53a) Tơ itro CH3CH(OH)COOH (14) (20) (53) (54) (55) Andehit fomic CH 2=CH-CN Axit acril Metyl acrilat (15) ic Axit poliacrylic Anlyl acrilat (56) (56b) (16) (57) (58) (59) (NH Vinyl axetilen Buta-1,3-dien 4)2CO3 Axit fomic Polibutadien Poli(metyl acrilat) (59a) (14b) (17) (106) (60) Cao su buna-N (103) (61) CO2 Metyl fomiat 2-clo buta-1,3-dien Poli c loropren (104) Vinyl axetat Poli(vinyl axetat) (92) (70) (93) (71) (72) (105) Axit axetic …? (69) +NaOH (X) đặc +CO2 + dd Br (25c) P (P) (H) 2 (M) 2O5 Poli (ancol vinylic) p,t0 +H Br 2O 2/Fe (74) (25e) (76) Magie etylbromua (25d) t0 (75) (73) +NaOHđặc X ? +CO + dd Br 2 (68) 2 + CO2 + HCl ● (Y) Isoheptan Toluen (Q) (K) (N) p,t0 +H2O (107) (97) Cumen Axeton + phenol Br ? 2/as +NaOHdd +CuO Kali benzoat (A) (B) (D) (E) benzyl bezoat (77) t0 (78) t0 (79) (80) (81) (98) (99) Axit benzoic
Thầy Trần Thiếu Lượng (84) (85) (82) (83) +Cu(OH)2 ● P ropan (A +Cl2 +NaOH 1) 3-clopropen (A2) Glixerol ? (101) +H (86) 2O t0 Metyl metacrilat (102) Thủy tinh hữu cơ
(tặ g các e học si h
sắp LTĐH & học si h ô tập HK II, chuẩn bị lên 12. Cố lên nhé)
Phương pháp công nghiệp ● CH xt, to H2SO4, to 4 + H2O Ō CO + H2
● CH2=CH2 + HOH Ō CH3CH2OH (ancol etylic) ZnO CO + 2H men
2 Ō CH3OH (ancol metylic)
● (C6H10O5)n + nH2O Ō nC6H12O6 (glucozơ) 4000, 200 atm ● CH Cu men
4 + ½ O2 Ō CH3OH (ancol metylic)
C6H12O6 Ō 2C2H5OH + 2CO2 2000, 100 atm ● xt, to CH PdCl2, CuCl2
3OH + ½ O2 Ō HCHO + H2O
● CH2=CH2 + ½ O2 Ō CH3CHO (andehit axetic) ● xt, to CH men
4 + O2 Ō HCHO (andehit fomic) + H2O
● (CH3)2CH-C6H5 Ō CH3OCH3 + C6H5OH (phenol) ● CH men giấm xt, to
3CH2OH + O2 Ō CH3COOH + H2O ● CH3CHO + ½ O2 Ō CH3COOH (axit axetic) ● CH xt, to
3OH + CO Ō CH3COOH (axit axetic)
Thầy Trần Thiếu lượng 1
Sơ đồ tư duy HÓA HỌC HỮU CƠ 11 & 12-ban KHTN & CƠ BẢN
Hoµn thµnh chuçi ph¶n øng CaO, to 1. CH
25a. CH3CH2-Br + KCN Ō CH3CH2-CN + KBr 3COONa + NaOH Ō CH4 + Na2CO3 H+ xt, to
25b. CH3CH2CN + 2H2O Ō CH3CH2COOH + NH3 2. C3H8 Ō CH4 + C2H4
25c. CH3CH2Br + Mg Ō CH3CH2MgBr 3. C xt, to 4H10 Ō CH4 + C3H8
25d. CH3CH2MgBr + CO2 Ō CH3CH2COOMgBr
4. Al4C3 + 12H2O Ō 3CH4 + Al(OH)3
25e. CH3CH2COOMgBr + HClŌCH3CH2COOH (?) 5. CH xt, to + ½ MgCl2 + ½ MgBr2 4 + H2O Ō CO + 3H2 t0 xt, to, p
26. C2H5Br + NaOH Ō C2H5OH + NaBr 6. CO + 2H 2 Ō CH3OH
27. C2H5OH + HBr đặc Ō C2H5Br + H2O 7. C xt, to 6H14 Ō (C6H6) + 4H2 28. CH to
3CH2OH + CuO Ō CH3CHO + Cu + H2O xt, to 8.
(C6H12) Ō (C6H6) + 4H2 Ni, to 29. CH 3CHO + H2 as Ō CH3CH2OH 9. CH 4 + Cl2 Ō CH3Cl + HCl xt, to 30. CH 3CHO + ½ O2 Ō CH3COOH 10. CH t0 3Cl + NaOH Ō CH3OH + NaCl
(hay: CH3CHO + Br2 + H2O → CH3COOH + 2HBr)
11. CH3OH + HCl đặc Ō CH3Cl + HOH
31. CH2=CH2 + HBr Ō CH3CH2Br 12. CH t0 3OH + CuO Ō HCHO + Cu + H2O 32. H+, to CH 2=CH2 + H2O Ō CH3CH2OH Ni, to 13. HCHO + H 2 Ō CH3OH 33. CH PdCl2-CuCl2 2=CH2 + ½ O2 Ō CH3CHO 14. HCHO + 4[Ag(NH t0 3)2]OH Ō (NH4)2CO3 p, xt, to 34. nCH 2=CH2 Ō –(CH2–CH2–)n + 4Ag + 3NH3 + 2H2O 35. CH H2SO4 đ
3COOH + C2H5OH ⇌ HCOOCH3 + H2O 14b.(NH to
4)2CO3 + 2HCl ŌCO2 + NH4Cl + H2O xt, to 36. 3C 2H2 xt, to Ō (C6H6) 15. HCHO + ½ O 2 Ō HCOOH Br 37. + Br Fe, to 2 Ō (C6H5Br) + HBr
(hay: HCHO + Br2 + H2O → HCOOH + 2HBr) ONa 38a. C p, to
6H5Br + NaOHđặc Ō (C6H5ONa) + HBr
16. HCOOH + 2[Ag(NH3)2]OH Ō (NH4)2CO3 OH + 2Ag + 2NH3 + H2O
38. C6H5ONa + CO2 + H2O Ō ō + NaHCO3 H 17. HCOOH + CH 2SO4 đ 38b. (HCO) 3OH ⇌ HCOOCH3 + H2O
2O +C6H5OH Ō HCOO-C6H5 + HCOOH to OH OH as 18. CH Br Br 4 + Cl2 Ō CH3Cl + HCl 39. + 3Br2 Ō + 3HBr 19. CH Cu, OH 4 + ½ O2 Ō CH3OH OH 200o, 100at Br O NO 2N 2 20. CH xt, to H2SO4 đ 4 + O2 Ō HCHO
40. + 3HNO3 Ō ō + 3H2O to 1500o OH OH 21. 2CH NO2 4 Ō C2H2 + 3H2 Pd, to
41. + 3H Ni, to 2 Ō (C6H11OH) 22. C2H2 + H2 Ō C2H4 OH Ni, to O 23. C 2H4 + H2 Ō C2H6 42. + CuO Ō t0 + Cu + H2O 24. C xt, to Br 2H6 Ō C2H4 + H2 O O as 25. C t0 2H6 + Br2 Ō C2H5Br + HBr 43. + Br2 Ō + HBr
Thầy Trần Thiếu lượng 2
Sơ đồ tư duy HÓA HỌC HỮU CƠ 11 & 12-ban KHTN & CƠ BẢN C2H5 62. (C men 6H10O5)n + nH2O Ō nC6H12O6 44. C (H+,to)
6H5Br + C2H5Br + 2Na Ō + NaBr (H%kém) 63. C men 6H12O6 Ō 2C2H5-OH + 2CO2 C rượu 44b. 2H5 C xt, to 6H6 + CH2=CH2 Ō 64. C men 2H5-OH + O2 Ō CH3COOH + H2O CH as CH-CH giấm 44c. 2CH 3 + Br 3 2 Ō + HBr Br
65. CH3CH=O + HCN Ō CH3–CH(OH)CN CH=CH 44d. CH - CH 3+ KOH C2Ō H5 O
H, t0 2 + KBr + H Br 2O 66. CH H+
3–CH–CN + H2O Ō CH3–CH COOH 45. OH OH C 2H5 CH=CH2 H2SO4 xt, to
67. CH3-CH-COOH Ō CH2=CH-COOH + H2O Ō 180o + H 2 OH 46. CH nCH CH=CH2 xt, to 3 2=CH-CH=CH2 + n Ō xt, t0 p
68. (CH3)2CHCH2CH2CH2CH3 Ō + 4H2 (C7H16) (C6H5-CH3) –(CH2CH=CH-CH2-CH-CH2–)n CH3 47. Br CH=CH 2 –(CH–CH2–)n 69-73.
CH 3 + HBr (X) o n Ō xt, t Fe, to CH p 3 + Br2 1:1 48. CH as 2=CH2 + Cl2 Ō CH2Cl–CH2Cl 70. CH 3 + HBr (Y) Br 49. CH to p,t0 Br 2Cl-CH2Cl + 2NaOH Ō
+ 2NaOH đặc Ō CH 3 ONa CH2OH-CH2OH + 2NaCl (
P) + NaBr + H2O CH3 500o CH3 50. CH ONa 2Cl-CH2Cl Ō CH2=CH-Cl + HCl 71. + CO OH
2 + H2O Ō ō + NaHCO3 xt (H) 51. CH≡CH + HCl Ō CH 2=CH-Cl CH3 CH3 52. nCH xt, to OH OH 2=CH-Cl Ō p –(CH2–CH–)n (M)
72. + 2Br2 Ō ō + 2HBr Cl Br trắng 53. CH≡CH + HCN Ō xt CH Br 2=CH-CN CH3 CH3 53a. nCH xt, to 2=CH-CN Ō –(CH2–CH–)n p 74. + 2NaOH đặc Ō t0 + NaBr + H2O CN (Q) 54. CH H+ 2=CH-CN + H2O Ō Br CH ONa 3 CH3 CH2=CH-COOH + NH3
75. + CO2 + H2O Ō ō + NaHCO3 55. nCH xt, to (K)
2=CH-COOH Ō –(CH2–CH–)n p CH OH CH ONa 3 COOH 3 56. CH H2SO4 đ 2=CHCOOH + CH3OH ⇌
76. + 2Br2 Ō ō ( N) + 2HBr to Br Br trắng CH OH OH CH 2=CH-COO-CH3 + H2O 3 CH2Br as 56b. nCH xt, to 77. + Br (A)
2=CH-COO-CH3 Ō –(CH2–CH–)n 2 Ō + HBr p 1:1 o COO-CH 57. 2CH≡CH Ō xt, t CH 3 2=CH-C≡CH CH2Br CH2OH t0 58. CH Pd, to 78. + NaOH (B)
2=CH-C≡CH + H2 Ō CH2=CH-CH=CH2 Ō + NaBr 59. nCH xt, to 2=CH-CH=CH2 Ō CH p 2OH CHO –(CH 2CH=CH-CH2–)n 79. + CuO Ō t0 ( D ) + Cu + H2O 59a. nCH xt, to 2=CH-CH=CH2 + n CH2=CH-CN Ō p CHO COOH
–(CH2CH=CH-CH2-CH2–CH–)n 80. + ½ O xt, to 2 Ō (E) CN 60. CH xt, to
2=CH-C≡CH + HCl Ō CH2=CH-C=CH2
(hay C6H5-CHO + Br2 + H2O → C6H5-COOH + HBr) 61. CH xt, to 2=CH-C=CH2 Ō p –(CH2-CH=C-CH2–)n Cl Cl
Thầy Trần Thiếu lượng 3
Sơ đồ tư duy HÓA HỌC HỮU CƠ 11 & 12-ban KHTN & CƠ BẢN 81. C H2SO4 đ
94. 3CH2=CH2 + 2KMnO4 + 4H2O Ō 6H5-COOH + C6H5-CH2OH ⇌ to 3CH C 2OH-CH2OH + 2MnO2 + 2KOH 6H5-COO-CH2-C6H5 + H2O xt, to Ancol 95. CH 82. C
3-CH2Br + KOH Ō CH2=CH2 + KCl + H2O (A to 3H8 Ō CH3CH=CH2 1) + H2 Ag, to 500o 96. CH 83. CH 2=CH2 + ½ O2 Ō CH2 – CH2
3CH=CH2 +Cl2 Ō ClCH2CH=CH2 + HCl O 98. CH 84. ClCH 3 COOK 2CH=CH2 + Cl2 + H2O Ō
+ 2KMnO4 + H2O Ō + MnO2 + 2KOH ( A 2 ) Cl CH2-CHOH-CH2Cl + HCl to 85. ClCH COOK 2CH=CH2 + NaOH Ō 99. COOH CH + HCl Ō + KCl CH 2OH-CHOH-CH2OH + NaCl 3COO 100. (CH 86. 2C 3CO)2O + C6H5-OH Ō + CH3COOH
3H8O3+ Cu(OH)2 Ō (C3H7O3)2Cu +2H2O H2SO4 đặc H+, to 87. CH=CH CH–CH 2 + H 101. CH2=C 3 –COOH + CH3OH ⇌ 2O Ō t0 OH CH3 88. CH2=C(CH3)-COO-CH3 + H2O CH–CH xt, to COO-CH3 3 C (R) to –CH3 102. nCH2=C-COO-CH3 Ō p OH –(CH2– C –)n + CuO Ō O + Cu + H2O CH 3
Phenyl metyl xeton CH3 89. 103. CH3COOH + CH≡CH Ō CH3COOCH=CH2 C–CH 3 Ni, to + H CH–CH3 104. nCH xt, to 2 O Ō 3COOCH=CH2 Ō p –(CH–CH OH (R) 2–)n CH 90. 3COO –(CH–CH –) to 105. 2 n to,H+ + nNaOH Ō C – CH 3 + Br C–CH Br 2 Ō 2 + HBr CH3COO O (CH (?) –(CH–CH –) 3COOH) nCH O 3COONa + 2 n 91. CN OH C–CH xt, t0 3 + HCN Ō C–CH3 106. + CH 3-CH=CH2 Ō C6H5–CH(CH3 )2 O OH xt, to 1) + O 92. CH 107. C 2
3OH + CO Ō CH3COOH 6H5–CH(CH3 )2 Ō CH3COCH3 + P 2) H2SO4 20% 93. 2CH 2O5, to 3COOH Ō (CH3CO)2O + H2O C6H5-OH
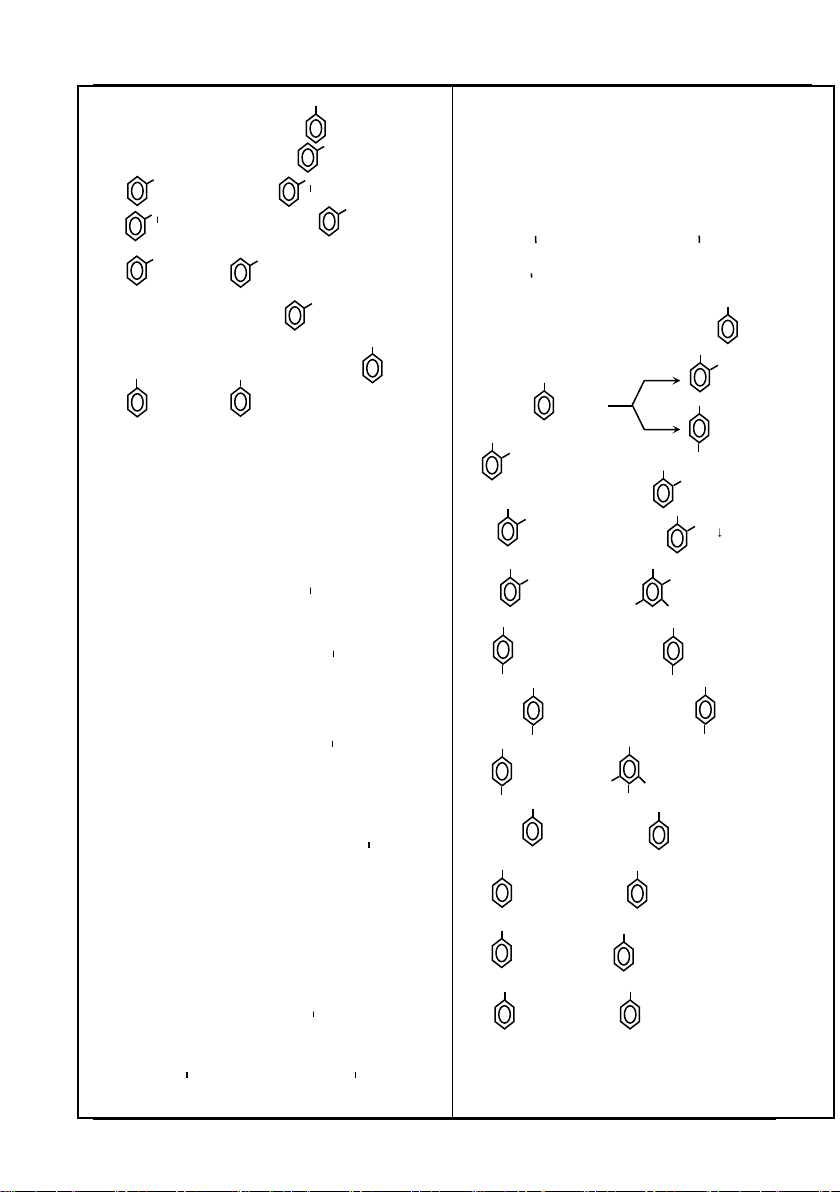
Dựa theo sơ đồ ở trang 1. Bạn có thể
1) Căn cứ vào tên cho sẵn, qua phần minh họa để biết được công thức cấu tạo.
2) Biết chất đầu và chất cuối, bạn tìm sẽ được các chất và các phản ứng trung
gian và viết các phản ứng đó. Đối chiếu với minh họa để kiểm tra phản ứng đúng hay sai.
Biết chất trung gian, bạn cũng có thể xác định chất đầu hoặc chất cuối (nếu
biết loại đồng đẳng của chất đầu hoặc đặc điểm của chất cuối).
3) Tìm số phản ứng trung gian và xem còn có phản ứng nào khác không ?
4) Bạn có thể tự đặt ra câu hỏi và định hướng câu trả lời một cách đa dạng …
Thầy Trần Thiếu lượng 4
Sơ đồ tư duy HÓA HỌC HỮU CƠ 11 & 12-ban KHTN & CƠ BẢN
Để làm ví dụ cụ thể, sau đây là một số câu liên quan trong Bộ Đề thi ĐH
và CĐ của các năm gần và mới đây: (đáp án có gạch dưới và chữ nghiêng)
Câu 1: (CĐ)(Cho sơ đồ chuyển hóa sau (mỗi mũi tên là một phương trình phản
ứng): Tinh bột → X → Y → Z → metyl axetat.
Các chất Y, Z trong sơ đồ trên lần lượt là: A. C2H5OH, CH3COOH. B. CH3COOH, CH3OH. C. CH3COOH, C2H5OH. D. C2H4, CH3COOH.
Hướng : Phản ứng 62-63-64-35 (thay etyl axetat bằng metyl axetat) Câu 2: (2010-K.B)
Cho sơ đồ chuyển hoá sau: + Z C xt, t0 +H2, t0
2H2 Ō ↓ Ō Y Ō Cao su buna-N. Pd, PdCO p, xt, t0 3
Các chất ↓, Y, Z lần lượt là:
A. axetanđehit; ancol etylic; buta-1,3-đien.
B. vinylaxetilen; buta-1,3-đien; stiren.
C. vinylaxetilen; buta-1,3-đien; acrilonitrin.
D. benzen; xiclohexan; amoniac.
Hướng : Phản ứng 57-58-59a và kiểm tra lại bài giải.
Câu 3: (CĐ 2011) Sản phẩm chủ yếu trong hỗn hợp thu được khi cho toluen phản ứng
với brom theo tỉ lệ số mol 1:1 (có mặt bột sắt) là
A. p-bromtoluen và m-bromtoluen. B. o-bromtoluen và m-bromtoluen. C. benzyl bromua.
D. o-bromtoluen và p-bromtoluen.
Hướng : Các em có thể theo dõi trên sơ đồ phản ứng số 69-73 và kiểm tra dựa trên bài giải nhé.
Câu 4: (CĐ 2011) + KCN
Cho sơ đồ chuyển hóa: CH H3O+, t0 3CH2Cl Ō ↓ Ō Y.
Trong sơ đồ trên, ↓ và Y lần lượt là
A. CH3CH2CN và CH3CH2CHO.
B. CH3CH2CN và CH3CH2COOH.
C. CH3CH2NH2 và CH3CH2COOH. D. CH3CH2CN và CH3CH2OH.
Hướng : Các em có thể theo dõi trên sơ đồ phản ứng số 25a và 25b (thay Br bằng
Cl) và kiểm tra dựa trên lại bài giải của sơ đồ.
Câu 5: (ĐH A 2011) Cho sơ đồ phản ứng: CH≡CH Ō + H CN ↓; ↓ Tr ùŌ
ng h ợ p polime Y; X + CH2=CH-CH=CH2 Ō polime Z.
Y và Z lần lượt dùng để chế tạo polime nào sau đây ?
A. Tơ olon và cao su buna-N.
B. Tơ nilon-6,6 và cao su cloropren.
C. Tơ nitron và cao su buna-S.
D. Tơ capron và cao su buna.
Thầy Trần Thiếu lượng 5
Sơ đồ tư duy HÓA HỌC HỮU CƠ 11 & 12-ban KHTN & CƠ BẢN
Hướng : Có thể theo dõi trên sơ đồ phản ứng số 53-53a-59a và kiểm tra lại trên bài giải.
Câu 6: (ĐH A 2011) Cho dãy chuyển hoá sau: Benzen Ō + C2 H4 ↓ Ō + Br2 , a s Y K Ō OH/C2 H5 Z
OH (trong đó ↓, Y, Z là sản phẩm chính). xt, t0 tỷ lệ mol 1:1 t0
Tên gọi của Y, Z lần lượt là
A. benzylbromua và toluen.
B. 2-brom-1-phenylbenzen và stiren.
C. 1-brom-2-phenyletan và stiren.
D. 1-brom-1-phenyletan và stiren.
Hướng : Có thể theo dõi trên sơ đồ phản ứng số 44c-44d và kiểm tra bài giải.
Câu 7: (ĐH B 2011) Cho sơ đồ phản ứng : (1) X + O xt , t0 2 Ō axit cacboxylic Y1 xt , t0 xt , t0
(2) X + H2 Ō ancol Y2 (3) Y1 + Y2 ⇌ Y3 + H2O
Biết Y3 có công thức phân tử C6H10O2. Tên gọi của ↓ là:
A. anđehit acrylic B. anđehit propionic C. anđehit metacrylic D. andehit axetic
Câu 8: (ĐH B 2011) Cho sơ đồ phản ứng: + H CH + HCN 2O 3CHO Ō ↓1 Ō X2 t0 + HCl + Mg C + CO2 2H5Br Ō Y1 Ō Y2 Ō Y3 ete
Các chất hữu cơ ↓1, X2, Y1, Y2, Y3 là các sản phẩm chính. Hai chất X2, Y3 lần lượt là
A. axit 3-hiđrôxipropanoic và ancol propylic.
B. axit axetic và ancol propylic.
C. axit 2-hiđrôxipropanoic và axit propanoic.
D. axit axetic và axit propanoic.
Hướng : Có thể theo dõi trên sơ đồ phản ứng số 65-66 và 25c-25d-25e, kiểm tra lại bài giải.
Câu 9: Cho sơ đồ phản ứng: H CuO +Br Stiren Ō 2O (↓) Ō (Y) Ō (Z 2 ) H+, t0 t0 H+
Trong đó ↓, Y, Z đều là các sản phẩm chính. Công thức của ↓, Y, Z lần lượt là
A.C6H5CH2CH2OH,C6H5CH2CHO, m-BrC6H4CH2COOH
B. C6H5CHOHCH3, C6H5COCH3, C6H5COCH2Br.
C. C6H5CH2CH2OH, C6H5CH2CHO, C6H5CH2COOH.
Thầy Trần Thiếu lượng 6
Sơ đồ tư duy HÓA HỌC HỮU CƠ 11 & 12-ban KHTN & CƠ BẢN
D. C6H5CHOHCH3, C6H5COCH3, m-BrC6H4COCH3.
Hướng : Có thể theo dõi trên sơ đồ phản ứng số 87-88-90 và kiểm tra lại trên bài giải.
Câu 10: (ĐH A 2012) Cho sơ đồ phản ứng : xuctac (a) X + H 2O Y
(b) Y + AgNO3 + NH3 + H2O amoni gluconat + Ag + NH4NO3 xuctac (c) Y E + Z anh sang (d) Z + H 2O X + G chat diepluc ↓, Y, Z lần lượt là:
A. Tinh bột, glucozơ, etanol. B. Tinh bột, glucozơ, cacbon đioxit.
C. Xenlulozơ, saccarozơ, cacbon đioxit. D. ↓enlulozơ, fructozơ, cacbon đioxit.
Hướng : Phản ứng a (số 62)
-c (số 63)- d: 6nCO ↑
2 + 5nH2O → (C6H10O5)n + 6nO2
Câu 11: (ĐH A 2012) Hợp chất ↓ có công thức C8H14O4. Từ ↓ thực hiện các phản ứng (theo đúng tỉ lệ mol):
(a) X + 2NaOH X1 + X2 + H2O (b) X1 + H2SO4 X3 + Na2SO4
(c) nX3 + nX4 nilon-6,6 + 2nH2O (d) 2X2 + X3 X5 + 2H2O
Phân tử khối của ↓5 là
A. 198. B. 202. C. 216. D. 174. Giải :
K = 2 Ō có 2 liên kết , vì tạo H2O và X2 tác dụng lại ↓3 tỉ lệ 2: 1. Chứng tỏ :
↓ có 1 nhóm este, còn lại 1 nhóm –COOH (tạo nước). X3 tạo nilong-6,6 Ō X3 là axit adipic:
a) HOOC-[CH2]4-COO-C2H5 + 2NaOH Ō NaOOC-[CH2]4-COONa + C2H5OH + H2O (X) (X1)
b) NaOOC-[CH2]4-COONa + H2SO4 Ō HOOC-[CH2]4-COOH + Na2SO4 (X1) nat (X3) axit adipic
c) nHOOC-[CH2]4-COOH+ nH2N-[CH2]6-NH2→(‒OC-[CH2]4-CO-NH-[CH2]6-NH‒)n+ 2nH2O (X3) (X4) nilong-6,6 d) 2C - -
2H5OH + nHOOC-[CH2]4-COOH ⇌ C2H5 OOC-[CH2]4 COOC2H5 + 2H2O
2(X2) (X3) axit adipic (X5 ; M = 202)
Câu 12: (ĐH A 2012) Cho sơ đồ chuyển hóa sau: (a) C3H4O2 + NaOH X + Y
(b) X + H2SO4 (loãng) Z + T
(c) Z + dung dịch AgNO3/NH3 (dư) E + Ag + NH4NO3
(d) Y + dung dịch AgNO3/NH3 (dư) F + Ag +NH4NO3
Chất E và chất F theo thứ tự là
A. (NH4)2CO3 và CH3COOH B. HCOONH4 và CH3COONH4
C. (NH4)2CO3 và CH3COONH4 D. HCOONH4 và CH3CHO
Giải : C3H4O2 Ō HCOO-CH=CH2
a) HCOO-CH=CH2 + NaOH Ō HCOONa + CH3CHO (X) (Y)
b) HCOONa + H2SO4 loãng Ō HCOOH + Na2SO4 (X) (Z) (T)
Thầy Trần Thiếu lượng 7
Sơ đồ tư duy HÓA HỌC HỮU CƠ 11 & 12-ban KHTN & CƠ BẢN
c) HCOOH (Z) + 2[Ag(NH3)2]OH Ō (NH4)2CO3 (E) + 2Ag + 2NH3 + H2O
d) CH3CHO (Y) + 2[Ag(NH3)2]OH Ō CH3COONH4 (F) + 2Ag + 2NH3 + H2O KCN H O
Câu 13. (ĐH A 2012) Cho sơ đồ chuyển hóa : CH 3Cl X 3 Y 0 t
Công thức cấu tạo ↓, Y lần lượt là: A. CH3NH2, CH3COOH B. CH3NH2, CH3COONH4
C. CH3CN, CH3COOH D. CH3CN, CH3CHO
Giải : CH3Cl + KCN Ō CH3CN (X) + KCN H O CH 3CN (X) + 2H2O 3 CH 0 3COOH (Y) + NH3 t
Câu 14: (ĐH B 2012) Cho dãy chuyển hóa sau: CaC2 → X → Y → Z.
Tên gọi của ↓ và Z lần lượt là
A. axetilen và ancol etylic.
B. axetilen và etylen glicol. C. etan và etanal
D. etilen và ancol etylic. Giải
CaC2 + H2O Ō C2H2 (axetilen) + Ca(OH)2
C2H2 + H2 (xt Pd/PbCO3) Ō C2H4
C2H4 + H2O (xt HgSO4) → C2H5OH (ancol etylic).
Câu 15: (ĐH B 2012) Cho phương trình hóa học :
2X + 2NaOH Ō 2CH4 + K2CO3 + Na2CO3 Chất ↓ là A. CH2(COOK)2 B. CH2(COONa)2 C. CH3COOK D. CH3COONa Giải
Loại B và D vì sau phản ứng có K nên ↓ phải chứa K
Sau phản ứng có 2K mà trước phản ứng có 2↓ => mỗi ↓ có chứa 1Kali => Chọn C
(nếu để ý 1 chút, bảo toàn C có (2 + 1 + 1): 2 = 2 => X có 2C)
Câu 16: Cho sơ đồ phản ứng: NaOH AgNO / NH NaOH Este X (C
4HnO2) Y 3 3 Z C 0 2H3O2Na. t 0 t 0 t
Công thức cấu tạo của ↓ thỏa mãn sơ đồ đã cho là A. CH2=CHCOOCH3. B. CH3COOCH2CH3. C. HCOOCH2CH2CH3.
D. CH3COOCH=CH2. Giải
Vì C2H3O2Na có công thức cấu tạo là CH3‒COONa Ō Z là CH3COOH Ō Y là CH3CHO
Vậy : C4HnO2 = CH3COOCH=CH2.
Câu 17: Cho các phản ứng sau X + 2NaOH → 2Y + H2O (1) Y + HCl (loãng) Ō Z + NaCl (2)
Biết ↓ là chất hữu cơ có công thức phân tử C6H10O5. Khi cho 0,1 mol Z tác dụng
hết với Na (dư) thì số mol H2 thu được là
A. 0,20 B. 0,15 C. 0,10 D. 0,05 Giải :
K = 2 Ō có 2 liên kết , vì tạo H2O và X tác dụng lại NaOH tỉ lệ 1: 2. Chứng tỏ :
Thầy Trần Thiếu lượng 8
Sơ đồ tư duy HÓA HỌC HỮU CƠ 11 & 12-ban KHTN & CƠ BẢN
↓ có 1 nhóm este, còn lại 1 nhóm –COOH. Mạch cacbon trong gốc axit với ancol
bằng nhau (vì tạo thành 2 chất Y): HO‒CH2‒CH2‒COO‒CH2‒CH2‒COOH (↓)
HO‒CH2‒CH2‒COO‒CH2‒CH2‒COOH + 2NaOH Ō 2HO‒CH2‒CH2‒COONa + H2O (X) 2(Y)
HO‒CH2‒CH2‒COONa + HCl Ō HO‒CH2‒CH2‒COOH + NaCl (Y) (Z)
HO‒CH2‒CH2‒COOH + 2Na Ō NaO‒CH2‒CH2‒COONa + H2 ↑
0,1 mol …………………………………………….> 0,1 mol.
Câu 18: (ĐH B 2013) (tự cập nhật tháng 7/2013)
………………………………………………………………………………………………………
……………………………………………………… Chúc thành công
Thầy Trần Thiếu lượng 9




