




Preview text:
Công nghệ vật liệu cấu trúc nano
Nanostructured materials processing technology
Giảng viên: Hoàng Văn Vương, PhD.
Viện: Khoa học và Kỹ thuật vật liệu Học kỳ: 20212
Hanoi University of Science and Technology www.hust.edu.vn Nội dung HUST – MSE
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi
2.1.4. Phương pháp lắng đọng hơi hóa học (CVD)
2.1.5. Các phương pháp khác: lắng đọng nhiệt phun phủ,
mạ điện, khử sinh học
Hanoi University of Science and Technology www.hust.edu.vn
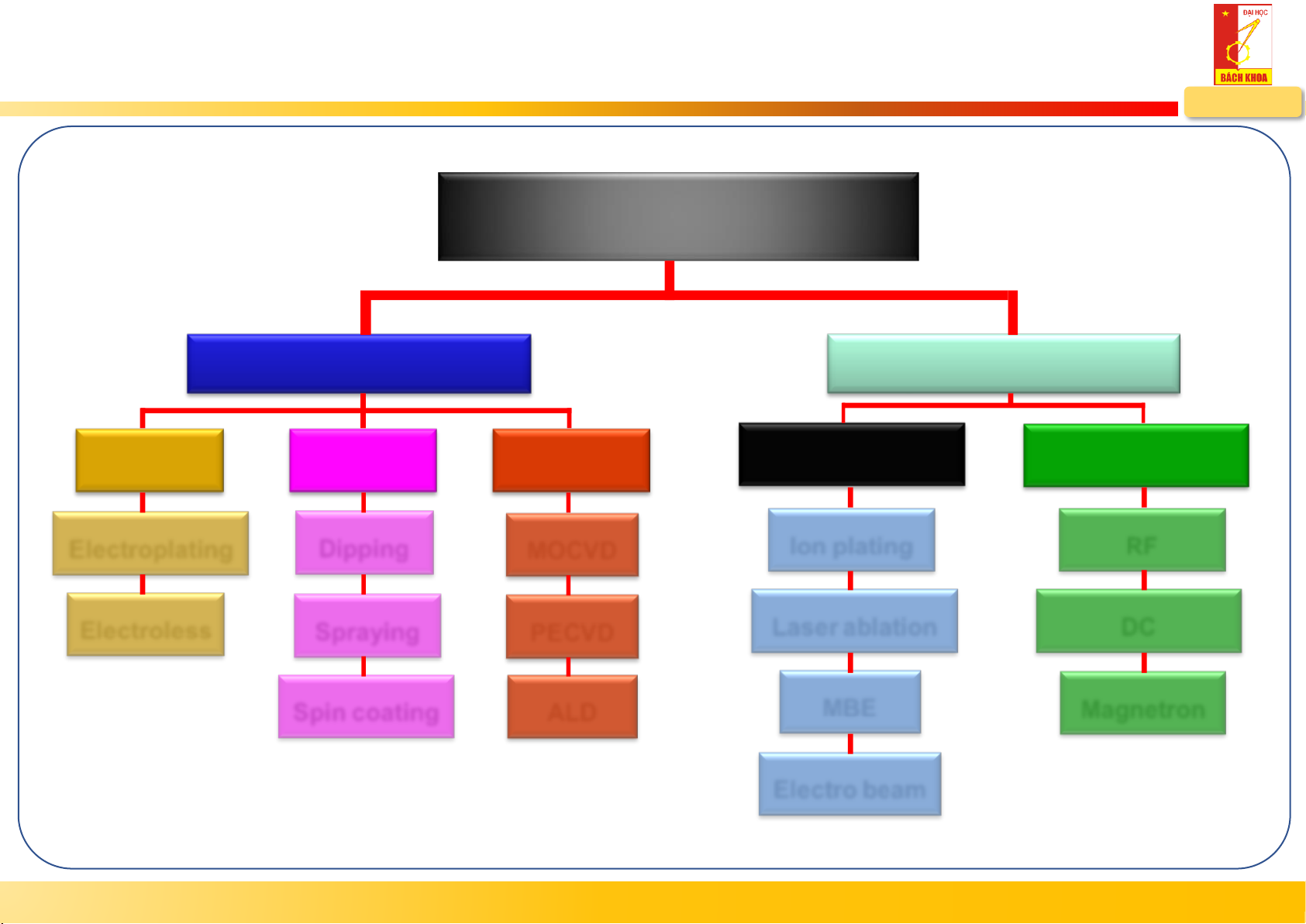
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE Thin Film Deposition Chemical Process Physical Process Plating Sol-Gel CVD Evaporation Sputtering Electroplating Dipping MOCVD Ion plating RF Electroless Spraying PECVD Laser ablation DC Spin coating ALD MBE Magnetron Electro beam
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
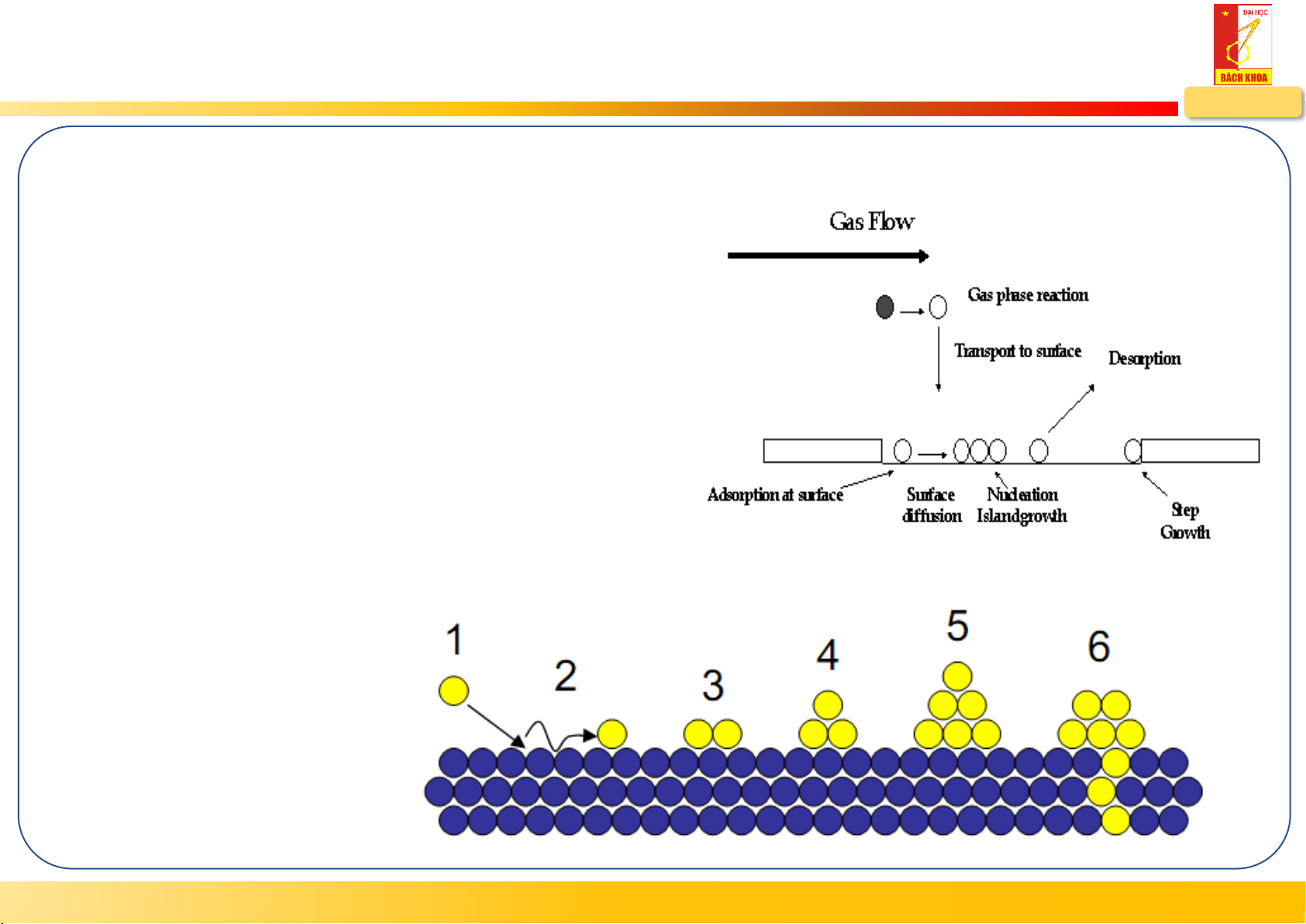
Các giai đoạn hình thành màng mỏng
1. Hấp phụ vật lý (physisorption)
2. Khuếch tán bề mặt (surface diffusion)
3. Hình thành liên kết hóa học (chemical bonding formation)
Hấp phụ hóa học (chemisorption) -
Liên kết phân tử - phân tử - Liên kết đế - phân tử 4. Tạo mầm (Nucleation)
5. Hình thành cấu trúc vi mô (Microstructure formation) - Cấu trúc tinh thể - Khuyết tật 6. Biến đổi thể khối - Khuếch tán - Phát triển hạt
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
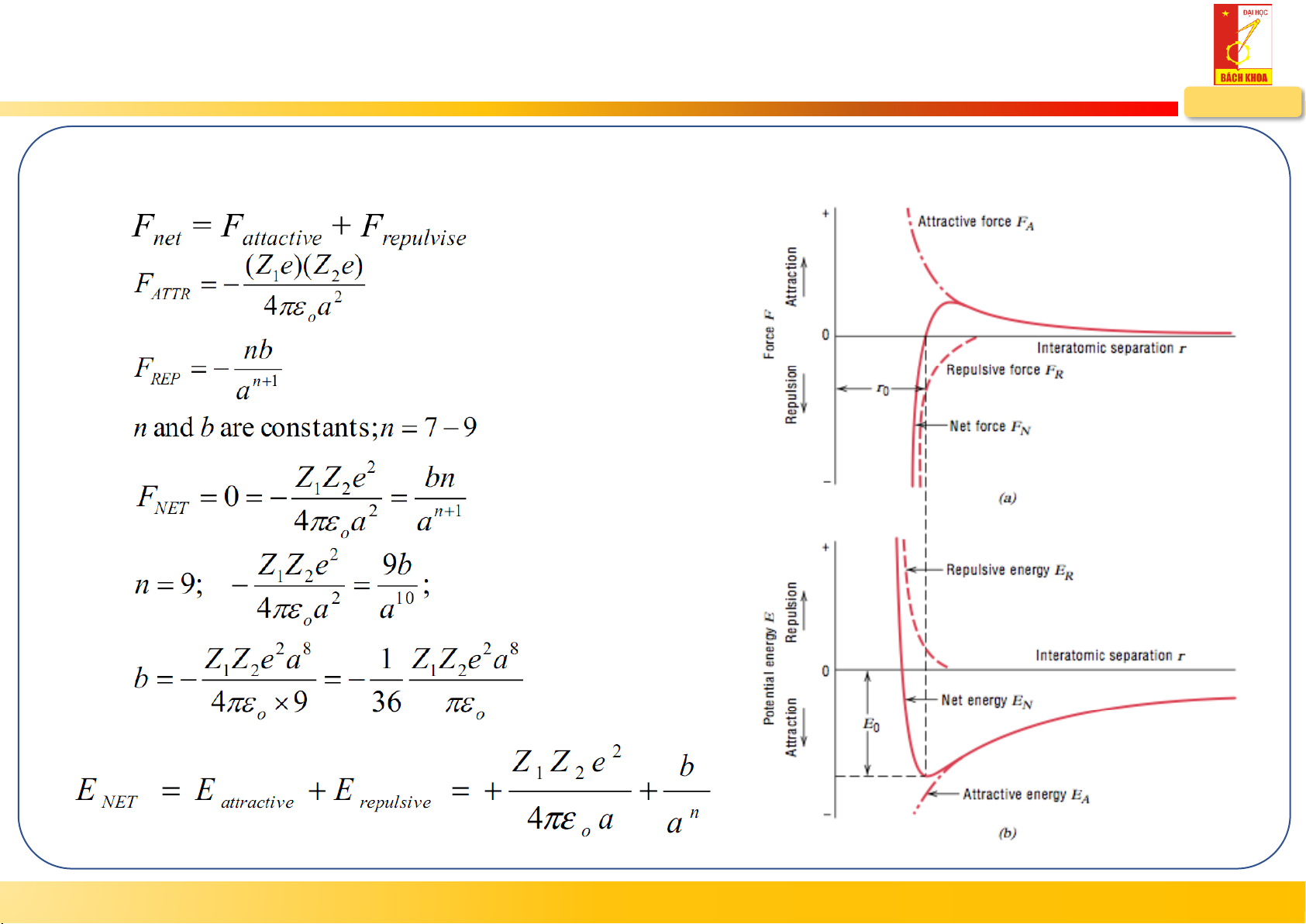
Lực tương tác và nội năng
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
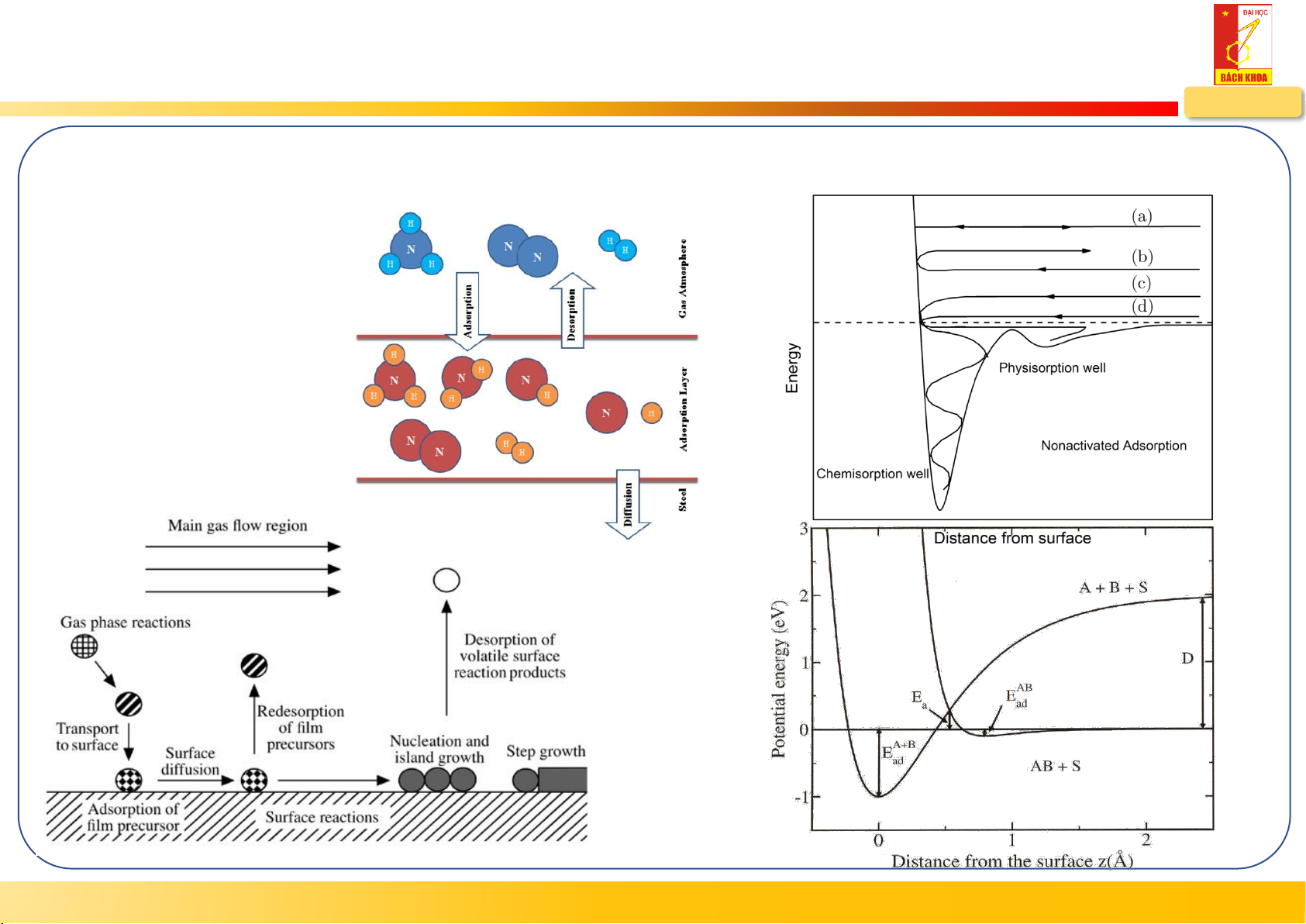
Cơ sở quá trình tương tác (a) Tán xạ đàn hồi
(b) Tán xạ không đàn hồi (c) Hấp phụ hóa học (d) Hấp phụ vật lý Khuếch tán bề mặt Phản ứng bề mặt Thoát khí Ediss
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
Hấp phụ vật lý và hóa học gyrenE Hấp phụ vật lý Hấp phụ hóa học Activation barrier
LIÊN KẾT TẦM XA, YẾU (<0,4 eV)
LIÊN KẾT TẦM GẦN, MẠNH (>0,4eV) E Liên kết Van der Waals
Liên kết hóa học (cộng hóa trị, ion, kim diss z loại) E Physisorption well ads
KHÔNG CÓ TÍNH CHỌN LỌC BỀ MẶT CÓ TÍNH CHỌN LỌC Chemisorption well
Xảy ra giữa các phân tử trên bất kỳ bề mặt
Hấp phụ hóa học chỉ xảy ra ở những nào.
nguyên tố trên bề mặt vật liệu nhất định. - H = 5 ….. 35 kJ mol-1 -H = 35 ….. 500 kJ mol-1 ads ads
Không kích hoạt với trạng thái cân bằng
Có thể được kích hoạt, đạt trạng thái cân
đạt được tương đối nhanh chóng. bằng chậm.
Nhiệt độ hấp phụ thấp Nhiệt độ hấp phụ cao
Không phản ứng bề mặt.
Phản ứng bề mặt có thể diễn ra: - Phân ly, BET Isotherm Model tái cấu trúc, xúc tác. HẤP PHỤ ĐA LỚP HẤP PHỤ ĐƠN LỚP Không tạo pha thứ 2 Tạo pha thứ 2 BET Isotherm Langmuir Isotherm THUẬN NGHỊCH BẤT THUẬN NGHỊCH Langmuir Isotherm Model
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
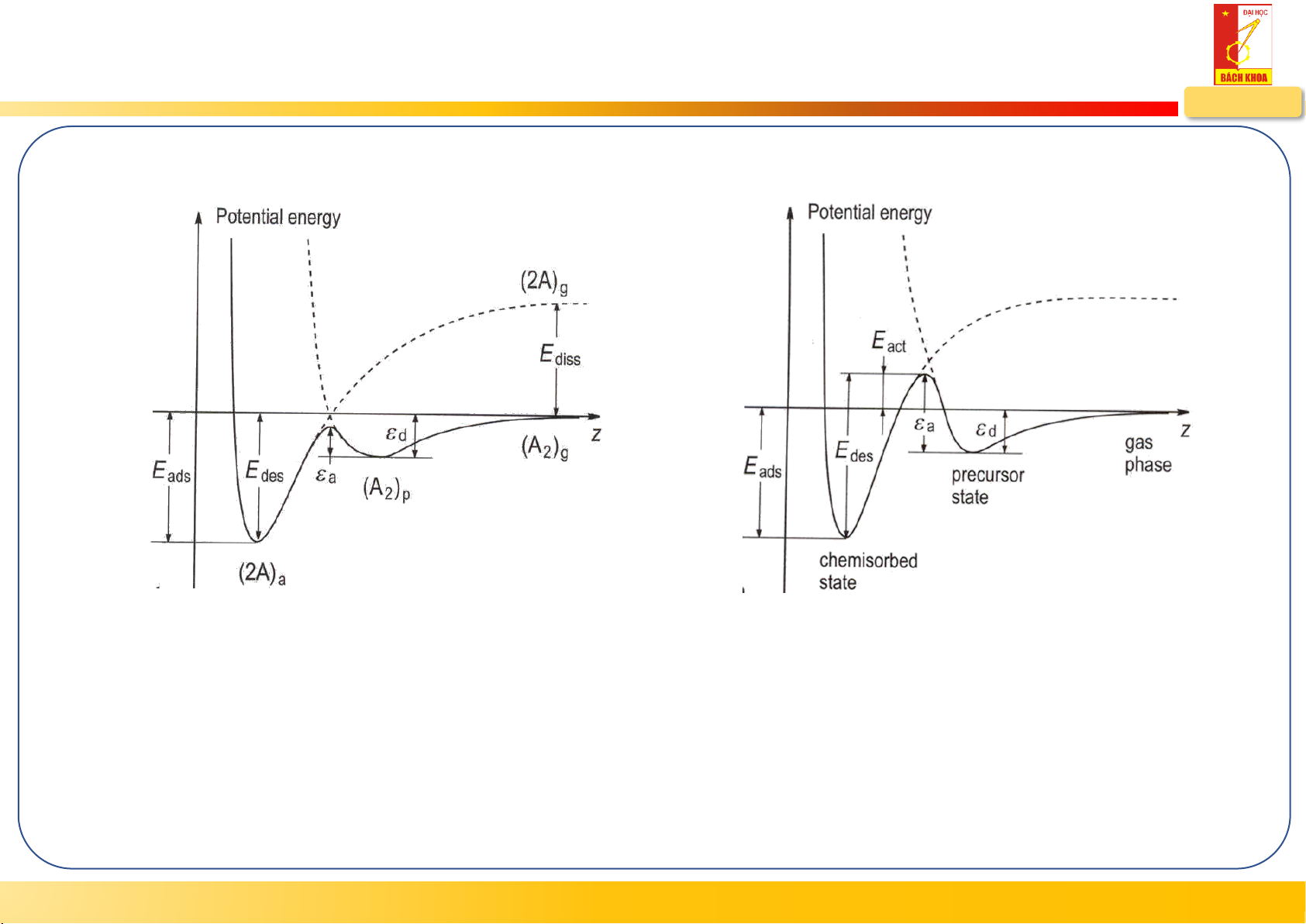
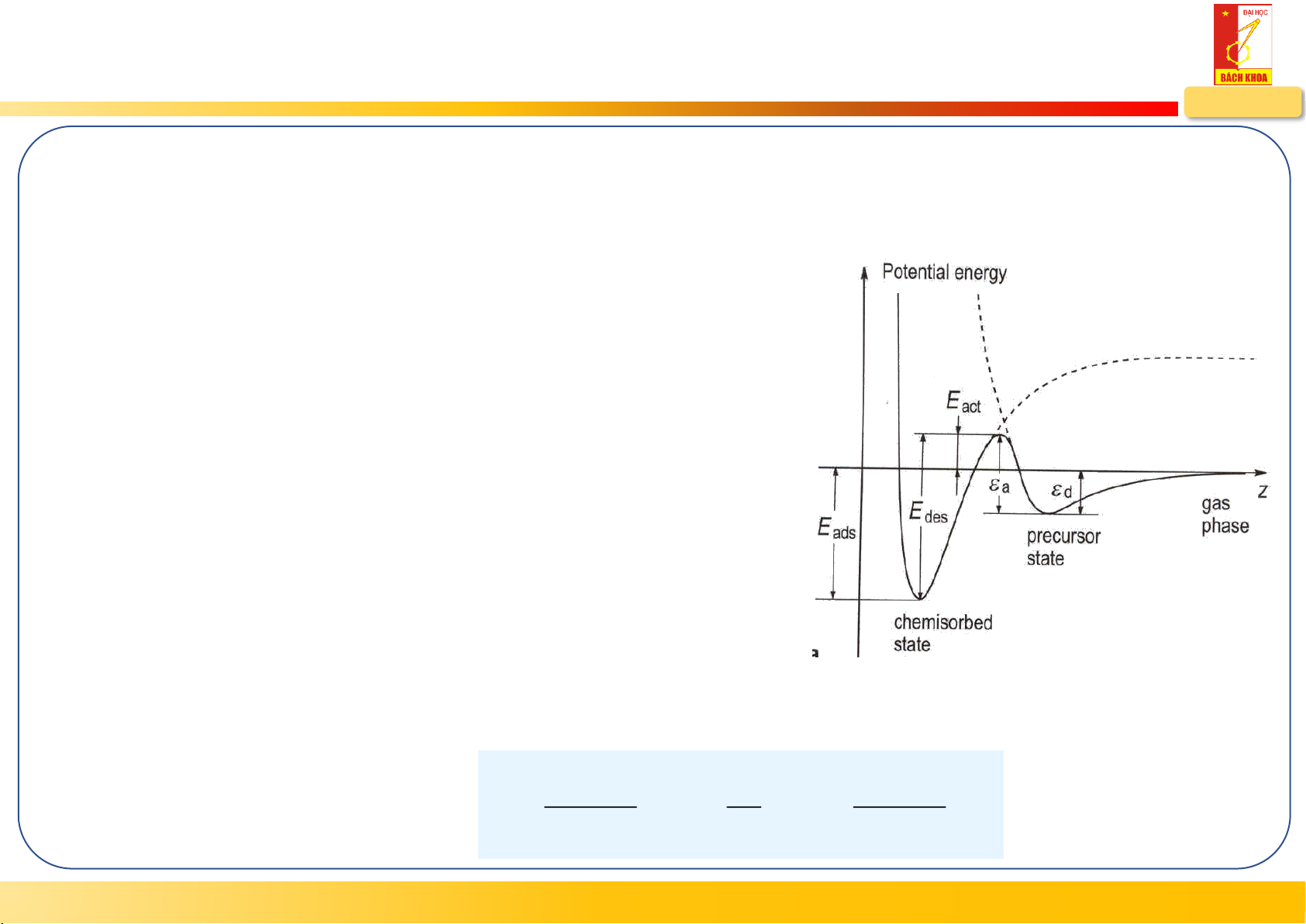
Chuyển trạng thái hấp phụ vật lý và hóa học Z’
Hấp phụ vật lý phân tử và hóa học phân ly
- Tồn tại năng lượng hoạt hóa cho quá trình hấp
giao nhau ở điểm chuyển tiếp Z’ phụ hóa học, Eact
- Tồn tại trạng thái tiền chất với hàng rào năng lượng: = E + a act d
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
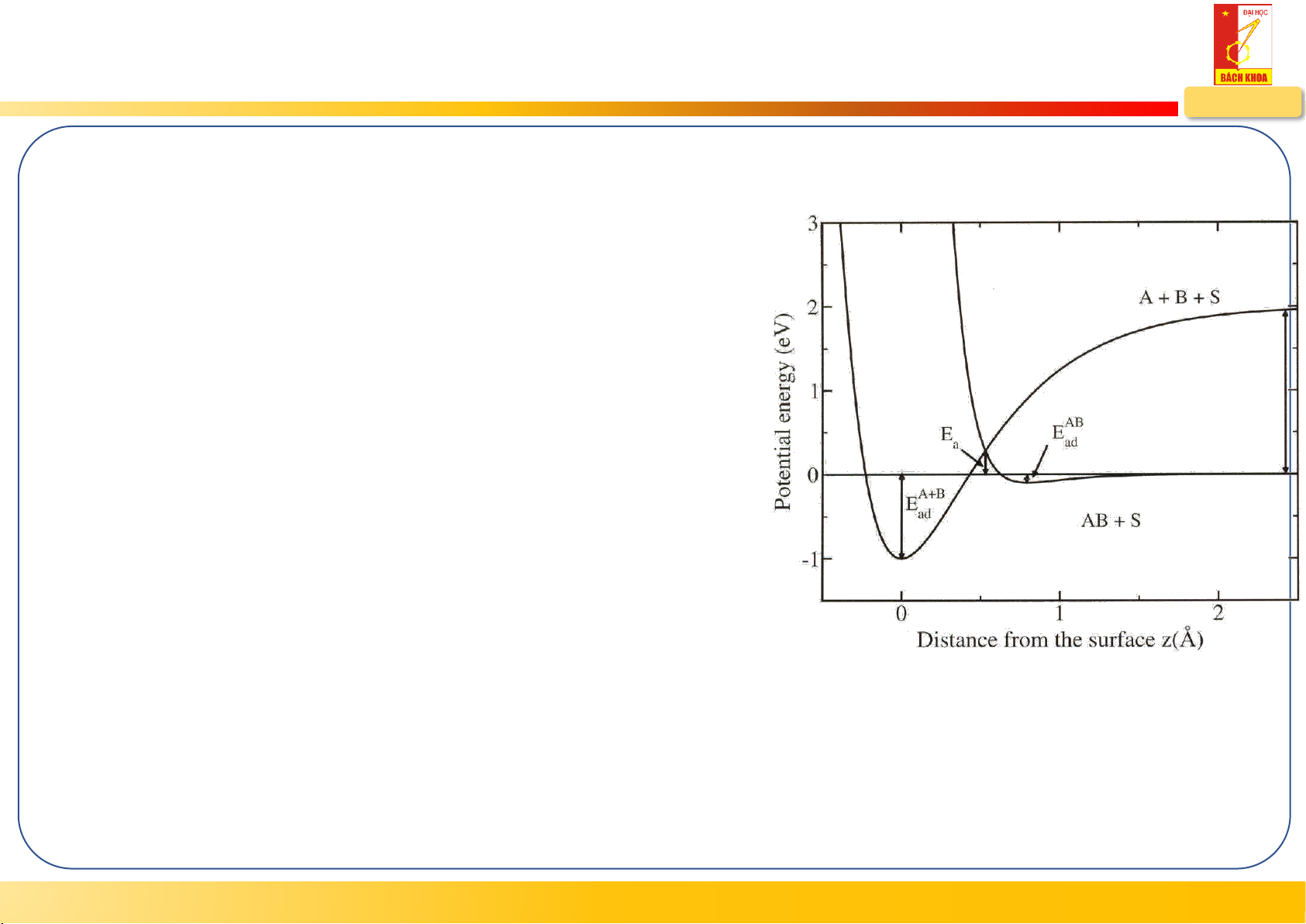
Hấp phụ hóa học phân ly: phân tử phân ly và tạo liên kết hóa học với n
guyên tử bề mặt (e.g., O O + O on Fe) 2
Năng lượng phân ly của phân tử AB: E = E( )
A + E(B) − E( AB) diss E E = 4.5 eV, 5.2 eV and 9.8 eV diss diss for H , O and N 2 2 2
Năng lượng hấp phụ phân ly: ( A+ ) E B
= E(AB) + E(2S) − E (A + S) − E (B + S) ads 0 0
For O on Fe, since O + Fe bond strength is ~ 4.2 eV, the dissociative E is ~ 3.2 eV 2 ads
Hanoi University of Science and Technology www.hust.edu.vn
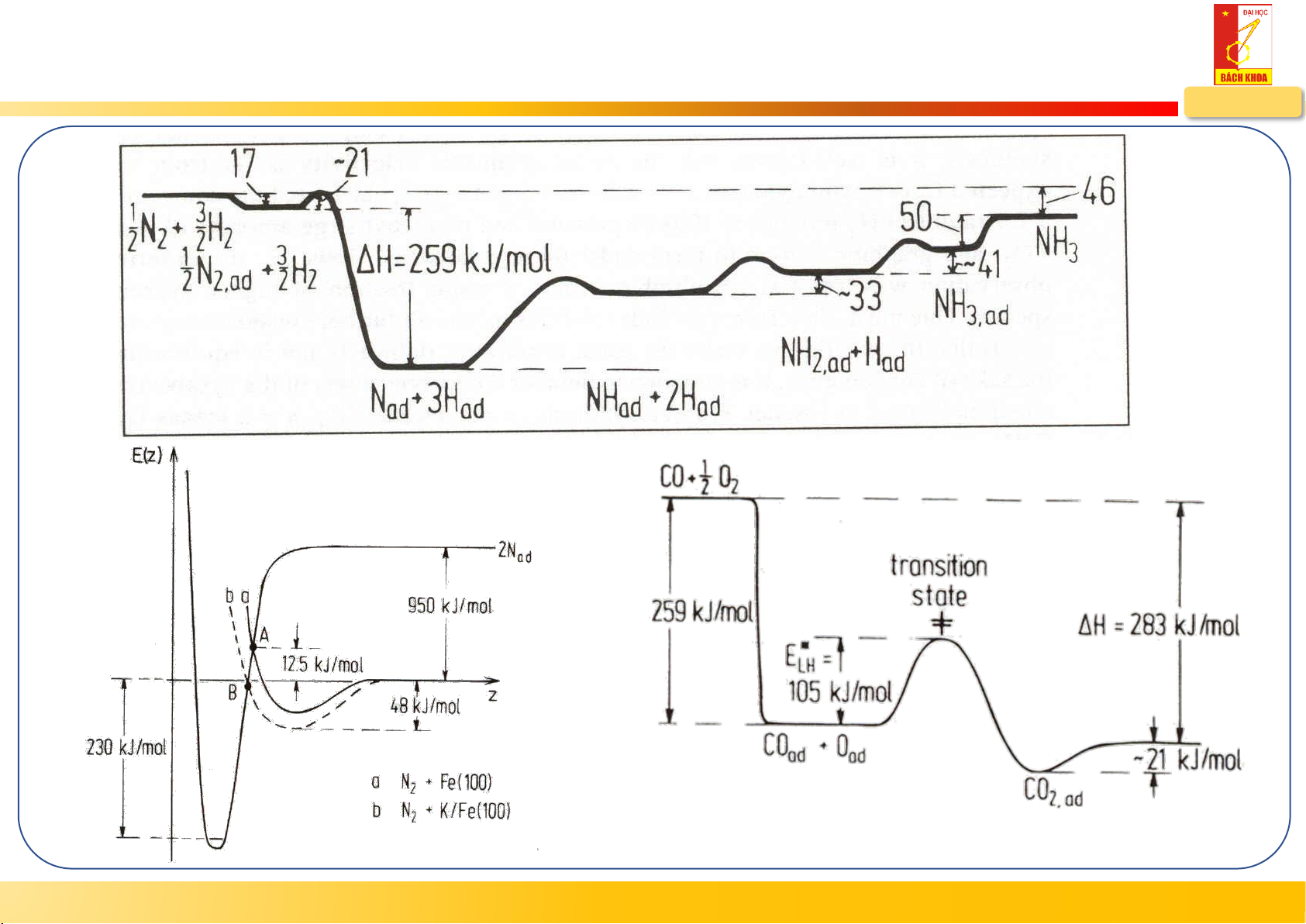
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE Oxy hóa CO: CO + ½O → CO 2 2
Nhiệt lượng: H = 283 kJ/mol r
Hàng rao thế phân ly O : ~ 5 eV 2
Phương pháp Haber-Bosch tổng hợp NH3 ½N + 3/2H → NH 2 2 3
Nhiệt lượng: H = 46 kJ/mol r
Hàng rào thế phân ly N : ~ 9.8 eV! 2
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE CO oxidation on Pt(111
Hanoi University of Science and Technology www.hust.edu.vn
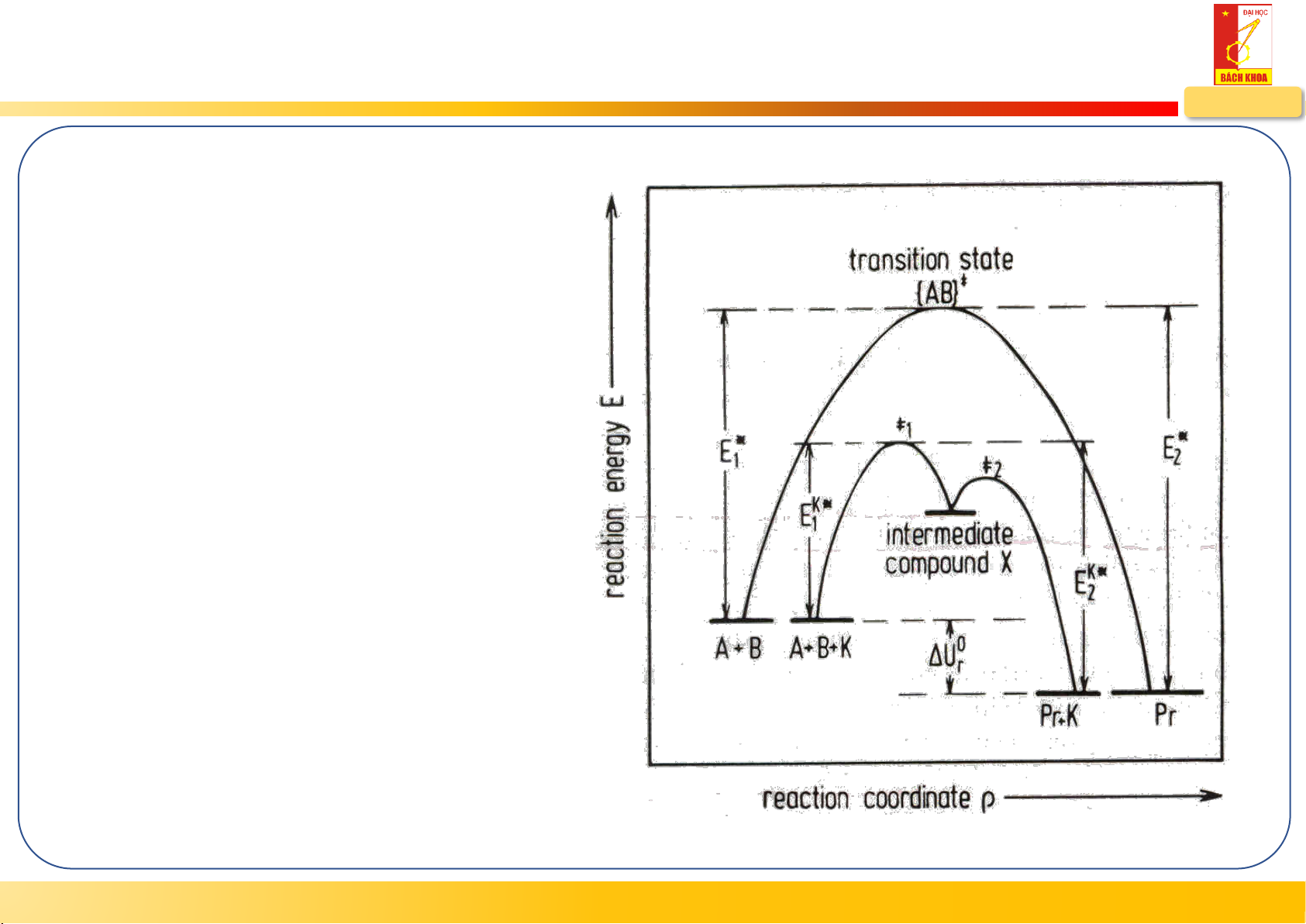
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
Trong hấp phụ hóa học: E
>> kT: hệ số bám dính ban đầu s des 0
1 & độc lập với nhiệt độ T
Trong hấp phụ hóa học phân ly với trạng thái ban đầ
u hấp phụ vật lý với năng lượng liên kết và hàng d
rào năng lượng , hệ số bám dính s phụ thuộc vào a 0 nhiệt độ T
Độ che phủ của phân tử: p
Tốc độ giải hấp phụ: k = exp( − / kT) d p d d
Tốc độ hấp phụ hóa học k = exp( − / kT) a p a a 1 − k a d − d a Hệ số s = = 1+ exp bám dính ban đầu − 0 k + k a d a kT
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
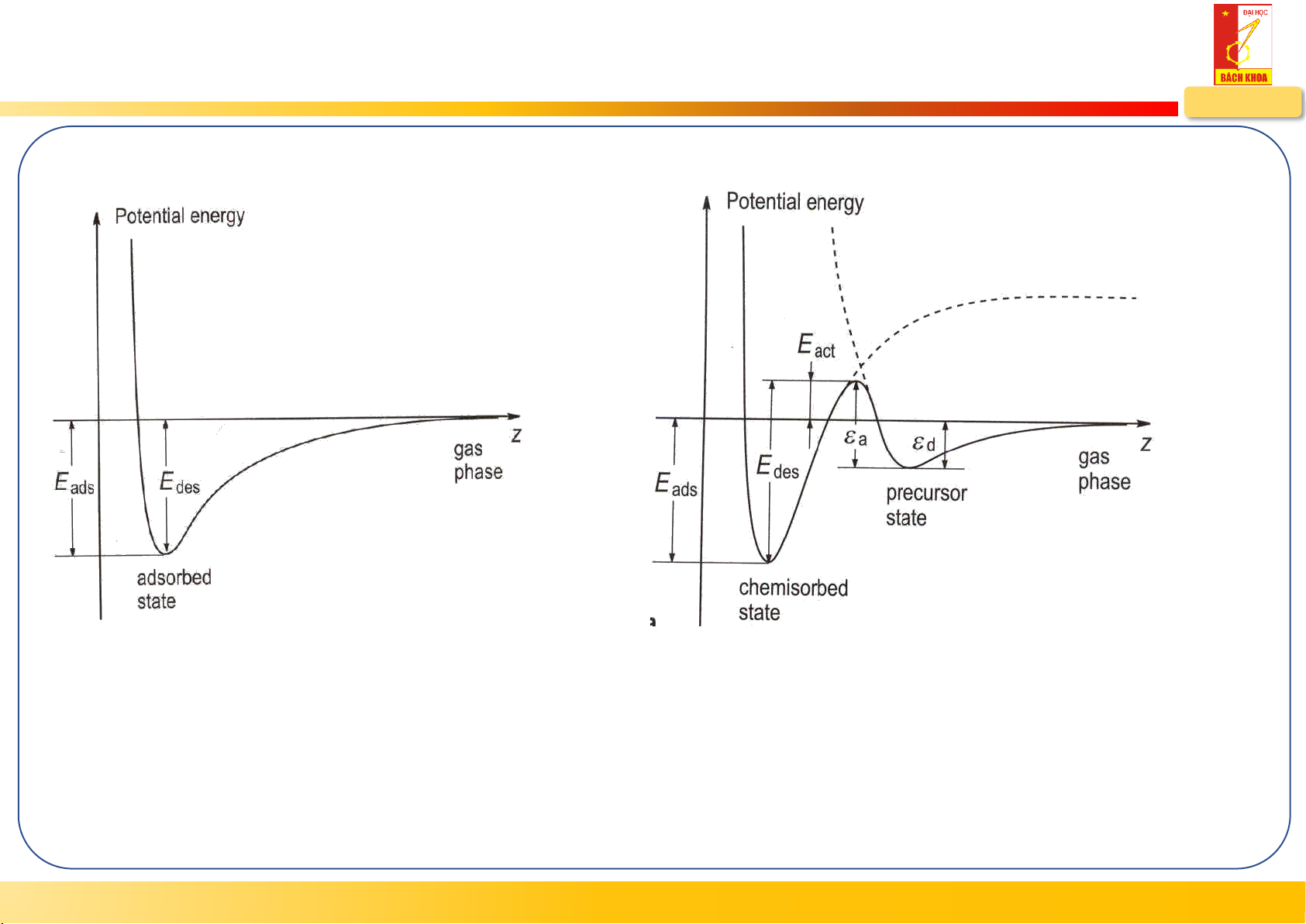
Năng lượng hoạt hóa cho quá trình giải hấp phụ (thoát khí)
Hấp phụ vật lý và hóa học không phân ly:
Năng lượng tái tạo hợp chất của hấp phụ hóa họ E = E c phân ly: des ads E = E + E des ads act
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
Khuếch tán và độ che phủ
• Khuếch tán trạng thái- ổn định.
Khuếch tán trạng thái-không ổn định.
Định luật Fick I và hệ số khuếch tán
Nếu nông độ C không những là hàm của x mà còn
Định luật này nêu lên quan hệ giữa dòng
phụ thuộc vào thời gian t thì để thuận tiện người ta
nguyên tử khuếch tán J qua một đơn vị bề
sử dụng định luật FickII
mặt vuông góc với phương khuếch tán và
Định luật FickII trong trường hợp hệ số khuếch tán Gradient nồng độ
không phụ thuộc nồng độ như sau: J = -DdC/dx
∂C/∂t = ∂/∂x(D∂C/∂x) Trong đó:
Nghiệm của phương trình trên trong trường hợp kh
- Dấu trừ chỉ dòng khuếch tán theo chiều
uếch tán một chất có nồng độ Cs trên bề mặt vào b giảm nông độ
ên trong mẫu với nồng độ ban đầu Co ( Cs>Co).
- D hệ số khuếch tán ( cm2/s)
(Cx-Co)/(Cs-Co) = 1-erf {x/2Dt}
Trong một số trường hợp:
Trong đó erf{…} là hàm sai của đại lượng được tí D = D .exp(-Q/RT) 0
nh sẵn trong sổ tay toán học D : hằng số (cm^2/s) 0 Q: hoạt năng khuếch tán
T: nhiệt độ khuếch tán (K)
R: hằng số khí (R = 1,98cal/mol)
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
Khuếch tán và độ che phủ
• Độ che phủ, , được xác định bởi tỉ số giữa số phân tử bị h
ấp phụ tạo thành đơn lớp và số phân tử tiếp cận trên đơn v
ị diện tích bề mặt, là hàm của thời gian.
• Với P là áp suất riêng phần của các nguyên tử ở pha hơi và k và k
là tốc độ hấp phụ và giải hấp phụ: ads des KP = k 1− exp − k 1 ( + KP t ) ads K = des 1+ KP kdes
• Nếu KP >> 1, ở khoảng thời gian đủ dài: KP = 1+ KP
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
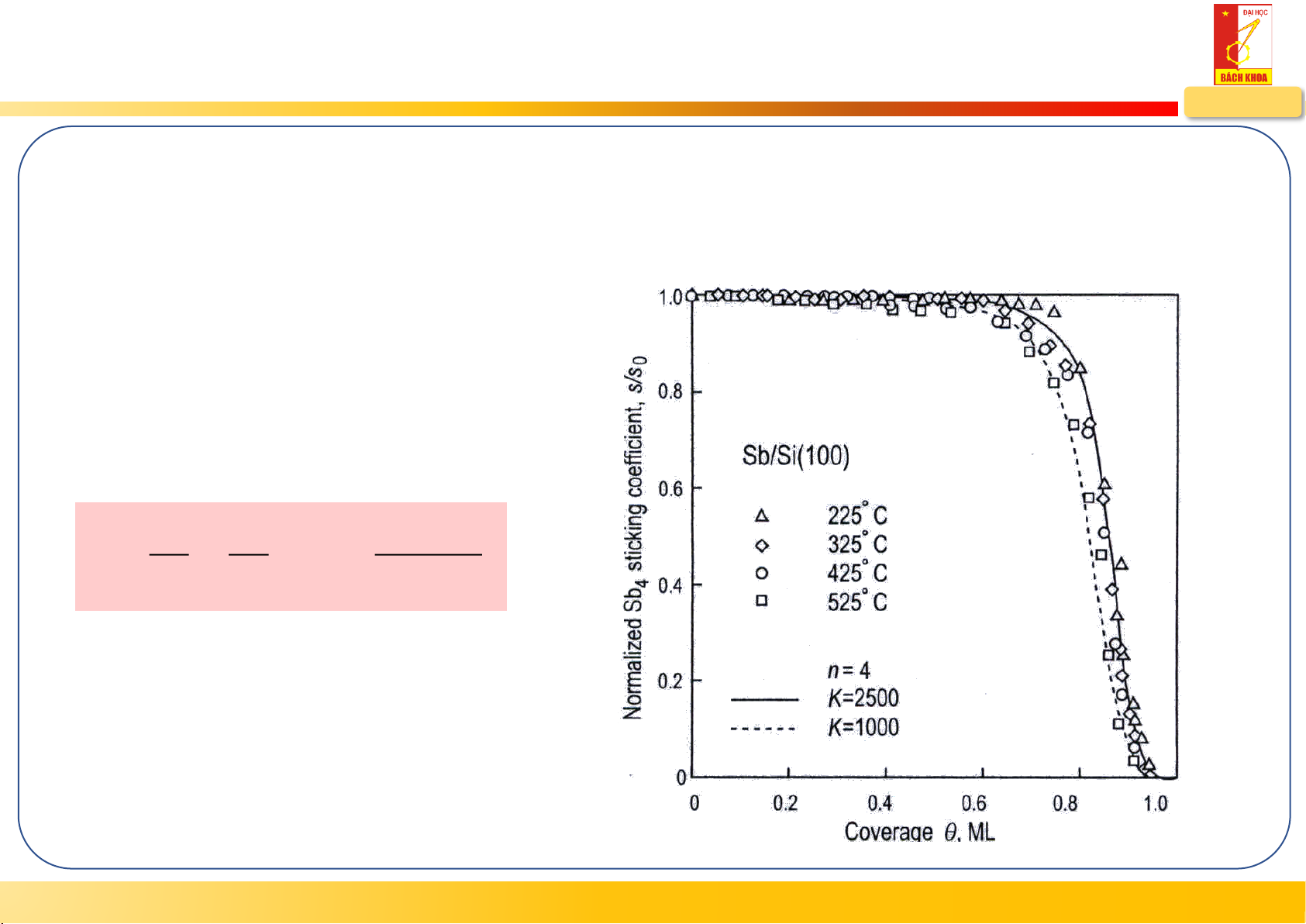
Khuếch tán và độ che phủ
Hấp phụ hóa học Sb trên bề mặt Si 4
K phụ thuộc vào nhiệt độ T k a a − a d K = = exp − k d d kT
Ở nhiệt độ cao, K giảm thì ε > ε , a d
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
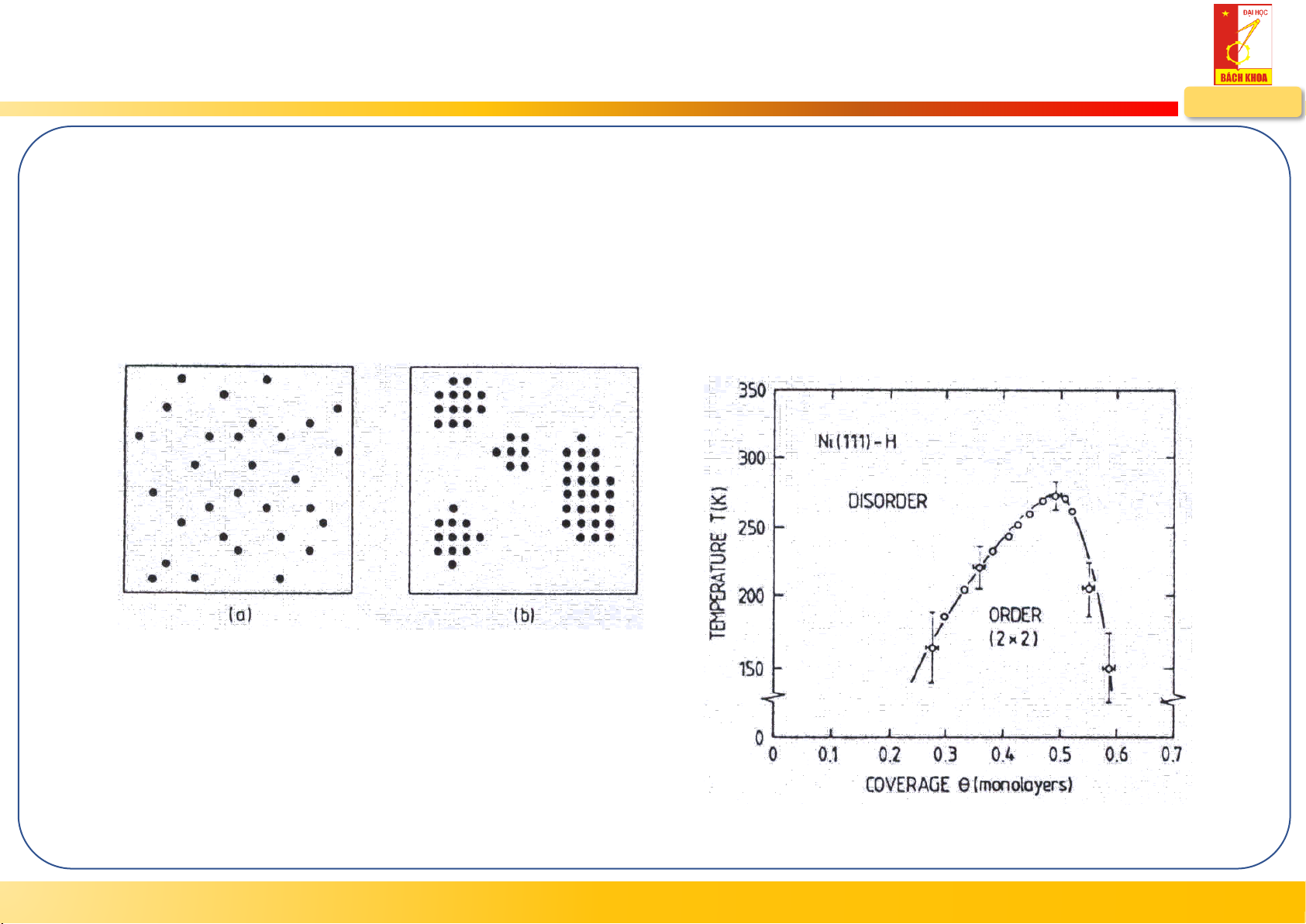
Sự sắp xếp chất hấp phụ trên bề mặt
Phụ thuộc độ che phủ , tương tác giữa chất hấp phụ với phụ, chất hấp phụ và bề mặt, and T
, xác định theo số đơn lớp ML (monolayer), can be measured using XPS, AES or EELS
Low & high T, 2-D gas phase
High & low T, 2-D order phase
High & high T, 2-D liquid phase
Giản đồ pha và sự chuyển tiếp
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
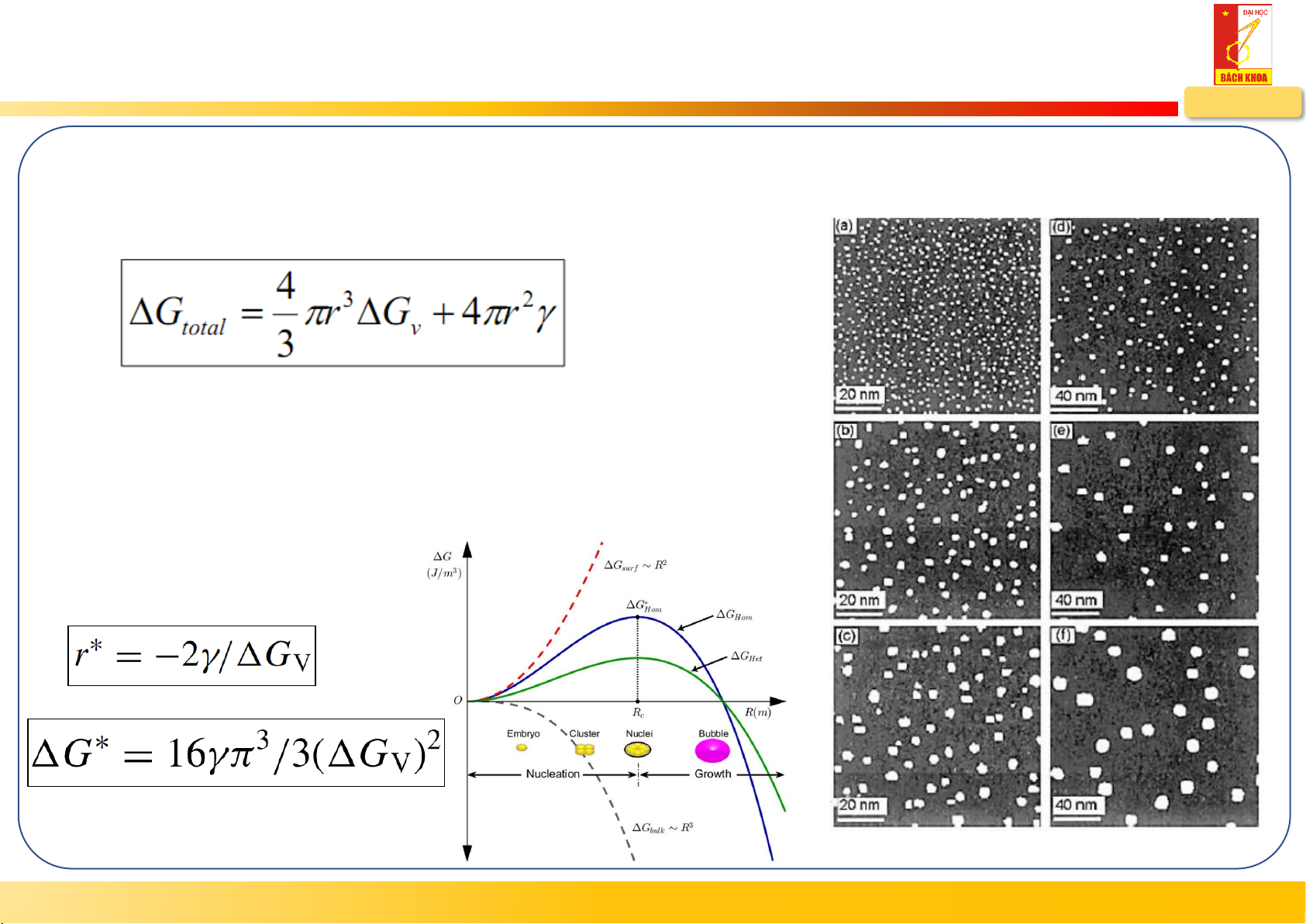
Tạo mầm và phát triển mầm (Nucleation and growth)
• Mầm đồng thể (Homogeneous nucleation) G
- Sự thay đổi tổng năng lượng tự do total r - Bán kính mầm G
- Năng lượng tự do thể tích
- Năng lượng tự do bề mặt riêng • d(G)/dr = 0
F. Stavale, L. Gomes – DIMAT/INMETRO (2009)
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
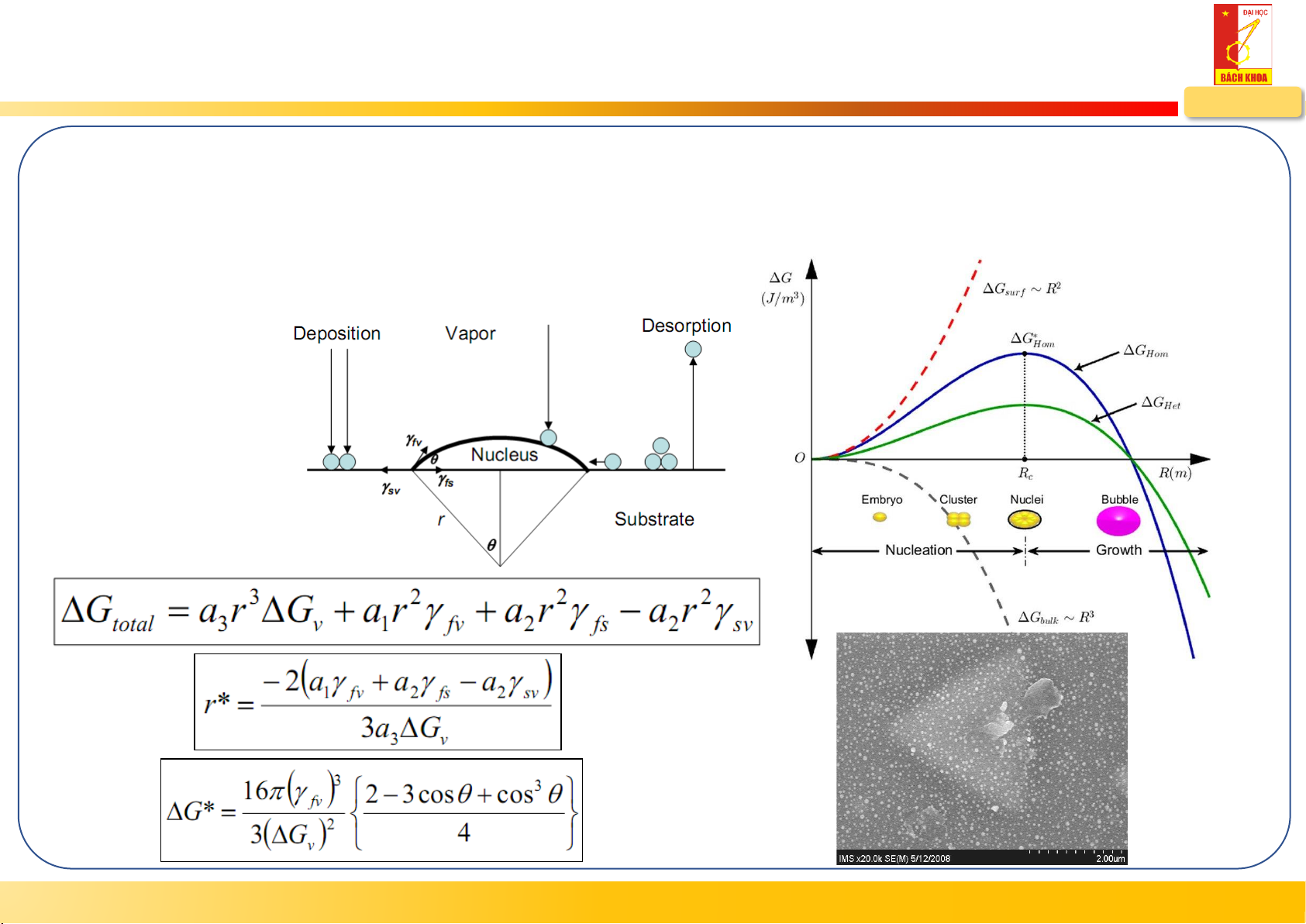
Tạo mầm và phát triển mầm (Nucleation and growth)
• Mầm dị thể (Heterogeneous nucleation) phụ thuộc vào năng lượng bề mặt tươ
ng đối giữa các mawtn ranh giới pha: - Đế – hơi - Màng – đế - Màng – hơi
Hanoi University of Science and Technology www.hust.edu.vn
2.1.3. Cơ sở lý thuyết phương pháp lắng đọng pha hơi HUST – MSE
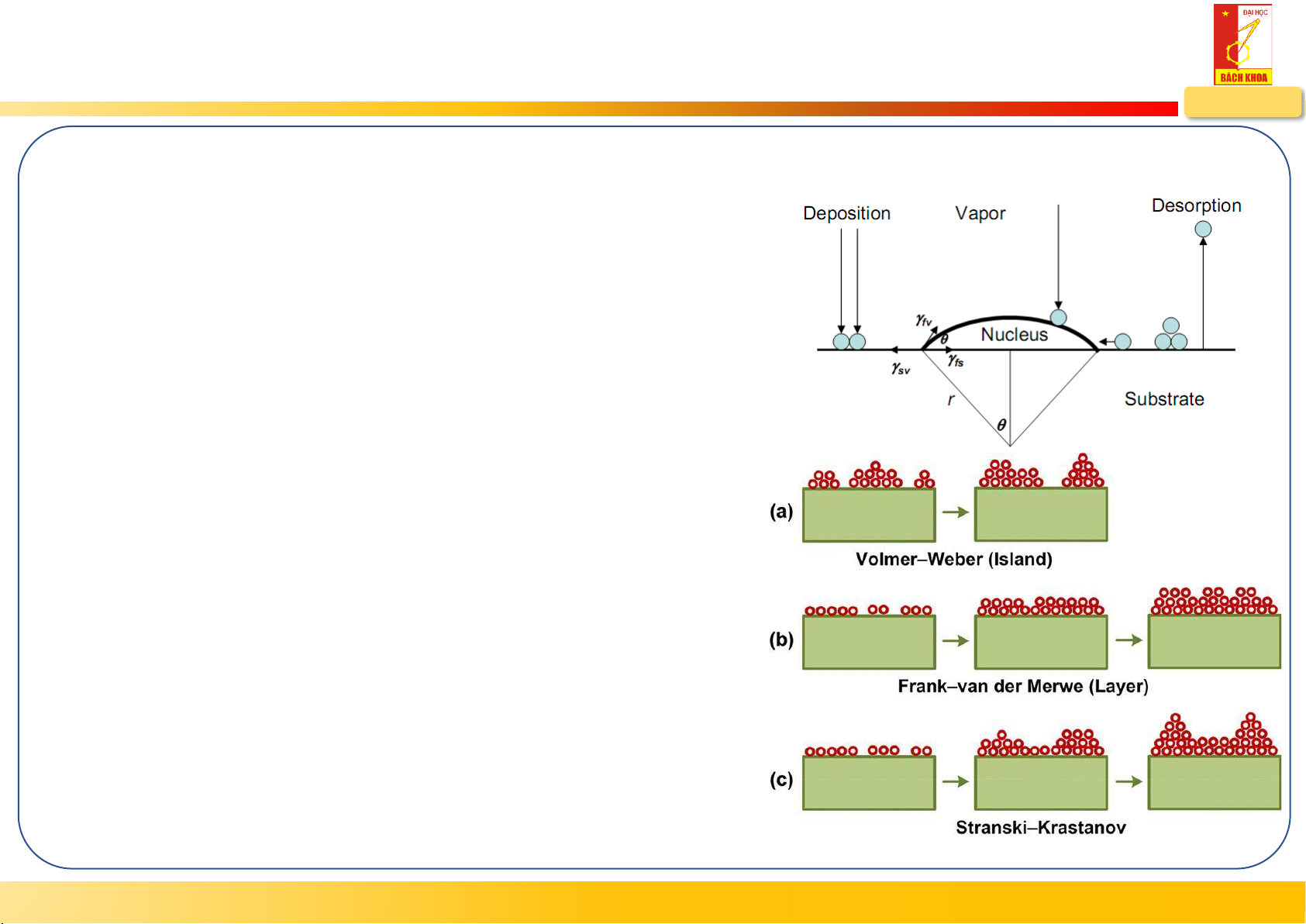
3 mô hình phát triển mầm
• Mô hình Volmer – Weber (Island growth – 3D)
- Island growth (low diffusion): < + sv fv fs
• Mô hình Frank – van der Merwe (Layer – 2D)
- Layer growth (fast diffusion): + sv fv fs
• Mô hình Stranki – Krastanov (Mixed growth)
- Mixed growth: > + sv fv fs
- Ban đầu hình thành mang 2D, sau đó hình thành 3D
Hanoi University of Science and Technology www.hust.edu.vn



