



Preview text:
Chương 5 Hydrocacbon no
5.1. Phân loại, nguồn gốc
Khái niệm: RH no là hợp chất hữu cơ trong phân tử chỉ chứa liên kết đơn ()
Phân loại: RH no mạch hở (ankan): C H (n1) n 2n+2
RH no mạch vòng (cycloankan) C H (n3) n 2n
Nguồn gốc:
Từ dầu mỏ: Ankan, RH thơm,… Khí thiên nhiên: C C 1 4 Khí bùn ao: CH4
Hợp chất thiên nhiên: terpen, steroid,…. 5.2. Danh pháp
5.2.1. Danh pháp của ankan (alkane)
Tên thường: - Mạch thẳng: thêm tiếp đầu ngữ n (normal)
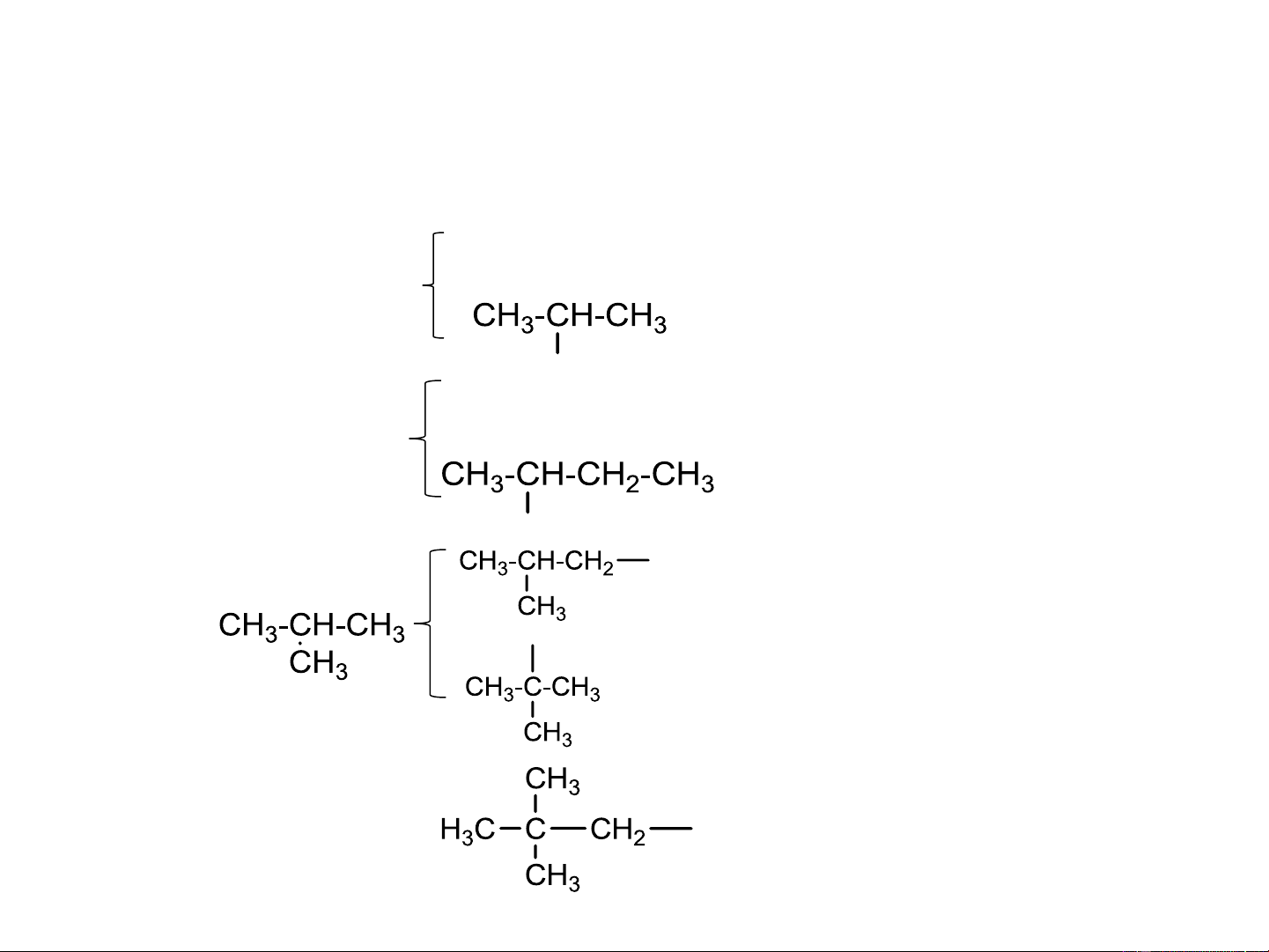
- Mạch nhánh (C2): thêm tiếp đầu ngữ iso Tên IUPAC:
- Mạch thẳng (bảng tên gọi)
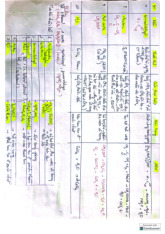
-Đối với mạch phức tạp:
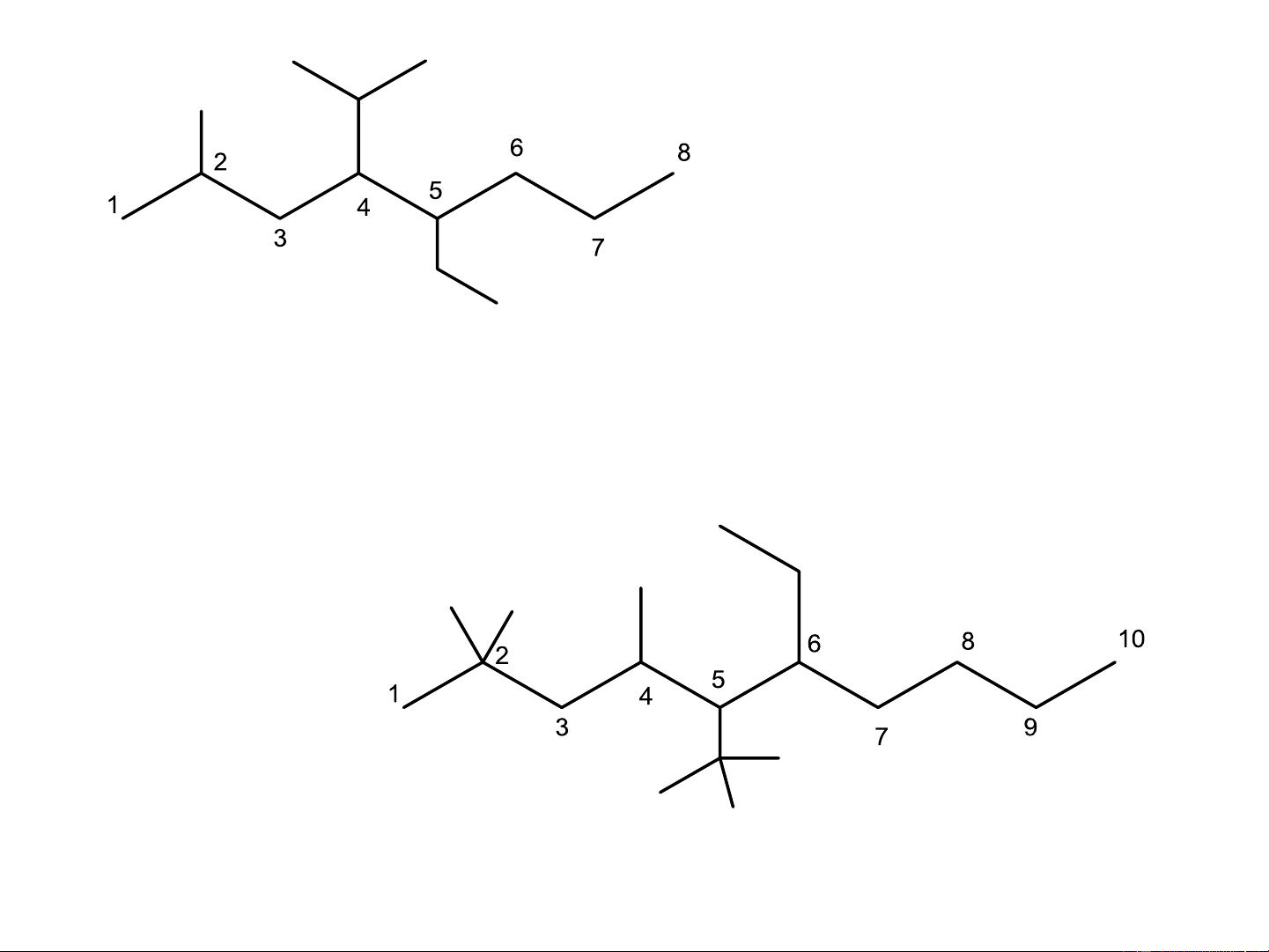
+ Chọn mạch C dài nhất làm mạch chính
+ Đánh số sao cho tổng số thứ tự nhóm thế là nhỏ nhất
Gọi tên: số tt nhóm thế + tên nhóm thế (gốc) + tên mạch chính Methane CH -CH Methyl (-Me) 4 3 Ethane C H -C H Ethyl (-Et) 2 6 2 5 Propane C H -C H Propyl (-Pr) 3 8 3 7 Iso propyl (i-Pr-) Butane C H -C H Butyl (-But) 4 10 4 9 Sec-butyl (1-methyl-propyl) Iso-butyl (2-methyl propyl)
Tert-butyl (1,1-dimethyl ethyl) Pentane C H 5 10
Neopentyl (2,2-dimetyl-propyl)
5.2.2. Danh pháp của cycloankan (cylcloalkanes)
1. Các hợp chất 1 vòng (monocyclic compounds)
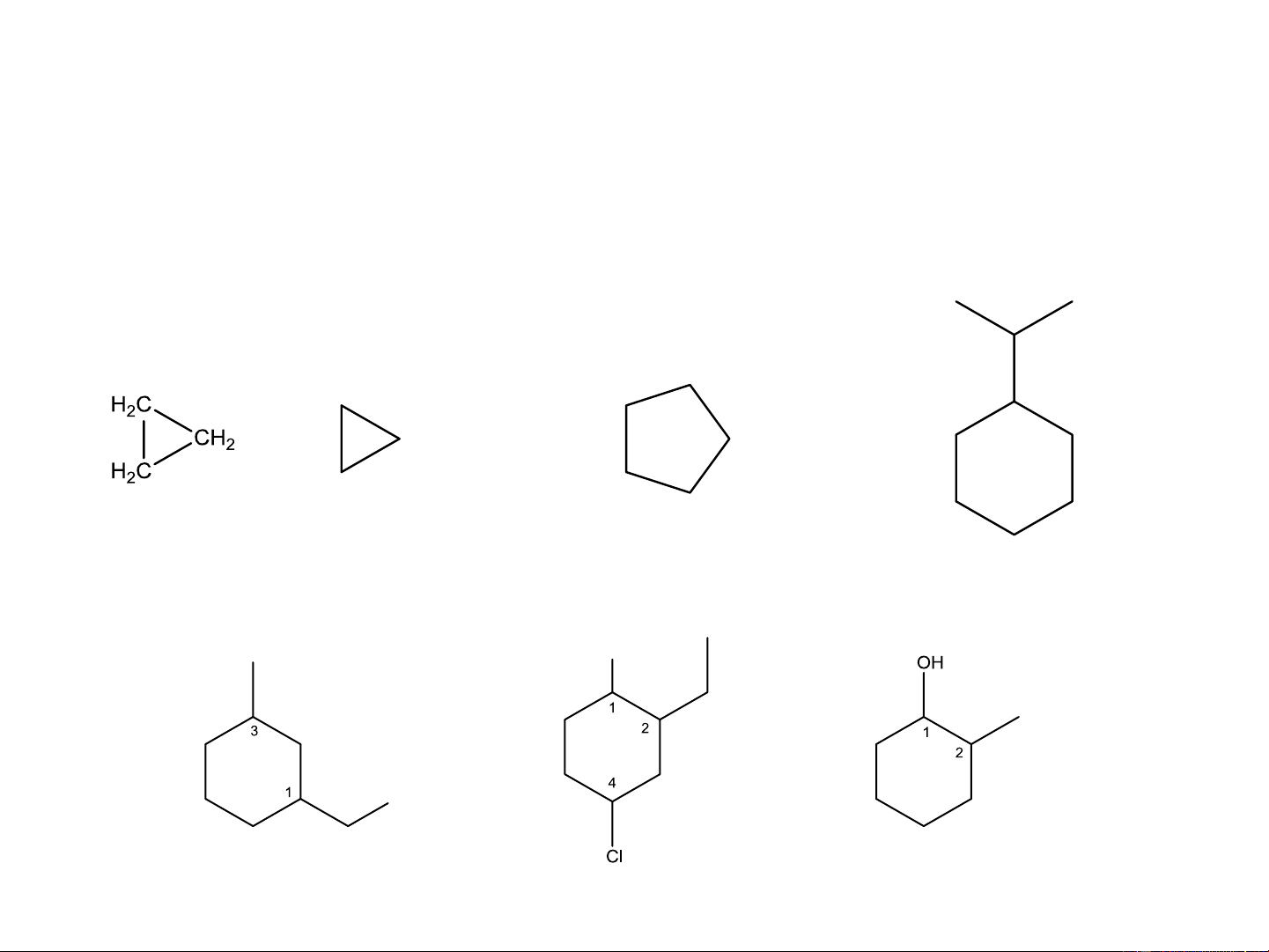
Tên nhóm thế + tên vòng (đánh số sao cho stt nhóm thế là nhỏ nhất) cyclopropan cyclopentan isopropylcyclohexan
2. Các hợp chất có 2 vòng trở lên
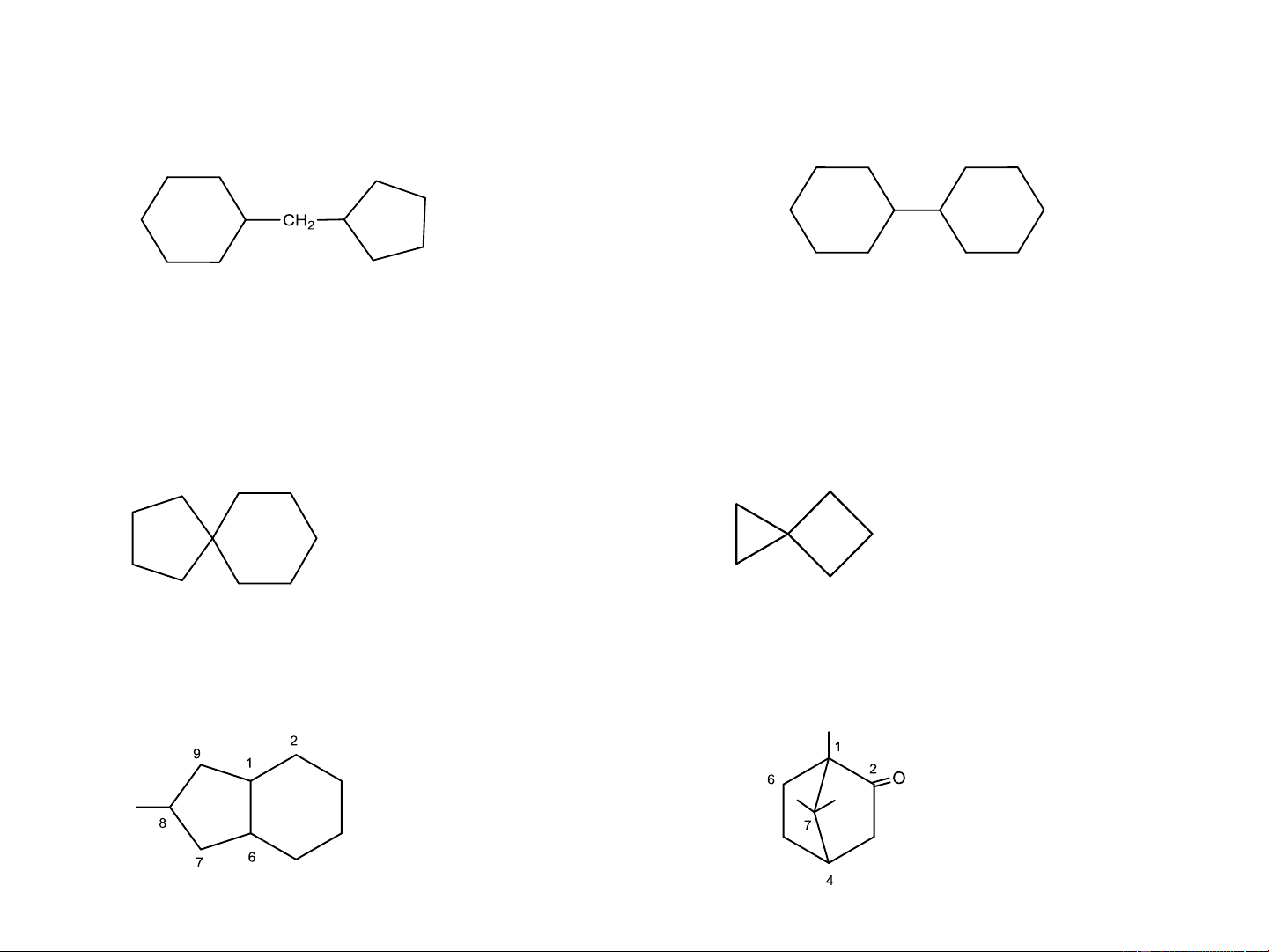
a. Hai vòng không có nguyên tử cacbon chung: gọi theo tên gốc Cyclopentyl cyclohexyl methan
b. Hai vòng có 1 nguyên tử cacbon chung:
Spiro [n,m]+ tên RH tương ứng (n,m: số mắt xích) Spiro [4,5] decan
c. Vòng có 2 nguyên tử cacbon chung:
Bicyclo [n,m,r]+ tên RH tương ứng (n,m,r: số mắt xích) Camphor 8-methylbicyclo [4,3,0] nonan
5.3. Cấu trúc của hydrocacbon no
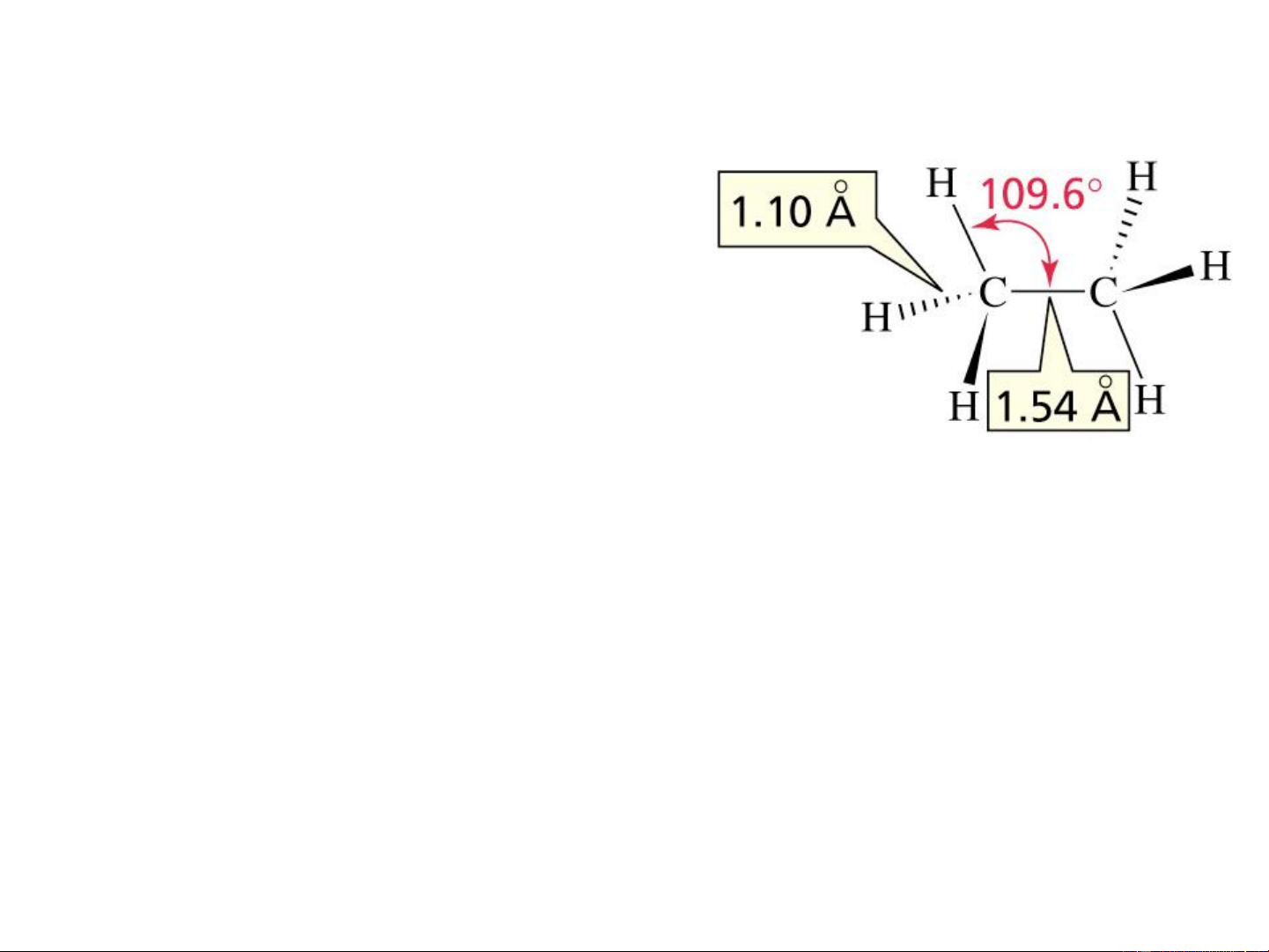
5.3.1. Cấu trúc của ankan C-sp3
Liên kết không phân cực hoặc rất ít phân cực
Phản ứng ở các liên kết C-C: Phản ứng cắt mạch C-H: Phản ứng thế
Phân cắt liên kết đồng ly cơ chế gốc tự do (S ) R
Nhiều trung tâm phản ứng, sản phẩm thường là hỗn hợp chất
5.3.2. Hóa lập thể của hợp chất vòng (Cycloalkane)
a. Vòng 3, 4 cạnh (cyclopropan, cyclobutan)
C sp3, góc liên kết 109,5o
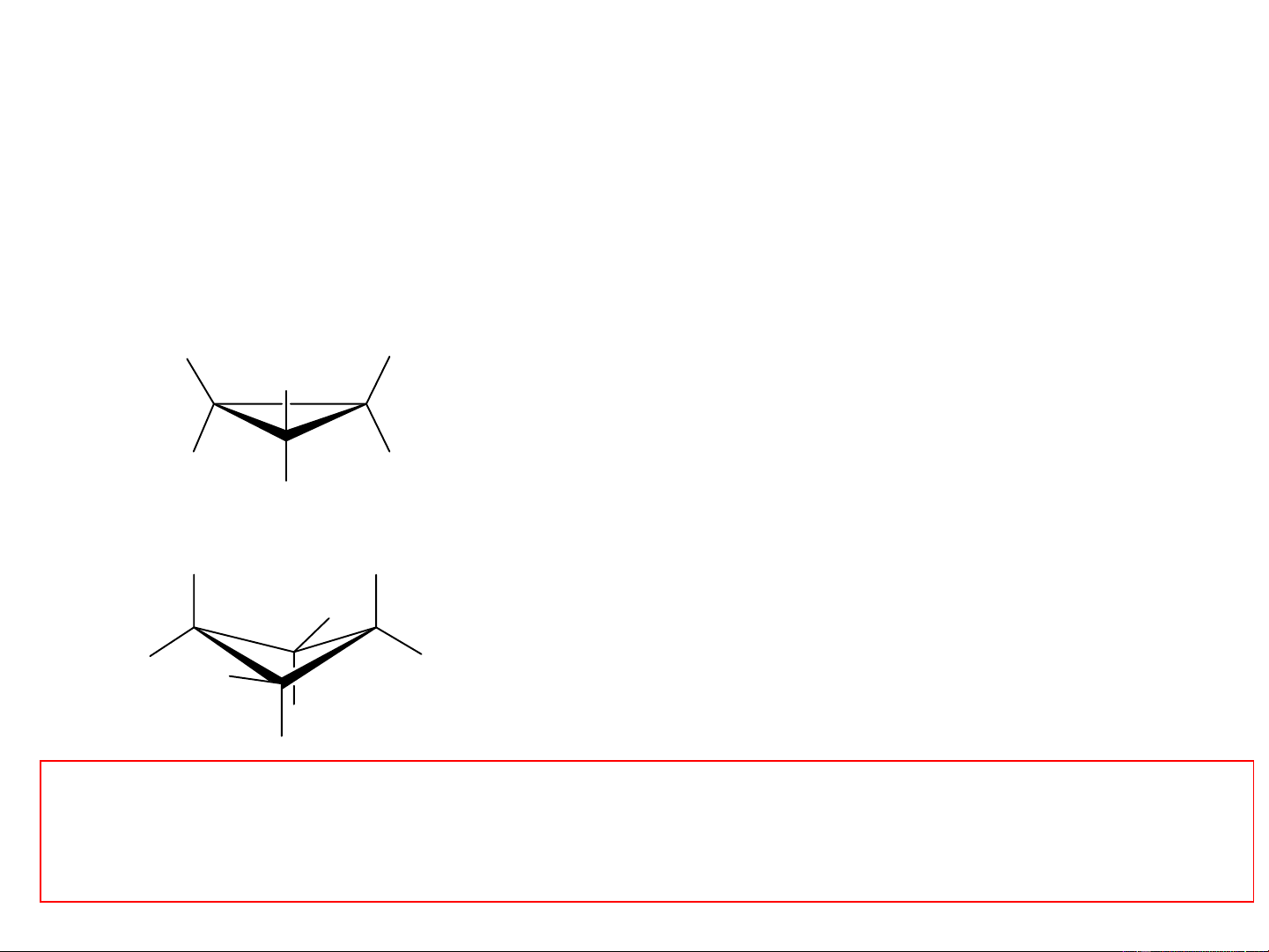
3 ngt C trong vòng 3 cạnh đồng phẳng Góc liên kết CCC = 60o
4 ngt C trong vòng 4 cạnh ở dạng gấp Góc liên kết CCC = 88o
Lưu ý: Các góc liên kết bị co hẹp lại, liên kết bị biến dạng
liên kết C-C kém bền dễ tham gia phản ứng cộng hợp, oxi hóa mở vòng
5.3.2. Hóa lập thể của hợp chất vòng (Cycloalkane)
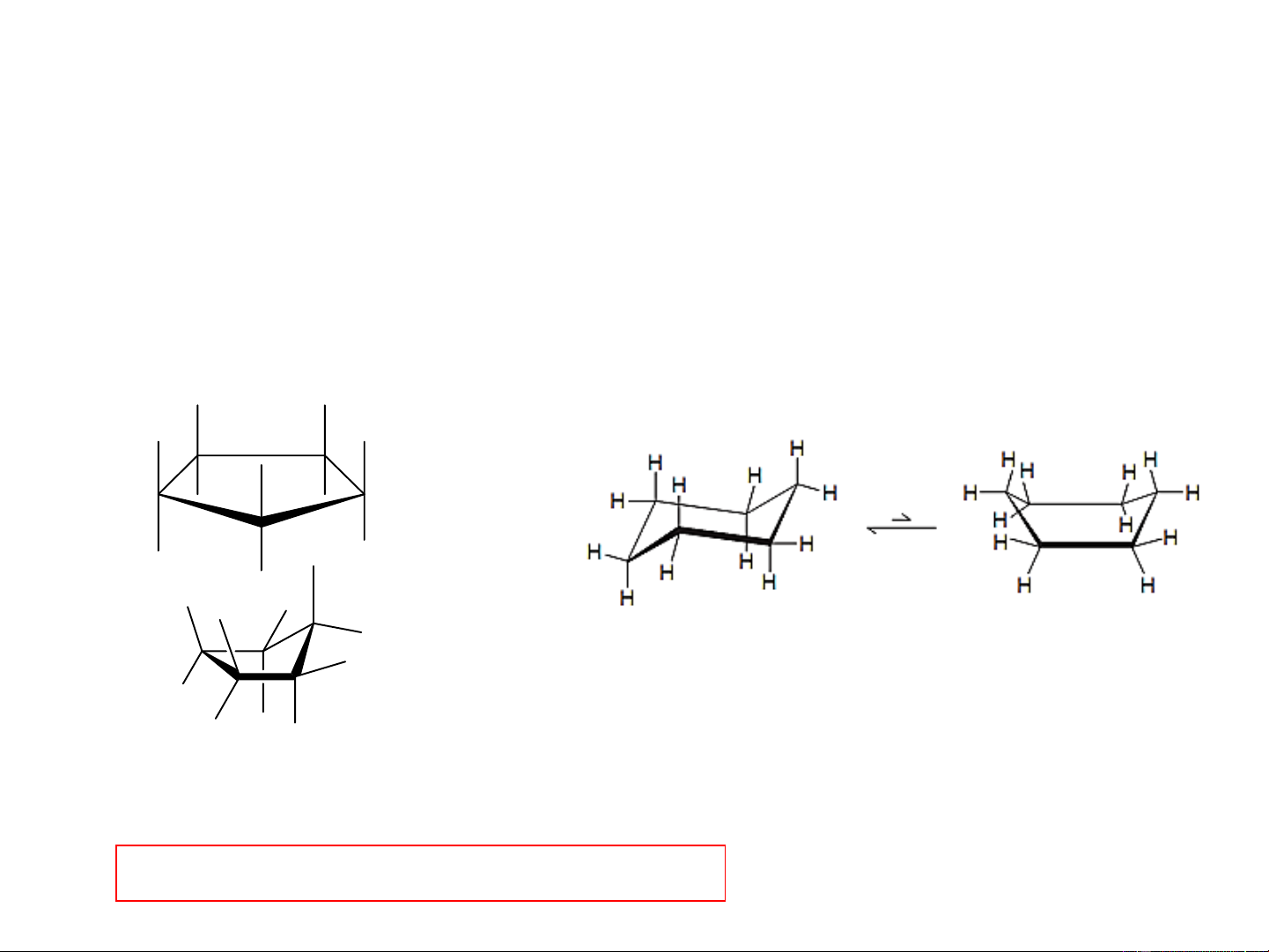
b. Vòng 5, 6 cạnh (cyclopentan, cyclohexan)
C sp3, góc liên kết 109,5o , Có cấu trúc không gian, vòng bền vững hơn cyclopentan cyclohexan Dạng ghế 99% Dạng thuyền 1% Dạng nửa ghế
Tính chất hóa học tương tự ankan
5.4. Tính chất vật lý
5.5. Các phương pháp điều chế
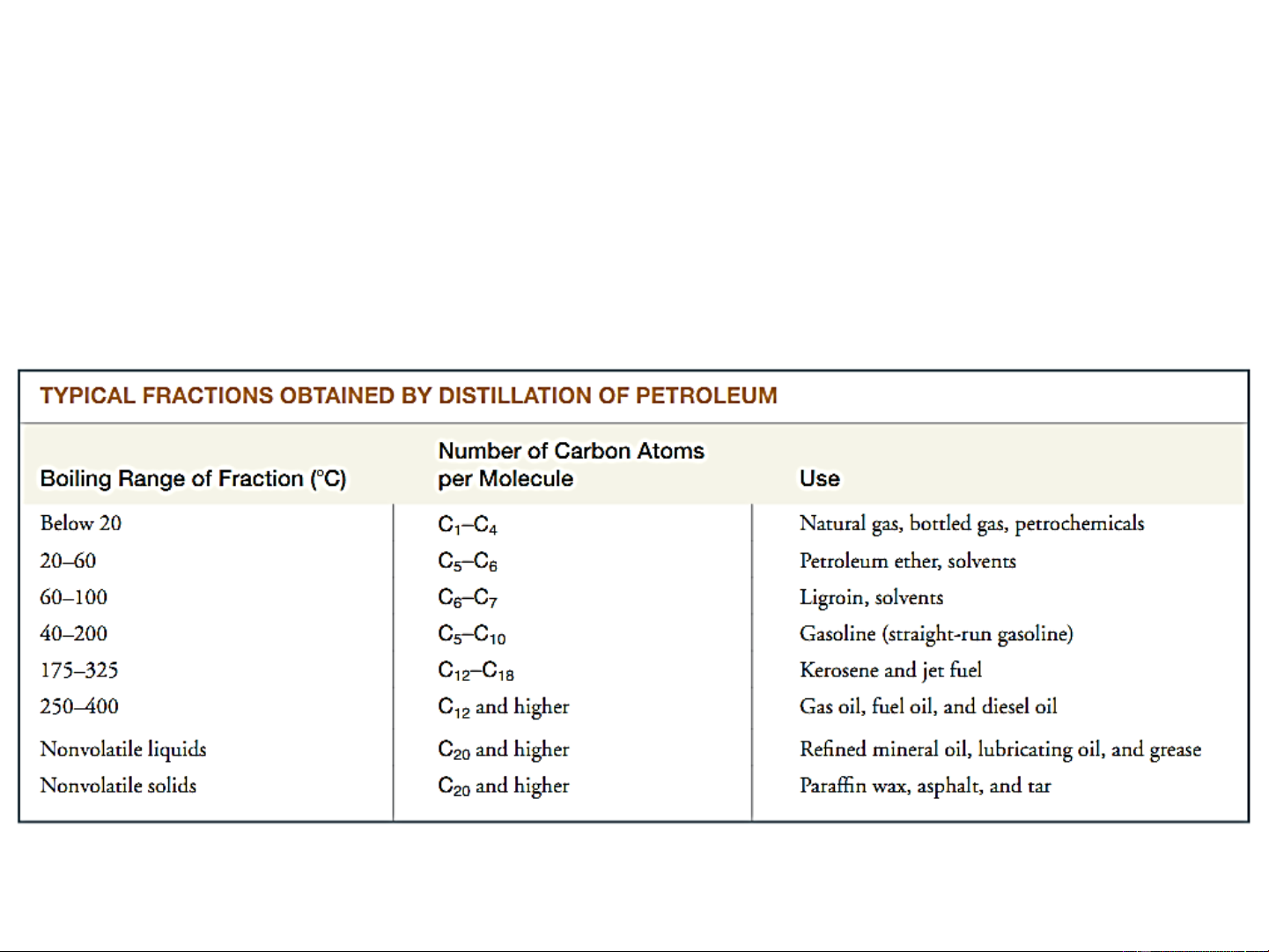
Trong công nghiệp:
- Cất phân đoạn dầu mỏ - Cracking dầu mỏ
1. Phương pháp giữ nguyên mạch cacbon
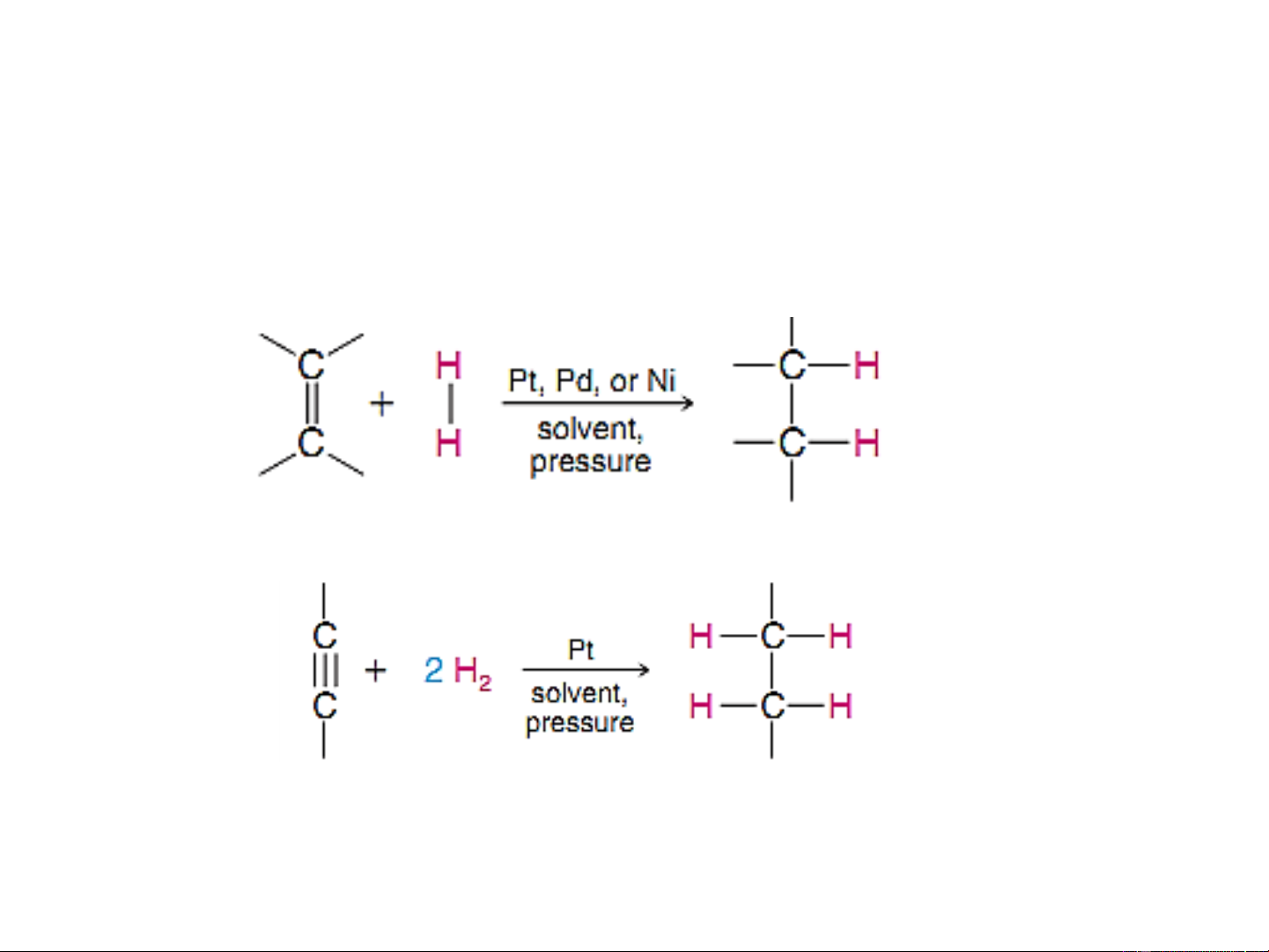
a. Hidro hóa các anken, ankin
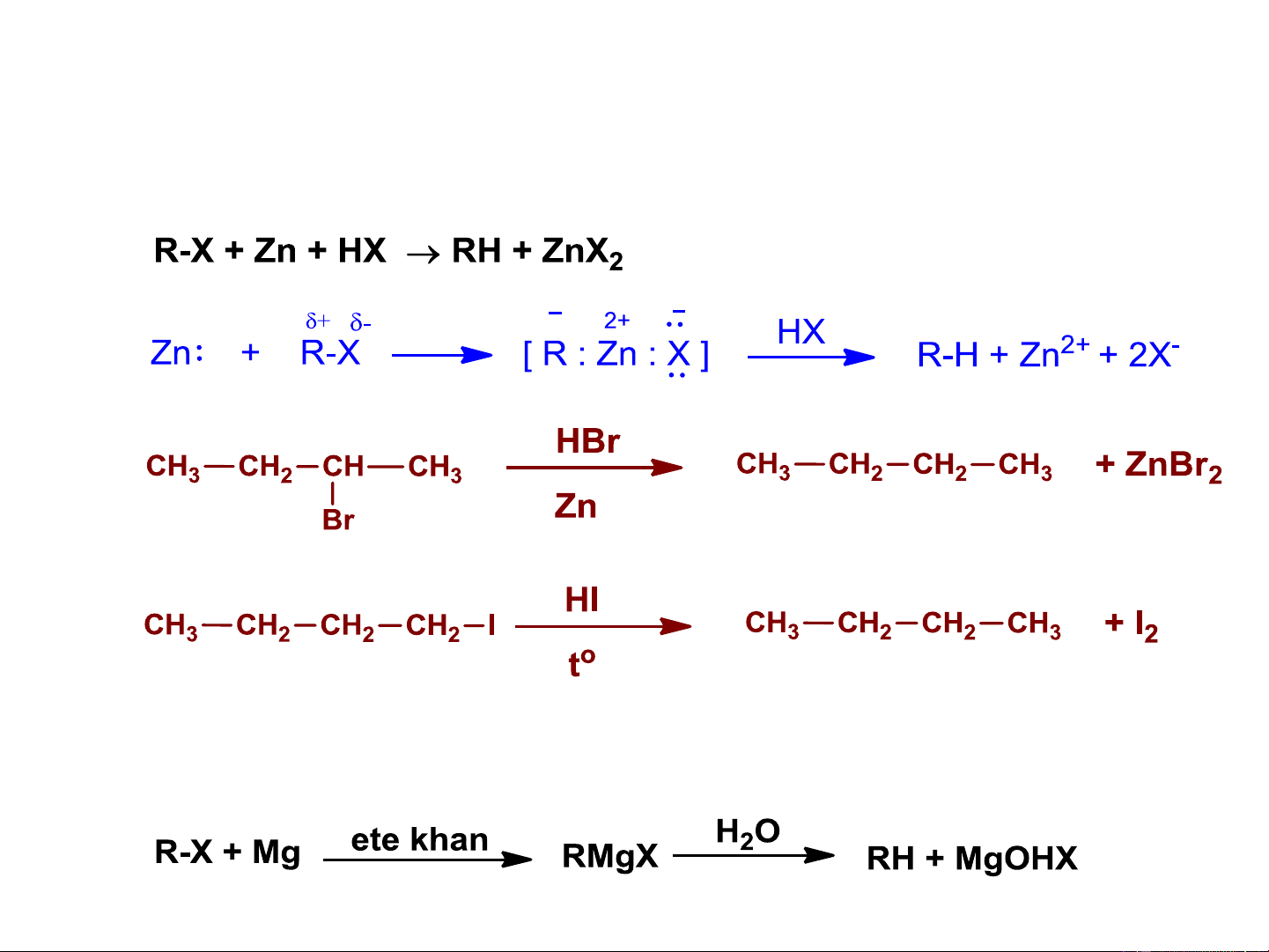
b. Khử hóa các ankyl halogenua
Khử trực tiếp:
Khử gián tiếp qua hợp chất cơ magie Ankyl magie halogenua
2. Phương pháp tăng mạch cacbon
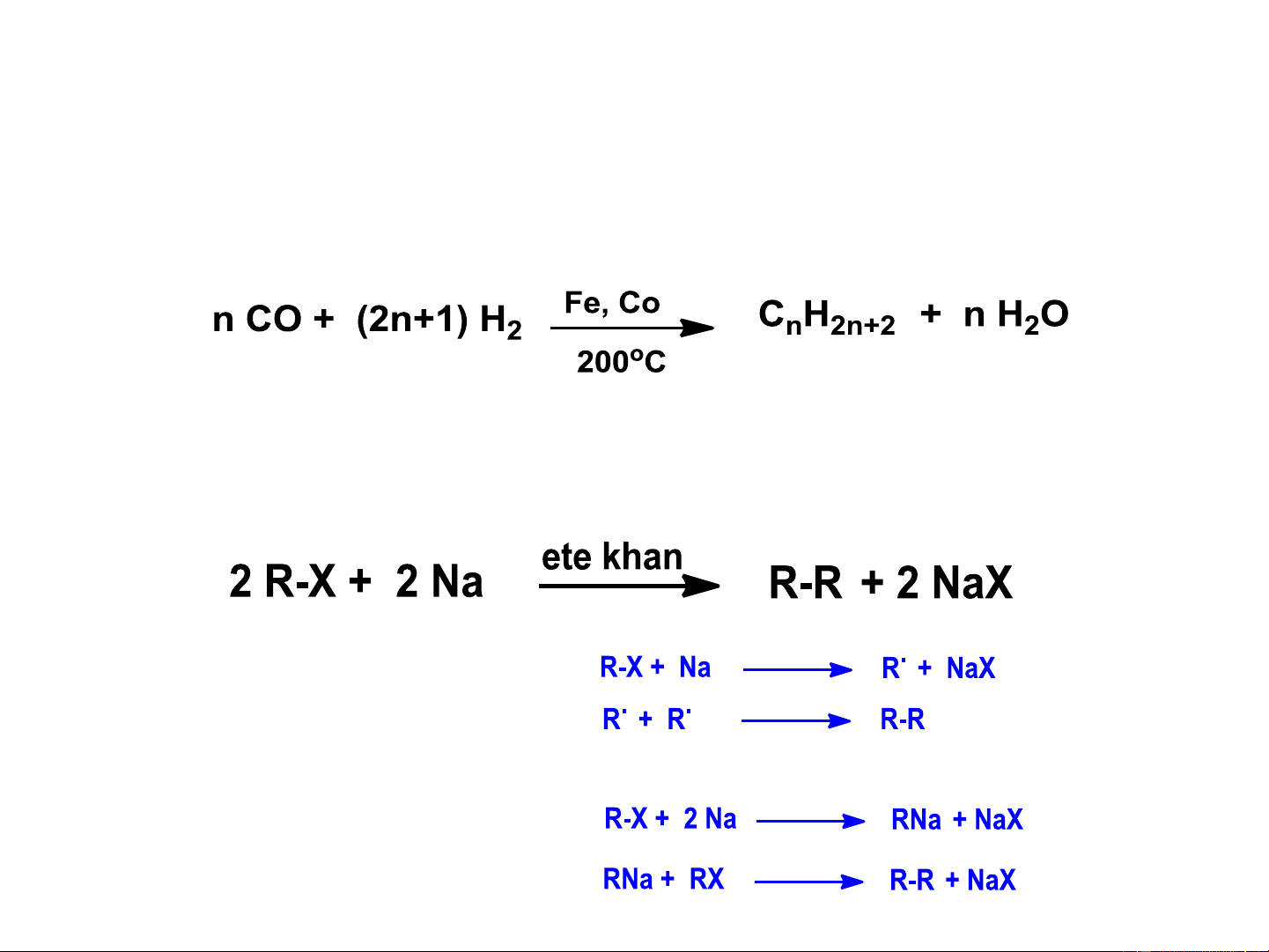
a. Phương pháp Fischer-Trop (từ CO & H ) 2
b. Tổng hợp Wurtz Cơ chế gốc
Cơ chế cơ kim
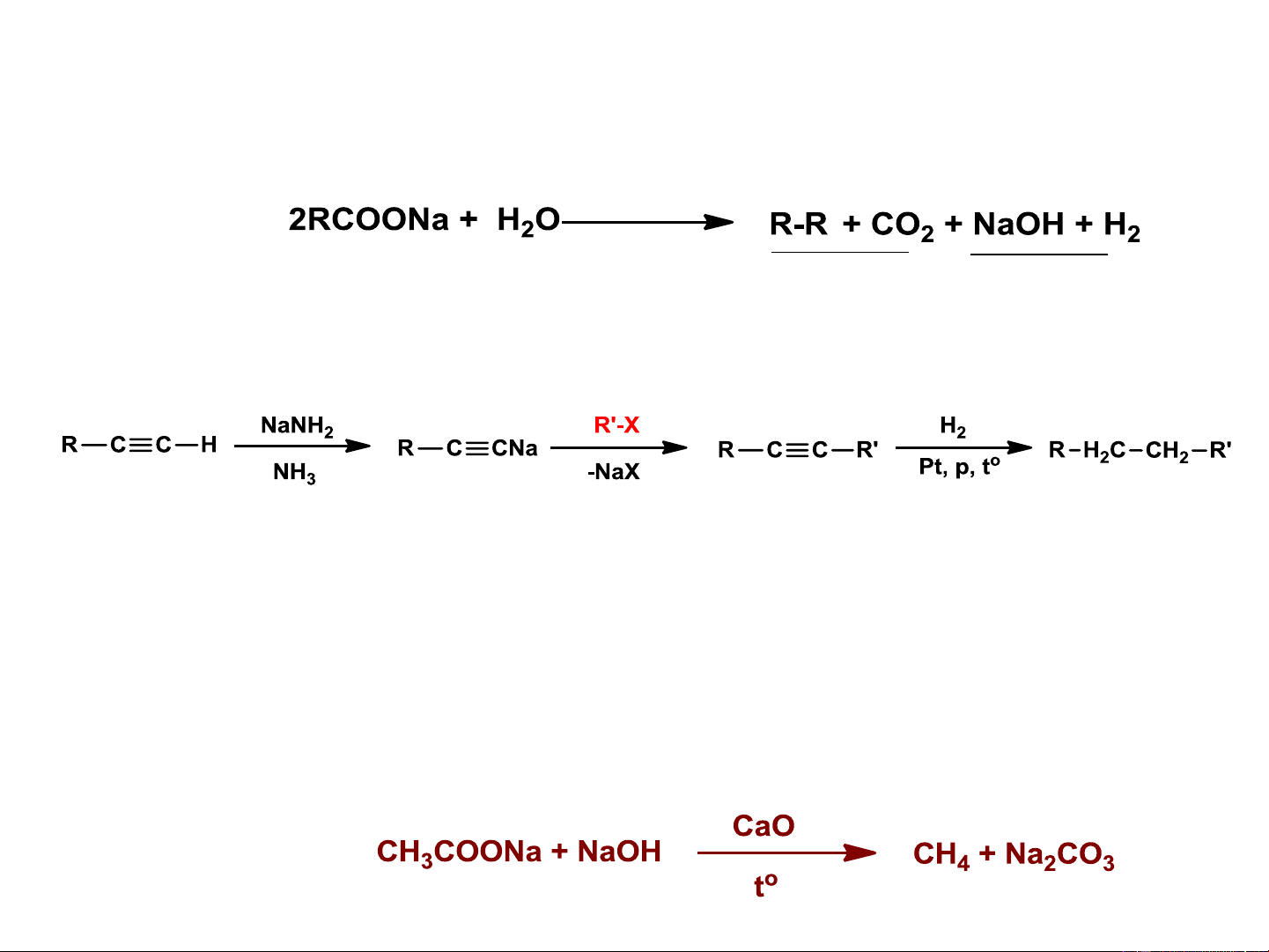
c. Tổng hợp Kolbe: điện phân muối của acid hữu cơ đpdd Phản ứng anot catot
d. Ankyl hóa các ankin-1
3. Phương pháp giảm mạch cacbon
Nhiệt phân muối của acid hữu cơ (phản ứng vôi tôi xút) Ví dụ
5.6. Tính chất hóa học
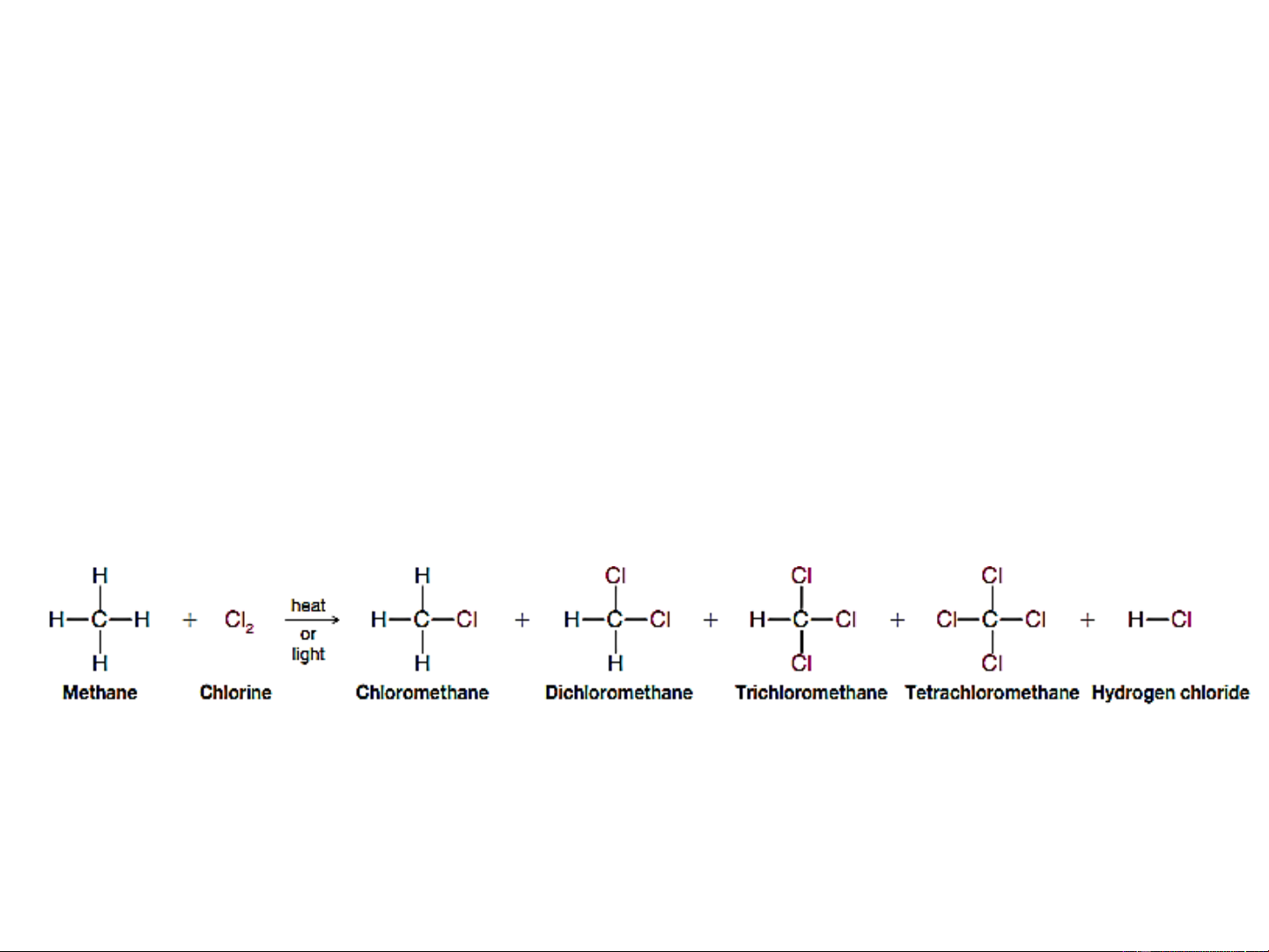
5.6.1. Phản ứng thế halogen a/s Phản ứng R-H + X RX + HX 2 a/s Ví dụ
CH + Cl CH Cl + HCl (CH Cl , CHCl , CCl ) 4 2 3 2 2 3 4
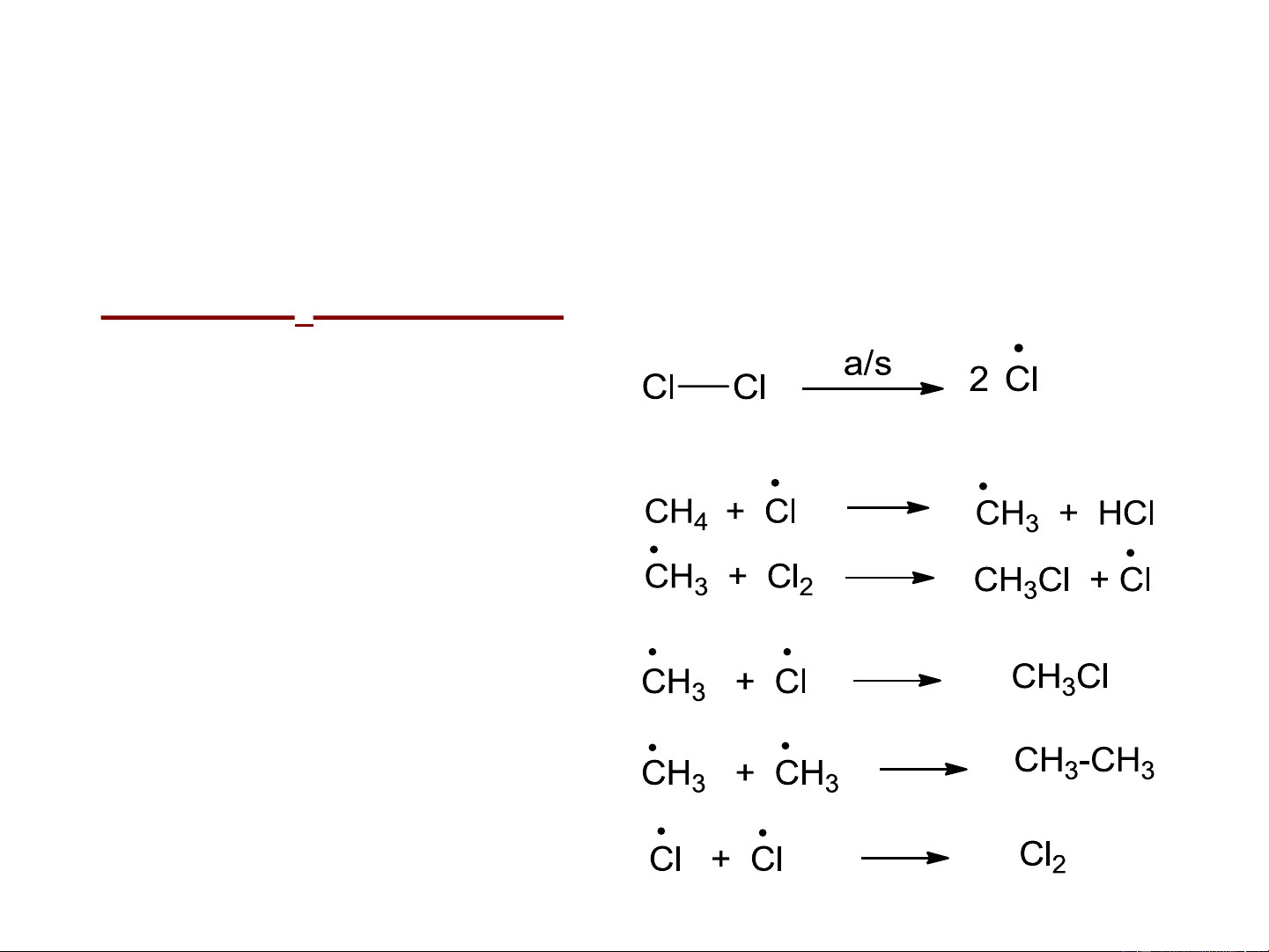
a. Cơ chế thế gốc tự do (S ) R a/s
Phản ứng: CH + Cl CH Cl + HCl Ho = -102 KJ/mol 4 2 3 Clometan (methylclorua)
Cơ chế: S (3 giai đoạn) R GĐ 1: Khơi mào
GĐ 2: Phát triển mạch GĐ 3: Tắt mạch
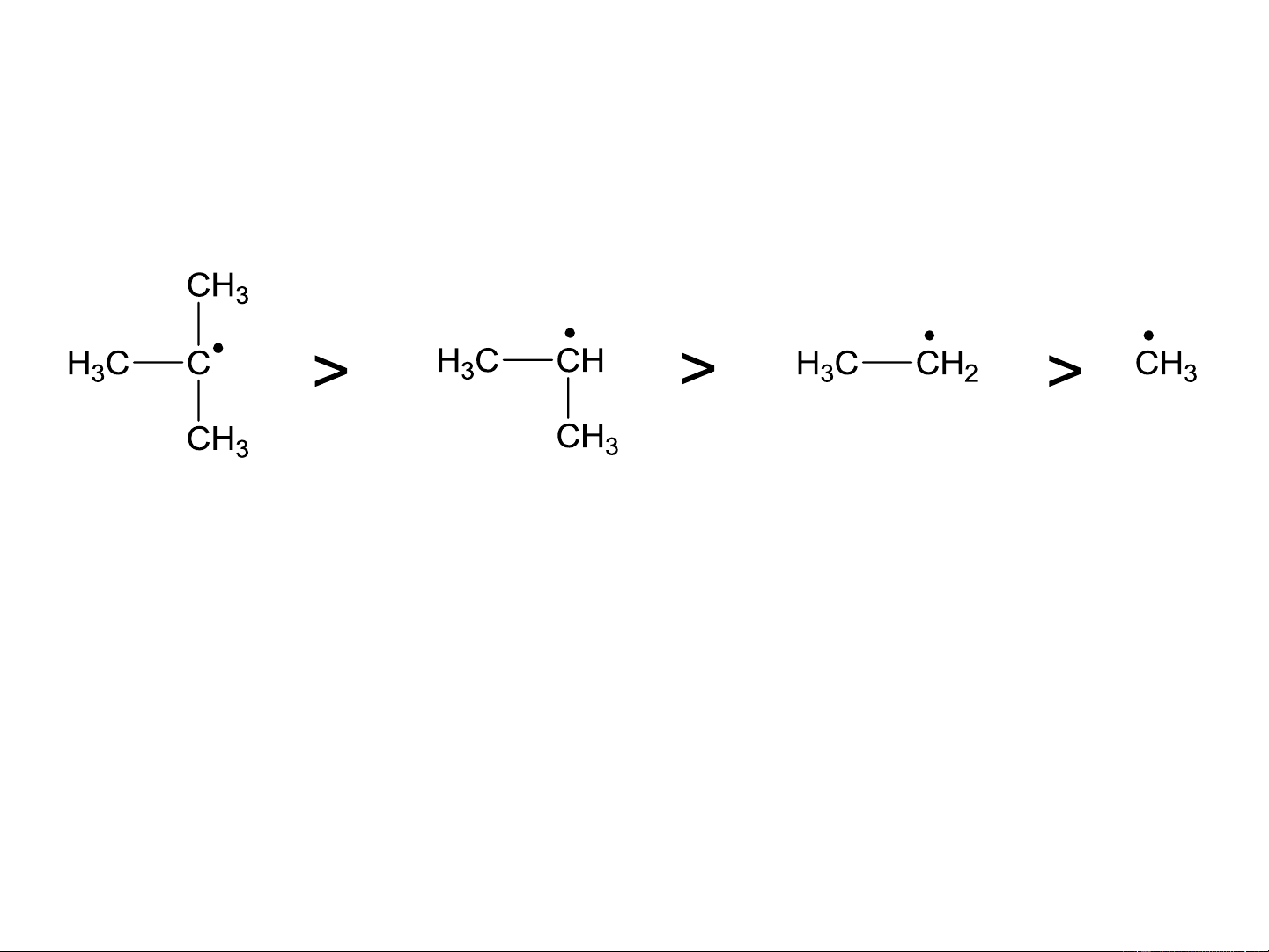
b. Khả năng phản ứng thế của các gốc hydrocacbon
Độ bền gốc: 3o > 2o > 1o > gốc methyl