Câu hỏi:
04/07/2025 95Điện phân dung dịch A chứa 0,4 mol M(NO3)2 và 1 mol NaNO3 với điện cực trơ trong thời gian 48 phút 15 giây thì thu được 11,52 gam kim loại M bên catot. Cho các phát biểu sau:
1. M là Cu.
2. Cường độ dòng điện đã dùng bằng 10 (A).
3. Thời gian điện phân dung dịch mất hết M2+ với cường độ dòng điện 12 (A) là là 48 phút 15 giây.
Trong các phát biểu trên, số phát biểu đúng là?
0
1
2
3
Trả lời:
 Trả lời bởi Docx
Trả lời bởi Docx
catot(-) ← M(NO3)2 (dung dịch); NaNO3(dung dịch) → anot(+)
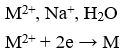
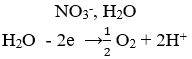
Phương trình điện phân:
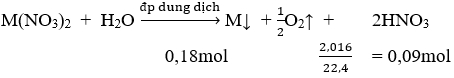
⇒ M = 11,52/0,18 = 64 đ.v.c ⇒ M là Cu
Theo định luật Faraday mCu = (64/2). [(I.2895)/96500] = 11,52 ⇒ I = 12A
Điện phân hết 0,18 mol Cu2+ tạo ra 0,18 mol Cu cần t1 = 2895s
Vậy điện phân hết 0,4 mol Cu2+ tạo ra 0,4 mol Cu cần t2 = (0,4.2895)/0,18 = 6433
Vậy chỉ có phát biểu đầu tiên đúng.
→ Đáp án B
CÂU HỎI HOT CÙNG CHỦ ĐỀ

